第六单元碳和碳的化合物复习导学案
文档属性
| 名称 | 第六单元碳和碳的化合物复习导学案 |
|
|
| 格式 | zip | ||
| 文件大小 | 154.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2011-12-26 00:00:00 | ||
图片预览

文档简介
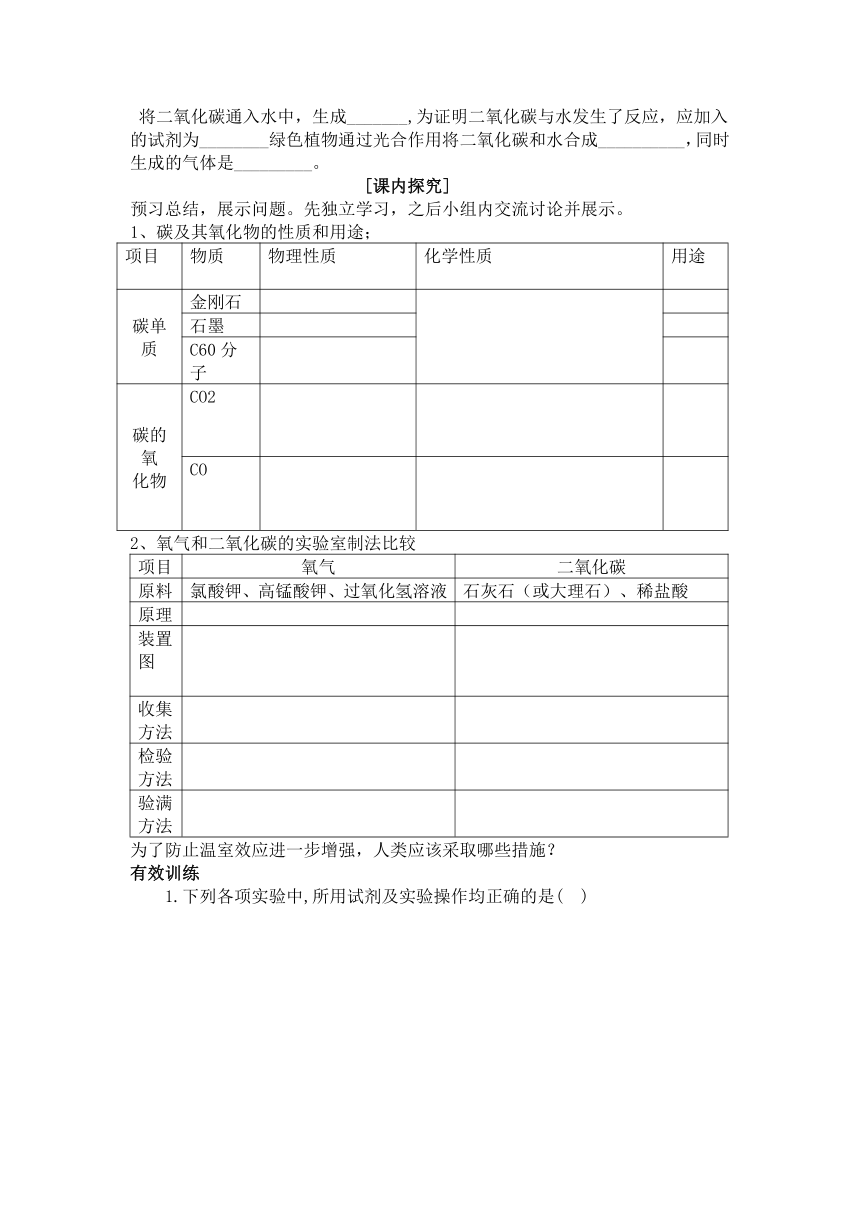
第六单元《碳和碳的氧化物》复习学案
教学目标:(1)碳单质的性质和用途;
(2)实验室制取二氧化碳的反应原理、装置、收集方法和检验方法;
(3)CO2、CO的性质、用途以及对生活和环境的影响;
(4)通过讨论一些实际问题,培养学生分析问题和解决问题的能力;
教学重难点:1、碳单质、CO2、CO的化学性质。2、实验室制取二氧化碳的方法。
[课前延伸]构建知识网络,总结研究方法
按照下表所列顺序,回忆所学知识,填写相关内容,形成本单元知识网络,总结出研究方法。 请同学们自主完成,提出你认为还应补充的内容以及你还有哪些疑问。
____________
单质 ___________ 化学性质
____________
碳 物理性质:__________ _____
二氧化碳 化学性质:__________ __________ ___________
实验室制法 原理:_______________________
装置:
氧化物 验满:_______________________
收集方法:_____________
物理性质:___________ _____________ ________
化学性质:____________ ____________ ________
一氧化碳 用途:____________ ___________
自我检测
1、1985年科学家发现了一种组成为C60的物质,下列说法正确的是( )
A、它是一种新型的化合物 B、它是由碳原子构成的物质
C、它与金刚石一样具有很大的硬度 D、它的一个分子由60个碳原子构成
2、下列物质中,肯定是纯净物的( )
A、木炭 B、只含有一种元素的物质 C、金刚石 D、铅笔芯
3、实验室制取二氧化碳时,向盛有石灰石的容器中加入稀盐酸后,过一会儿石灰石表面几乎无气泡产生,其原因可能是( ) A、发生装置的气密性不好 B、没有加热 C、石灰石中含有碳酸钙较少D、加入的是稀硫酸
4、二氧化碳的下述用途没有利用其化学性质的( )A、二氧化碳用作气体肥料 B、二氧化碳用于灭火 C、干冰用于人工降雨 D、二氧化碳用来制二氧化碳
5、反应条件在化学反应中起着重要的作用,反应物相同但条件不同,生成物可能不同。
将二氧化碳通入水中,生成_______,为证明二氧化碳与水发生了反应,应加入的试剂为________绿色植物通过光合作用将二氧化碳和水合成__________,同时生成的气体是_________。
[课内探究]
预习总结,展示问题。先独立学习,之后小组内交流讨论并展示。
1、碳及其氧化物的性质和用途;
项目 物质 物理性质 化学性质 用途
碳单质 金刚石
石墨
C60分子
碳的氧化物 CO2
CO
氧气和二氧化碳的实验室制法比较
项目 氧气 二氧化碳
原料 氯酸钾、高锰酸钾、过氧化氢溶液 石灰石(或大理石)、稀盐酸
原理
装置图
收集方法
检验方法
验满方法
为了防止温室效应进一步增强,人类应该采取哪些措施?
有效训练
1.下列各项实验中,所用试剂及实验操作均正确的是( )
2.关于一氧化碳燃烧()说法正确的是( )
(A)反应过程中吸收大量的热 (B)反应前后分子个数不变
(C)参加反应的一氧化碳和氧气的质量比为2∶1
(D)化学方程式中反应物的化学计量数之比表示为V(CO)∶V(O2)=2∶1
3.有关H2、CO、C三种物质的下列说法正确的是
A.都是目前最理想的清洁燃料 B.与金属氧化物发生的反应都属于置换反应
C.在氧气中燃烧,都产生淡蓝色火焰 D.与金属氧化物反应后,一定有化合物生成
4.贝壳(含CaCO3)煅烧后得CaO,CaO加到海水(含有MgCl2)池中得Mg(OH)2沉淀,Mg(OH)2与盐酸反应得MgCl2溶液。上述生产过程中没有涉及到的反应类型是
A.化合反应 B.置换反应 C.复分解反应 D.分解反应
5继“分子足球”C60之后,科学家又发现另一种“分子足球”N60。一定条件下N60中积累的巨大能量会在一瞬间释放出来,是未来的火箭燃料,N60属于
A.金属单质 B.非金属单质 C.化合物 D.混合物
6.利用图8装置可进行气体性质的探究实验.甲的玻璃管中盛放黑色粉末(CuO或C),乙的洗气瓶中盛放无色溶液(澄清石灰水或NaOH溶液).
(1)写出仪器的名称: a______ , b______ .(2)根据要求填表
(3)上述两实验中,在导管c的尖嘴处都用火柴点燃,其目的是否完全相同 简述理由.
五、小结 本节课你的收获是什么?[课后延伸]
1、为了研究CO2的性质,需要制取并收集干燥的CO2气体。以下是老师提供的一些实验装置。
(1)制取并收集干燥的CO2气体,可采用的装置组合是 (填字母)。
2实验室制取CO2的化学方程式为 。
3若在上述实验中气体无法收集满,则可能的原因是 。
4、某厂用石灰石高温煅烧制得生石灰,若每天消耗含杂质5%的石灰石原料300吨。请根据计算回答下列问题:⑴ 理论上每天可生产氧化钙多少吨(假设杂质受热不分解)?
⑵ 若每吨石灰石以100元的价格买入,制得的生石灰(含原杂质)以每吨250元卖出,扣除每吨石灰石原料生产的加工费30元,则该厂每天可获利润多少元?
26.(10分)某化学研究小组对当地的石灰石样品进行了研究。称取石灰石样品8g,把40g稀盐酸分四次加入样品中,测得实验数据见下表(假设石灰石样品中杂质不溶于水、不与盐酸反应,二氧化碳不溶解)。
实验序号 加入稀盐酸的质量/g 剩余物质的质量/g
第1次 10 5.5
第2次 10 3
第3次 10 1.6
第4次 10 m
(1)第4次剩余物质的质量m= g(2)石灰石样品中CaCO3的质量分数为 。(3)计算稀盐酸的溶质质量分数。
稀HCl
NaOH溶液
浓H2SO4
CaCO3
A
B
C
D
E
F
教学目标:(1)碳单质的性质和用途;
(2)实验室制取二氧化碳的反应原理、装置、收集方法和检验方法;
(3)CO2、CO的性质、用途以及对生活和环境的影响;
(4)通过讨论一些实际问题,培养学生分析问题和解决问题的能力;
教学重难点:1、碳单质、CO2、CO的化学性质。2、实验室制取二氧化碳的方法。
[课前延伸]构建知识网络,总结研究方法
按照下表所列顺序,回忆所学知识,填写相关内容,形成本单元知识网络,总结出研究方法。 请同学们自主完成,提出你认为还应补充的内容以及你还有哪些疑问。
____________
单质 ___________ 化学性质
____________
碳 物理性质:__________ _____
二氧化碳 化学性质:__________ __________ ___________
实验室制法 原理:_______________________
装置:
氧化物 验满:_______________________
收集方法:_____________
物理性质:___________ _____________ ________
化学性质:____________ ____________ ________
一氧化碳 用途:____________ ___________
自我检测
1、1985年科学家发现了一种组成为C60的物质,下列说法正确的是( )
A、它是一种新型的化合物 B、它是由碳原子构成的物质
C、它与金刚石一样具有很大的硬度 D、它的一个分子由60个碳原子构成
2、下列物质中,肯定是纯净物的( )
A、木炭 B、只含有一种元素的物质 C、金刚石 D、铅笔芯
3、实验室制取二氧化碳时,向盛有石灰石的容器中加入稀盐酸后,过一会儿石灰石表面几乎无气泡产生,其原因可能是( ) A、发生装置的气密性不好 B、没有加热 C、石灰石中含有碳酸钙较少D、加入的是稀硫酸
4、二氧化碳的下述用途没有利用其化学性质的( )A、二氧化碳用作气体肥料 B、二氧化碳用于灭火 C、干冰用于人工降雨 D、二氧化碳用来制二氧化碳
5、反应条件在化学反应中起着重要的作用,反应物相同但条件不同,生成物可能不同。
将二氧化碳通入水中,生成_______,为证明二氧化碳与水发生了反应,应加入的试剂为________绿色植物通过光合作用将二氧化碳和水合成__________,同时生成的气体是_________。
[课内探究]
预习总结,展示问题。先独立学习,之后小组内交流讨论并展示。
1、碳及其氧化物的性质和用途;
项目 物质 物理性质 化学性质 用途
碳单质 金刚石
石墨
C60分子
碳的氧化物 CO2
CO
氧气和二氧化碳的实验室制法比较
项目 氧气 二氧化碳
原料 氯酸钾、高锰酸钾、过氧化氢溶液 石灰石(或大理石)、稀盐酸
原理
装置图
收集方法
检验方法
验满方法
为了防止温室效应进一步增强,人类应该采取哪些措施?
有效训练
1.下列各项实验中,所用试剂及实验操作均正确的是( )
2.关于一氧化碳燃烧()说法正确的是( )
(A)反应过程中吸收大量的热 (B)反应前后分子个数不变
(C)参加反应的一氧化碳和氧气的质量比为2∶1
(D)化学方程式中反应物的化学计量数之比表示为V(CO)∶V(O2)=2∶1
3.有关H2、CO、C三种物质的下列说法正确的是
A.都是目前最理想的清洁燃料 B.与金属氧化物发生的反应都属于置换反应
C.在氧气中燃烧,都产生淡蓝色火焰 D.与金属氧化物反应后,一定有化合物生成
4.贝壳(含CaCO3)煅烧后得CaO,CaO加到海水(含有MgCl2)池中得Mg(OH)2沉淀,Mg(OH)2与盐酸反应得MgCl2溶液。上述生产过程中没有涉及到的反应类型是
A.化合反应 B.置换反应 C.复分解反应 D.分解反应
5继“分子足球”C60之后,科学家又发现另一种“分子足球”N60。一定条件下N60中积累的巨大能量会在一瞬间释放出来,是未来的火箭燃料,N60属于
A.金属单质 B.非金属单质 C.化合物 D.混合物
6.利用图8装置可进行气体性质的探究实验.甲的玻璃管中盛放黑色粉末(CuO或C),乙的洗气瓶中盛放无色溶液(澄清石灰水或NaOH溶液).
(1)写出仪器的名称: a______ , b______ .(2)根据要求填表
(3)上述两实验中,在导管c的尖嘴处都用火柴点燃,其目的是否完全相同 简述理由.
五、小结 本节课你的收获是什么?[课后延伸]
1、为了研究CO2的性质,需要制取并收集干燥的CO2气体。以下是老师提供的一些实验装置。
(1)制取并收集干燥的CO2气体,可采用的装置组合是 (填字母)。
2实验室制取CO2的化学方程式为 。
3若在上述实验中气体无法收集满,则可能的原因是 。
4、某厂用石灰石高温煅烧制得生石灰,若每天消耗含杂质5%的石灰石原料300吨。请根据计算回答下列问题:⑴ 理论上每天可生产氧化钙多少吨(假设杂质受热不分解)?
⑵ 若每吨石灰石以100元的价格买入,制得的生石灰(含原杂质)以每吨250元卖出,扣除每吨石灰石原料生产的加工费30元,则该厂每天可获利润多少元?
26.(10分)某化学研究小组对当地的石灰石样品进行了研究。称取石灰石样品8g,把40g稀盐酸分四次加入样品中,测得实验数据见下表(假设石灰石样品中杂质不溶于水、不与盐酸反应,二氧化碳不溶解)。
实验序号 加入稀盐酸的质量/g 剩余物质的质量/g
第1次 10 5.5
第2次 10 3
第3次 10 1.6
第4次 10 m
(1)第4次剩余物质的质量m= g(2)石灰石样品中CaCO3的质量分数为 。(3)计算稀盐酸的溶质质量分数。
稀HCl
NaOH溶液
浓H2SO4
CaCO3
A
B
C
D
E
F
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
