2020-2021学年人教版九年级下化学第八单元 金属和金属材料课题 2 金属的化学性质(30张PPT)
文档属性
| 名称 | 2020-2021学年人教版九年级下化学第八单元 金属和金属材料课题 2 金属的化学性质(30张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-02 00:00:00 | ||
图片预览










文档简介
金属与氧气的反应
强
弱
Au
Fe
Na
Mg
Al
Cu
活泼程度
与O2反应的难易
常温
高温
真金不怕火炼
20℃
近来,本市接连发生利用假金佛、假金元宝等进行诈骗的案件,警方迅速行动,在昌平、大兴等地打掉了数个以此为生的“金佛(元宝)”诈骗团伙,涉案金额达数百万元。
这些不法分子常以黄铜(铜、锌合金)自制假金佛、假金元宝以及假金条。因为黄铜单纯从颜色、外型上看,与黄金极为相似,普通市民很难区分,他们正是利用这点疯狂进行诈骗犯罪。
你有办法吗?
如果有一天碰巧你遇到了这件事,你能用什么方法来揭穿他们吗?
如何辨别真假金佛
资料:假黄金:黄铜
(铜、锌合金)
请看执法人员的方法
金属的化学性质
中学化学
九年级下学期 第十章 第二节
【实验目的】
探究金属镁、锌、铁、铜与稀盐酸的反应
金属与酸的反应
【实验药品】
金属:镁条、锌粒、铁丝、铜片
酸 : 稀盐酸
【实验】镁、锌、铁、铜与稀盐酸的反应
【实验操作】分别将少量镁、锌、铁、铜放在试管中,再加入少量稀盐酸(HCl)。
金属与酸的反应
先加入固体
再倒入液体
【提出问题】
1.是否所有的金属都能与稀盐酸反应?
2.可以和稀盐酸反应的金属,反应的现象相同吗?
3.哪些因素会影响反应的剧烈程度?
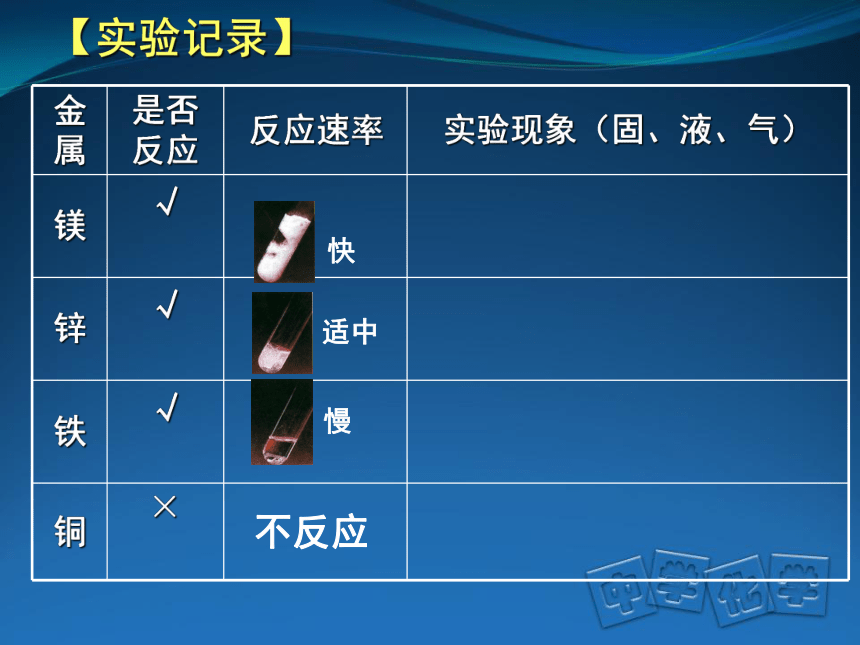
【实验记录】
金属
是否反应
反应速率
实验现象(固、液、气)
镁
√
锌
√
铁
√
铜
×
快
适中
慢
不反应
Mg Zn Fe Cu
强
弱
金属活动性
与酸是否反应及反应速率
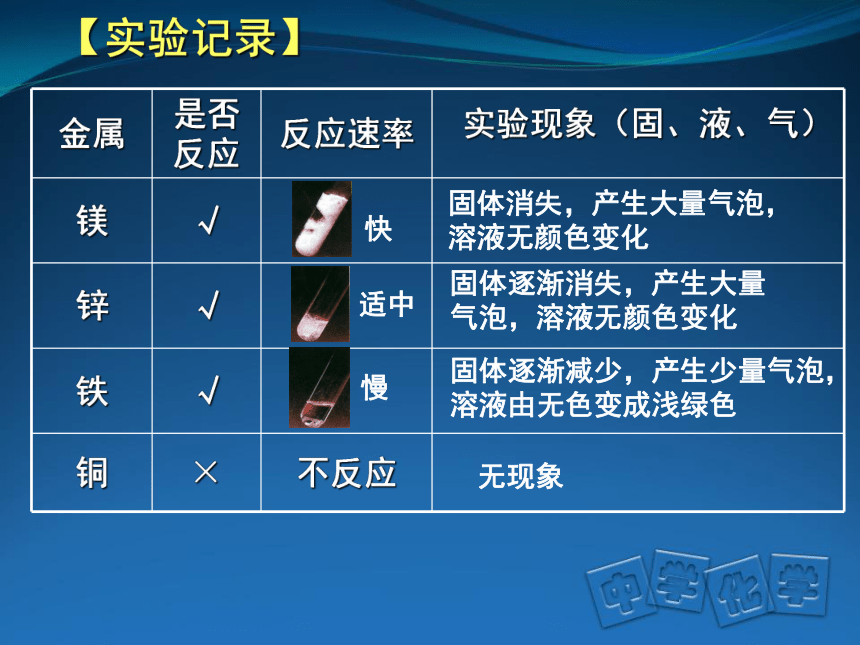
【实验记录】
金属
是否反应
反应速率
镁
√
锌
√
铁
√
铜
×
不反应
实验现象(固、液、气)
固体消失,产生大量气泡,溶液无颜色变化
固体逐渐消失,产生大量气泡,溶液无颜色变化
固体逐渐减少,产生少量气泡,溶液由无色变成浅绿色
无现象
快
适中
慢
【实验药品】
金属:镁条、锌粒、铁丝、铜片
酸 : 稀盐酸
问题4.通过已提供实验药品能否根据控制变量分析出四种金属与稀盐酸反应的情况?
问题5.如何改进实验方案设计完成实验探究?
【实验目的】
探究金属镁、锌、铁、铜与稀盐酸的反应
在环境相同时,取形状、大小相同的镁、锌、铁、铜四种金属分别于四只同样的试管中,倒入等浓度、等体积的的稀盐酸,测量相同时间内产生气体的体积
?
Mg + HCl =
Zn + HCl =
Fe + HCl =
小资料:氯气是一种黄绿色有毒的气体,氢气是无色无味的可燃性气体
MgCl2 + H2↑
2
ZnCl2 + H2↑
2
FeCl2 + H2↑
2
小资料:二价亚铁的溶液是浅绿色,
三价的铁的溶液是黄色
单质
单质
化合物
化合物
置换反应
Zn + H2SO4 =
Mg + H2SO4 =
Fe + H2SO4 =
MgSO4 + H2↑
ZnSO4 + H2↑
FeSO4 + H2↑
你有办法吗?
如果有一天碰巧你遇到了这件事,你能用什么方法来揭穿他们吗?
小资料:
黄金是一种具有金黄色光泽的金属、化学性质极不活泼。黄铜的外形与黄金非常相似,所以不法分子常用黄铜(Zn,Cu合金)来冒充黄金。
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A} 微 粒
物 质
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A} 物 质
微 粒
Fe
稀盐酸
小资料:稀盐酸是氯化氢气体的水溶液
Cl-
H+
H2O
Fe
反应物
生成物
Fe2+
Cl-
H2O
H2
FeCl2
溶液
H2
金属与酸反应的微观实质
H+
H+
H+
H+
Cl-
Cl-
Cl-
Cl-
Fe
Fe
Cl-
Cl-
Cl-
Cl-
Fe2+
Fe2+
金属与酸反应的微观实质
H2
H
H
H
H
失1e
H+
H+
H+
H+
Fe
Fe
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Fe2+
Fe2+
H2
金属与酸反应的微观实质
H
H
H
H
金属与酸反应的微观实质
Fe原子失掉两个电子变成Fe2+,
每个H+得到一个电子变成H原子在构成H2
小结:在一个化学反应里有失电子的微粒就有得电子的微粒。
问题5:请同学们分析锌与稀盐酸,镁与稀盐酸反应的微观实质。
Fe + 2HCl = FeCl2 + H2↑
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
元素
反应前
反应后
同种元素反应前后化合价变化情况
Fe
H
Cl
0
+2
+1
+1
0
0
-1
-1
-1
小结:在化学反应中有化合价升高的元素就有化合 价降低的元素。
Fe + 2HCl = FeCl2 + H2↑
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
元素
反应前
反应后
同种元素化合价变化情况
Fe
H
Cl
反应前后微粒种类
0
+2
+1
0
-1
-1
Fe
Fe2+
H+
H2
Cl-
Cl-
总结:化学反应中有电子的得与失就有化合价的降低和升高。
+1
-1
0
Fe + 2HCl = FeCl2 + H2↑
金属与酸反应的定量分析
56
反应前后溶液质量的变化
金属铁中加入一定质量的稀盐酸,反应前后溶液质量的变化,并在直角坐标中表示出变化的趋势?
71
H+
Cl-
Fe2+
Cl-
溶液质量增加
0
溶液质量
时间/t
2
71
总结
1.工业冶炼金属锰的原理是
3MnO2+4Al 3Mn+2Al2O3,该反应属于
A.置换反应 B.化合反应
C.分解反应 D.复分解反应
练习
练习
2.如下图所示:气球中装有一定量的铁粉,试管中装有适量的稀盐酸,拿起气球,使
铁粉进入试管,写出反的化学应方程
式 ,描述实验现象
。
练习
3.根据下图所示,回答下列问题:
(1)写出该反应的化学方程式
(2)该反应中化合价发生变化的元素是
(3)发生变化微粒是
强
弱
Au
Fe
Na
Mg
Al
Cu
活泼程度
与O2反应的难易
常温
高温
真金不怕火炼
20℃
近来,本市接连发生利用假金佛、假金元宝等进行诈骗的案件,警方迅速行动,在昌平、大兴等地打掉了数个以此为生的“金佛(元宝)”诈骗团伙,涉案金额达数百万元。
这些不法分子常以黄铜(铜、锌合金)自制假金佛、假金元宝以及假金条。因为黄铜单纯从颜色、外型上看,与黄金极为相似,普通市民很难区分,他们正是利用这点疯狂进行诈骗犯罪。
你有办法吗?
如果有一天碰巧你遇到了这件事,你能用什么方法来揭穿他们吗?
如何辨别真假金佛
资料:假黄金:黄铜
(铜、锌合金)
请看执法人员的方法
金属的化学性质
中学化学
九年级下学期 第十章 第二节
【实验目的】
探究金属镁、锌、铁、铜与稀盐酸的反应
金属与酸的反应
【实验药品】
金属:镁条、锌粒、铁丝、铜片
酸 : 稀盐酸
【实验】镁、锌、铁、铜与稀盐酸的反应
【实验操作】分别将少量镁、锌、铁、铜放在试管中,再加入少量稀盐酸(HCl)。
金属与酸的反应
先加入固体
再倒入液体
【提出问题】
1.是否所有的金属都能与稀盐酸反应?
2.可以和稀盐酸反应的金属,反应的现象相同吗?
3.哪些因素会影响反应的剧烈程度?
【实验记录】
金属
是否反应
反应速率
实验现象(固、液、气)
镁
√
锌
√
铁
√
铜
×
快
适中
慢
不反应
Mg Zn Fe Cu
强
弱
金属活动性
与酸是否反应及反应速率
【实验记录】
金属
是否反应
反应速率
镁
√
锌
√
铁
√
铜
×
不反应
实验现象(固、液、气)
固体消失,产生大量气泡,溶液无颜色变化
固体逐渐消失,产生大量气泡,溶液无颜色变化
固体逐渐减少,产生少量气泡,溶液由无色变成浅绿色
无现象
快
适中
慢
【实验药品】
金属:镁条、锌粒、铁丝、铜片
酸 : 稀盐酸
问题4.通过已提供实验药品能否根据控制变量分析出四种金属与稀盐酸反应的情况?
问题5.如何改进实验方案设计完成实验探究?
【实验目的】
探究金属镁、锌、铁、铜与稀盐酸的反应
在环境相同时,取形状、大小相同的镁、锌、铁、铜四种金属分别于四只同样的试管中,倒入等浓度、等体积的的稀盐酸,测量相同时间内产生气体的体积
?
Mg + HCl =
Zn + HCl =
Fe + HCl =
小资料:氯气是一种黄绿色有毒的气体,氢气是无色无味的可燃性气体
MgCl2 + H2↑
2
ZnCl2 + H2↑
2
FeCl2 + H2↑
2
小资料:二价亚铁的溶液是浅绿色,
三价的铁的溶液是黄色
单质
单质
化合物
化合物
置换反应
Zn + H2SO4 =
Mg + H2SO4 =
Fe + H2SO4 =
MgSO4 + H2↑
ZnSO4 + H2↑
FeSO4 + H2↑
你有办法吗?
如果有一天碰巧你遇到了这件事,你能用什么方法来揭穿他们吗?
小资料:
黄金是一种具有金黄色光泽的金属、化学性质极不活泼。黄铜的外形与黄金非常相似,所以不法分子常用黄铜(Zn,Cu合金)来冒充黄金。
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A} 微 粒
物 质
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A} 物 质
微 粒
Fe
稀盐酸
小资料:稀盐酸是氯化氢气体的水溶液
Cl-
H+
H2O
Fe
反应物
生成物
Fe2+
Cl-
H2O
H2
FeCl2
溶液
H2
金属与酸反应的微观实质
H+
H+
H+
H+
Cl-
Cl-
Cl-
Cl-
Fe
Fe
Cl-
Cl-
Cl-
Cl-
Fe2+
Fe2+
金属与酸反应的微观实质
H2
H
H
H
H
失1e
H+
H+
H+
H+
Fe
Fe
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Fe2+
Fe2+
H2
金属与酸反应的微观实质
H
H
H
H
金属与酸反应的微观实质
Fe原子失掉两个电子变成Fe2+,
每个H+得到一个电子变成H原子在构成H2
小结:在一个化学反应里有失电子的微粒就有得电子的微粒。
问题5:请同学们分析锌与稀盐酸,镁与稀盐酸反应的微观实质。
Fe + 2HCl = FeCl2 + H2↑
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
元素
反应前
反应后
同种元素反应前后化合价变化情况
Fe
H
Cl
0
+2
+1
+1
0
0
-1
-1
-1
小结:在化学反应中有化合价升高的元素就有化合 价降低的元素。
Fe + 2HCl = FeCl2 + H2↑
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
元素
反应前
反应后
同种元素化合价变化情况
Fe
H
Cl
反应前后微粒种类
0
+2
+1
0
-1
-1
Fe
Fe2+
H+
H2
Cl-
Cl-
总结:化学反应中有电子的得与失就有化合价的降低和升高。
+1
-1
0
Fe + 2HCl = FeCl2 + H2↑
金属与酸反应的定量分析
56
反应前后溶液质量的变化
金属铁中加入一定质量的稀盐酸,反应前后溶液质量的变化,并在直角坐标中表示出变化的趋势?
71
H+
Cl-
Fe2+
Cl-
溶液质量增加
0
溶液质量
时间/t
2
71
总结
1.工业冶炼金属锰的原理是
3MnO2+4Al 3Mn+2Al2O3,该反应属于
A.置换反应 B.化合反应
C.分解反应 D.复分解反应
练习
练习
2.如下图所示:气球中装有一定量的铁粉,试管中装有适量的稀盐酸,拿起气球,使
铁粉进入试管,写出反的化学应方程
式 ,描述实验现象
。
练习
3.根据下图所示,回答下列问题:
(1)写出该反应的化学方程式
(2)该反应中化合价发生变化的元素是
(3)发生变化微粒是
同课章节目录
