鲁教版五四制八年级第三单元物质构成的奥秘习题(含解析)
文档属性
| 名称 | 鲁教版五四制八年级第三单元物质构成的奥秘习题(含解析) |
|
|
| 格式 | zip | ||
| 文件大小 | 262.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-02 00:00:00 | ||
图片预览




文档简介
物质构成的奥秘
一、单选题
下列关于分子、原子的叙述中,不正确的是
A.
分子、原子的质量和体积都很小
B.
由分子构成的物质,分子是保持其化学性质的最小粒子
C.
固体物质很难压缩,因为分子之间没有间隔
D.
原子是化学变化中的最小粒子
根据如图有关信息判断,下列说法中,错误的是
A.
钠元素属于金属元素
B.
在化合物中,钠元素常显价
C.
钠元素的原子核外有11个电子
D.
钠元素的相对原子质量为克
下列关于?Na、两种粒子的判断中,正确的是
核电荷数相同核外电子数相等电子层结构完全相同质量几乎相等化学性质相同比Na稳定
A.
B.
C.
D.
推理是化学学习中常用的思维方法,下列推理正确的是
A.
碱性溶液能使无色酚酞溶液变红,所以使无色酚酞溶液变红的溶液一定呈碱性
B.
氯化钠、硫酸铜等盐中都含有金属元素,所以盐中一定都含有金属元素
C.
离子是带电的粒子,所以带电的粒子一定是离子
D.
置换反应有单质和化合物生成,所以有单质和化合物生成的反应一定是置换反应
下列有关铁的说法错误的是
A.
如图信息,铁的相对原子质量为
B.
生铁和钢的性能差异较大,主要原因是钢的含碳量大于生铁
C.
铁在氧气中燃烧时火星四射,生成黑色固体
D.
铁有良好的导热性,常用来制作炊具
下列各组物质中,组成元素的种类完全相同的是
A.
冰和干冰
B.
金刚石和石墨
C.
石灰石和生石灰
D.
烧碱和纯碱
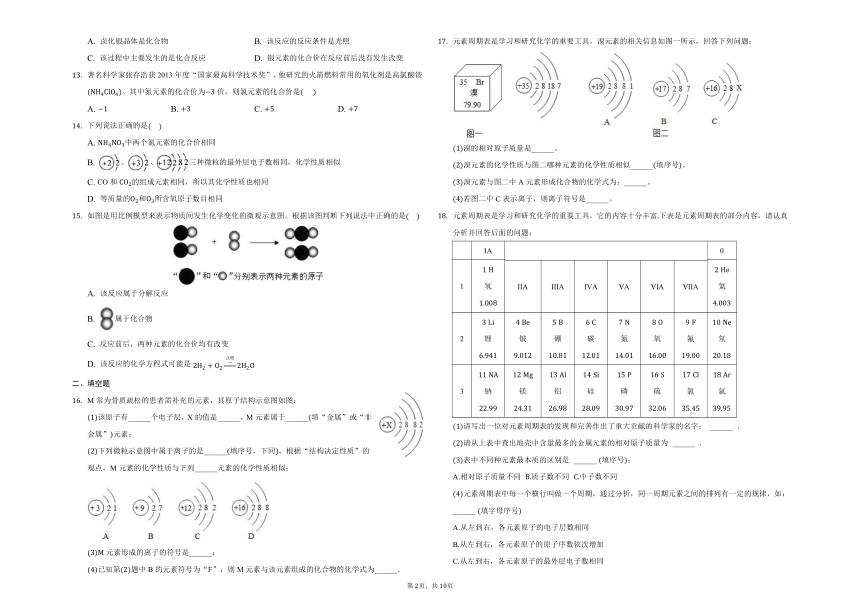
根据如图中提供的信息判断,下列说法正确的是
A.
两种微粒化学性质相似
B.
在化学反应中易形成阴离子
C.
硒原子的相对原子质量为
D.
属于金属元素
根据图中提供的信息判断,下列说法正确的是
A.
属于同种元素
B.
硒元素的相对原子质量为
C.
的化学性质相似
D.
属于离子,其离子符号为
决定元素种类的是原子的
A.
最外层电子数
B.
电子数
C.
中子数
D.
质子数
锂在元素周期表中的信息如图甲所示,图乙表示某粒子的结构示意图。下列说法正确的是
A.
由图甲可知锂的相对原子质量为
B.
锂原子核外有3个电子,金属锂能与反应生成
C.
时,图乙表示氩原子的结构示意图
D.
时,图乙所示原子容易得到一个电子形成
如图是微信热传的“苯宝宝表情包”,苯化学式是一种重要的化工原料,有关本的说法正确的是
A.
苯分子由碳、氢两种元素组成
B.
苯有6个碳原子和6个氢原子构成
C.
苯中碳氢两种元素的质量比为1:1
D.
苯中氢元素的质量分数小于
传统的胶片相机的胶卷中悬浮着的光敏物质是卤化银主要成分是溴化银颗粒,当你拍摄时,光线通过相机的镜头照射到卤化银晶体时,卤化银晶体便转化为黑色金属银颗粒。有关该过程的说法完全正确的是
A.
卤化银晶体是化合物
B.
该反应的反应条件是光照
C.
该过程中主要发生的是化合反应
D.
银元素的化合价在反应前后没有发生改变
著名科学家张存浩获2013年度“国家最高科学技术奖”,他研究的火箭燃料常用的氧化剂是高氯酸铵。其中氮元素的化合价为价,则氯元素的化合价是???
A.
B.
C.
D.
下列说法正确的是
A.
中两个氮元素的化合价相同
B.
、、三种微粒的最外层电子数相同,化学性质相似
C.
CO和的组成元素相同,所以其化学性质也相同
D.
等质量的和所含氧原子数目相同
如图是用比例模型来表示物质间发生化学变化的微观示意图。根据该图判断下列说法中正确的是
A.
该反应属于分解反应
B.
属于化合物
C.
反应前后,两种元素的化合价均有改变
D.
该反应的化学方程式可能是
二、填空题
M常为骨质疏松的患者需补充的元素,其原子结构示意图如图:
该原子有______个电子层,X的值是______,M元素属于______填“金属”或“非金属”元素;
下列微粒示意图中属于离子的是______填序号,下同,根据“结构决定性质”的观点,M元素的化学性质与下列______元素的化学性质相似;
元素形成的离子的符号是______;
已知第题中B的元素符号为“F”,则M元素与该元素组成的化合物的化学式为______.
元素周期表是学习和研究化学的重要工具。溴元素的相关信息如图一所示,回答下列问题:
溴的相对原子质量是______。
溴元素的化学性质与图二哪种元素的化学性质相似______填序号。
溴元素与图二中A元素形成化合物的化学式为:______。
若图二中C表示离子,则离子符号是______。
元素周期表是学习和研究化学的重要工具,它的内容十分丰富下表是元素周期表的部分内容,请认真分析并回答后面的问题:
IA
0
1
氢
氦
IIA
IIIA
IVA
VA
VIA
VIIA
2
锂
铍
硼
碳
氮
氧
氟
氖
3
钠
镁
铝
硅
磷
硫
氯
氩
请写出一位对元素周期表的发现和完善作出了重大贡献的科学家的名字:
______
.
请从上表中查出地壳中含量最多的金属元素的相对原子质量为
______
.
表中不同种元素最本质的区别是
______
填序号:
A.相对原子质量不同
质子数不同
中子数不同
元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如:
______
填字母序号
A.从左到右,各元素原子的电子层数相同
B.从左到右,各元素原子的原子序数依次增加
C.从左到右,各元素原子的最外层电子数相同
元素周期表中,原子序数为12的镁元素的原子在化学反应中易
______
填“得到”或“失去”电子说明元素的化学性质与原子的
______
关系密切.
用化学用语填空:
个乙醇分子________;
个亚铁离子________;
相对分子质量最小的氧化物________;
标出二氧化硅中硅元素的化合价________;
硫酸铵的化学式为________。
用化学符号填空氢原子____;
个氧分子_____;
个钾离子____;
铁元素____;
醋酸________;
碳酸根离子____;
小苏打____;
生石灰____;
熟石灰____;?
碳酸铵中氮元素的化合价____。
按要求用化学符号填空。
个氢原子;______;
标出氧化铁中铁元素的化合价______。
钛合金广泛用于航天、船舶等。2020年11月24日4时30分,在中国文昌航天发射场,用长征五号遥五运载火箭成功发射探月工程嫦娥五号探测器,顺利将探测器送入预定轨道。2020年10月27日中国载人潜水器“奋斗者”号,在西太平洋马里亚纳海沟成功下潜突破1万米,达到10058米,创造了中国载人深潜的新纪录,对我国未来的海洋开发意义重大。
钛合金有很多优良的性能,如
______
选填字母。
A.熔点低
B.机械性能好
C.抗腐蚀性非常好
D.密度小
工业上通常是在高温下用四氯化钛与金属镁发生反应获得金属钛和氯化镁,该反应的化学方程式为
______
,反应后钛元素的化合价
______
填“升高”或“降低”。
钛合金与人体有很好的相容性,因此医疗上可用来制造
______
。
在“宏观”“微观”“符号”三者之间建立联系是化学特有的思维方式,请根据要求填空。
个氮分子:
______用符号表示;
符号的名称
______
;
硝酸中氮元素的化合价为
______
;
最清洁的气体燃料
______用化学式表示。
三、计算题
加碘盐通常在食盐中加碘酸钾。如图是超市销售的一种加碘盐标签上的部分文字说明。请回答下列问题:
碘酸钾中碘元素的化合价为
______
。
碘酸钾的相对分子质量为
______
。
碘酸钾中钾元素、碘元素和氧元素的原子个数比为
______
。
碘酸钾中钾元素、碘元素和氧元素的质量比为
______
。
碘酸钾中碘元素的质量分数是
______
保留到。
每袋该食盐中碘元素的质量为
______
mg。
碘酸钾中含碘
______
mg。
______
mg碘酸钾中含碘127mg。
果糖主要存在于蜂蜜、水果中,具有口感好,甜度高等优点,是天然糖中甜度最高的糖。请回答:
果糖的组成元素是______写元素符号;
果糖分子中各元素原子个数比是______按化学式中元素符号顺序。
答案和解析
1.【答案】C
【解析】解:A、分子、原子的质量和体积都很小,正确;
B、由分子构成的物质,分子是保持其化学性质的最小粒子,正确;
C、分子之间有间隔,错误;
D、原子是化学变化中的最小粒子,正确。
故选:C。
A、分子、原子的质量和体积都很小;
B、由分子构成的物质,分子是保持其化学性质的最小粒子;
C、分子之间有间隔;
D、原子是化学变化中的最小粒子.
本题考查分子、原子的结构,分子、原子之间的关系及在化学变化中能否再分,基础性强.
2.【答案】D
【解析】解:A、钠元素属于金属元素,该选项说法正确;
B、反应中钠原子最外层的1个电子容易失去,因此在化合物中,钠元素常显价,该选项说法正确;
C、钠元素的原子核外有11个电子,该选项说法正确;
D、钠元素的相对原子质量为,单位不是g,该选项说法不正确。
故选:D。
原子中,核电荷数核内质子数核外电子数原子序数;
最外层电子数小于4的,反应中容易失去电子,大于4的反应中容易得到电子。
元素周期表反映了元素之间的内在联系,要注意理解和应用。
3.【答案】C
【解析】解:Na失去一个电子变为,最外层电子数、电子层、核外电子数均发生改变,由于核电荷数质子数,两者均不变;由于原子的质量主要集中在原子核上,故失去一个电子对质量影响很小,质量几乎相等;具有8个电子的稳定结构,故比Na稳定。故正确。
故选:C。
根据原子转化成离子时电子层排布发生的变化进行分析解答本题,钠原子失去一个电子变成钠离子。
本题考查了原子和离子相互转化和原子核外电子排布的知识,解题时要会灵活应用。
4.【答案】A
【解析】解:碱性溶液能使酚酞溶液变红,所以使酚酞变红的溶液一定呈碱性,故正确;
B.盐是由金属离子或铵根离子和酸根离子组成的化合物,盐中不一定都含有金属,如硝酸铵中不含金属元素,属于盐,故错误;
C.离子是带电的粒子,但是带电的粒子不一定是离子,如质子、电子等,故错误;
D.置换反应的反应物和生成物均是一种单质和一种化合物,所以只有生成物是一种单质和一种化合物不一定是置换反应,如一氧化碳和氧化铜的反应等就是这种情况,故错误。
故选:A。
A.根据酸碱指示剂的变色情况考虑;
B.盐是由金属离子或铵根离子和酸根离子组成的化合物;
C.根据带电的微粒来分析;
D.根据置换反应的概念来分析解答。
逻辑推理是一种科学的学习方法,应提倡学生学习这种学习方法,但应注意推理的合理性、正确性。
5.【答案】B
【解析】解:A、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,铁的相对原子质量为,故选项说法正确.
B、生铁和钢的性能差异较大,主要原因是含碳量不同,钢的含碳量低于生铁,故选项说法错误。
C、铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体,故选项说法正确。
D、铁有良好的导热性,常用来制作炊具,故选项说法正确。
故选:B。
A、根据图中元素周期表可以获得的信息:汉字下面的数字表示相对原子质量,进行分析判断。
B、生铁是含碳量为的铁合金,钢是含碳量为的铁合金。
C、根据铁丝在氧气中燃烧的现象进行分析判断.
D、根据金属的物理性质与用途,进行分析判断。
本题难度不大,掌握金属的化学性质、物理性质与用途、生铁和钢的组成成分等是正确解答本题的关键。
6.【答案】B
【解析】解:A、根据冰是由水分子构成的,固态的二氧化碳叫做干冰,故A错误;
B、碳元素就有金钢石、石墨、无定形碳等同素异形体,故正确;
C、根据石灰石的主要成分是碳酸钙;生石灰的主要成分是氧化钙CaO,故C错误;
D、烧碱是NaOH,又名苛性钠,火碱;纯碱,又名苏打,故D错误。
故选:B。
A、根据冰是由水分子构成的,固态的二氧化碳叫做干冰,进行分析解答;
B、同素异形体,是相同元素组成,不同形态的单质.如碳元素就有金钢石、石墨、无定形碳等同素异形体进行分析解答;
C、根据石灰石的主要成分是碳酸钙;生石灰的主要成分是氧化钙CaO,进行分析解答;
D、烧碱是NaOH又名苛性钠,火碱;纯碱;又名苏打进行分析解答.
本题主要考查物质的元素组成,须牢记物质的名称和正常的成分,并能进行分析解题.
7.【答案】A
【解析】解:A、两种微粒化学性质相似,是因为它们最外层电子数相等,该选项说法正确;
B、是钠原子,最外层电子数是1,在化学反应中易失去电子形成阳离子,该选项说法不正确;
C、硒原子的相对原子质量为,单位不是g,该选项说法不正确;
D、是氯元素,氯元素属于非金属元素,该选项说法不正确。
故选:A。
A、最外层电子数相等的元素化学性质相似;
B、一般情况下,最外层电子数小于4的,反应中容易失去电子,大于4的反应中容易得到电子,等于4的,既不容易得到电子,也不容易失去电子;
C、相对原子质量是原子的相对质量;
D、除汞外,金属元素的名称都带金字旁,非金属元素的名称不带金字旁。
元素周期表反映了元素之间的内在联系,要注意理解和应用。
8.【答案】C
【解析】解:元素是具有相同质子数的一类原子的总称,而中,质子数不同,所以不属于同种元素,选项说法错误;
B.根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为,相对原子质量单位是“1”,不是“克”,选项说法错误;
C.由粒子结构示意图可知,的最外层电子数相同,均为8个,均属于稳定结构,化学性质相似,选项说法正确;
D.由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。所以镁离子符号为,选项说法错误。
故选:C。
A.根据元素的概念来分析;
B.根据相对原子质量的单位来分析;
C.根据最外层电子数决定元素的化学性质来分析;
D.根据离子符号的写法来分析。
本题难度不大,灵活运用元素周期表中元素的信息原子序数、元素符号、元素名称、相对原子质量、原子结构示意图的含义是正确解答本题的关键。
9.【答案】D
【解析】解:元素是具有相同核电荷数即核内质子数的一类原子的总称,不同种元素最本质的区别是核电荷数即核内质子数不同,所以决定元素的种类的是核电荷数即核内质子数。
A、决定元素的种类的是核电荷数即核内质子数,不是最外层电子数,故选项错误。
B、决定元素的种类的是核电荷数即核内质子数,不是电子数,故选项错误。
C、决定元素的种类的是核电荷数即核内质子数,不是中子数,故选项错误。
D、决定元素的种类的是核电荷数即核内质子数,故选项正确。
故选:D。
根据元素是具有相同核电荷数即核内质子数的一类原子的总称,据此进行分析解答.
本题很简单,考查学生对元素概念的理解与掌握及灵活应用进行解题的能力.
10.【答案】D
【解析】解:A、由图甲可知锂的相对原子质量为,单位不是g,说法错误;
B、锂原子核外有3个电子,其原子结构示意图为,最外层是一个电子,形成的化合价为,故金属锂与氧气反应生成的氧化锂的化学式为,说法错误;
C、时,图乙表示氯离子的结构示意图,说法错误;
D、时,图乙所示原子容易得到一个电子形成,说法正确;
故选:D。
根据元素周期表中的一个单元格的意义以及原子结构示意图的知识进行分析解答即可。
本题考查的是元素周期表中一个单元格的意义,完成此题,可以依据已有的知识进行。
11.【答案】D
【解析】解:分子是由原子构成的,物质是由元素组成的,苯分子是由碳原子与氢原子构成的,苯是由碳、氢两种元素组成的,故错误;
B.苯是由苯分子构成的,而不是由原子直接构成的,故错误;
C.由苯的化学式可知,其中碳元素和氢元素的质量比为:::1,故错误;
D.苯中氢元素的质量分数为:,故正确。
故选:D。
A.根据分子结构来分析;
B.根据物质的结构来分析;
C.根据化合物中元素质量比的计算方法来分析;
D.根据化合物中元素质量分数的计算方法来分析。
考查了化学式的意义以及有关化学式的计算,难度较小。
12.【答案】B
【解析】
【分析】
本题难度不大,理解题意,掌握化合价的原则、化合反应的概念,混合物与化合物的特征等是正确解答本题的关键。
【解答】
A.卤化银颗粒主要是溴化银AgBr,属于混合物,故选项说法错误;
B.光线通过相机的镜头射到卤化银晶体时,卤化银晶体便转化为黑色金属银颗粒,该反应的反应条件是光照,故选项说法正确;
C.卤化银晶体便转化为黑色金属银颗粒,同时生成溴,该过程中主要发生的是分解反应,故选项说法错误;
D.银元素的化合价在反应前后发生了改变,由价变为0价,故选项说法错误。
故选B。
13.【答案】D
【解析】
【试题解析】
【分析】
本题考查化合价解题的关键是掌握“在化合物中,正负化合价的代数和为零”的原则并能灵活应用解决问题。
【解答】
根据“在化合物中,正负化合价的代数和为零”的原则,其中铵根为价,氧元素为价,设氯的化合价为x,则,解得。故D符合题意。
故选D。
14.【答案】D
【解析】解:A、硝酸铵中铵根显价,氢元素显价,设铵根中氮元素的化合价是x,由原子团中元素的化合价代数和等于原子团的化合价,可得:,则价。
硝酸根显价,氧元素显价,设硝酸根中氮元素的化合价是y,由原子团中元素的化合价代数和等于原子团的化合价,可得:,则价。故选项说法错误。
B、三种微粒依次是氦原子、锂离子和镁原子,氦原子和锂离子化学性质稳定,而镁原子化学性质活泼,故选项说法错误。
C、CO和的组成元素相同,但分子构成不同,所以其化学性质不相同,故选项说法错误。
D、等质量的和所含氧元素的质量相等,氧原子的质量都相同,则含氧原子数目相同,故选项说法正确。
故选:D。
A、根据原子团中元素的化合价代数和等于原子团的化合价,结合硝酸铵的化学式进行判断。
B、根据微粒结构进行分析判断。
C、根据分子的性质进行判断。
D、根据氧元素和氧原子的质量分析。
本题难度不大,掌握原子团中元素的化合价代数和等于原子团的化合价、物质的构成等是正确解答本题的关键。
15.【答案】C
【解析】解:A、由微观反应示意图可知,反应物是两种,生成物是一种,不是分解反应,故A不正确;
B、是由同种元素组成的纯净物,属于单质,故B不正确;
C、由微观反应示意图可知,反应物是一种化合物和一种单质,生成物是一种化合物,所以该反应中一定存在着元素化合价的改变,故正确;
D、由微观反应示意图可知,反应物是一种化合物和一种单质,不符合氢气燃烧的化学反应,故D不正确;
故选:C。
分析表示物质间发生化学变化的微观示意图,一种反应物有2个分子参加该反应,其分子由两个不同的原子构成的,为化合物分子;另一反应物只有1个分子参加该反应,其分子同两个相同的原子构成,为单质的分子;反应后生成了2个生成物的分子,其分子由两个同种原子和一个其它原子共三个原子构成,为化合物分子。
分子由原子构成,构成相同的分子为同种物质的分子,构成不同的分子为不同种物质的分子,同种原子构成的分子为单质分子。
16.【答案】4
?
20
?
金属
?
D
?
C
?
?
【解析】解:由M原子结构示意图可知,其中x表示质子数或核电荷数,核外电子数是20,核外共有四个电子层,在原子中,核电荷数质子数核外电子数,金属元素最外层电子一般少于4个,所以x值为20,可判断该元素为金属元素.
、B、C粒子中质子数电子数,为原子;D粒子中质子数电子数,是阴离子.其中C原子的最外层电子数与M原子的最外层电子数相同,具有相同的化学性质.
由于该元素的核电荷数为20,该原子在发生化学变化时易失掉最外层的两个电子而带两个单位的负电荷,所以该离子的符号为;
原子的最外层电子数为7,在化学反应中易得到1个电子,带1个单位的负电荷,形成化合物中显示价.而M原子的最外层电子数为2,在化学反应中易失去2个电子,带2个单位的正电荷,所以在形成化合物中显示价.根据化合物的化学式的书写原则可写出该化合物的化学式.因为20号元素是Ca元素,所以形成的化合物就是氟化钙.
故答案为:;20;金属;;C;;;
依据该原子结构意图提供的信息分析解答;
依据离子的核外电子数与核内质子数不同判断属于离子的示意图,依据最外层电子数决定元素的化学性质判断与M元素化学性质相似的微粒;
依据M元素形成的离子的得失电子的情况可写出钙离子的符号;
依据两者发生化学变化时得失电子的情况判断两者的化合价,进而可写出该化合物的化学式;
本题题目情境源于生活,符合化学学科源于生活,用于生活的理念,题目定位起点较低,属基础题,但又不乏创新性,如书写氟化钙或氟化镁的化学式,不错的题目.
17.【答案】
?
B
?
KBr
?
【解析】解:由溴元素在元素周期中的信息可知,溴的相对原子质量是;故填:;
元素的化学性质与原子的最外层电子数关系密切,故决定元素化学性质的是最外层电子数;溴原子的最外层电子数为7,则与溴元素的化学性质相似的原子结构示意图中最外层电子数与之相同,即与溴元素的化学性质相似的原子结构示意图中最外层电子数也应为故填:B;
溴元素的最外层有7个电子,在化学反应中易得到一个电子而显价,A元素是钾元素,钾原子的最外层有1个电子,在化学反应中易失去1个电子而显价,二者组成的化合物的化学式为KBr;故填:KBr;
号元素是硫元素,硫原子的最外层有6个电子,在化学反应中易得到2个电子而形成带有2个单位负电荷的硫离子;故填:。
根据元素周期表的信息来分析;
根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,据此进行分析判断;
根据元素的化合价以及化学式的写法来分析;
根据离子符号的写法来分析。
本题难度不大,掌握核外电子在化学变化中的作用、元素的化学性质与它的原子的最外层电子数目的关系是正确解答此类题的关键。
18.【答案】门捷列夫?
?
B?
AB?
失去?
最外层电子数
【解析】解:门捷列夫对元素周期表的发现和完善作出了重大贡献;
地壳中含量最多的金属元素为铝元素;根据元素周期表的内容,查知其相对原子质量为;
根据元素的概念,可知不同种元素最本质的区别是质子数不同;
元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律:从左到右,各元素原子的电子层数相同;从左到右,各元素原子的原子序数依次增加;但各元素原子的最外层电子数不相同,而是逐渐增加;
元素周期表中,原子序数为12的镁元素的原子最外层电子数是2,在化学反应中易失去电子,说明元素的化学性质与原子的最外层电子数关系密切;
故答案为:
门捷列夫;
;
;
;
失去;最外层电子数.
门捷列夫对元素周期表的发现和完善作出了重大贡献;
先明确地壳中含量最多的金属元素,再根据元素周期表的部分内容,查知其相对原子质量;
元素是具有相同核电荷数核内质子数的一类原子的总称;
根据元素周期表分析、归纳同一周期元素之间的排列规律;
由元素周期表中,原子序数为12的镁元素的原子结构示意图可知其最外层电子数,推测其得失电子情况.
了解并掌握元素周期表的特点及其应用、核外电子在化学反应中的作用、地壳中元素的分布与含量等知识,并会总结、分析、归纳.
19.【答案】
【解析】
【分析】
本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目。
【解答】
由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则2个乙醇分子可表示为;
由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字,故3个亚铁离子可表示为;
相对分子质量为构成分子的各原子的相对原子质量之和;氧化物是只含有两种元素且其中一种元素是氧元素的化合物,相对分子质量最小的氧化物是水,其化学式为;
元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以二氧化硅中硅元素的化合价表示为;
硫酸铵中铵根显价,硫酸根显价,故硫酸铵的化学式为。
20.【答案】?
?
?
?
??
?
??
【解析】
【分析】
本题主要考查学生对化学用语的书写和理解能力,题目重点考查了学生对化学符号的书写,考查全面,注重基础,题目难度较小。化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目。
【解答】
原子用元素符号表示,故氢原子可以表示为H;
每个氧分子由2个氧原子构成,表示多个分子在化学式前面加数字,故2个氧分子可以表示为;
每个钾离子带1个单位正电荷,表示多个离子是在离子符号前价数字,故3个钾离子可以表示为;
元素用元素符号表示,故铁元素可以表示为Fe;
醋酸的化学式为,故填;
每个碳酸根离子带2个单位负电荷,故碳酸根离子可以表示为??;
小苏打是碳酸氢钠的俗称,钠元素的化合价是,碳酸氢根的化合价是,根据化合物中元素化合价代数和为零可知,碳酸氢钠中钠原子和碳酸氢根的个数比是1:1,故小苏打的化学式为?;
生石灰是氧化钙的俗称,其化学式为CaO;
熟石灰是氢氧化钙的俗称,其化学式为;
元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,设碳酸铵中氮元素的化合价为x,氢元素的化合价为价,氧元素为价,碳元素为价,化合物中正负化合价的代数和为0,即,解得,表示为。
21.【答案】2H
?
【解析】解:个氢原子就是在氢元素符号的前面加上数字2,故填:2H;
氧化铁中铁元素的化合价为,故填:。
本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目。
本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易。
22.【答案】BCD?
?
降低?
人造骨骼
【解析】解:钛合金的熔点高,不符合题意,故错误;
B.机械性能好,符合题意,故正确;
C.抗腐蚀性非常好,符合题意,故正确;
D.密度小,符合题意,故正确。
故选BCD;
在高温下用四氯化钛与金属镁发生反应获得金属钛和氯化镁,该反应的化学方程式为
;钛的化合价由原来的价变成0价,故反应后钛元素的化合价降低;
钛合金与人体有很好的相容性,且性质稳定,抗腐蚀性强,所以可用来制造人造骨骼;
故答案为:;
;降低;
人造骨骼。
钛和钛合金具有很多优良的性能,如熔点高,硬度小,可塑性好,易于加工,机械性能强等,尤其是钛和钛合金的抗腐蚀性能非常好,据此解答;
用四氯化钛与金属镁发生反应获得金属钛和氯化镁,据此解答;
钛合金与人体有很好的相容性,性质决定用途,据此解答。
本题考查学生合金的性质和用途,化学方程式的书写等知识的掌握,难度系数不大。
23.【答案】
镁离子
【解析】
【分析】
本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目。
24.【答案】?
214?
1:1:3?
39:127:48?
?
10?
254?
214
25.【答案】、H、O;
:2:1。
第2页,共2页
第1页,共1页
一、单选题
下列关于分子、原子的叙述中,不正确的是
A.
分子、原子的质量和体积都很小
B.
由分子构成的物质,分子是保持其化学性质的最小粒子
C.
固体物质很难压缩,因为分子之间没有间隔
D.
原子是化学变化中的最小粒子
根据如图有关信息判断,下列说法中,错误的是
A.
钠元素属于金属元素
B.
在化合物中,钠元素常显价
C.
钠元素的原子核外有11个电子
D.
钠元素的相对原子质量为克
下列关于?Na、两种粒子的判断中,正确的是
核电荷数相同核外电子数相等电子层结构完全相同质量几乎相等化学性质相同比Na稳定
A.
B.
C.
D.
推理是化学学习中常用的思维方法,下列推理正确的是
A.
碱性溶液能使无色酚酞溶液变红,所以使无色酚酞溶液变红的溶液一定呈碱性
B.
氯化钠、硫酸铜等盐中都含有金属元素,所以盐中一定都含有金属元素
C.
离子是带电的粒子,所以带电的粒子一定是离子
D.
置换反应有单质和化合物生成,所以有单质和化合物生成的反应一定是置换反应
下列有关铁的说法错误的是
A.
如图信息,铁的相对原子质量为
B.
生铁和钢的性能差异较大,主要原因是钢的含碳量大于生铁
C.
铁在氧气中燃烧时火星四射,生成黑色固体
D.
铁有良好的导热性,常用来制作炊具
下列各组物质中,组成元素的种类完全相同的是
A.
冰和干冰
B.
金刚石和石墨
C.
石灰石和生石灰
D.
烧碱和纯碱
根据如图中提供的信息判断,下列说法正确的是
A.
两种微粒化学性质相似
B.
在化学反应中易形成阴离子
C.
硒原子的相对原子质量为
D.
属于金属元素
根据图中提供的信息判断,下列说法正确的是
A.
属于同种元素
B.
硒元素的相对原子质量为
C.
的化学性质相似
D.
属于离子,其离子符号为
决定元素种类的是原子的
A.
最外层电子数
B.
电子数
C.
中子数
D.
质子数
锂在元素周期表中的信息如图甲所示,图乙表示某粒子的结构示意图。下列说法正确的是
A.
由图甲可知锂的相对原子质量为
B.
锂原子核外有3个电子,金属锂能与反应生成
C.
时,图乙表示氩原子的结构示意图
D.
时,图乙所示原子容易得到一个电子形成
如图是微信热传的“苯宝宝表情包”,苯化学式是一种重要的化工原料,有关本的说法正确的是
A.
苯分子由碳、氢两种元素组成
B.
苯有6个碳原子和6个氢原子构成
C.
苯中碳氢两种元素的质量比为1:1
D.
苯中氢元素的质量分数小于
传统的胶片相机的胶卷中悬浮着的光敏物质是卤化银主要成分是溴化银颗粒,当你拍摄时,光线通过相机的镜头照射到卤化银晶体时,卤化银晶体便转化为黑色金属银颗粒。有关该过程的说法完全正确的是
A.
卤化银晶体是化合物
B.
该反应的反应条件是光照
C.
该过程中主要发生的是化合反应
D.
银元素的化合价在反应前后没有发生改变
著名科学家张存浩获2013年度“国家最高科学技术奖”,他研究的火箭燃料常用的氧化剂是高氯酸铵。其中氮元素的化合价为价,则氯元素的化合价是???
A.
B.
C.
D.
下列说法正确的是
A.
中两个氮元素的化合价相同
B.
、、三种微粒的最外层电子数相同,化学性质相似
C.
CO和的组成元素相同,所以其化学性质也相同
D.
等质量的和所含氧原子数目相同
如图是用比例模型来表示物质间发生化学变化的微观示意图。根据该图判断下列说法中正确的是
A.
该反应属于分解反应
B.
属于化合物
C.
反应前后,两种元素的化合价均有改变
D.
该反应的化学方程式可能是
二、填空题
M常为骨质疏松的患者需补充的元素,其原子结构示意图如图:
该原子有______个电子层,X的值是______,M元素属于______填“金属”或“非金属”元素;
下列微粒示意图中属于离子的是______填序号,下同,根据“结构决定性质”的观点,M元素的化学性质与下列______元素的化学性质相似;
元素形成的离子的符号是______;
已知第题中B的元素符号为“F”,则M元素与该元素组成的化合物的化学式为______.
元素周期表是学习和研究化学的重要工具。溴元素的相关信息如图一所示,回答下列问题:
溴的相对原子质量是______。
溴元素的化学性质与图二哪种元素的化学性质相似______填序号。
溴元素与图二中A元素形成化合物的化学式为:______。
若图二中C表示离子,则离子符号是______。
元素周期表是学习和研究化学的重要工具,它的内容十分丰富下表是元素周期表的部分内容,请认真分析并回答后面的问题:
IA
0
1
氢
氦
IIA
IIIA
IVA
VA
VIA
VIIA
2
锂
铍
硼
碳
氮
氧
氟
氖
3
钠
镁
铝
硅
磷
硫
氯
氩
请写出一位对元素周期表的发现和完善作出了重大贡献的科学家的名字:
______
.
请从上表中查出地壳中含量最多的金属元素的相对原子质量为
______
.
表中不同种元素最本质的区别是
______
填序号:
A.相对原子质量不同
质子数不同
中子数不同
元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如:
______
填字母序号
A.从左到右,各元素原子的电子层数相同
B.从左到右,各元素原子的原子序数依次增加
C.从左到右,各元素原子的最外层电子数相同
元素周期表中,原子序数为12的镁元素的原子在化学反应中易
______
填“得到”或“失去”电子说明元素的化学性质与原子的
______
关系密切.
用化学用语填空:
个乙醇分子________;
个亚铁离子________;
相对分子质量最小的氧化物________;
标出二氧化硅中硅元素的化合价________;
硫酸铵的化学式为________。
用化学符号填空氢原子____;
个氧分子_____;
个钾离子____;
铁元素____;
醋酸________;
碳酸根离子____;
小苏打____;
生石灰____;
熟石灰____;?
碳酸铵中氮元素的化合价____。
按要求用化学符号填空。
个氢原子;______;
标出氧化铁中铁元素的化合价______。
钛合金广泛用于航天、船舶等。2020年11月24日4时30分,在中国文昌航天发射场,用长征五号遥五运载火箭成功发射探月工程嫦娥五号探测器,顺利将探测器送入预定轨道。2020年10月27日中国载人潜水器“奋斗者”号,在西太平洋马里亚纳海沟成功下潜突破1万米,达到10058米,创造了中国载人深潜的新纪录,对我国未来的海洋开发意义重大。
钛合金有很多优良的性能,如
______
选填字母。
A.熔点低
B.机械性能好
C.抗腐蚀性非常好
D.密度小
工业上通常是在高温下用四氯化钛与金属镁发生反应获得金属钛和氯化镁,该反应的化学方程式为
______
,反应后钛元素的化合价
______
填“升高”或“降低”。
钛合金与人体有很好的相容性,因此医疗上可用来制造
______
。
在“宏观”“微观”“符号”三者之间建立联系是化学特有的思维方式,请根据要求填空。
个氮分子:
______用符号表示;
符号的名称
______
;
硝酸中氮元素的化合价为
______
;
最清洁的气体燃料
______用化学式表示。
三、计算题
加碘盐通常在食盐中加碘酸钾。如图是超市销售的一种加碘盐标签上的部分文字说明。请回答下列问题:
碘酸钾中碘元素的化合价为
______
。
碘酸钾的相对分子质量为
______
。
碘酸钾中钾元素、碘元素和氧元素的原子个数比为
______
。
碘酸钾中钾元素、碘元素和氧元素的质量比为
______
。
碘酸钾中碘元素的质量分数是
______
保留到。
每袋该食盐中碘元素的质量为
______
mg。
碘酸钾中含碘
______
mg。
______
mg碘酸钾中含碘127mg。
果糖主要存在于蜂蜜、水果中,具有口感好,甜度高等优点,是天然糖中甜度最高的糖。请回答:
果糖的组成元素是______写元素符号;
果糖分子中各元素原子个数比是______按化学式中元素符号顺序。
答案和解析
1.【答案】C
【解析】解:A、分子、原子的质量和体积都很小,正确;
B、由分子构成的物质,分子是保持其化学性质的最小粒子,正确;
C、分子之间有间隔,错误;
D、原子是化学变化中的最小粒子,正确。
故选:C。
A、分子、原子的质量和体积都很小;
B、由分子构成的物质,分子是保持其化学性质的最小粒子;
C、分子之间有间隔;
D、原子是化学变化中的最小粒子.
本题考查分子、原子的结构,分子、原子之间的关系及在化学变化中能否再分,基础性强.
2.【答案】D
【解析】解:A、钠元素属于金属元素,该选项说法正确;
B、反应中钠原子最外层的1个电子容易失去,因此在化合物中,钠元素常显价,该选项说法正确;
C、钠元素的原子核外有11个电子,该选项说法正确;
D、钠元素的相对原子质量为,单位不是g,该选项说法不正确。
故选:D。
原子中,核电荷数核内质子数核外电子数原子序数;
最外层电子数小于4的,反应中容易失去电子,大于4的反应中容易得到电子。
元素周期表反映了元素之间的内在联系,要注意理解和应用。
3.【答案】C
【解析】解:Na失去一个电子变为,最外层电子数、电子层、核外电子数均发生改变,由于核电荷数质子数,两者均不变;由于原子的质量主要集中在原子核上,故失去一个电子对质量影响很小,质量几乎相等;具有8个电子的稳定结构,故比Na稳定。故正确。
故选:C。
根据原子转化成离子时电子层排布发生的变化进行分析解答本题,钠原子失去一个电子变成钠离子。
本题考查了原子和离子相互转化和原子核外电子排布的知识,解题时要会灵活应用。
4.【答案】A
【解析】解:碱性溶液能使酚酞溶液变红,所以使酚酞变红的溶液一定呈碱性,故正确;
B.盐是由金属离子或铵根离子和酸根离子组成的化合物,盐中不一定都含有金属,如硝酸铵中不含金属元素,属于盐,故错误;
C.离子是带电的粒子,但是带电的粒子不一定是离子,如质子、电子等,故错误;
D.置换反应的反应物和生成物均是一种单质和一种化合物,所以只有生成物是一种单质和一种化合物不一定是置换反应,如一氧化碳和氧化铜的反应等就是这种情况,故错误。
故选:A。
A.根据酸碱指示剂的变色情况考虑;
B.盐是由金属离子或铵根离子和酸根离子组成的化合物;
C.根据带电的微粒来分析;
D.根据置换反应的概念来分析解答。
逻辑推理是一种科学的学习方法,应提倡学生学习这种学习方法,但应注意推理的合理性、正确性。
5.【答案】B
【解析】解:A、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,铁的相对原子质量为,故选项说法正确.
B、生铁和钢的性能差异较大,主要原因是含碳量不同,钢的含碳量低于生铁,故选项说法错误。
C、铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体,故选项说法正确。
D、铁有良好的导热性,常用来制作炊具,故选项说法正确。
故选:B。
A、根据图中元素周期表可以获得的信息:汉字下面的数字表示相对原子质量,进行分析判断。
B、生铁是含碳量为的铁合金,钢是含碳量为的铁合金。
C、根据铁丝在氧气中燃烧的现象进行分析判断.
D、根据金属的物理性质与用途,进行分析判断。
本题难度不大,掌握金属的化学性质、物理性质与用途、生铁和钢的组成成分等是正确解答本题的关键。
6.【答案】B
【解析】解:A、根据冰是由水分子构成的,固态的二氧化碳叫做干冰,故A错误;
B、碳元素就有金钢石、石墨、无定形碳等同素异形体,故正确;
C、根据石灰石的主要成分是碳酸钙;生石灰的主要成分是氧化钙CaO,故C错误;
D、烧碱是NaOH,又名苛性钠,火碱;纯碱,又名苏打,故D错误。
故选:B。
A、根据冰是由水分子构成的,固态的二氧化碳叫做干冰,进行分析解答;
B、同素异形体,是相同元素组成,不同形态的单质.如碳元素就有金钢石、石墨、无定形碳等同素异形体进行分析解答;
C、根据石灰石的主要成分是碳酸钙;生石灰的主要成分是氧化钙CaO,进行分析解答;
D、烧碱是NaOH又名苛性钠,火碱;纯碱;又名苏打进行分析解答.
本题主要考查物质的元素组成,须牢记物质的名称和正常的成分,并能进行分析解题.
7.【答案】A
【解析】解:A、两种微粒化学性质相似,是因为它们最外层电子数相等,该选项说法正确;
B、是钠原子,最外层电子数是1,在化学反应中易失去电子形成阳离子,该选项说法不正确;
C、硒原子的相对原子质量为,单位不是g,该选项说法不正确;
D、是氯元素,氯元素属于非金属元素,该选项说法不正确。
故选:A。
A、最外层电子数相等的元素化学性质相似;
B、一般情况下,最外层电子数小于4的,反应中容易失去电子,大于4的反应中容易得到电子,等于4的,既不容易得到电子,也不容易失去电子;
C、相对原子质量是原子的相对质量;
D、除汞外,金属元素的名称都带金字旁,非金属元素的名称不带金字旁。
元素周期表反映了元素之间的内在联系,要注意理解和应用。
8.【答案】C
【解析】解:元素是具有相同质子数的一类原子的总称,而中,质子数不同,所以不属于同种元素,选项说法错误;
B.根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为,相对原子质量单位是“1”,不是“克”,选项说法错误;
C.由粒子结构示意图可知,的最外层电子数相同,均为8个,均属于稳定结构,化学性质相似,选项说法正确;
D.由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。所以镁离子符号为,选项说法错误。
故选:C。
A.根据元素的概念来分析;
B.根据相对原子质量的单位来分析;
C.根据最外层电子数决定元素的化学性质来分析;
D.根据离子符号的写法来分析。
本题难度不大,灵活运用元素周期表中元素的信息原子序数、元素符号、元素名称、相对原子质量、原子结构示意图的含义是正确解答本题的关键。
9.【答案】D
【解析】解:元素是具有相同核电荷数即核内质子数的一类原子的总称,不同种元素最本质的区别是核电荷数即核内质子数不同,所以决定元素的种类的是核电荷数即核内质子数。
A、决定元素的种类的是核电荷数即核内质子数,不是最外层电子数,故选项错误。
B、决定元素的种类的是核电荷数即核内质子数,不是电子数,故选项错误。
C、决定元素的种类的是核电荷数即核内质子数,不是中子数,故选项错误。
D、决定元素的种类的是核电荷数即核内质子数,故选项正确。
故选:D。
根据元素是具有相同核电荷数即核内质子数的一类原子的总称,据此进行分析解答.
本题很简单,考查学生对元素概念的理解与掌握及灵活应用进行解题的能力.
10.【答案】D
【解析】解:A、由图甲可知锂的相对原子质量为,单位不是g,说法错误;
B、锂原子核外有3个电子,其原子结构示意图为,最外层是一个电子,形成的化合价为,故金属锂与氧气反应生成的氧化锂的化学式为,说法错误;
C、时,图乙表示氯离子的结构示意图,说法错误;
D、时,图乙所示原子容易得到一个电子形成,说法正确;
故选:D。
根据元素周期表中的一个单元格的意义以及原子结构示意图的知识进行分析解答即可。
本题考查的是元素周期表中一个单元格的意义,完成此题,可以依据已有的知识进行。
11.【答案】D
【解析】解:分子是由原子构成的,物质是由元素组成的,苯分子是由碳原子与氢原子构成的,苯是由碳、氢两种元素组成的,故错误;
B.苯是由苯分子构成的,而不是由原子直接构成的,故错误;
C.由苯的化学式可知,其中碳元素和氢元素的质量比为:::1,故错误;
D.苯中氢元素的质量分数为:,故正确。
故选:D。
A.根据分子结构来分析;
B.根据物质的结构来分析;
C.根据化合物中元素质量比的计算方法来分析;
D.根据化合物中元素质量分数的计算方法来分析。
考查了化学式的意义以及有关化学式的计算,难度较小。
12.【答案】B
【解析】
【分析】
本题难度不大,理解题意,掌握化合价的原则、化合反应的概念,混合物与化合物的特征等是正确解答本题的关键。
【解答】
A.卤化银颗粒主要是溴化银AgBr,属于混合物,故选项说法错误;
B.光线通过相机的镜头射到卤化银晶体时,卤化银晶体便转化为黑色金属银颗粒,该反应的反应条件是光照,故选项说法正确;
C.卤化银晶体便转化为黑色金属银颗粒,同时生成溴,该过程中主要发生的是分解反应,故选项说法错误;
D.银元素的化合价在反应前后发生了改变,由价变为0价,故选项说法错误。
故选B。
13.【答案】D
【解析】
【试题解析】
【分析】
本题考查化合价解题的关键是掌握“在化合物中,正负化合价的代数和为零”的原则并能灵活应用解决问题。
【解答】
根据“在化合物中,正负化合价的代数和为零”的原则,其中铵根为价,氧元素为价,设氯的化合价为x,则,解得。故D符合题意。
故选D。
14.【答案】D
【解析】解:A、硝酸铵中铵根显价,氢元素显价,设铵根中氮元素的化合价是x,由原子团中元素的化合价代数和等于原子团的化合价,可得:,则价。
硝酸根显价,氧元素显价,设硝酸根中氮元素的化合价是y,由原子团中元素的化合价代数和等于原子团的化合价,可得:,则价。故选项说法错误。
B、三种微粒依次是氦原子、锂离子和镁原子,氦原子和锂离子化学性质稳定,而镁原子化学性质活泼,故选项说法错误。
C、CO和的组成元素相同,但分子构成不同,所以其化学性质不相同,故选项说法错误。
D、等质量的和所含氧元素的质量相等,氧原子的质量都相同,则含氧原子数目相同,故选项说法正确。
故选:D。
A、根据原子团中元素的化合价代数和等于原子团的化合价,结合硝酸铵的化学式进行判断。
B、根据微粒结构进行分析判断。
C、根据分子的性质进行判断。
D、根据氧元素和氧原子的质量分析。
本题难度不大,掌握原子团中元素的化合价代数和等于原子团的化合价、物质的构成等是正确解答本题的关键。
15.【答案】C
【解析】解:A、由微观反应示意图可知,反应物是两种,生成物是一种,不是分解反应,故A不正确;
B、是由同种元素组成的纯净物,属于单质,故B不正确;
C、由微观反应示意图可知,反应物是一种化合物和一种单质,生成物是一种化合物,所以该反应中一定存在着元素化合价的改变,故正确;
D、由微观反应示意图可知,反应物是一种化合物和一种单质,不符合氢气燃烧的化学反应,故D不正确;
故选:C。
分析表示物质间发生化学变化的微观示意图,一种反应物有2个分子参加该反应,其分子由两个不同的原子构成的,为化合物分子;另一反应物只有1个分子参加该反应,其分子同两个相同的原子构成,为单质的分子;反应后生成了2个生成物的分子,其分子由两个同种原子和一个其它原子共三个原子构成,为化合物分子。
分子由原子构成,构成相同的分子为同种物质的分子,构成不同的分子为不同种物质的分子,同种原子构成的分子为单质分子。
16.【答案】4
?
20
?
金属
?
D
?
C
?
?
【解析】解:由M原子结构示意图可知,其中x表示质子数或核电荷数,核外电子数是20,核外共有四个电子层,在原子中,核电荷数质子数核外电子数,金属元素最外层电子一般少于4个,所以x值为20,可判断该元素为金属元素.
、B、C粒子中质子数电子数,为原子;D粒子中质子数电子数,是阴离子.其中C原子的最外层电子数与M原子的最外层电子数相同,具有相同的化学性质.
由于该元素的核电荷数为20,该原子在发生化学变化时易失掉最外层的两个电子而带两个单位的负电荷,所以该离子的符号为;
原子的最外层电子数为7,在化学反应中易得到1个电子,带1个单位的负电荷,形成化合物中显示价.而M原子的最外层电子数为2,在化学反应中易失去2个电子,带2个单位的正电荷,所以在形成化合物中显示价.根据化合物的化学式的书写原则可写出该化合物的化学式.因为20号元素是Ca元素,所以形成的化合物就是氟化钙.
故答案为:;20;金属;;C;;;
依据该原子结构意图提供的信息分析解答;
依据离子的核外电子数与核内质子数不同判断属于离子的示意图,依据最外层电子数决定元素的化学性质判断与M元素化学性质相似的微粒;
依据M元素形成的离子的得失电子的情况可写出钙离子的符号;
依据两者发生化学变化时得失电子的情况判断两者的化合价,进而可写出该化合物的化学式;
本题题目情境源于生活,符合化学学科源于生活,用于生活的理念,题目定位起点较低,属基础题,但又不乏创新性,如书写氟化钙或氟化镁的化学式,不错的题目.
17.【答案】
?
B
?
KBr
?
【解析】解:由溴元素在元素周期中的信息可知,溴的相对原子质量是;故填:;
元素的化学性质与原子的最外层电子数关系密切,故决定元素化学性质的是最外层电子数;溴原子的最外层电子数为7,则与溴元素的化学性质相似的原子结构示意图中最外层电子数与之相同,即与溴元素的化学性质相似的原子结构示意图中最外层电子数也应为故填:B;
溴元素的最外层有7个电子,在化学反应中易得到一个电子而显价,A元素是钾元素,钾原子的最外层有1个电子,在化学反应中易失去1个电子而显价,二者组成的化合物的化学式为KBr;故填:KBr;
号元素是硫元素,硫原子的最外层有6个电子,在化学反应中易得到2个电子而形成带有2个单位负电荷的硫离子;故填:。
根据元素周期表的信息来分析;
根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,据此进行分析判断;
根据元素的化合价以及化学式的写法来分析;
根据离子符号的写法来分析。
本题难度不大,掌握核外电子在化学变化中的作用、元素的化学性质与它的原子的最外层电子数目的关系是正确解答此类题的关键。
18.【答案】门捷列夫?
?
B?
AB?
失去?
最外层电子数
【解析】解:门捷列夫对元素周期表的发现和完善作出了重大贡献;
地壳中含量最多的金属元素为铝元素;根据元素周期表的内容,查知其相对原子质量为;
根据元素的概念,可知不同种元素最本质的区别是质子数不同;
元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律:从左到右,各元素原子的电子层数相同;从左到右,各元素原子的原子序数依次增加;但各元素原子的最外层电子数不相同,而是逐渐增加;
元素周期表中,原子序数为12的镁元素的原子最外层电子数是2,在化学反应中易失去电子,说明元素的化学性质与原子的最外层电子数关系密切;
故答案为:
门捷列夫;
;
;
;
失去;最外层电子数.
门捷列夫对元素周期表的发现和完善作出了重大贡献;
先明确地壳中含量最多的金属元素,再根据元素周期表的部分内容,查知其相对原子质量;
元素是具有相同核电荷数核内质子数的一类原子的总称;
根据元素周期表分析、归纳同一周期元素之间的排列规律;
由元素周期表中,原子序数为12的镁元素的原子结构示意图可知其最外层电子数,推测其得失电子情况.
了解并掌握元素周期表的特点及其应用、核外电子在化学反应中的作用、地壳中元素的分布与含量等知识,并会总结、分析、归纳.
19.【答案】
【解析】
【分析】
本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目。
【解答】
由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则2个乙醇分子可表示为;
由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字,故3个亚铁离子可表示为;
相对分子质量为构成分子的各原子的相对原子质量之和;氧化物是只含有两种元素且其中一种元素是氧元素的化合物,相对分子质量最小的氧化物是水,其化学式为;
元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以二氧化硅中硅元素的化合价表示为;
硫酸铵中铵根显价,硫酸根显价,故硫酸铵的化学式为。
20.【答案】?
?
?
?
??
?
??
【解析】
【分析】
本题主要考查学生对化学用语的书写和理解能力,题目重点考查了学生对化学符号的书写,考查全面,注重基础,题目难度较小。化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目。
【解答】
原子用元素符号表示,故氢原子可以表示为H;
每个氧分子由2个氧原子构成,表示多个分子在化学式前面加数字,故2个氧分子可以表示为;
每个钾离子带1个单位正电荷,表示多个离子是在离子符号前价数字,故3个钾离子可以表示为;
元素用元素符号表示,故铁元素可以表示为Fe;
醋酸的化学式为,故填;
每个碳酸根离子带2个单位负电荷,故碳酸根离子可以表示为??;
小苏打是碳酸氢钠的俗称,钠元素的化合价是,碳酸氢根的化合价是,根据化合物中元素化合价代数和为零可知,碳酸氢钠中钠原子和碳酸氢根的个数比是1:1,故小苏打的化学式为?;
生石灰是氧化钙的俗称,其化学式为CaO;
熟石灰是氢氧化钙的俗称,其化学式为;
元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,设碳酸铵中氮元素的化合价为x,氢元素的化合价为价,氧元素为价,碳元素为价,化合物中正负化合价的代数和为0,即,解得,表示为。
21.【答案】2H
?
【解析】解:个氢原子就是在氢元素符号的前面加上数字2,故填:2H;
氧化铁中铁元素的化合价为,故填:。
本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目。
本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易。
22.【答案】BCD?
?
降低?
人造骨骼
【解析】解:钛合金的熔点高,不符合题意,故错误;
B.机械性能好,符合题意,故正确;
C.抗腐蚀性非常好,符合题意,故正确;
D.密度小,符合题意,故正确。
故选BCD;
在高温下用四氯化钛与金属镁发生反应获得金属钛和氯化镁,该反应的化学方程式为
;钛的化合价由原来的价变成0价,故反应后钛元素的化合价降低;
钛合金与人体有很好的相容性,且性质稳定,抗腐蚀性强,所以可用来制造人造骨骼;
故答案为:;
;降低;
人造骨骼。
钛和钛合金具有很多优良的性能,如熔点高,硬度小,可塑性好,易于加工,机械性能强等,尤其是钛和钛合金的抗腐蚀性能非常好,据此解答;
用四氯化钛与金属镁发生反应获得金属钛和氯化镁,据此解答;
钛合金与人体有很好的相容性,性质决定用途,据此解答。
本题考查学生合金的性质和用途,化学方程式的书写等知识的掌握,难度系数不大。
23.【答案】
镁离子
【解析】
【分析】
本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目。
24.【答案】?
214?
1:1:3?
39:127:48?
?
10?
254?
214
25.【答案】、H、O;
:2:1。
第2页,共2页
第1页,共1页
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
