2021年人教版九年级化学第九单元溶液单元卷(含答案)
文档属性
| 名称 | 2021年人教版九年级化学第九单元溶液单元卷(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 257.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-02 23:22:48 | ||
图片预览


文档简介
人教版九年级化学第九单元溶液单元卷
一、选择题
1.下列有关溶液的说法中,错误的是(
)
A.外界条件不改变,溶质不会从溶液中分离出来
B.物质的溶解过程通常会伴随着能量的变化
C.溶液中的溶质以分子或离子的形式均匀分散在溶剂中保持静止不动
D.改变条件能够使饱和溶液与不饱和溶液相互转化
2.小军同学需要快速配制一杯可口的白糖溶液,下列措施不能达到目的的是(
)
A.
用冰水溶解
B.
用热水溶解
C.
把白糖碾成粉末后溶解
D.
溶解时用筷子搅拌
3.欲将某温度下的一杯饱和的硝酸钾溶液变成不饱和溶液,可采取的方法是(
)
A.加热
B.降温
C.加硝酸钾固体
D.加该温度下的硝酸钾饱和溶液
4.用15%的葡萄糖溶液配制150g
5%葡萄糖溶液,下列做法不正确的是( )
A.取用15%的葡萄糖溶液50g
B.使用量筒、烧杯和漏斗等仪器
C.加水100g
D.量水时选用规格100mL的量筒
5.能证实A物质的溶液在20
℃时是饱和溶液的事实是(
)
A.降温到10
℃有A晶体析出
B.蒸发掉10
g水,有A晶体析出
C.加热到30
℃时,再加A物质能继续溶解
D.20
℃时,向上述溶液中加入少量A晶体,溶液质量不变
6.对于多数固体溶质的不饱和溶液,要使之成为饱和溶液的方法有( )
①降低温度;②升高温度;③加同种溶质;④加溶剂;⑤恒温蒸发溶剂
A.①③⑤???
B.②③④???
C.①②③???
D.②③⑤
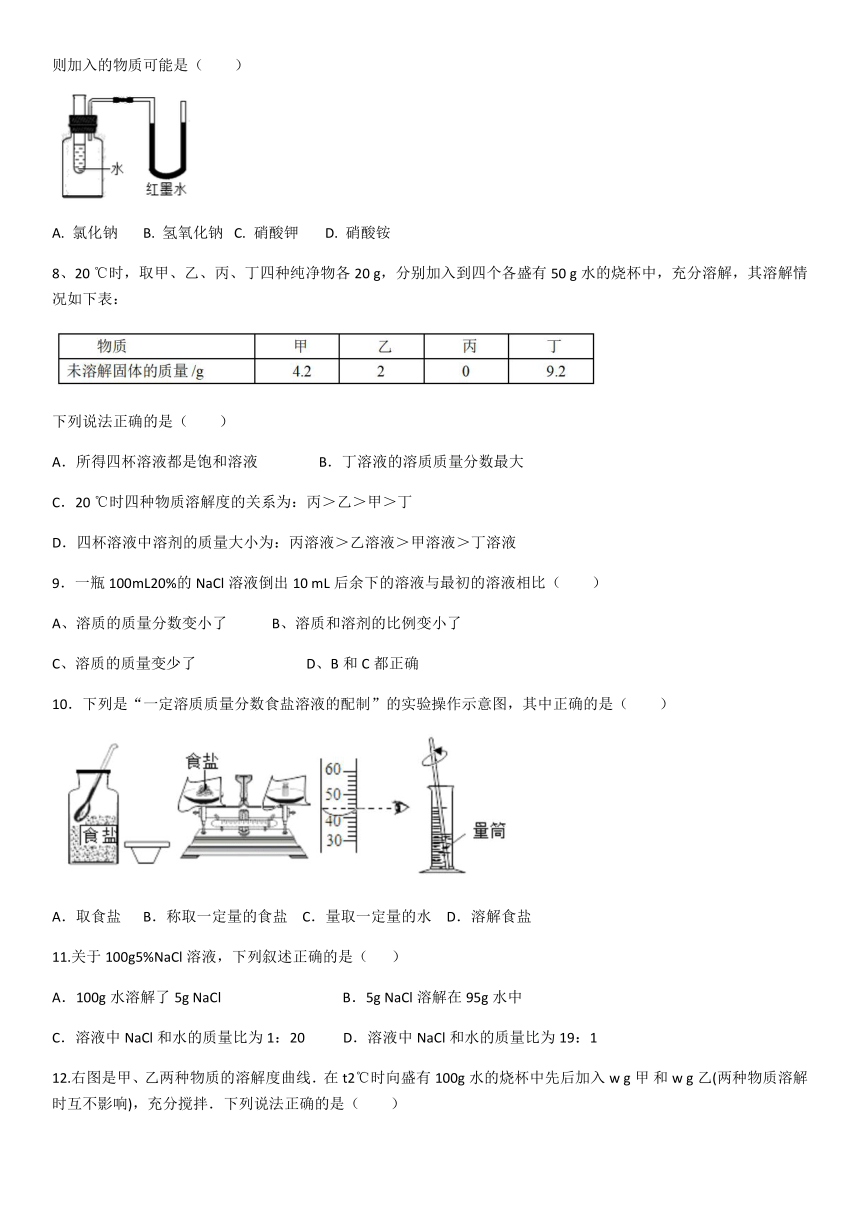
7.如图所示,向试管里的水中加入某种物质后,U形管右边支管的红墨水液面上升,左边支管的红墨水液面下降,则加入的物质可能是(
)
A.
氯化钠
B.
氢氧化钠
C.
硝酸钾
D.
硝酸铵
8、20?℃时,取甲、乙、丙、丁四种纯净物各20?g,分别加入到四个各盛有50
g水的烧杯中,充分溶解,其溶解情况如下表:
下列说法正确的是(
)
A.所得四杯溶液都是饱和溶液
B.丁溶液的溶质质量分数最大
C.20?℃时四种物质溶解度的关系为:丙>乙>甲>丁
D.四杯溶液中溶剂的质量大小为:丙溶液>乙溶液>甲溶液>丁溶液
9.一瓶100mL20%的NaCl溶液倒出10
mL后余下的溶液与最初的溶液相比( )
A、溶质的质量分数变小了????
B、溶质和溶剂的比例变小了?
C、溶质的质量变少了?
D、B和C都正确
10.下列是“一定溶质质量分数食盐溶液的配制”的实验操作示意图,其中正确的是( )
A.取食盐
B.称取一定量的食盐
C.量取一定量的水
D.溶解食盐
11.关于100g5%NaCl溶液,下列叙述正确的是(
)
A.100g水溶解了5g
NaCl
B.5g
NaCl溶解在95g水中
溶液中NaCl和水的质量比为1:20
D.溶液中NaCl和水的质量比为19:1
12.右图是甲、乙两种物质的溶解度曲线.在t2℃时向盛有100g水的烧杯中先后加入w?g甲?和w?g乙(两种物质溶解时互不影响),充分搅拌.下列说法正确的是(
)
A.
甲物质的溶解度随温度升高而减小
B.
温度从t2℃降低到t1℃时,得到甲、乙的饱和溶液
C.
t2℃时,甲物质的溶液为饱和溶液,乙物质的溶液为不饱和溶液
D.
温度从降低t2℃到t1℃时,甲、乙的溶质质量分数相等,得到甲、乙的不饱和溶液
二、填空题
13.在实验室里配制100
g溶质的质量分数为10%的NaCl溶液。
(1)用NaCl固体和蒸馏水配制溶液时,用到的玻璃仪器有
。
(2)用浓溶液配制稀溶液时,计算的依据是
。
(3)下列配制方法可以达到上述实验目的的是
A.
将10
g
NaCl固体与100
g水混合溶解
B.
向50
g溶质的质量分数为20%的NaCl溶液中加入50
g水
14、溶液在生产和科研中具有广泛的用途,与人们的生活密不可分。?
(1)衣服上沾有的油污,可用汽油洗去,是因为汽油能?_________油污;也可用洗涤剂,因为洗涤剂有
功能。?(填“溶解”或“乳化”)
(2)喝了冰镇汽水以后,常常会打嗝。这种现象说明气体的溶解度与?_____
___有关。
(3)某固体物质的溶解度随温度的升高而减小,?20℃时,要使接近饱和的该物质的溶液变为饱和溶液,通常可采用三种方法,它们分别是
、
、
。
15、20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3.请结合图示回答下列问题:
(1)图1中一定为饱和溶液的是 ???
.
(2)图2中甲、乙两溶液中溶质质量分数的大小关系为
????
.
(3)图3中表示乙的溶解度曲线是 ?
;P点表示的含义是 ????
?
?
??????? .
16.根据如图中A、B、C三种物质(均不含结晶水)的溶解度曲线,回答下列问题:
(1)t1
℃时,A、B、C三种物质的溶解度由大到小的顺序是____________。
(2)t2
℃时,向100
g水中加入20
gA物质,充分溶解后,所得溶液是________(填“饱和”或“不饱和”)溶液。
(3)将t3
℃时等质量A、B的饱和溶液分别降温至t2
℃,对所得溶液的叙述正确的是________(填序号)。
①溶质质量:A>B
②溶剂质量:A<B
③溶质质量分数:A=B
④析出溶质质量:A>B
17.请回忆“溶液”相关知识,并回答下列问题:
(1)现有一杯硝酸钾溶液,实验测得其上部密度为ag/cm3,下部密度为bg/cm3,则a与b的关系是a
b(填“<”或“>”或“=”符号).
(2)如图为硝酸钾在水中的溶解度曲线,X、Y两点分别表示硝酸钾的两种溶液(溶剂质量都是100g),据图分析:表示硝酸钾的饱和溶液的是
(选填“X”或“Y”),要使X、Y中的不饱和溶液恰好变为同温度下的饱和溶液,可采取的措施为
.
三、实验题
18.由128克硝酸钾、60克氯化钠组成的混合物投入200g热水溶解,对该溶液进行如图实验(假设实验过程中无损耗)。
(1)两种物质溶解在水中,用玻璃棒搅拌的目的是
。
(2)实验时温度t的范围为
。
(3)操作1用到的实验仪器有
。
A.酒精灯
B.铁架台
C.漏斗
D.玻璃棒
E.蒸发皿
(4)定量述晶体1的组成
。
(5)溶液2为
(填物质名称)的饱和溶液。
(6)关于溶液中NaC1的质量分数:溶液1
溶液2(选填“>“、“<”或“=“)
(7)关于上述实验说法错误的是
。
A.晶体1与晶体2比较,晶体1中KNO3的纯度更高
B.溶液1中KNO3为饱和溶液,NaCl为不饱和溶液
C.溶液1恒温蒸发90g水后,与溶液2的成分相同
D.溶液2将水蒸干就可得到纯净的KNO3固体
四、计算题
19、配制50g溶质质量分数8%的葡萄糖溶液,需要固体葡萄糖的质量是多少?若用溶质质量分数20%的葡萄糖溶液多少克加水也可稀释成50g溶质质量分数8%的溶液。
人教版九年级化学第九单元溶液单元卷
一、选择题
1-5、CAABD
6-10、ABCCB
11-12、BD
二、填空题
13、(1)烧杯、玻璃棒、量筒
(2)稀释前后溶质的质量分数不变
(3)B
14、(1)溶解
乳化
(2)温度
(3)升温、加溶质、恒温蒸发溶剂
15、(1)甲
(2)相等
(3)N
30℃时,M、N的溶解度相等
16、(1)B>C>A
(2)不饱和
(3)②③
17、(1)=
(2)X
加入溶质或恒温蒸发溶剂
三、实验题
18、(1)加快溶解
(2)≥40℃
(3)BCD
(4)32.4g硝酸钾
氯化钠和硝酸钾
>
(7)CD
四、计算题
19、
4g
20g
一、选择题
1.下列有关溶液的说法中,错误的是(
)
A.外界条件不改变,溶质不会从溶液中分离出来
B.物质的溶解过程通常会伴随着能量的变化
C.溶液中的溶质以分子或离子的形式均匀分散在溶剂中保持静止不动
D.改变条件能够使饱和溶液与不饱和溶液相互转化
2.小军同学需要快速配制一杯可口的白糖溶液,下列措施不能达到目的的是(
)
A.
用冰水溶解
B.
用热水溶解
C.
把白糖碾成粉末后溶解
D.
溶解时用筷子搅拌
3.欲将某温度下的一杯饱和的硝酸钾溶液变成不饱和溶液,可采取的方法是(
)
A.加热
B.降温
C.加硝酸钾固体
D.加该温度下的硝酸钾饱和溶液
4.用15%的葡萄糖溶液配制150g
5%葡萄糖溶液,下列做法不正确的是( )
A.取用15%的葡萄糖溶液50g
B.使用量筒、烧杯和漏斗等仪器
C.加水100g
D.量水时选用规格100mL的量筒
5.能证实A物质的溶液在20
℃时是饱和溶液的事实是(
)
A.降温到10
℃有A晶体析出
B.蒸发掉10
g水,有A晶体析出
C.加热到30
℃时,再加A物质能继续溶解
D.20
℃时,向上述溶液中加入少量A晶体,溶液质量不变
6.对于多数固体溶质的不饱和溶液,要使之成为饱和溶液的方法有( )
①降低温度;②升高温度;③加同种溶质;④加溶剂;⑤恒温蒸发溶剂
A.①③⑤???
B.②③④???
C.①②③???
D.②③⑤
7.如图所示,向试管里的水中加入某种物质后,U形管右边支管的红墨水液面上升,左边支管的红墨水液面下降,则加入的物质可能是(
)
A.
氯化钠
B.
氢氧化钠
C.
硝酸钾
D.
硝酸铵
8、20?℃时,取甲、乙、丙、丁四种纯净物各20?g,分别加入到四个各盛有50
g水的烧杯中,充分溶解,其溶解情况如下表:
下列说法正确的是(
)
A.所得四杯溶液都是饱和溶液
B.丁溶液的溶质质量分数最大
C.20?℃时四种物质溶解度的关系为:丙>乙>甲>丁
D.四杯溶液中溶剂的质量大小为:丙溶液>乙溶液>甲溶液>丁溶液
9.一瓶100mL20%的NaCl溶液倒出10
mL后余下的溶液与最初的溶液相比( )
A、溶质的质量分数变小了????
B、溶质和溶剂的比例变小了?
C、溶质的质量变少了?
D、B和C都正确
10.下列是“一定溶质质量分数食盐溶液的配制”的实验操作示意图,其中正确的是( )
A.取食盐
B.称取一定量的食盐
C.量取一定量的水
D.溶解食盐
11.关于100g5%NaCl溶液,下列叙述正确的是(
)
A.100g水溶解了5g
NaCl
B.5g
NaCl溶解在95g水中
溶液中NaCl和水的质量比为1:20
D.溶液中NaCl和水的质量比为19:1
12.右图是甲、乙两种物质的溶解度曲线.在t2℃时向盛有100g水的烧杯中先后加入w?g甲?和w?g乙(两种物质溶解时互不影响),充分搅拌.下列说法正确的是(
)
A.
甲物质的溶解度随温度升高而减小
B.
温度从t2℃降低到t1℃时,得到甲、乙的饱和溶液
C.
t2℃时,甲物质的溶液为饱和溶液,乙物质的溶液为不饱和溶液
D.
温度从降低t2℃到t1℃时,甲、乙的溶质质量分数相等,得到甲、乙的不饱和溶液
二、填空题
13.在实验室里配制100
g溶质的质量分数为10%的NaCl溶液。
(1)用NaCl固体和蒸馏水配制溶液时,用到的玻璃仪器有
。
(2)用浓溶液配制稀溶液时,计算的依据是
。
(3)下列配制方法可以达到上述实验目的的是
A.
将10
g
NaCl固体与100
g水混合溶解
B.
向50
g溶质的质量分数为20%的NaCl溶液中加入50
g水
14、溶液在生产和科研中具有广泛的用途,与人们的生活密不可分。?
(1)衣服上沾有的油污,可用汽油洗去,是因为汽油能?_________油污;也可用洗涤剂,因为洗涤剂有
功能。?(填“溶解”或“乳化”)
(2)喝了冰镇汽水以后,常常会打嗝。这种现象说明气体的溶解度与?_____
___有关。
(3)某固体物质的溶解度随温度的升高而减小,?20℃时,要使接近饱和的该物质的溶液变为饱和溶液,通常可采用三种方法,它们分别是
、
、
。
15、20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3.请结合图示回答下列问题:
(1)图1中一定为饱和溶液的是 ???
.
(2)图2中甲、乙两溶液中溶质质量分数的大小关系为
????
.
(3)图3中表示乙的溶解度曲线是 ?
;P点表示的含义是 ????
?
?
??????? .
16.根据如图中A、B、C三种物质(均不含结晶水)的溶解度曲线,回答下列问题:
(1)t1
℃时,A、B、C三种物质的溶解度由大到小的顺序是____________。
(2)t2
℃时,向100
g水中加入20
gA物质,充分溶解后,所得溶液是________(填“饱和”或“不饱和”)溶液。
(3)将t3
℃时等质量A、B的饱和溶液分别降温至t2
℃,对所得溶液的叙述正确的是________(填序号)。
①溶质质量:A>B
②溶剂质量:A<B
③溶质质量分数:A=B
④析出溶质质量:A>B
17.请回忆“溶液”相关知识,并回答下列问题:
(1)现有一杯硝酸钾溶液,实验测得其上部密度为ag/cm3,下部密度为bg/cm3,则a与b的关系是a
b(填“<”或“>”或“=”符号).
(2)如图为硝酸钾在水中的溶解度曲线,X、Y两点分别表示硝酸钾的两种溶液(溶剂质量都是100g),据图分析:表示硝酸钾的饱和溶液的是
(选填“X”或“Y”),要使X、Y中的不饱和溶液恰好变为同温度下的饱和溶液,可采取的措施为
.
三、实验题
18.由128克硝酸钾、60克氯化钠组成的混合物投入200g热水溶解,对该溶液进行如图实验(假设实验过程中无损耗)。
(1)两种物质溶解在水中,用玻璃棒搅拌的目的是
。
(2)实验时温度t的范围为
。
(3)操作1用到的实验仪器有
。
A.酒精灯
B.铁架台
C.漏斗
D.玻璃棒
E.蒸发皿
(4)定量述晶体1的组成
。
(5)溶液2为
(填物质名称)的饱和溶液。
(6)关于溶液中NaC1的质量分数:溶液1
溶液2(选填“>“、“<”或“=“)
(7)关于上述实验说法错误的是
。
A.晶体1与晶体2比较,晶体1中KNO3的纯度更高
B.溶液1中KNO3为饱和溶液,NaCl为不饱和溶液
C.溶液1恒温蒸发90g水后,与溶液2的成分相同
D.溶液2将水蒸干就可得到纯净的KNO3固体
四、计算题
19、配制50g溶质质量分数8%的葡萄糖溶液,需要固体葡萄糖的质量是多少?若用溶质质量分数20%的葡萄糖溶液多少克加水也可稀释成50g溶质质量分数8%的溶液。
人教版九年级化学第九单元溶液单元卷
一、选择题
1-5、CAABD
6-10、ABCCB
11-12、BD
二、填空题
13、(1)烧杯、玻璃棒、量筒
(2)稀释前后溶质的质量分数不变
(3)B
14、(1)溶解
乳化
(2)温度
(3)升温、加溶质、恒温蒸发溶剂
15、(1)甲
(2)相等
(3)N
30℃时,M、N的溶解度相等
16、(1)B>C>A
(2)不饱和
(3)②③
17、(1)=
(2)X
加入溶质或恒温蒸发溶剂
三、实验题
18、(1)加快溶解
(2)≥40℃
(3)BCD
(4)32.4g硝酸钾
氯化钠和硝酸钾
>
(7)CD
四、计算题
19、
4g
20g
同课章节目录
