【新教材】2020-2021学年人教版(2019)高二化学选择性必修3 2.1 烷烃 课件(22张ppt)
文档属性
| 名称 | 【新教材】2020-2021学年人教版(2019)高二化学选择性必修3 2.1 烷烃 课件(22张ppt) |  | |
| 格式 | ppt | ||
| 文件大小 | 5.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-04 21:46:16 | ||
图片预览






文档简介
第二章 烃
第一节 烷烃
一、烷烃的结构与性质
(一)定义:
碳原子之间都以单键结合,剩余碳原子全部跟氢原子结合,使每个原子的化合价都达到“饱和”的链烃叫饱和链烃,或叫烷烃
(二)通式:CnH2n+2(n≥1)
(三)物理性质:
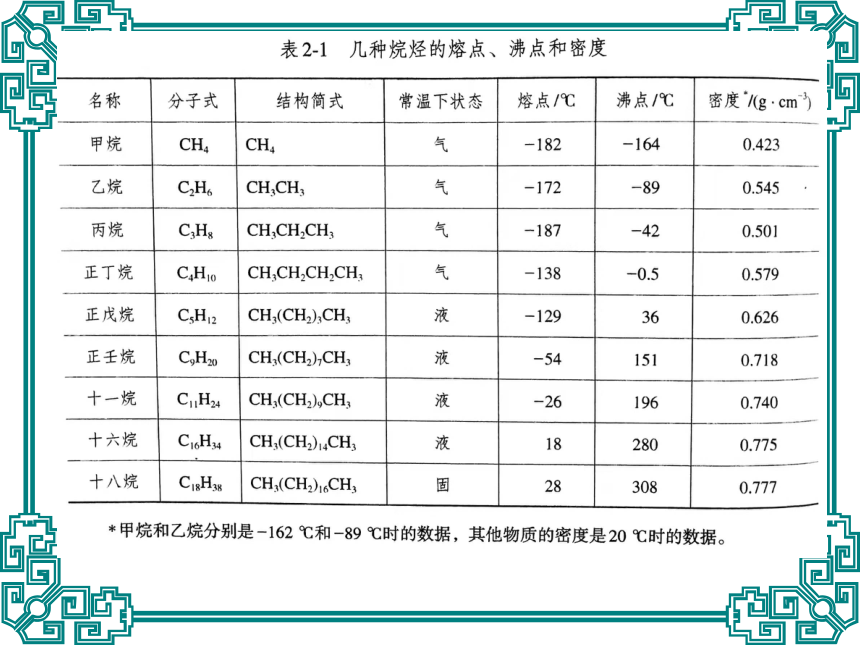
1、随着碳原子数的增多,熔沸点依次升高,密度依次增大(密度小于水);
C1——C4为气态(但新戊烷为气体),
C5——C16为液态,C17以上的为固态
2、溶解性:不溶于水,易溶于有机溶剂。液态烷烃
都可做有机溶剂
3、质量分数:随着碳原子数的增多,氢原子的质量分数逐渐减小,碳原子的质量分数逐渐增大,所以CH4是氢原子质量分数最大的烷烃
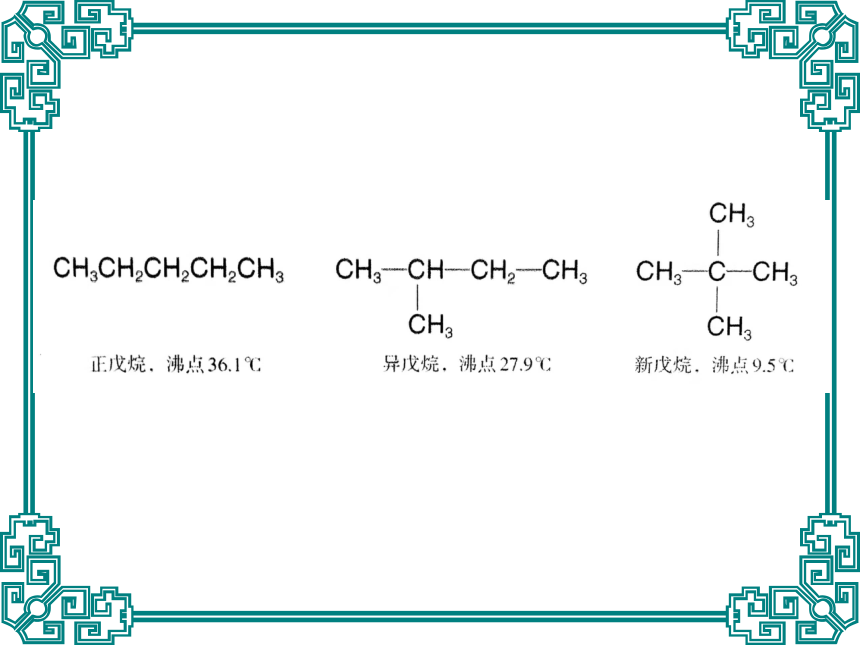
4、同分异构体的熔沸点:支链越多,熔沸点越低
CH4
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
CH3CH2CH2CH2CH3
CH4
C2H6
C3H8
C4H10
C5H12
sp3
sp3
sp3
sp3
sp3
σ键
σ键
σ键
σ键
σ键
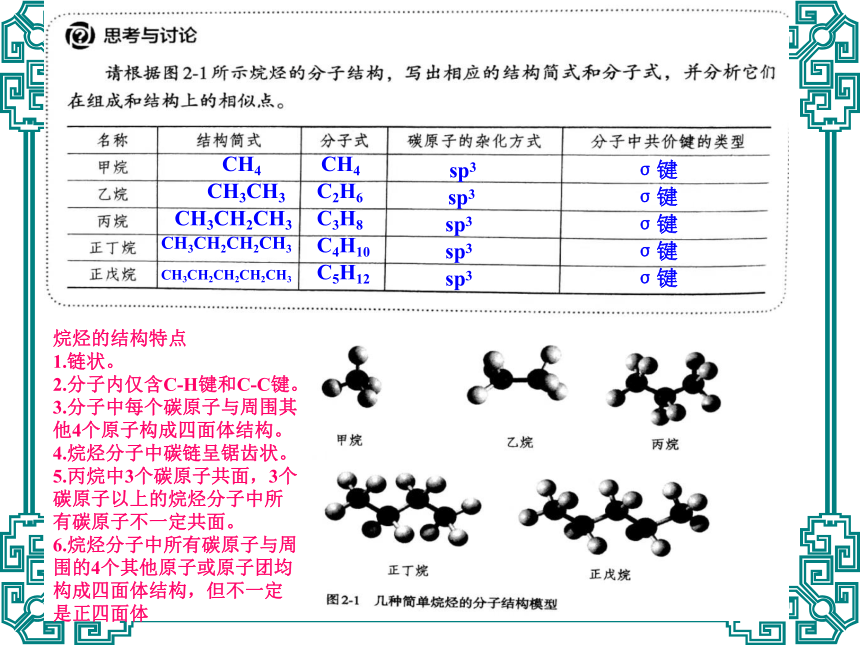
烷烃的结构特点
1.链状。
2.分子内仅含C-H键和C-C键。
3.分子中每个碳原子与周围其他4个原子构成四面体结构。
4.烷烃分子中碳链呈锯齿状。
5.丙烷中3个碳原子共面,3个碳原子以上的烷烃分子中所有碳原子不一定共面。
6.烷烃分子中所有碳原子与周围的4个其他原子或原子团均构成四面体结构,但不一定是正四面体
(四)结构特点:
烷烃的结构与甲烷的相似,其分子中的碳原子都采取sp3杂化,以伸向四面体4个顶点方向的sp3杂化轨道与其他碳原子或氢原子结合,形成σ键。烷烃分子中的共价键全部是单键。既有极性键又有非极性键(甲烷除外)。
(五)烷烃的存在形式
天然气、液化石油气、汽油、柴油、凡士林、石蜡等,它们的主要成分都是烷烃。
(六)代表物——甲烷
1、物理性质:
甲烷是一种无色、无臭的气体,在相同条件下,其密度比空气小,难溶于水
2、化学性质:
甲烷的化学性质比较稳定,常温下不能被酸性高锰酸钾溶液氧化,也不与强酸、强碱及溴的四氯化碳溶液反应。甲烷的主要化学性质表现为能在空气中燃烧(可燃性)和能在光照下与氯气发生取代反应。
(1)氧化反应:
CH4+2O2
CO2+2H2O(淡蓝色火焰)
使用前要验纯,防止爆炸
(2)受热分解:CH4
C+2H2(隔绝空气)
(3)取代反应:CH4+Cl2
CH3Cl+HCl
无色
难溶于水
易燃
不反应
不反应
不反应
取代反应
(4)可能的产物:CH3CH2Cl、CH3CHCl2、CH2ClCH2Cl、CH3CCl3、CH2CICHC12、CH2CICC13、CHCl2CHCl2、CHCl2CCl3、CCl3CCl3
答:(2) 2C8H18+25O2
16CO2+18H2O
(3)CH3CH3+Cl2 CH3CH2Cl+HCI上述反应属于取代反应,
乙烷分子中C—H键断裂,其中的氢原子被氯原子代替,生
成C—Cl键。
通常状况下,很稳定,不与强酸、强碱或
酸性KMnO4反应
1、氧化反应(可燃性):
CnH2n+2+
O2
nCO2+(n+1)H2O
注:当碳含量少时,产生淡蓝色火焰,但随着碳原子数的增多,碳的质量分数逐渐增大,有黑烟产生
(七)化学性质:
①在光照条件下;②与纯卤素反应;
③1mol卤素单质只能取代1molH
④连锁反应,有多种产物(卤代烃和卤化氢气体)
2、取代反应:有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
(1)烷烃取代反应的特点:
(2)举例:
CH3CH2Cl+HCl
CH3CH3+Cl2
3、受热分解:烷烃在隔绝空气的条件下,加热或加催化剂可发生裂化或裂解
通式:一分子烷烃
一分子烷烃+一分子烯烃
举例:
(七)同系物
1、定义:
结构相似,在组成上相差一个或若干个CH2原子团的物质互称为同系物
2、特点:
(3)在分子组成上相差一个或若干个“CH2”原子团,所以同系物一定具有不同的分子式,但相对分子质量的差值一定是14的整数倍。
注:
①判断有机物之间是否互为同系物,首先要看两种物质是否属于同一类物质,然后再看其分子组成
②具有相同通式的有机物除烷烃外都不能确定是否互为同系物
例题:
D
(1)通式相同,结构相似,化学性质相似属于同一类物质;
(2)物理性质一般随碳原子数目的增多而呈规律性变化,如随着碳原子数的增多,同系物的溶沸点逐渐升高,密度逐渐增大 ;
(一)烃基
1、定义:烃分子中去掉1个氢原子所剩余的原子团叫烃基
2、表示方法:-R
3、举例:
烷基:-CnH2n+1,苯基: 或-C6H5,
4、特点:呈电中性,不能单独存在
5、常见烃基:甲基(-CH3)、乙基(-CH2CH3、-C2H5)、
丙基(-CH2CH2CH3正丙基,(CH3)2 CH-异丙基)
丁基(CH3CH2CH2CH2、 、 、 )
二、烷烃的命名
烯基:乙烯基(-CH=CH2)
(二)烷烃的命名
1、习惯命名法:根据分子里所含碳原子数目来命名
(1)碳原子数≤10时,用天干命名:甲、乙、丙、丁、戊、己、庚、辛、壬、癸
(2)碳原子数>10时,用数字命名,
举例:C17H36
十七烷
(3)区分同分异构体时:
①无支链,称“正某烷”
②有一个支链,称“异某烷”
③有两个支链,称“新某烷”
例:CH3CH2CH2CH2CH2CH3
正己烷
异庚烷
例:
例:
新壬烷
2、系统命名法:
(1)选主链、称某烷:“二原则”即“链长,支多”
例:
(2)编位号,定支链:“三原则”即“近、简、小”
例:
3、取代基,写在前,标位置,短线连:
取代基位置用阿拉伯数字标明,取代基个数用汉字标明,阿拉伯数字之间用“,”号相连,数字与汉字之间用“—”相连
4、不同基,简到繁,相同基,合并算:
取代基有多种时,简单的在前,复杂的在后
3-甲基-庚烷
2-甲基-戊烷
2,3,6-三甲基-庚烷
3-甲基-4-乙基-庚烷
2,4-二甲基-6-乙基-辛烷
2,5-二甲基-3-乙基-己烷
谢谢倾听!
第一节 烷烃
一、烷烃的结构与性质
(一)定义:
碳原子之间都以单键结合,剩余碳原子全部跟氢原子结合,使每个原子的化合价都达到“饱和”的链烃叫饱和链烃,或叫烷烃
(二)通式:CnH2n+2(n≥1)
(三)物理性质:
1、随着碳原子数的增多,熔沸点依次升高,密度依次增大(密度小于水);
C1——C4为气态(但新戊烷为气体),
C5——C16为液态,C17以上的为固态
2、溶解性:不溶于水,易溶于有机溶剂。液态烷烃
都可做有机溶剂
3、质量分数:随着碳原子数的增多,氢原子的质量分数逐渐减小,碳原子的质量分数逐渐增大,所以CH4是氢原子质量分数最大的烷烃
4、同分异构体的熔沸点:支链越多,熔沸点越低
CH4
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
CH3CH2CH2CH2CH3
CH4
C2H6
C3H8
C4H10
C5H12
sp3
sp3
sp3
sp3
sp3
σ键
σ键
σ键
σ键
σ键
烷烃的结构特点
1.链状。
2.分子内仅含C-H键和C-C键。
3.分子中每个碳原子与周围其他4个原子构成四面体结构。
4.烷烃分子中碳链呈锯齿状。
5.丙烷中3个碳原子共面,3个碳原子以上的烷烃分子中所有碳原子不一定共面。
6.烷烃分子中所有碳原子与周围的4个其他原子或原子团均构成四面体结构,但不一定是正四面体
(四)结构特点:
烷烃的结构与甲烷的相似,其分子中的碳原子都采取sp3杂化,以伸向四面体4个顶点方向的sp3杂化轨道与其他碳原子或氢原子结合,形成σ键。烷烃分子中的共价键全部是单键。既有极性键又有非极性键(甲烷除外)。
(五)烷烃的存在形式
天然气、液化石油气、汽油、柴油、凡士林、石蜡等,它们的主要成分都是烷烃。
(六)代表物——甲烷
1、物理性质:
甲烷是一种无色、无臭的气体,在相同条件下,其密度比空气小,难溶于水
2、化学性质:
甲烷的化学性质比较稳定,常温下不能被酸性高锰酸钾溶液氧化,也不与强酸、强碱及溴的四氯化碳溶液反应。甲烷的主要化学性质表现为能在空气中燃烧(可燃性)和能在光照下与氯气发生取代反应。
(1)氧化反应:
CH4+2O2
CO2+2H2O(淡蓝色火焰)
使用前要验纯,防止爆炸
(2)受热分解:CH4
C+2H2(隔绝空气)
(3)取代反应:CH4+Cl2
CH3Cl+HCl
无色
难溶于水
易燃
不反应
不反应
不反应
取代反应
(4)可能的产物:CH3CH2Cl、CH3CHCl2、CH2ClCH2Cl、CH3CCl3、CH2CICHC12、CH2CICC13、CHCl2CHCl2、CHCl2CCl3、CCl3CCl3
答:(2) 2C8H18+25O2
16CO2+18H2O
(3)CH3CH3+Cl2 CH3CH2Cl+HCI上述反应属于取代反应,
乙烷分子中C—H键断裂,其中的氢原子被氯原子代替,生
成C—Cl键。
通常状况下,很稳定,不与强酸、强碱或
酸性KMnO4反应
1、氧化反应(可燃性):
CnH2n+2+
O2
nCO2+(n+1)H2O
注:当碳含量少时,产生淡蓝色火焰,但随着碳原子数的增多,碳的质量分数逐渐增大,有黑烟产生
(七)化学性质:
①在光照条件下;②与纯卤素反应;
③1mol卤素单质只能取代1molH
④连锁反应,有多种产物(卤代烃和卤化氢气体)
2、取代反应:有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
(1)烷烃取代反应的特点:
(2)举例:
CH3CH2Cl+HCl
CH3CH3+Cl2
3、受热分解:烷烃在隔绝空气的条件下,加热或加催化剂可发生裂化或裂解
通式:一分子烷烃
一分子烷烃+一分子烯烃
举例:
(七)同系物
1、定义:
结构相似,在组成上相差一个或若干个CH2原子团的物质互称为同系物
2、特点:
(3)在分子组成上相差一个或若干个“CH2”原子团,所以同系物一定具有不同的分子式,但相对分子质量的差值一定是14的整数倍。
注:
①判断有机物之间是否互为同系物,首先要看两种物质是否属于同一类物质,然后再看其分子组成
②具有相同通式的有机物除烷烃外都不能确定是否互为同系物
例题:
D
(1)通式相同,结构相似,化学性质相似属于同一类物质;
(2)物理性质一般随碳原子数目的增多而呈规律性变化,如随着碳原子数的增多,同系物的溶沸点逐渐升高,密度逐渐增大 ;
(一)烃基
1、定义:烃分子中去掉1个氢原子所剩余的原子团叫烃基
2、表示方法:-R
3、举例:
烷基:-CnH2n+1,苯基: 或-C6H5,
4、特点:呈电中性,不能单独存在
5、常见烃基:甲基(-CH3)、乙基(-CH2CH3、-C2H5)、
丙基(-CH2CH2CH3正丙基,(CH3)2 CH-异丙基)
丁基(CH3CH2CH2CH2、 、 、 )
二、烷烃的命名
烯基:乙烯基(-CH=CH2)
(二)烷烃的命名
1、习惯命名法:根据分子里所含碳原子数目来命名
(1)碳原子数≤10时,用天干命名:甲、乙、丙、丁、戊、己、庚、辛、壬、癸
(2)碳原子数>10时,用数字命名,
举例:C17H36
十七烷
(3)区分同分异构体时:
①无支链,称“正某烷”
②有一个支链,称“异某烷”
③有两个支链,称“新某烷”
例:CH3CH2CH2CH2CH2CH3
正己烷
异庚烷
例:
例:
新壬烷
2、系统命名法:
(1)选主链、称某烷:“二原则”即“链长,支多”
例:
(2)编位号,定支链:“三原则”即“近、简、小”
例:
3、取代基,写在前,标位置,短线连:
取代基位置用阿拉伯数字标明,取代基个数用汉字标明,阿拉伯数字之间用“,”号相连,数字与汉字之间用“—”相连
4、不同基,简到繁,相同基,合并算:
取代基有多种时,简单的在前,复杂的在后
3-甲基-庚烷
2-甲基-戊烷
2,3,6-三甲基-庚烷
3-甲基-4-乙基-庚烷
2,4-二甲基-6-乙基-辛烷
2,5-二甲基-3-乙基-己烷
谢谢倾听!
