山东省临清市人教版化学必修1课件:第1章 第2节 化学计量在实验中的应用(2)
文档属性
| 名称 | 山东省临清市人教版化学必修1课件:第1章 第2节 化学计量在实验中的应用(2) |  | |
| 格式 | rar | ||
| 文件大小 | 577.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-01-01 21:18:39 | ||
图片预览





文档简介
(共19张PPT)
第二节 化学计量在实验中的应用
(第二课时)
临清实高 李丽 审核:李宁
500g
问题探究:宏观物质的质量与肉眼看不见的微观粒子之间必然存在着某种联系,如何建立这种联系呢?
500g
宏观物质
微观粒子
物质的量
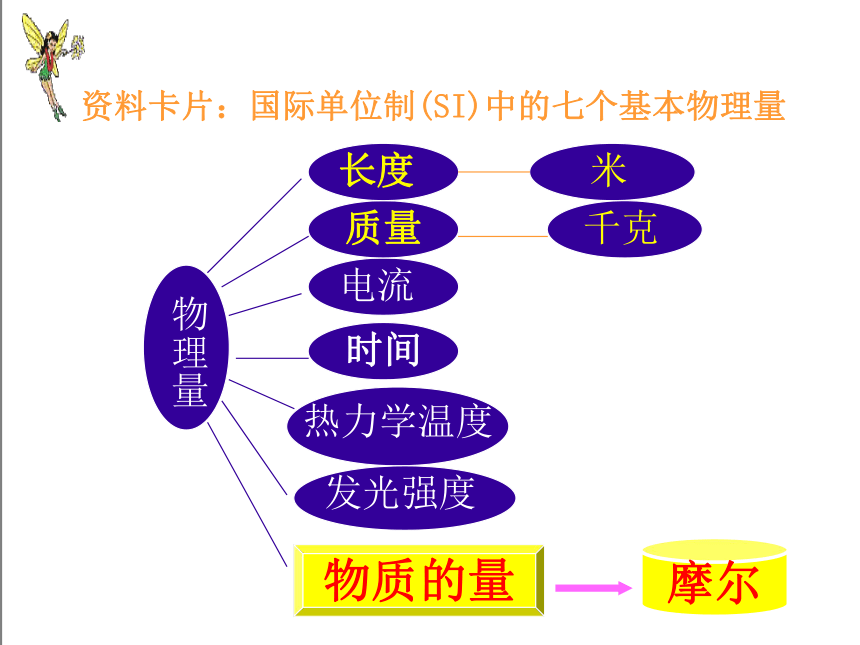
资料卡片:国际单位制(SI)中的七个基本物理量
电流
热力学温度
发光强度
质量
时间
长度
物理量
米
千克
物质的量
摩尔
一、物质的量
定义:
表示含有一定数目粒子的集合体
思考:计量的标准呢?
碳原子
6.02×1023
碳单质
0.012kg 12C
1 mol
得知:1摩尔12C的质量为12g
二、摩尔质量
定义:单位物质的量的物质所具有的质量
符号: M
单位:g mol
表达: M( 12C )=12 g mol
其他物质的摩尔质量?
例如:C ﹢ O2 = CO2
结论:
微粒数目都扩大NA倍之后的质量比为多少
质量比:12 : 32 : 44
任何物质,1摩尔的质量与它的相对质量 数值相同
此时都为1摩尔。质量比还是12 : 32 : 44
已知1摩尔C 质量是12 g
所以1摩尔O2 和1摩尔CO2质量分别是32 g 和 44 g
计算与提高
2molCu的质量是_________,
摩尔质量是_________
5molSO2的质量是_________。
摩尔质量是_________
128 g
320 g
64 g/mol
64 g/mol
根据以上问题能否得出
物质的量( n ),
质量( m )
与摩尔质量( M )三者之间的关系?
思考与交流
小结
÷NA
×NA
÷M
×M
N,n,m之间的相互转化
N
n
m
÷NA
×M
×NA
÷M
联系微观和宏观物质的桥梁
1、 2molFe的质量是_______,1.5molSO2的质量是________。
2 、 24.5克H2SO4的物质的量是___________。
112g
96g
0.25mol
3、 88gCO2中含有多少克氧元素?
64g
4、3.01 ×1022个OH- 的物质的量为( )
质量为 ( )
0.05mol
0.85g
5、48g氧元素中含有( )个O
1.806×1024
6、对于物质的量相同的H2SO4和H3PO4,下列说法不正确的是
A、分子数相同 B、氧原子数相同
C、原子总数相同 D、氢原子数相同
CD
3、NA个氧原子的质量为16g。 ( )
判断
1、摩尔质量就是该物质的的相对分子质量或相对原子质量( )
4、 SO42-的摩尔质量是96 ( )
5、112g的铁粉中含有2 NA 个铁原子( )
不对
不对
对
对
2、 NA个水分子的质量即水的摩尔质量。( )
不对
1、等物质的量的 SO2 和 SO3 相比较,下列结论中错误的是
A、它们的分子数之比为 1 :1
B、它们所含氧原子数目之比为 2 :3
C、它们的质量之比为 1 :1
D、它们所含原子数目之比为 3 :4
√
计算
2、等质量的SO2和SO3中硫原子的物质
的量之比是( )。
5:4
3、下列物质中,物质的量最大的是 ,含分子个数最多的是 ,含原子个数最多的是 ,质量最大的是 。
A、6 g H2
B、0 . 5 mol CO2
C、1 . 204×10 24 个HCl 分子
D、147 g H2SO4
E、92 g C2H5OH(乙醇)
A
A
E
D
[第一课时作业]
1.“物质的量”是指( )
A.物质的质量 B.物质的微观粒子数
C.物质的质量与微观粒子数
D.能把物质的质量同微观粒子数联系起来的一 个基本物理量
2.下列说法中正确地是( )
A.1 mol氧 B.1 molH2SO4 C.1 mol米 D.1 mol面粉
3.在1 molH2O中( )
A.含1molH B.含6.02×1023个氢原子
C.含6.02×1023个水分子 D.含3.01×1023个氧原子
4. 下列说法不正确的是( )
A.Na的摩尔质量为23g
B. Na的摩尔质量为23
C. Na的摩尔质量为23g/mol
D. Na的摩尔质量为23g×10-2kg/mol
5. 下列气体中所含分子数目最多的是( )
A.1gH2 B.10gCO2
C.30gCl2 D.17g NH3
第二节 化学计量在实验中的应用
(第二课时)
临清实高 李丽 审核:李宁
500g
问题探究:宏观物质的质量与肉眼看不见的微观粒子之间必然存在着某种联系,如何建立这种联系呢?
500g
宏观物质
微观粒子
物质的量
资料卡片:国际单位制(SI)中的七个基本物理量
电流
热力学温度
发光强度
质量
时间
长度
物理量
米
千克
物质的量
摩尔
一、物质的量
定义:
表示含有一定数目粒子的集合体
思考:计量的标准呢?
碳原子
6.02×1023
碳单质
0.012kg 12C
1 mol
得知:1摩尔12C的质量为12g
二、摩尔质量
定义:单位物质的量的物质所具有的质量
符号: M
单位:g mol
表达: M( 12C )=12 g mol
其他物质的摩尔质量?
例如:C ﹢ O2 = CO2
结论:
微粒数目都扩大NA倍之后的质量比为多少
质量比:12 : 32 : 44
任何物质,1摩尔的质量与它的相对质量 数值相同
此时都为1摩尔。质量比还是12 : 32 : 44
已知1摩尔C 质量是12 g
所以1摩尔O2 和1摩尔CO2质量分别是32 g 和 44 g
计算与提高
2molCu的质量是_________,
摩尔质量是_________
5molSO2的质量是_________。
摩尔质量是_________
128 g
320 g
64 g/mol
64 g/mol
根据以上问题能否得出
物质的量( n ),
质量( m )
与摩尔质量( M )三者之间的关系?
思考与交流
小结
÷NA
×NA
÷M
×M
N,n,m之间的相互转化
N
n
m
÷NA
×M
×NA
÷M
联系微观和宏观物质的桥梁
1、 2molFe的质量是_______,1.5molSO2的质量是________。
2 、 24.5克H2SO4的物质的量是___________。
112g
96g
0.25mol
3、 88gCO2中含有多少克氧元素?
64g
4、3.01 ×1022个OH- 的物质的量为( )
质量为 ( )
0.05mol
0.85g
5、48g氧元素中含有( )个O
1.806×1024
6、对于物质的量相同的H2SO4和H3PO4,下列说法不正确的是
A、分子数相同 B、氧原子数相同
C、原子总数相同 D、氢原子数相同
CD
3、NA个氧原子的质量为16g。 ( )
判断
1、摩尔质量就是该物质的的相对分子质量或相对原子质量( )
4、 SO42-的摩尔质量是96 ( )
5、112g的铁粉中含有2 NA 个铁原子( )
不对
不对
对
对
2、 NA个水分子的质量即水的摩尔质量。( )
不对
1、等物质的量的 SO2 和 SO3 相比较,下列结论中错误的是
A、它们的分子数之比为 1 :1
B、它们所含氧原子数目之比为 2 :3
C、它们的质量之比为 1 :1
D、它们所含原子数目之比为 3 :4
√
计算
2、等质量的SO2和SO3中硫原子的物质
的量之比是( )。
5:4
3、下列物质中,物质的量最大的是 ,含分子个数最多的是 ,含原子个数最多的是 ,质量最大的是 。
A、6 g H2
B、0 . 5 mol CO2
C、1 . 204×10 24 个HCl 分子
D、147 g H2SO4
E、92 g C2H5OH(乙醇)
A
A
E
D
[第一课时作业]
1.“物质的量”是指( )
A.物质的质量 B.物质的微观粒子数
C.物质的质量与微观粒子数
D.能把物质的质量同微观粒子数联系起来的一 个基本物理量
2.下列说法中正确地是( )
A.1 mol氧 B.1 molH2SO4 C.1 mol米 D.1 mol面粉
3.在1 molH2O中( )
A.含1molH B.含6.02×1023个氢原子
C.含6.02×1023个水分子 D.含3.01×1023个氧原子
4. 下列说法不正确的是( )
A.Na的摩尔质量为23g
B. Na的摩尔质量为23
C. Na的摩尔质量为23g/mol
D. Na的摩尔质量为23g×10-2kg/mol
5. 下列气体中所含分子数目最多的是( )
A.1gH2 B.10gCO2
C.30gCl2 D.17g NH3
