8.3 理想气体状态方程(共22张ppt)
文档属性
| 名称 | 8.3 理想气体状态方程(共22张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 物理 | ||
| 更新时间 | 2021-03-05 00:00:00 | ||
图片预览







文档简介
(共22张PPT)
三大气体实验定律内容是什么?
公式:
pV
=C1
2、査理定律:
公式:
1、玻意耳定律:
3、盖-吕萨克定律:
公式:
由于分子热运动的平均动能与温度有关,分子势能与物体的体积有关,
所以说一定质量的物体内能是由物体的温度和体积来决定。
读一读·思一思
辨一辨·议一议
一、理想气体
认真阅读课本第23页“理想气体”部分。
问题1.什么是理想气体?
答案:在任何温度、任何压强下都遵从气体实验定律的气体叫作理想气体。
问题2.实际气体可视为理想气体的条件是什么?
答案:实际气体在温度不太低(不低于零下几十摄氏度)、压强不太高(不超过大气压的几倍)时,可以当成理想气体。
理想气体具有那些特点呢?
3、理想气体是不存在的,是一种理想模型。
2、理想气体分子本身的大小与分子间的距离相比忽略不计,分子可视为质点.由于分子本身没有体积,即它所占据的空间可以被无限压缩。
解释:气体分子间距离比r0大得多,相互作用的引力和斥力几乎为零(可以忽略不计),所以体积改变时分子势能始终不变为0.
1、一定质量的理想气体的内能仅由温度决定
,与气体的体积无关.
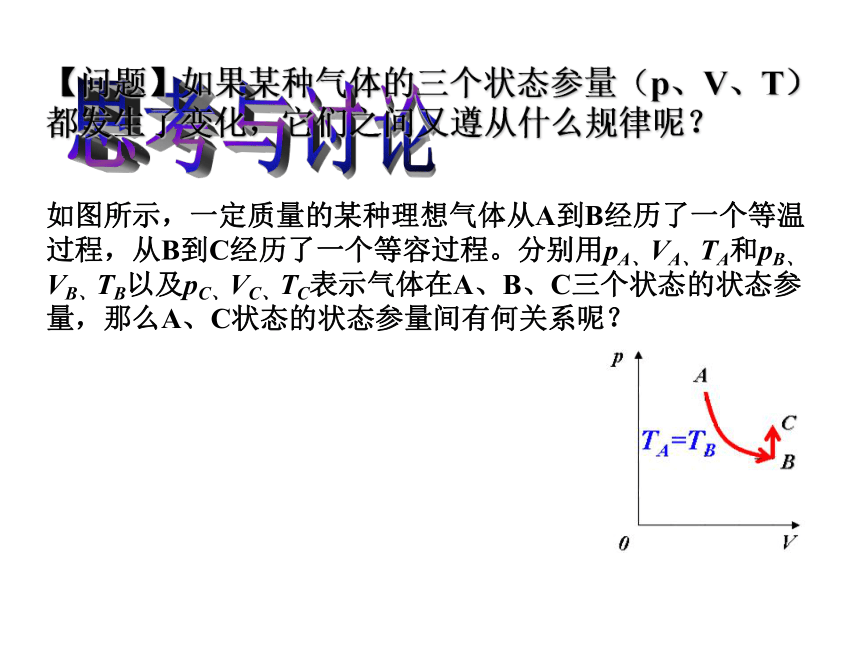
如图所示,一定质量的某种理想气体从A到B经历了一个等温过程,从B到C经历了一个等容过程。分别用pA、VA、TA和pB、VB、TB以及pC、VC、TC表示气体在A、B、C三个状态的状态参量,那么A、C状态的状态参量间有何关系呢?
【问题】如果某种气体的三个状态参量(p、V、T)都发生了变化,它们之间又遵从什么规律呢?
推导过程
从A→B为等温变化:由玻意耳定律
pAVA=pBVB
从B→C为等容变化:由查理定律
VB=VC
状态A下的三个参量PA、VA、TA
状态B下的三个参量PB、VB、TB
状态C下的三个参量PC、VC、TC
TA=TB
可得:
可得:
可得:
因为VB=VC
因为
pAVA=pBVB
又因为
TA=TB
二、理想气体的状态方程
1、内容:一定质量的某种理想气体在从一个状态变化到另一个状态时,尽管p、V、T都可能改变,但是压强跟体积的乘积与热力学温度的比值保持不变。
2、表达式:
或
3、使用条件:
一定质量的某种理想气体.
对公式1的理解
一定质量的某种理想气体在从一个状态变化到另一个状态时,尽管p、V、T都可能改变,但是压强跟体积的乘积与热力学温度的比值保持不变。
注:恒量C由理想气体的质量和种类决定。
例题1、对一定质量的某种理想气体来说,下列说法可能正确的是(
)
A、保持压强和体积不变而改变它的温度。
B、保持压强不变,同时升高温度并减小体积。
C、保持温度不变,同时增加体积并减小压强。
D、保持体积不变,同时增加压强并降低温度。
C
理想气体状态方程与气体实验定律的关系
对公式2的理解
V0
初态
末态
V0
例题3、如图所示,水平放置的气缸内壁光滑,活塞厚度不计,在A、B两处设有限制装置卡销,使活塞只能在A、B之间运动,B左面气缸的容积为V0.A、B之间的容积为0.1V0,开始时活塞在B处,缸内气体的压强为0.9p0(p0为大气压强),温度为297
K,现缓慢加热缸内气体,当温度达到399.3
K时,活塞到达A处.求:
(1)活塞刚离开B处时的温度TB;
(2)缸内气体最后的压强p;
(3)在图乙中画出整个过程的p-V图线.
V0
1、卡销在这起到什么作用?
2、未加热时该气体的三个状态参量是否都已知?
3、刚加热时,活塞会不会立即向右运动?满足什么条件活塞即将向右运动?
6、缓缓移动的过程中,分析活塞受力的情况?
问题导引
V0
4、即将运动时三个状态参量是否都已知,若未知怎么求出?
8、刚到达A端时三个气体状态参量是否都已知,若未知怎么求出?
10、最终温度时三个气体状态参量是否都已知,若未知能否求出?
5、在运动前三个状态参量是否都改变?
7、活塞缓缓移动的过程中三个状态参量是否都改变?
9、到达A端气体的三个状态参量是否还要变化?若变化怎样变化?
(1)活塞即将离开B处时的温度TB;
(2)缸内气体最后的压强p;
(3)在图乙中画出整个过程的p-V图线.
0.1V0
小
结:
一、理想气体:
在任何温度和任何压强下都能严格地遵从气体实验定律的气体
二、理想气体的状态方程
或
注意:恒量C由理想气体的质量和种类决定。
【总结提升】应用理想气体状态方程解题的一般步骤
(1)明确所研究的气体,即一定质量的理想气体.
(2)确定气体在始末状态的参量p1、V1、T1及p2、V2、T2.
(3)由状态方程列式求解.
(4)讨论结果的合理性.
考查内容
相关联的两部分气体
【典例】用销钉固定的活塞把容器
分成A、B两部分,其容积之比VA∶
VB=2∶1,如图所示,起初A中有温度
为127
℃、压强为1.8×105
Pa的空
气,B中有温度为27
℃,压强为1.2×105
Pa的空气,拔去销
钉,使活塞可以无摩擦地移动但不漏气,由于容器壁缓慢导
热,最后都变成室温27
℃,活塞也停住,求最后A、B中气体
的压强.
【规范解答】对A气体,初态:pA=1.8×105
Pa,
TA=(273+127)
K=400
K.
末态:T′A=(273+27)
K=300
K,
由理想气体状态方程
得:
①
对B气体,初态:pB=1.2×105
Pa,TB=300
K.
末态:TB′=(273+27)
K=300
K.
由理想气体状态方程
得:
②
又VA+VB=VA′+VB′
③
VA∶VB=2∶1
④
pA′=pB′
⑤
由①②③④⑤得pA′=pB′=1.3×105
Pa.
答案:均为1.3×105
Pa
三大气体实验定律内容是什么?
公式:
pV
=C1
2、査理定律:
公式:
1、玻意耳定律:
3、盖-吕萨克定律:
公式:
由于分子热运动的平均动能与温度有关,分子势能与物体的体积有关,
所以说一定质量的物体内能是由物体的温度和体积来决定。
读一读·思一思
辨一辨·议一议
一、理想气体
认真阅读课本第23页“理想气体”部分。
问题1.什么是理想气体?
答案:在任何温度、任何压强下都遵从气体实验定律的气体叫作理想气体。
问题2.实际气体可视为理想气体的条件是什么?
答案:实际气体在温度不太低(不低于零下几十摄氏度)、压强不太高(不超过大气压的几倍)时,可以当成理想气体。
理想气体具有那些特点呢?
3、理想气体是不存在的,是一种理想模型。
2、理想气体分子本身的大小与分子间的距离相比忽略不计,分子可视为质点.由于分子本身没有体积,即它所占据的空间可以被无限压缩。
解释:气体分子间距离比r0大得多,相互作用的引力和斥力几乎为零(可以忽略不计),所以体积改变时分子势能始终不变为0.
1、一定质量的理想气体的内能仅由温度决定
,与气体的体积无关.
如图所示,一定质量的某种理想气体从A到B经历了一个等温过程,从B到C经历了一个等容过程。分别用pA、VA、TA和pB、VB、TB以及pC、VC、TC表示气体在A、B、C三个状态的状态参量,那么A、C状态的状态参量间有何关系呢?
【问题】如果某种气体的三个状态参量(p、V、T)都发生了变化,它们之间又遵从什么规律呢?
推导过程
从A→B为等温变化:由玻意耳定律
pAVA=pBVB
从B→C为等容变化:由查理定律
VB=VC
状态A下的三个参量PA、VA、TA
状态B下的三个参量PB、VB、TB
状态C下的三个参量PC、VC、TC
TA=TB
可得:
可得:
可得:
因为VB=VC
因为
pAVA=pBVB
又因为
TA=TB
二、理想气体的状态方程
1、内容:一定质量的某种理想气体在从一个状态变化到另一个状态时,尽管p、V、T都可能改变,但是压强跟体积的乘积与热力学温度的比值保持不变。
2、表达式:
或
3、使用条件:
一定质量的某种理想气体.
对公式1的理解
一定质量的某种理想气体在从一个状态变化到另一个状态时,尽管p、V、T都可能改变,但是压强跟体积的乘积与热力学温度的比值保持不变。
注:恒量C由理想气体的质量和种类决定。
例题1、对一定质量的某种理想气体来说,下列说法可能正确的是(
)
A、保持压强和体积不变而改变它的温度。
B、保持压强不变,同时升高温度并减小体积。
C、保持温度不变,同时增加体积并减小压强。
D、保持体积不变,同时增加压强并降低温度。
C
理想气体状态方程与气体实验定律的关系
对公式2的理解
V0
初态
末态
V0
例题3、如图所示,水平放置的气缸内壁光滑,活塞厚度不计,在A、B两处设有限制装置卡销,使活塞只能在A、B之间运动,B左面气缸的容积为V0.A、B之间的容积为0.1V0,开始时活塞在B处,缸内气体的压强为0.9p0(p0为大气压强),温度为297
K,现缓慢加热缸内气体,当温度达到399.3
K时,活塞到达A处.求:
(1)活塞刚离开B处时的温度TB;
(2)缸内气体最后的压强p;
(3)在图乙中画出整个过程的p-V图线.
V0
1、卡销在这起到什么作用?
2、未加热时该气体的三个状态参量是否都已知?
3、刚加热时,活塞会不会立即向右运动?满足什么条件活塞即将向右运动?
6、缓缓移动的过程中,分析活塞受力的情况?
问题导引
V0
4、即将运动时三个状态参量是否都已知,若未知怎么求出?
8、刚到达A端时三个气体状态参量是否都已知,若未知怎么求出?
10、最终温度时三个气体状态参量是否都已知,若未知能否求出?
5、在运动前三个状态参量是否都改变?
7、活塞缓缓移动的过程中三个状态参量是否都改变?
9、到达A端气体的三个状态参量是否还要变化?若变化怎样变化?
(1)活塞即将离开B处时的温度TB;
(2)缸内气体最后的压强p;
(3)在图乙中画出整个过程的p-V图线.
0.1V0
小
结:
一、理想气体:
在任何温度和任何压强下都能严格地遵从气体实验定律的气体
二、理想气体的状态方程
或
注意:恒量C由理想气体的质量和种类决定。
【总结提升】应用理想气体状态方程解题的一般步骤
(1)明确所研究的气体,即一定质量的理想气体.
(2)确定气体在始末状态的参量p1、V1、T1及p2、V2、T2.
(3)由状态方程列式求解.
(4)讨论结果的合理性.
考查内容
相关联的两部分气体
【典例】用销钉固定的活塞把容器
分成A、B两部分,其容积之比VA∶
VB=2∶1,如图所示,起初A中有温度
为127
℃、压强为1.8×105
Pa的空
气,B中有温度为27
℃,压强为1.2×105
Pa的空气,拔去销
钉,使活塞可以无摩擦地移动但不漏气,由于容器壁缓慢导
热,最后都变成室温27
℃,活塞也停住,求最后A、B中气体
的压强.
【规范解答】对A气体,初态:pA=1.8×105
Pa,
TA=(273+127)
K=400
K.
末态:T′A=(273+27)
K=300
K,
由理想气体状态方程
得:
①
对B气体,初态:pB=1.2×105
Pa,TB=300
K.
末态:TB′=(273+27)
K=300
K.
由理想气体状态方程
得:
②
又VA+VB=VA′+VB′
③
VA∶VB=2∶1
④
pA′=pB′
⑤
由①②③④⑤得pA′=pB′=1.3×105
Pa.
答案:均为1.3×105
Pa
