2020_2021学年人教版(五四学制)化学九年级全册 第二单元 课题1 溶液的形成 课件(19张PPT)
文档属性
| 名称 | 2020_2021学年人教版(五四学制)化学九年级全册 第二单元 课题1 溶液的形成 课件(19张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-05 00:00:00 | ||
图片预览




文档简介
溶液的形成
自制盐汽水(上)
主要原料:
蔗糖、食盐、小苏打、柠檬酸、水
步骤:
1、向约300mL纯净水中分别加入1号袋中食盐、2号袋中蔗糖(两包),振荡。
蔗糖分子扩散
一、溶液形成及实质
钠离子、氯离子扩散
实质:
构成物质的微粒在水分子的作用下,逐渐向水里扩散,
最终均一地分散到水分子中间,形成溶液。
泥+水
油+水
混合物
二、溶液的特征
特征:
、均一性
溶液各部分性质一样
、稳定性
指外界条件不变时,溶质与溶剂不会分离
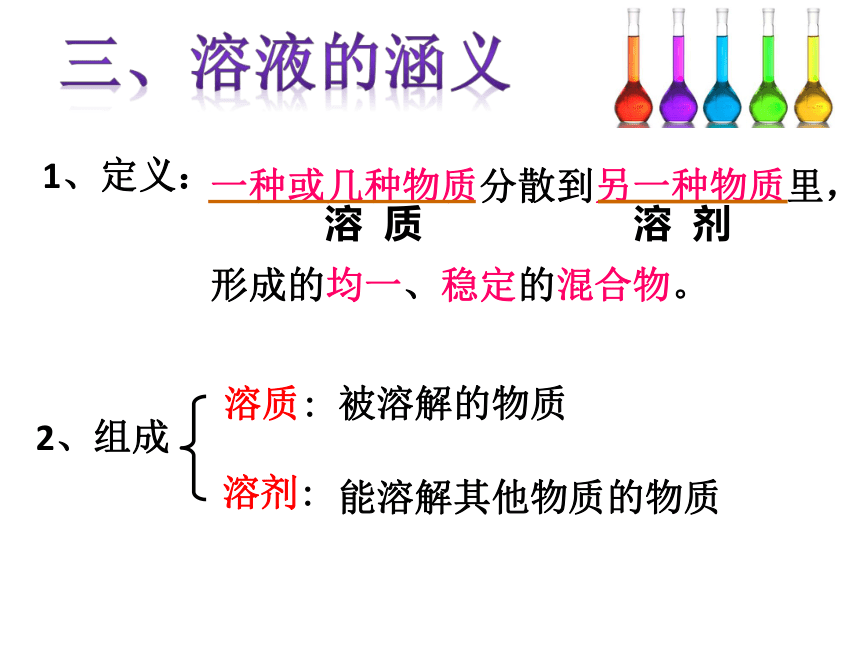
一种或几种物质分散到另一种物质里,形成的均一、稳定的混合物。
1、定义:
被溶解的物质
能溶解其他物质的物质
溶 质
溶 剂
溶质:
溶剂:
2、组成
三、溶液的涵义
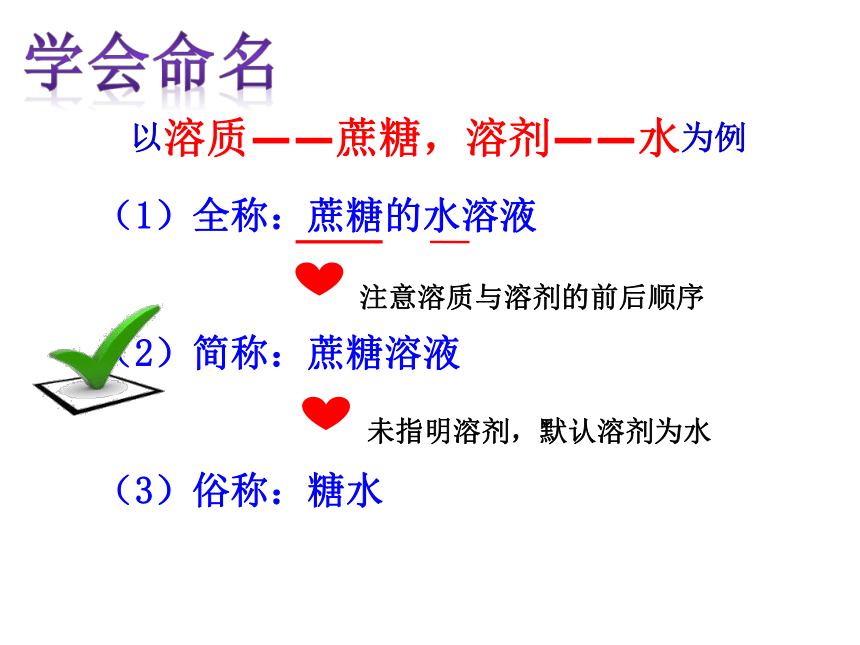
学会命名
以溶质——蔗糖,溶剂——水为例
(1)全称:蔗糖的水溶液
(2)简称:蔗糖溶液
(3)俗称:糖水
注意溶质与溶剂的前后顺序
未指明溶剂,默认溶剂为水
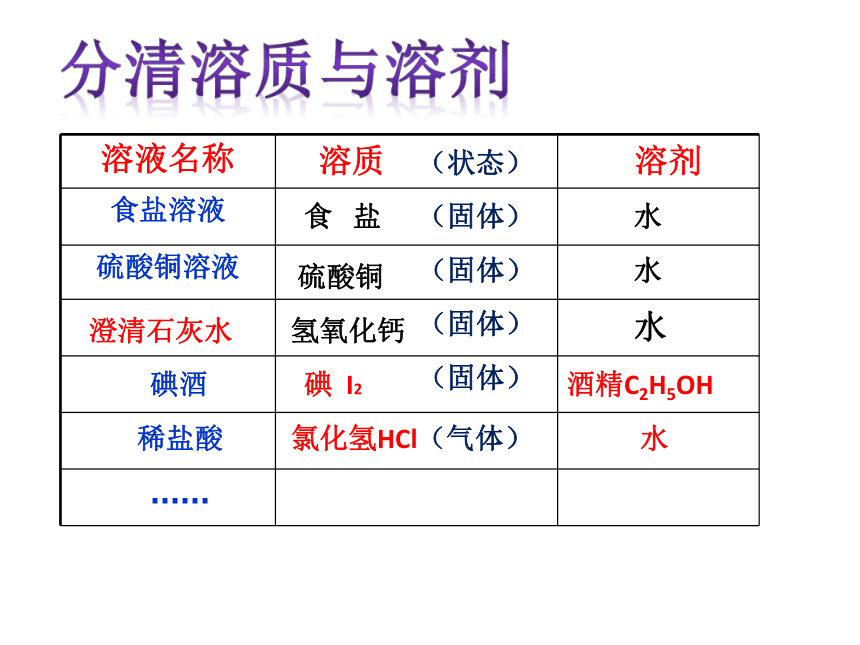
溶液名称
溶质
溶剂
食盐溶液
硫酸铜溶液
碘 I2
酒精C2H5OH
水
氯化氢HCl(气体)
氢氧化钙
水
分清溶质与溶剂
碘酒
稀盐酸
……
硫酸铜
食 盐
氢氧化钙溶液
澄清石灰水
水
水
(状态)
(固体)
(固体)
(固体)
(固体)
实验探究一
液体能做溶质吗?
振荡前现象
振荡后现象
静置后现象
结论
不分层
酒精与水能够互溶
——酒精是否能溶于水
溶液名称
溶质
溶剂
食盐溶液
碘 I2
酒精C2H5OH
水
氯化氢HCl (气体)
碘酒
稀盐酸
食 盐
水
(状态)
(固体)
(固体)
分清溶质与溶剂
75%医用酒精
酒精 (液体)
水
固液混合,固为质;气液混合,气为质;
液液混合,少为质;只要有水,水为剂。
小窍门
90mL汽油+10mL油脂
油脂(液或固体)
汽油
碘 能溶于汽油
KMnO4易溶于水
KMnO4 难溶于汽油
碘几乎不溶水
+
+
+
+
实验探究二
不同的物质在相同的溶剂中溶解性不同
相同的物质在不同的溶剂中溶解性不同
溶质、溶剂的性质决定溶解性
结论
——影响溶解的因素
自制盐汽水(下)
2、加入3号袋中小苏打(碳酸氢钠),4号袋中柠檬酸,立即旋紧瓶盖,静置片刻。
温馨提醒:
冷藏后,
口感更佳!
自制速冷冰袋
1 取240克某固体,装入塑料袋。
?2 取200毫升水,倒入装有该固体的塑料袋中,把袋口封上,手持袋子上下晃动,袋中的液体迅速变得冰凉。
?3 按上述方法,制作多个冰袋,将冰袋和饮料一起放入保温袋中,半小时后,就能喝到冰凉爽口的饮料了。
实验探究三
溶解时的放热和吸热现象
——物质溶解前后液体温度的变化
实验仪器:电子温度计、试管、烧杯等
固体:氯化钠(NaCl) 、硝酸铵(NH4NO3) 、氢氧化钠(NaOH)
(1)测量水的温度
(2)向物质中加水,塞上试管塞,振荡
(3)溶解后,量溶液的温度
具体步骤
实验现象及结论
氯化钠溶解,溶液温度无明显变化
硝酸铵溶解,溶液温度降低
氢氧化钠溶解,溶液温度升高
所以,现在你知道,自制冰袋中放的固体是什么了吗?
物质在溶解过程中有热量的变化,有些物质溶解时会出现吸热现象,有些物质在溶解时会出现放热现象。
生活应用
溶液
1、烧杯中有100毫升NaCl溶液,请比较A处和B处密度的大小( )
A:?A > ?B B: ?A < ?B
C:?A= ?B D: 不能确定
C
课堂反馈
2、下列叙述正确的是( )
A.任何均一、稳定的液体都是溶液
B.溶液都是无色的
C.溶液中只能含一种溶质
D.如果温度不变,溶剂也不蒸发,溶质是不会从溶液中析出来的
D
3、如图若液体是水、固体为氢氧化钠,气球如何变化?为什么?
气球胀大。因为,氢氧化钠溶解时放热,气体膨胀,压强增大。所以,气球胀大。
课堂反馈
学完本课题你应该知道
自制盐汽水(上)
主要原料:
蔗糖、食盐、小苏打、柠檬酸、水
步骤:
1、向约300mL纯净水中分别加入1号袋中食盐、2号袋中蔗糖(两包),振荡。
蔗糖分子扩散
一、溶液形成及实质
钠离子、氯离子扩散
实质:
构成物质的微粒在水分子的作用下,逐渐向水里扩散,
最终均一地分散到水分子中间,形成溶液。
泥+水
油+水
混合物
二、溶液的特征
特征:
、均一性
溶液各部分性质一样
、稳定性
指外界条件不变时,溶质与溶剂不会分离
一种或几种物质分散到另一种物质里,形成的均一、稳定的混合物。
1、定义:
被溶解的物质
能溶解其他物质的物质
溶 质
溶 剂
溶质:
溶剂:
2、组成
三、溶液的涵义
学会命名
以溶质——蔗糖,溶剂——水为例
(1)全称:蔗糖的水溶液
(2)简称:蔗糖溶液
(3)俗称:糖水
注意溶质与溶剂的前后顺序
未指明溶剂,默认溶剂为水
溶液名称
溶质
溶剂
食盐溶液
硫酸铜溶液
碘 I2
酒精C2H5OH
水
氯化氢HCl(气体)
氢氧化钙
水
分清溶质与溶剂
碘酒
稀盐酸
……
硫酸铜
食 盐
氢氧化钙溶液
澄清石灰水
水
水
(状态)
(固体)
(固体)
(固体)
(固体)
实验探究一
液体能做溶质吗?
振荡前现象
振荡后现象
静置后现象
结论
不分层
酒精与水能够互溶
——酒精是否能溶于水
溶液名称
溶质
溶剂
食盐溶液
碘 I2
酒精C2H5OH
水
氯化氢HCl (气体)
碘酒
稀盐酸
食 盐
水
(状态)
(固体)
(固体)
分清溶质与溶剂
75%医用酒精
酒精 (液体)
水
固液混合,固为质;气液混合,气为质;
液液混合,少为质;只要有水,水为剂。
小窍门
90mL汽油+10mL油脂
油脂(液或固体)
汽油
碘 能溶于汽油
KMnO4易溶于水
KMnO4 难溶于汽油
碘几乎不溶水
+
+
+
+
实验探究二
不同的物质在相同的溶剂中溶解性不同
相同的物质在不同的溶剂中溶解性不同
溶质、溶剂的性质决定溶解性
结论
——影响溶解的因素
自制盐汽水(下)
2、加入3号袋中小苏打(碳酸氢钠),4号袋中柠檬酸,立即旋紧瓶盖,静置片刻。
温馨提醒:
冷藏后,
口感更佳!
自制速冷冰袋
1 取240克某固体,装入塑料袋。
?2 取200毫升水,倒入装有该固体的塑料袋中,把袋口封上,手持袋子上下晃动,袋中的液体迅速变得冰凉。
?3 按上述方法,制作多个冰袋,将冰袋和饮料一起放入保温袋中,半小时后,就能喝到冰凉爽口的饮料了。
实验探究三
溶解时的放热和吸热现象
——物质溶解前后液体温度的变化
实验仪器:电子温度计、试管、烧杯等
固体:氯化钠(NaCl) 、硝酸铵(NH4NO3) 、氢氧化钠(NaOH)
(1)测量水的温度
(2)向物质中加水,塞上试管塞,振荡
(3)溶解后,量溶液的温度
具体步骤
实验现象及结论
氯化钠溶解,溶液温度无明显变化
硝酸铵溶解,溶液温度降低
氢氧化钠溶解,溶液温度升高
所以,现在你知道,自制冰袋中放的固体是什么了吗?
物质在溶解过程中有热量的变化,有些物质溶解时会出现吸热现象,有些物质在溶解时会出现放热现象。
生活应用
溶液
1、烧杯中有100毫升NaCl溶液,请比较A处和B处密度的大小( )
A:?A > ?B B: ?A < ?B
C:?A= ?B D: 不能确定
C
课堂反馈
2、下列叙述正确的是( )
A.任何均一、稳定的液体都是溶液
B.溶液都是无色的
C.溶液中只能含一种溶质
D.如果温度不变,溶剂也不蒸发,溶质是不会从溶液中析出来的
D
3、如图若液体是水、固体为氢氧化钠,气球如何变化?为什么?
气球胀大。因为,氢氧化钠溶解时放热,气体膨胀,压强增大。所以,气球胀大。
课堂反馈
学完本课题你应该知道
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
