2020——2021学年度九年级化学下册 第九单元 溶液 综合训练题
文档属性
| 名称 | 2020——2021学年度九年级化学下册 第九单元 溶液 综合训练题 |
|
|
| 格式 | docx | ||
| 文件大小 | 152.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-07 00:00:00 | ||
图片预览



文档简介
2020——2021学年度九年级化学下册
第九单元
溶液
综合训练题
一、选择题
1.逻辑推理是化学学习常用的思维方法,下列推理正确的是()
A.化合物是含有不同种元素的纯净物,所以含有不同种元素的纯净物一定是化合物
B.在化合物中金属元素显正价,所以非金属元素一定显负价
C.置换反应一定有单质生成,所以有单质生成的反应一定是置换反应
D.溶液具有均一性和稳定性,所以具有均一性和稳定性的液体一定是溶液
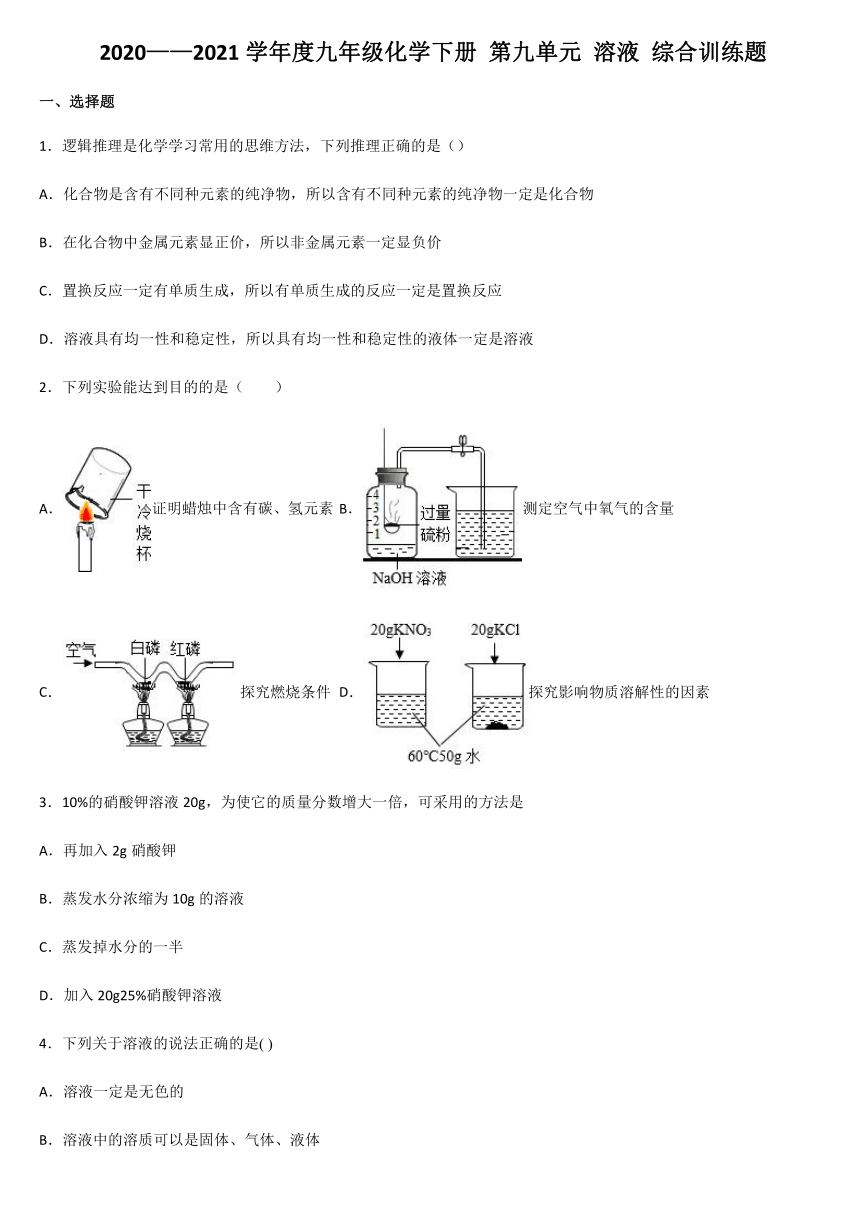
2.下列实验能达到目的的是( )
A.证明蜡烛中含有碳、氢元素
B.测定空气中氧气的含量
C.探究燃烧条件
D.探究影响物质溶解性的因素
3.10%的硝酸钾溶液20g,为使它的质量分数增大一倍,可采用的方法是
A.再加入2g硝酸钾
B.蒸发水分浓缩为10g的溶液
C.蒸发掉水分的一半
D.加入20g25%硝酸钾溶液
4.下列关于溶液的说法正确的是(
)
A.溶液一定是无色的
B.溶液中的溶质可以是固体、气体、液体
C.均一、稳定的液体一定是溶液
D.任何不饱和溶液降温后都会变成饱和溶液
5.提高科学核心价值观,学会从化学的角度分析问题。下列分析不正确的是()
A.液氧用于火箭发射——氧气具有可燃性
B.洗涤剂清洗油污——洗涤剂有乳化功能
C.氢能源未广泛应用——氢气制取成本高、贮存困难
D.氮气充入食品包装袋中防腐——氮气化学性质不活泼
6.下列关于水和溶液的说法不正确的是(
)
A.蔗糖溶于水可形成溶液
B.溶液由溶质和溶剂组成,所以溶液一定是混合物
C.将10%的KNO3溶液倒出一半,剩余溶液中溶质的质量分数为5%
D.改变条件,能够使饱和溶液与不饱和溶液相互转化
7.按如图所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液面升高。若液体X是水,则固体y可能是(
)
A.氢氧化钠
B.氯化钠
C.硝酸铵
D.二氧化锰
8.甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是()
A.甲的溶解度比乙大
B.20°C时,甲、乙两种溶液的溶质质量分数相等
C.40°C时,可以配制溶质质量分数为38%的甲溶液
D.40°C时,甲和乙各30g分别加入100g水中,充分溶解后同时等速降温,则乙溶液中先有固体结晶析出
9.工业纯碱中常含有少量的氯化钠。某学习小组对其组成展开探究。现取24
g纯碱样品,加入100
g水使其完全溶解,再加入96
g过量的氯化钙溶液,完全反应后,过滤、洗涤、干燥得沉淀20
g.通过已知数据,不能求出的量是( )
A.反应后溶液的总质量
B.参加反应的氯化钙的质量
C.样品中碳酸钠的质量分数
D.氯化钙溶液中溶质的质量分数
10.在一定温度下,某固态溶质(不含结晶水)的水溶液甲,经历如下变化:,下列结论正确的是( )
A.溶液甲可能是饱和溶液
B.溶液乙一定是不饱和溶液
C.溶液乙和溶液丙中的溶质质量分数可能相等
D.溶液丙若再蒸发5?g水,析出的晶体质量一定等于2?g
11.t℃时,将某硝酸钾溶液第一次蒸发掉l
0g水,冷却至原温度析出晶体1g;第二次蒸发掉10g水,冷却至原温度析出晶体3g;第三次再蒸发掉10g水,冷却至原温度析出晶体应为( )
A.等于3g
B.大于3g
C.等于lg
D.小于或等于lg
12.下列图像能正确反映对应变化关系的是
A.A
B.B
C.C
D.D
13.不能正确反映对应变化关系的图像是(
)
①一定质量稀盐酸中加入某物质②澄清石灰水中通入CO2
③加热氯酸钾制取氧气④敞口放置浓硫酸
A.①图中横坐标既可以表示加入金属铁的质量,也可以表示加入碳酸钙的质量
B.②图中纵坐标既可以溶质质量,又可表示溶液导电性
C.③图中横坐标既可以表示反应时间,也可以表示加入二氧化锰质量
D.④图中纵坐标既可以表示溶剂质量,又可表示溶质质量分数
14.t℃时,某物质的溶解度为
S
克/100
克水,其饱和溶液的质量分数为
C%,则
S
与C
的数值关系为( )
A.S>C
B.S=C
C.S<C
D.无法判断
二、填空题
15.如图是某同学在学完有关溶解度的相关知识后所做的实验,请回答下列问题:
(1)A、B、C、D四个烧杯中的溶液一定属于甲物质的饱和溶液的是________________(填字母),C中甲物质的溶质质量分数为________________(填表达式)。
(2)40℃时甲物质的溶解度________________(填“>”“<”或“=”)乙物质的溶解度。
(3)若两种物质的溶解度均随温度的升高而增大,则使D中固体溶解的方法为________________。
16.根据如图回答下列问题:
(1)P
点表示______;
(2)t2℃时,三种物质溶解度大小的关系是______(用“>”、“=”或“<”连接);
(3)t2℃时,将55克a物质放入
100克水中充分搅拌,得到溶液的质量为______克;
(4)若a中含有少量的c,可以通过______的方法得到纯净a。
17.已知某物质在不同温度下的溶解度数据如下表所示:
温度(℃)
0
20
40
60
80
溶解度(克)
12.6
15.3
20.0
25.0
38.2
如果要配制该物质溶质质量分数为20%的饱和溶液200克,需要水
克,此时溶液的温度应为
℃。
18.实验室配制溶质的质量分数为10%的NaCl溶液,经检验所得溶液的溶质质量分数偏小。请从实验操作上分析造成误差的两点原因。____________________、__________________
19.有Zn
、Cu、Ag、Zn(NO3)2溶液、Cu(NO3)2溶液、AgNO3溶液几种物质。
(1)Zn(NO3)2溶液中的溶剂是_____;饱和Cu(NO3)2溶液中_____溶解氯化钠(“能”、“不能”)。
(2)若要用上面药品验证Zn
、Cu、Ag三种金属的金属活泼性强弱,所用药品可选择Zn(NO3)2溶液、AgNO3溶液及_____,也可以选择Zn
、Ag及_____溶液。
(3)向含有AgNO3和Cu(NO3)2两种物质的混合物溶液中加入一定量的Zn,充分反应后过滤、洗涤,分别得到滤渣和滤液。若向滤渣中加入稀盐酸有气泡产生,则滤液中的溶质是_____;若向滤液中滴加稀盐酸,有白色沉淀生成,则滤液中含有的溶质是AgNO3和_____。
20.双氧水(H2O2)既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.
(1)小明配制了5%的双氧水600g,则600g溶液中溶质为____克,溶剂为_____克.
(2)小明用13%的双氧水溶液配制上述溶液,量水时仰视了刻度,则所配制的溶液中溶质的质量分数偏____.
三、简答题
21.如图是甲、乙两种固体物质的溶解度曲线,根据图回答问题:
(1)t1℃时,甲、乙两种物质的溶解度甲________乙(填“>”“=”或“<”)。
(2)若想从甲的饱和溶液中获得甲晶体,常采用____________方法。
(3)t2℃时,将15g甲放入装有50g水的烧杯中,所得溶液溶质的质量分数为________。
(4)A点状态中乙溶液属于________溶液(填“饱和”或“不饱和”)。
22.为什么用汽油或洗涤剂都能除去衣服上的油污___?
23.二氧化碳与金属钠反应生成金刚石和碳酸钠的化学方程式为3CO2+4NaC+2Na2CO3。
(1)在很多情况下,人们希望能够较快地溶解某些固体物质。某课外小组需一定溶质质量分数的硝酸钾溶液做实验,怎样使已结块的硝酸钾固体尽快溶于水中?请提出你的操作建议。
建议1:________________________________________________________________________;
建议2:________________________________________________________________________。
(2)某同学为验证汽水(用塑料瓶盛装)里溶有二氧化碳气体,它需将气体通入澄清的石灰水中。为使气体能迅速逸出,可采用的方法有________、________________。
24.在实验室里常常将固体药品配成溶液进行化学反应,以提高反应速率。试从微粒的角度说明溶质在溶液中是怎样存在的,由此说明为什么在溶液中进行的化学反应比较快。
四、综合应用题
25.如下图装置可用于气体的吸收、检验和分离等,请回答下列问题。
(1)利用装置
A(其中液体试剂足量)可以将二氧化碳和一氧化碳的混合气体进行分离。首先打开活塞
a,缓缓通入混合气体,广口瓶中观察到的现象是______,发生反应的化学方程式为__________;此时从导管
c
逸出的主要气体是_________,为了检验该气体,将导管按
c-d-e-f-g
顺序连接,B
处观察到的现象为_________,发生反应的化学方程式为____________。
(2)实验中
A
和
C
两处用到澄清石灰水,其中
A
处澄清石灰水的作用是___________
(3)装置
C
中还应进行的操作是_____________
;一段时间后,断开
AB
装置,关闭活塞
a,打开活塞
b,滴加足量的稀盐酸,此时逸出的主要气体是______________。
(4)现有36.5
g质量分数为20%的盐定质氢氧化钙溶液恰好完全反应,生成的氯化钙溶液中溶质的质量分数为22.2%。请计算所得氯化钙溶液的质量是_____________。
【参考答案】
1.A
2.B
3.B
4.B
5.A
6.C
7.A
8.D
9.D
10.C
11.A
12.B
13.D
14.A
15.B
(或
)
>
升高温度(或增加溶剂)
16.当温度为t1时,a、c
两物质的溶解度相等(或都是20g)
a>b>c
150克
降温结晶法(或冷却热饱和溶液法)
17.160g
60
18.药品受潮
称量时,药品与砝码放调(游码有度数)(或量取时,仰视度数;烧杯不干燥)
19.水(H2O)
能
Cu
Cu(NO3)2
Zn(NO3)2
Zn(NO3)2、Cu(NO3)2
20.30
570
小
21.=
降温结晶(冷却热饱和溶液)
20%
饱和
22.汽油除去衣服上的油污属于溶解现象,洗涤剂除去衣服上的油污属于乳化作用
23.用玻璃棒搅拌
加热溶解
振荡
将汽水瓶放热水中
24.溶液中溶质是以分子或离子的形式存在,所以在溶液中构成反应物的微粒接触面积大,反应速率快
25.
澄清石灰水变浑浊
Ca(OH)2
+
C02
=
CaCO3
+
2H20
CO
黑色固体变红色
Cu0+C0
Cu+C02
吸收二氧化碳
将尾气点燃
C02
50g
第九单元
溶液
综合训练题
一、选择题
1.逻辑推理是化学学习常用的思维方法,下列推理正确的是()
A.化合物是含有不同种元素的纯净物,所以含有不同种元素的纯净物一定是化合物
B.在化合物中金属元素显正价,所以非金属元素一定显负价
C.置换反应一定有单质生成,所以有单质生成的反应一定是置换反应
D.溶液具有均一性和稳定性,所以具有均一性和稳定性的液体一定是溶液
2.下列实验能达到目的的是( )
A.证明蜡烛中含有碳、氢元素
B.测定空气中氧气的含量
C.探究燃烧条件
D.探究影响物质溶解性的因素
3.10%的硝酸钾溶液20g,为使它的质量分数增大一倍,可采用的方法是
A.再加入2g硝酸钾
B.蒸发水分浓缩为10g的溶液
C.蒸发掉水分的一半
D.加入20g25%硝酸钾溶液
4.下列关于溶液的说法正确的是(
)
A.溶液一定是无色的
B.溶液中的溶质可以是固体、气体、液体
C.均一、稳定的液体一定是溶液
D.任何不饱和溶液降温后都会变成饱和溶液
5.提高科学核心价值观,学会从化学的角度分析问题。下列分析不正确的是()
A.液氧用于火箭发射——氧气具有可燃性
B.洗涤剂清洗油污——洗涤剂有乳化功能
C.氢能源未广泛应用——氢气制取成本高、贮存困难
D.氮气充入食品包装袋中防腐——氮气化学性质不活泼
6.下列关于水和溶液的说法不正确的是(
)
A.蔗糖溶于水可形成溶液
B.溶液由溶质和溶剂组成,所以溶液一定是混合物
C.将10%的KNO3溶液倒出一半,剩余溶液中溶质的质量分数为5%
D.改变条件,能够使饱和溶液与不饱和溶液相互转化
7.按如图所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液面升高。若液体X是水,则固体y可能是(
)
A.氢氧化钠
B.氯化钠
C.硝酸铵
D.二氧化锰
8.甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是()
A.甲的溶解度比乙大
B.20°C时,甲、乙两种溶液的溶质质量分数相等
C.40°C时,可以配制溶质质量分数为38%的甲溶液
D.40°C时,甲和乙各30g分别加入100g水中,充分溶解后同时等速降温,则乙溶液中先有固体结晶析出
9.工业纯碱中常含有少量的氯化钠。某学习小组对其组成展开探究。现取24
g纯碱样品,加入100
g水使其完全溶解,再加入96
g过量的氯化钙溶液,完全反应后,过滤、洗涤、干燥得沉淀20
g.通过已知数据,不能求出的量是( )
A.反应后溶液的总质量
B.参加反应的氯化钙的质量
C.样品中碳酸钠的质量分数
D.氯化钙溶液中溶质的质量分数
10.在一定温度下,某固态溶质(不含结晶水)的水溶液甲,经历如下变化:,下列结论正确的是( )
A.溶液甲可能是饱和溶液
B.溶液乙一定是不饱和溶液
C.溶液乙和溶液丙中的溶质质量分数可能相等
D.溶液丙若再蒸发5?g水,析出的晶体质量一定等于2?g
11.t℃时,将某硝酸钾溶液第一次蒸发掉l
0g水,冷却至原温度析出晶体1g;第二次蒸发掉10g水,冷却至原温度析出晶体3g;第三次再蒸发掉10g水,冷却至原温度析出晶体应为( )
A.等于3g
B.大于3g
C.等于lg
D.小于或等于lg
12.下列图像能正确反映对应变化关系的是
A.A
B.B
C.C
D.D
13.不能正确反映对应变化关系的图像是(
)
①一定质量稀盐酸中加入某物质②澄清石灰水中通入CO2
③加热氯酸钾制取氧气④敞口放置浓硫酸
A.①图中横坐标既可以表示加入金属铁的质量,也可以表示加入碳酸钙的质量
B.②图中纵坐标既可以溶质质量,又可表示溶液导电性
C.③图中横坐标既可以表示反应时间,也可以表示加入二氧化锰质量
D.④图中纵坐标既可以表示溶剂质量,又可表示溶质质量分数
14.t℃时,某物质的溶解度为
S
克/100
克水,其饱和溶液的质量分数为
C%,则
S
与C
的数值关系为( )
A.S>C
B.S=C
C.S<C
D.无法判断
二、填空题
15.如图是某同学在学完有关溶解度的相关知识后所做的实验,请回答下列问题:
(1)A、B、C、D四个烧杯中的溶液一定属于甲物质的饱和溶液的是________________(填字母),C中甲物质的溶质质量分数为________________(填表达式)。
(2)40℃时甲物质的溶解度________________(填“>”“<”或“=”)乙物质的溶解度。
(3)若两种物质的溶解度均随温度的升高而增大,则使D中固体溶解的方法为________________。
16.根据如图回答下列问题:
(1)P
点表示______;
(2)t2℃时,三种物质溶解度大小的关系是______(用“>”、“=”或“<”连接);
(3)t2℃时,将55克a物质放入
100克水中充分搅拌,得到溶液的质量为______克;
(4)若a中含有少量的c,可以通过______的方法得到纯净a。
17.已知某物质在不同温度下的溶解度数据如下表所示:
温度(℃)
0
20
40
60
80
溶解度(克)
12.6
15.3
20.0
25.0
38.2
如果要配制该物质溶质质量分数为20%的饱和溶液200克,需要水
克,此时溶液的温度应为
℃。
18.实验室配制溶质的质量分数为10%的NaCl溶液,经检验所得溶液的溶质质量分数偏小。请从实验操作上分析造成误差的两点原因。____________________、__________________
19.有Zn
、Cu、Ag、Zn(NO3)2溶液、Cu(NO3)2溶液、AgNO3溶液几种物质。
(1)Zn(NO3)2溶液中的溶剂是_____;饱和Cu(NO3)2溶液中_____溶解氯化钠(“能”、“不能”)。
(2)若要用上面药品验证Zn
、Cu、Ag三种金属的金属活泼性强弱,所用药品可选择Zn(NO3)2溶液、AgNO3溶液及_____,也可以选择Zn
、Ag及_____溶液。
(3)向含有AgNO3和Cu(NO3)2两种物质的混合物溶液中加入一定量的Zn,充分反应后过滤、洗涤,分别得到滤渣和滤液。若向滤渣中加入稀盐酸有气泡产生,则滤液中的溶质是_____;若向滤液中滴加稀盐酸,有白色沉淀生成,则滤液中含有的溶质是AgNO3和_____。
20.双氧水(H2O2)既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.
(1)小明配制了5%的双氧水600g,则600g溶液中溶质为____克,溶剂为_____克.
(2)小明用13%的双氧水溶液配制上述溶液,量水时仰视了刻度,则所配制的溶液中溶质的质量分数偏____.
三、简答题
21.如图是甲、乙两种固体物质的溶解度曲线,根据图回答问题:
(1)t1℃时,甲、乙两种物质的溶解度甲________乙(填“>”“=”或“<”)。
(2)若想从甲的饱和溶液中获得甲晶体,常采用____________方法。
(3)t2℃时,将15g甲放入装有50g水的烧杯中,所得溶液溶质的质量分数为________。
(4)A点状态中乙溶液属于________溶液(填“饱和”或“不饱和”)。
22.为什么用汽油或洗涤剂都能除去衣服上的油污___?
23.二氧化碳与金属钠反应生成金刚石和碳酸钠的化学方程式为3CO2+4NaC+2Na2CO3。
(1)在很多情况下,人们希望能够较快地溶解某些固体物质。某课外小组需一定溶质质量分数的硝酸钾溶液做实验,怎样使已结块的硝酸钾固体尽快溶于水中?请提出你的操作建议。
建议1:________________________________________________________________________;
建议2:________________________________________________________________________。
(2)某同学为验证汽水(用塑料瓶盛装)里溶有二氧化碳气体,它需将气体通入澄清的石灰水中。为使气体能迅速逸出,可采用的方法有________、________________。
24.在实验室里常常将固体药品配成溶液进行化学反应,以提高反应速率。试从微粒的角度说明溶质在溶液中是怎样存在的,由此说明为什么在溶液中进行的化学反应比较快。
四、综合应用题
25.如下图装置可用于气体的吸收、检验和分离等,请回答下列问题。
(1)利用装置
A(其中液体试剂足量)可以将二氧化碳和一氧化碳的混合气体进行分离。首先打开活塞
a,缓缓通入混合气体,广口瓶中观察到的现象是______,发生反应的化学方程式为__________;此时从导管
c
逸出的主要气体是_________,为了检验该气体,将导管按
c-d-e-f-g
顺序连接,B
处观察到的现象为_________,发生反应的化学方程式为____________。
(2)实验中
A
和
C
两处用到澄清石灰水,其中
A
处澄清石灰水的作用是___________
(3)装置
C
中还应进行的操作是_____________
;一段时间后,断开
AB
装置,关闭活塞
a,打开活塞
b,滴加足量的稀盐酸,此时逸出的主要气体是______________。
(4)现有36.5
g质量分数为20%的盐定质氢氧化钙溶液恰好完全反应,生成的氯化钙溶液中溶质的质量分数为22.2%。请计算所得氯化钙溶液的质量是_____________。
【参考答案】
1.A
2.B
3.B
4.B
5.A
6.C
7.A
8.D
9.D
10.C
11.A
12.B
13.D
14.A
15.B
(或
)
>
升高温度(或增加溶剂)
16.当温度为t1时,a、c
两物质的溶解度相等(或都是20g)
a>b>c
150克
降温结晶法(或冷却热饱和溶液法)
17.160g
60
18.药品受潮
称量时,药品与砝码放调(游码有度数)(或量取时,仰视度数;烧杯不干燥)
19.水(H2O)
能
Cu
Cu(NO3)2
Zn(NO3)2
Zn(NO3)2、Cu(NO3)2
20.30
570
小
21.=
降温结晶(冷却热饱和溶液)
20%
饱和
22.汽油除去衣服上的油污属于溶解现象,洗涤剂除去衣服上的油污属于乳化作用
23.用玻璃棒搅拌
加热溶解
振荡
将汽水瓶放热水中
24.溶液中溶质是以分子或离子的形式存在,所以在溶液中构成反应物的微粒接触面积大,反应速率快
25.
澄清石灰水变浑浊
Ca(OH)2
+
C02
=
CaCO3
+
2H20
CO
黑色固体变红色
Cu0+C0
Cu+C02
吸收二氧化碳
将尾气点燃
C02
50g
同课章节目录
