2021届山东高考化学复习 高三实验综合 pdf版含答案
文档属性
| 名称 | 2021届山东高考化学复习 高三实验综合 pdf版含答案 |

|
|
| 格式 | |||
| 文件大小 | 3.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-07 00:00:00 | ||
图片预览


文档简介
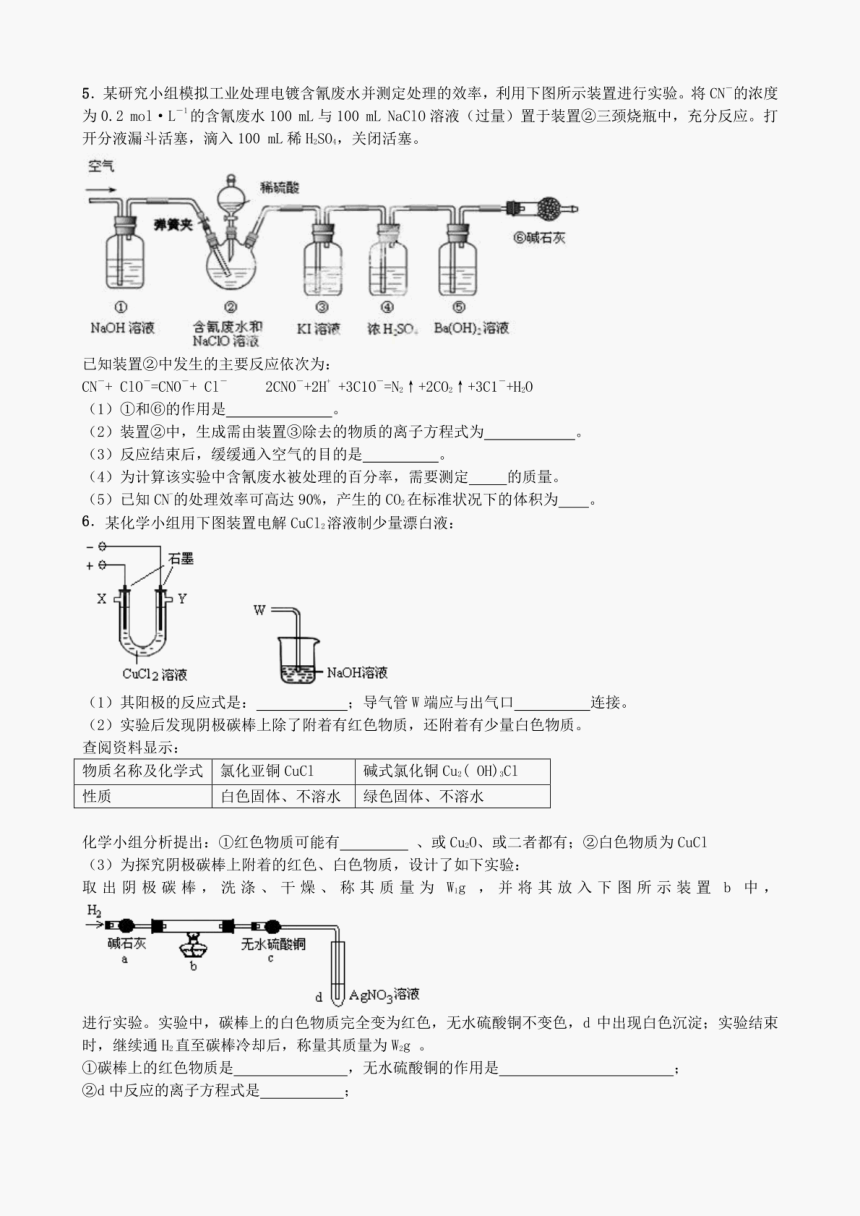
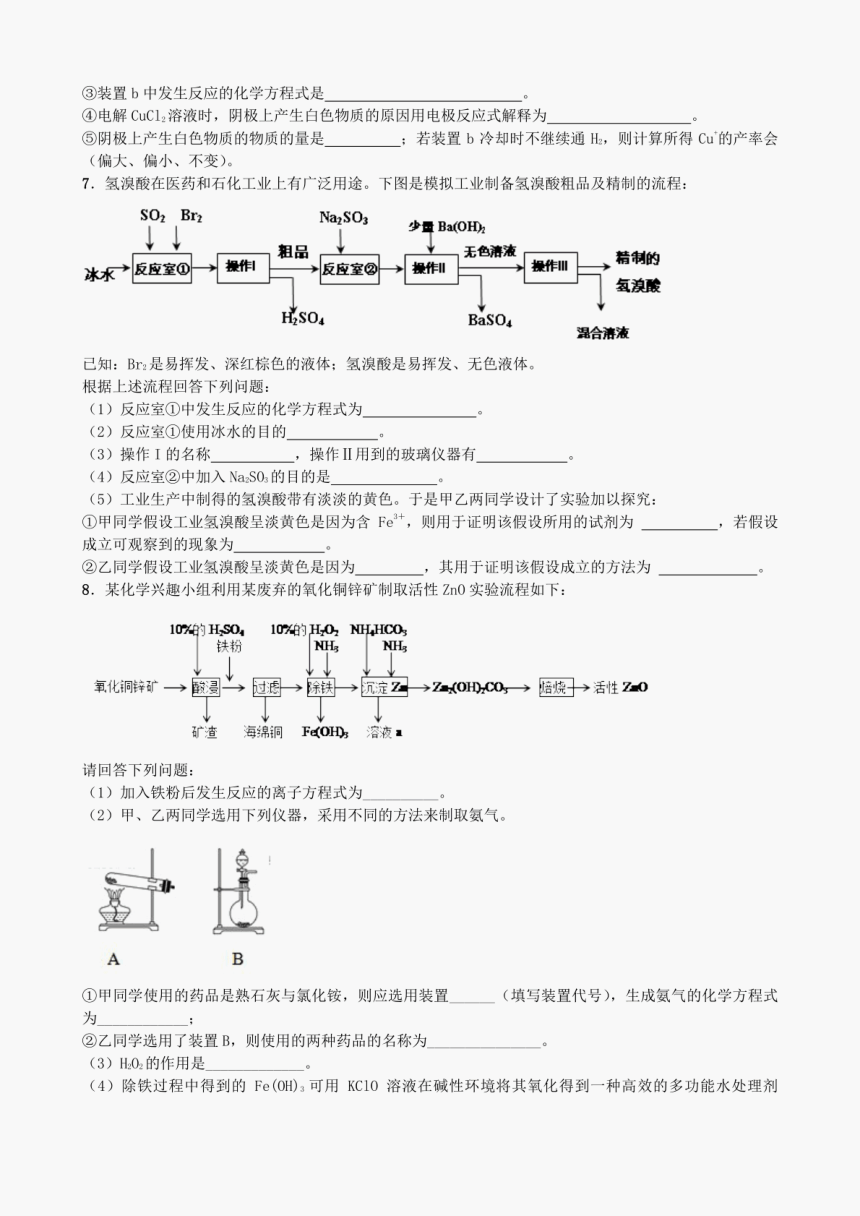
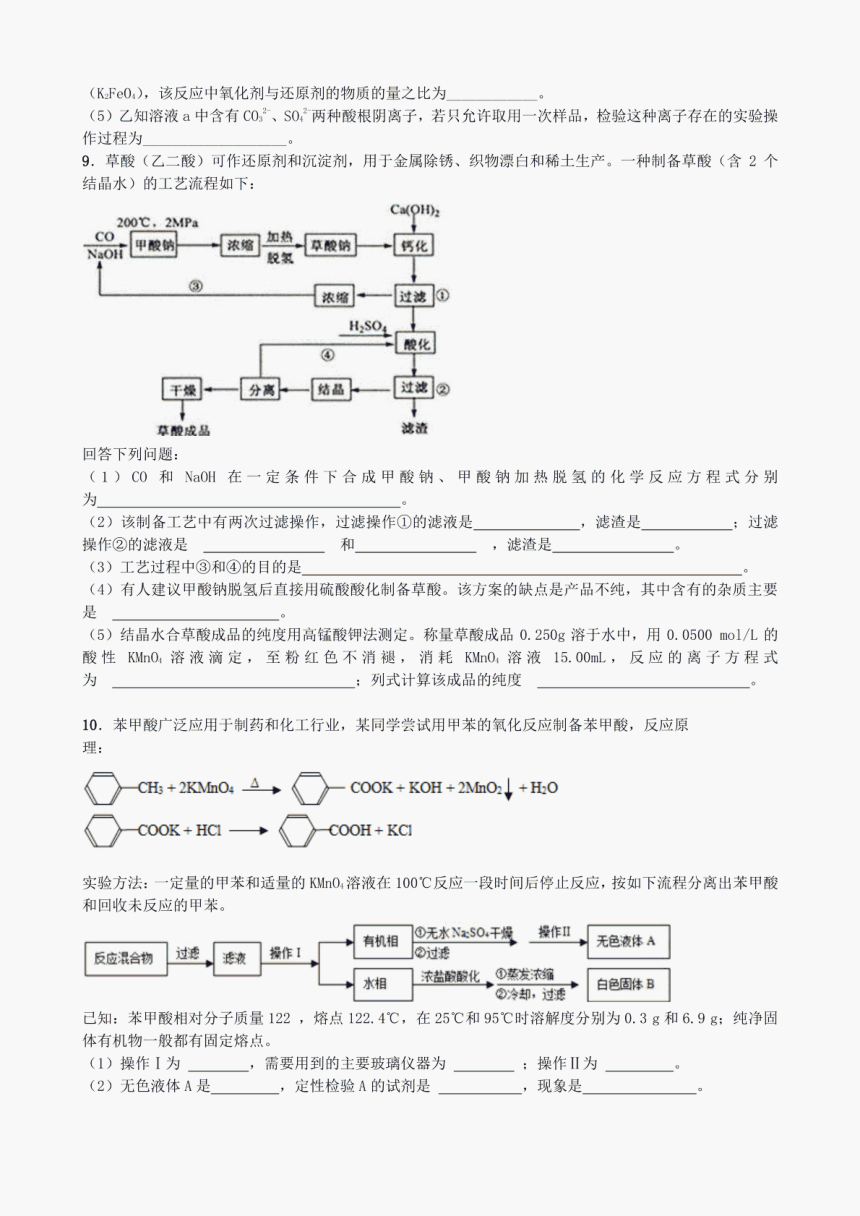
高三实验综合习题
1.有一瓶澄清的溶液,其中可能有NH、K、Na、Mg2、Ba、Al、Cl、I、、(0’s
SO:、410-、162O-,取该溶液进行以下实验:
(1)取pH试纸检验,溶液呈强酸性,可以排除
离子的存在;
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4层呈紫色,可以排除
离子的存
在
(3)另取岀部分溶液逐滴加入№aOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,溶液
均无沉淀产生,则又可以排除
离子的存在;
(4)取出部分上述碱性溶液滴加NaO3溶液后,有白色沉淀生成,证明
离子存在,又可排除
离子的存在
(5)将(3)得到的碱性溶液加热,有气体放岀,该气体能使湿润的红色石蕊试纸变蓝。根据上述实验事实确
定:该溶液中肯定存在的离子是
还不能确定是否存在的离子是
2.为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
[探究一](1)将已去除表面氧化物的铁钉(碳素钢)放λ冷浓硫酸中,10分钟后移λ硫酸铜溶液中,片刻后
取出观察,铁钉表面无明显变化,其原因是
(2)称取碳素钢6.0g放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe之外还可能含有Fe+。若要确认其中的Fe,应选用
(选填序号)。
A.KSCN溶液和氯水
B.铁粉和KSCN溶液
C.浓氨水
酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,发生SO+Br2+2HO=2HBr+HsSO4反应,然后加入足
量BaCl2溶液,经适当操作后得干燥固体4.66g。由此推知气体Y中SO的体积分数为
[探究二]根据上述实验中S02体积分数的分析,丙同学认为气体Y中还可能含有Q和Q两种气体,其中Q
气体,在标准状况下,密度为0.0893g·L。为此设计了下列探究实验装置(假设有关气体完全反应)。
Y气体N(用于载送
气体反应物和产物
加热CuO
酸性
无水
KMnO.
碱石灰硫酸铜
溶液
碱石灰
M
溶液
A
B
E
(3)装置B中试剂的作用是
(4)分析Y气体中的Q2气体是如何生成的
(用化学方程式表示)。
(5)己知洗气瓶M中盛装澄清石灰水,为确认Q的存在,需在装置中添加洗气瓶M于
(填序号)。
A.A之前
B.A-B间
C.B-C间
D.C-D间
(6)如果气体Y中含有Q1,预计实验现象应是
3.王老师在用酒精喷灯做“铁与水蒸气反应”后,该校高一化学硏究性小组同学对得到的黑色固体物质
进行了如下实验:
霁缴剌图
淡黄色溶液
AHKSCN「红色溶液新制氯水深红色溶液
溶液
D
过量
(1)甲同学认为:该黑色固体为四氧化三铁。请写出黑色固体溶于稀盐酸的化学方程式
(2)乙同学提出:根据上述实验现象甲同学的观点不可靠,理由是
(3)深红色溶液C放置一段时间后,发现红色褪去。关于溶液褪色的原因,同学们纷纷猜想
1.有一瓶澄清的溶液,其中可能有NH、K、Na、Mg2、Ba、Al、Cl、I、、(0’s
SO:、410-、162O-,取该溶液进行以下实验:
(1)取pH试纸检验,溶液呈强酸性,可以排除
离子的存在;
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4层呈紫色,可以排除
离子的存
在
(3)另取岀部分溶液逐滴加入№aOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,溶液
均无沉淀产生,则又可以排除
离子的存在;
(4)取出部分上述碱性溶液滴加NaO3溶液后,有白色沉淀生成,证明
离子存在,又可排除
离子的存在
(5)将(3)得到的碱性溶液加热,有气体放岀,该气体能使湿润的红色石蕊试纸变蓝。根据上述实验事实确
定:该溶液中肯定存在的离子是
还不能确定是否存在的离子是
2.为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
[探究一](1)将已去除表面氧化物的铁钉(碳素钢)放λ冷浓硫酸中,10分钟后移λ硫酸铜溶液中,片刻后
取出观察,铁钉表面无明显变化,其原因是
(2)称取碳素钢6.0g放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe之外还可能含有Fe+。若要确认其中的Fe,应选用
(选填序号)。
A.KSCN溶液和氯水
B.铁粉和KSCN溶液
C.浓氨水
酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,发生SO+Br2+2HO=2HBr+HsSO4反应,然后加入足
量BaCl2溶液,经适当操作后得干燥固体4.66g。由此推知气体Y中SO的体积分数为
[探究二]根据上述实验中S02体积分数的分析,丙同学认为气体Y中还可能含有Q和Q两种气体,其中Q
气体,在标准状况下,密度为0.0893g·L。为此设计了下列探究实验装置(假设有关气体完全反应)。
Y气体N(用于载送
气体反应物和产物
加热CuO
酸性
无水
KMnO.
碱石灰硫酸铜
溶液
碱石灰
M
溶液
A
B
E
(3)装置B中试剂的作用是
(4)分析Y气体中的Q2气体是如何生成的
(用化学方程式表示)。
(5)己知洗气瓶M中盛装澄清石灰水,为确认Q的存在,需在装置中添加洗气瓶M于
(填序号)。
A.A之前
B.A-B间
C.B-C间
D.C-D间
(6)如果气体Y中含有Q1,预计实验现象应是
3.王老师在用酒精喷灯做“铁与水蒸气反应”后,该校高一化学硏究性小组同学对得到的黑色固体物质
进行了如下实验:
霁缴剌图
淡黄色溶液
AHKSCN「红色溶液新制氯水深红色溶液
溶液
D
过量
(1)甲同学认为:该黑色固体为四氧化三铁。请写出黑色固体溶于稀盐酸的化学方程式
(2)乙同学提出:根据上述实验现象甲同学的观点不可靠,理由是
(3)深红色溶液C放置一段时间后,发现红色褪去。关于溶液褪色的原因,同学们纷纷猜想
同课章节目录
