2020-2021学年人教版高二化学选修5第二章2.1 脂肪烃(1) 课件 (35张ppt)
文档属性
| 名称 | 2020-2021学年人教版高二化学选修5第二章2.1 脂肪烃(1) 课件 (35张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 10.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-10 00:00:00 | ||
图片预览







文档简介
第二章
烃和卤代烃
2021.03: W
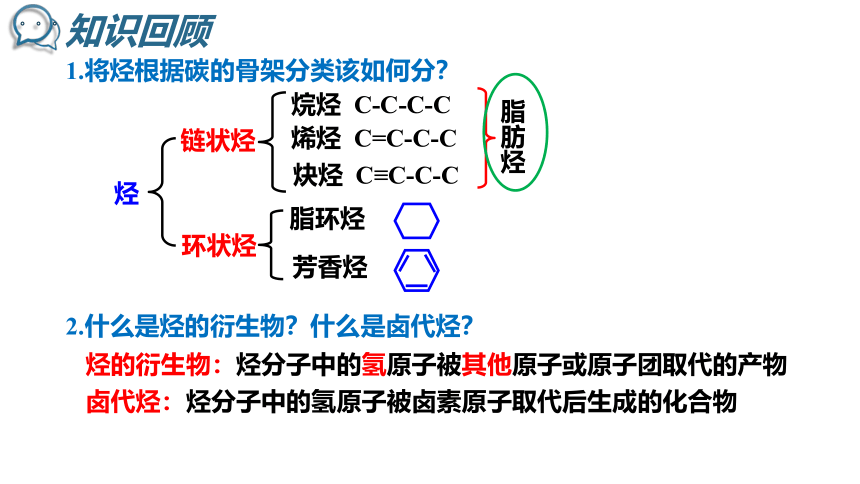
知识回顾
1.将烃根据碳的骨架分类该如何分?
链状烃
环状烃
烷烃 C-C-C-C
烯烃 C=C-C-C
炔烃 C≡C-C-C
脂环烃
芳香烃
脂肪烃
烃
2.什么是烃的衍生物?什么是卤代烃?
烃的衍生物:烃分子中的氢原子被其他原子或原子团取代的产物
卤代烃:烃分子中的氢原子被卤素原子取代后生成的化合物
学习
目标
第一节
脂肪烃
1.了解烷烃、烯烃的物理性质的变化与分子中碳原子数目的关系。
2.能以典型代表物为例,理解烷烃、烯烃的化学性质。
3.认识烷烃和烯烃的特征结构。
水果中的胡萝卜素
二十七烷
二十九烷
十一烷和十三烷
C10H16
自然界中存在的脂肪烃
1. 请根据表中给出的数据,以分子中碳原子数为横坐标,以沸点或相对密度为纵坐标,制作曲线图。通过所绘制的曲线图你能得到什么信息?
表2-1 部分烷烃的沸点和相对密度
名称
结构简式
沸点/℃
相对密度
甲烷
CH4
-161.5
0.466
乙烷
CH3CH3
-88.6
0.527
丁烷
CH3(CH2)2CH3
-0.5
0.5788
戊烷
CH3(CH2)3CH3
36.0
0.6262
壬烷
CH3(CH2)7CH3
150.8
0.718
十一烷
CH3(CH2)9CH3
194.5
0.741
思考交流
思考交流
名称
结构简式
沸点/℃
相对密度
乙烯
CH2=CH2
-161.5
0.466
丙烯
CH2=CHCH3
-88.6
0.527
1-丁烯
CH2=CHCH2CH3
-0.5
0.5788
1-戊烯
CH2= CH(CH2)2CH3
36.0
0.6262
1-己烯
CH2=CH(CH2)3CH3
150.8
0.718
1-庚烯
CH2= CH(CH2)4CH3
194.5
0.741
表2-2 部分烯烃的沸点和相对密度
沸点℃
分子中碳原子数
2 4 6 8 10 12 14 16
200
100
50
0
-100
分子中碳原子数
相对密度
2 4 6 8 10 12 14 16
0.6
0.4
0.2
0
烷烃
烷烃
烯烃
烯烃
脂肪烃的物理性质
一.烷烃和烯烃
1、烷烃和烯烃的物理性质
烷烃和烯烃的物理性质随着分子中碳原子数的递增,呈现规律性的变化
(1)熔沸点:随碳原子数增多,熔沸点增大。
烷烃的同分异构体熔沸点如何比较?
烷烃的同分异构体是支链越多熔沸点越低,如:
正戊烷>异戊烷>新戊烷
(2)状态:气态——→液态——→固态
N(C) ≤ 4
与新戊烷
?
碳原子在5~16之间
N(C) ≥ 17
?
(3)相对密度:随碳原子数增多,相对密度增大。
(4)溶解性:均不溶于水,易溶于有机溶剂。
烃的密度都比水小,相混时浮在水面上。
2、烷烃
(1)通式:
CnH2n+2 (n≥1)
?
(2)结构特点:
随碳原子数增多,碳原子质量分数 ,氢原子质量分数 。
增大
减小
环烷烃的通式 。
CnH2n (n≥3)
?
环烷烃不是烷烃
碳碳间均为单键,所有原子 共平面,烷烃中只有????键,碳原子的杂化方式为 。碳原子数不同的烷烃之间关系是 。
?
不能
sp3
同系物
2、烷烃
(3)化学性质:
①通常状况下,它们很稳定,不与酸、碱及氧化物反应,也难与其他物质化合。
不能使酸性高锰酸钾和溴水褪色
②氧化反应:
CH4 + 2O2 ? CO2 + 2H2O
点燃
火焰明亮,呈淡蓝色。
CnH2n+2 + 3????+????2O2 ? nCO2 + (n+1)H2O
?
点燃
③取代反应:
CH4
????????????
?
CH3Cl
????????????
?
CH2Cl2
????????????
?
CHCl3
????????????
?
CCl4
CH3CH3+Cl2 CH3CH2Cl+HCl
光
取代反应:有机物分子中某些原子或原子团被其它原子或原子团所代替的反应。
思考交流
2.如果1mol甲烷与氯气发生取代反应,生成等物质的量的四种有机物,则消耗氯气的物质的量为?若1mol甲烷与氯气全部生成CHCl3呢?
CH4
CH3Cl
CH2Cl2
CHCl3
CCl4
1mol
0.25mol
0.25mol
0.25mol
0.25mol
?(1+2+3+4)
?
0.25mol×
?
= 2.5mol
有多少物质的量的氢原子被取代,就消耗同样多物质的量的氯气。
消耗3mol氯气
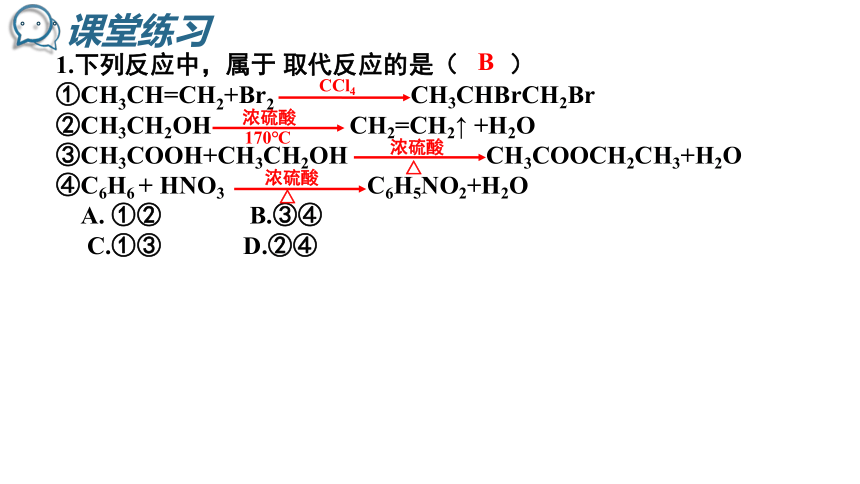
1.下列反应中,属于 取代反应的是( )
①CH3CH=CH2+Br2 CH3CHBrCH2Br
②CH3CH2OH CH2=CH2↑ +H2O
③CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O
④C6H6 + HNO3 C6H5NO2+H2O
A. ①② B.③④
C.①③ D.②④
CCl4
浓硫酸
170℃
浓硫酸
△
浓硫酸
△
B
课堂练习
2、烷烃
(3)化学性质:
④热分解:
C4H10 C2H4+C2H6
△
C4H10 CH4+C3H6
△
石油的裂化:
石油的裂解:
得到更多更高质量的汽油
得到乙烯、丙烯等短链不饱和烃。
CH4 C +2H2
1000℃以上
3、烯烃
(1)通式:
CnH2n (n≥2)
?
随碳原子数增多,碳原子质量分数 ,氢原子质量分数 。
不变
不变
环烷烃:CnH2n (n≥3)
?
单烯烃与同碳原子数的环烷烃是同分异构体
二烯烃:CnH2n-2
(n≥4)
?
最简单的二烯烃:
CH2=CH—CH=CH2
二烯烃与同碳原子数的单炔烃是同分异构体
思考:C4H8的同分异构体有哪些?
3、烯烃
(2)结构特点:
含有碳碳双键,乙烯所有原子 共平面,键角约为 。烯烃中含有????键和 键,碳原子的杂化方式为 。碳原子数不同的单烯烃之间关系是 。
?
能
sp3和sp2
同系物
????
?
思考:(1)CH2=CH—CH3一定有 个原子共平面,最多有 个原子共平面。
(2)CH2=CH—CH=CH2一定有 个原子共平面。
120°
?
6
7
10
3、烯烃
(3)化学性质:
①氧化反应:
烯烃能使酸性高锰酸钾和溴水褪色
燃烧:
C2H4 + 3O2 ? 2CO2 + 2H2O
点燃
火焰明亮,伴有黑烟。
CnH2n + 3????2O2 ? nCO2 + nH2O
?
点燃
与酸性高锰酸钾反应:
5CH2=CH2 + 12KMnO4 +18H2SO4
10CO2 ↑ + 12MnSO4 + 6K2SO4 + 28H2O
CH2=CH2 + KMnO4 +H2SO4 →
②加成反应:
(与H2、Br2、HX、H2O等)
CH3-CH=CH2 + H2 CH3CH2CH3
催化剂
CH2=CH2+Br2 CH2BrCH2Br
1,2-二溴乙烷
3、烯烃
(3)化学性质:
②加成反应:
(与H2、Br2、HX、H2O等)
CH2=CH2+H2O CH3CH2OH
催化剂
加压、加热
CH2=CH2+HBr CH3CH2Br
CH2=CH-CH3
CH2-CH-CH3
| |
H Br
CH2-CH-CH3
| |
Br H
主要产物
+ HBr
马氏规则,即氢多加氢。
加成反应:有机物分子中未饱和的碳原子跟其它原子或原子团直接结合生成别的物质的反应。
思考交流
3.思考:(1)如想制备一氯乙烷,是采用乙烷与氯气的取代反应还是用乙烯与氯化氢的加成反应,为什么?
(2)乙烯能使溴的CCl4褪色,甲同学认为发生了取代反应,乙同学认为发生了加成反应,哪一位同学正确呢?试设计实验验证。
(1)乙烯与HCl的加成反应副反应更少,产物相对纯净。
(2)方法:向反应后溶液中加AgNO3溶液或石蕊
现象:若发生取代反应则生成HBr,则有淡黄色沉淀或加石蕊会变红;
若发生加成反应,则无此现象。
3、烯烃
(3)化学性质:
②加成反应:
(与H2、Br2、HX、H2O等)
共轭二烯烃和1molBr2的1,2加成与1,4加成:
CH2=CH—CH=CH2 + 2Br2 →
CH2 — CH—CH — CH2
Br Br Br Br
1,2,3,4 – 四溴丁烷
CH2=CH-CH=CH2+Br2
CH2-CH-CH=CH2
| |
Br Br
1,2 加成
1,4 加成
CH2-CH-CH-CH2
1,2 Br
1,4 Br
(中间体)
3,4-二溴-1-丁烯
1,4-二溴-2-丁烯
1 2 3 4
CH2-CH=CH-CH2
| |
Br Br
3、烯烃
(3)化学性质:
②加聚反应:
nCH2==CH2
催化剂
CH2 CH2
[
]
n
加聚反应:通过加成反应聚合成高分子化合物的反应(加成聚合反应)。
单体
链节
聚合度
CH2 CH2
由相对分子质量小的化合物分子互相结合成相对分子质量大的高分子的反应叫做聚合反应。
加聚反应的通式:
nR1-CH==CH-R2
一定条件
CH CH
[
]
n
R1 R2
高聚物都是混合物
思考交流
4.思考:(1)聚乙烯能使溴水褪色吗?
(2)2.8g乙烯和聚乙烯的混合物中含有 个碳原子。
(3)写出下列物质的加聚反应方程式:
丙烯 2-甲基丙烯 2-丁烯 2,3-二甲基-2-丁烯
0.2NA
nCH2==CH-CH3
一定条件
CH2 CH
[
]
n
CH3
nCH3-CH==CH-CH3
一定条件
CH CH
[
]
n
CH3 CH3
nCH2==C-CH3
一定条件
CH2 C
[
]
n
CH3
CH3
CH3
CH3
CH3
nCH3-C == C -CH3
一定条件
C C
[
]
n
CH3 CH3
CH3
CH3
3、烯烃
(3)化学性质:
②加聚反应:
n CH2=C—CH=CH2
CH3
[ CH2—C=CH—CH2 ]n
CH3
催化剂
n CH2=CH—CH=CH2
[ CH2—CH=CH—CH2 ]n
催化剂
思考交流
5.写出下列反应式:
[ CH2-CH2-CH2-CH=CH-CH2 ] n
nCH2=CH2 + nCH2=CH-CH3
[ CH2-CH2-CH2-CH ] n
催化剂
CH3
|
或 [ CH2-CH2-CH-CH2 ] n
CH3
|
nCH2=CH2 + nCH2=CH-CH=CH2
催化剂
分子式
C2H6
结构式
键的类别
键角
键长(10-10米)
键能(KJ/mol)
空间各原子的位置
C—C
109?28ˊ
1.54
120?
1.33
C2H4
乙烷与乙烯的对比
348
2C和6H不在同一平面上
615
2C和4H在同一平面上
课堂练习
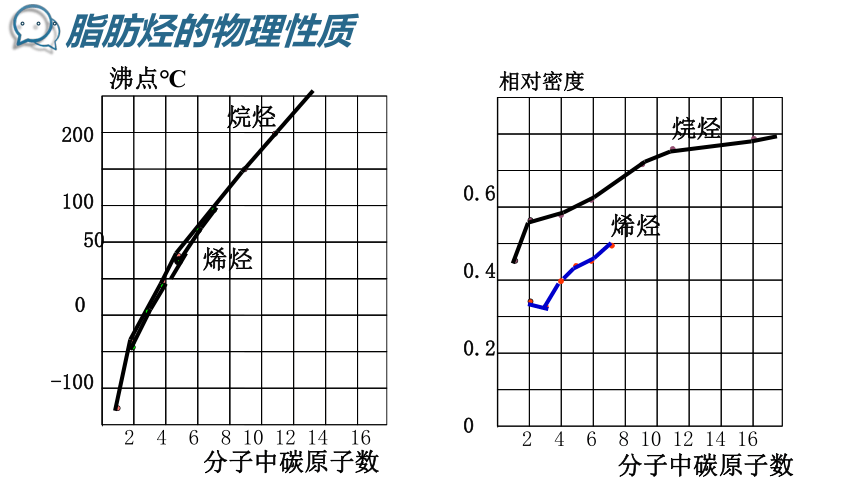
2.由下列数据:可判断丙烷的沸点可能是( )
A.高于-0.5℃ B.约是+30℃
C.约是-40℃ D.低于-89℃
C
C
物质
甲烷
乙烷
丁烷
戊烷
沸点
-162?C
-89?C
-1?C
+36?C
3.下列烷烃沸点最高的是( )
A.CH3CH2CH3 B.CH3CH2CH2CH3
C.CH3(CH2)3CH3 D.(CH3)2CHCH2CH3
二.烯烃的顺反异构
1、概念
由于碳碳双键不能旋转而导致分子中原子或原子团在空间的排列方式不同所产生的异构现象,称为顺反异构。
2、产生顺反异构的条件
双键两端的同一个碳原子上不能连有相同基团只有这样才会产生顺反异构体
C=C
A B
B A
C=C
A A
B C
C=C
A C
B D
C=C
A B
B C
观察学习
【思考】下列结构是否为顺反异构体?
顺-2-丁烯
C
H
C
H3C
H
CH3
C
H
C
H3C
H
CH3
反-2-丁烯
课堂练习
4.下列物质中没有顺反异构的是哪些?
(1)、 1,2-二氯乙烯
(2)、 1,2-二氯丙烯
(3)、 2-甲基-2-丁烯
(4)、 2-氯-2-丁烯
×
√
√
√
CHCl=CHCl
C=C
H Cl
Cl H
C=C
Cl Cl
H H
CHCl=CCl-CH3
CH3
CH3-C = CH -CH3
C=C
H Cl
Cl CH3
C=C
Cl Cl
H CH3
Cl
CH3-C = CH -CH3
C=C
CH3 Cl
Cl CH3
C=C
Cl H
CH3 CH3
5.始祖鸟烯(Pterodactyladiene)形状宛如一只展翅飞翔的鸟,其键线式结构表示如下,其中R1、R2为烷烃基。则下列有关始祖鸟烯的说法中正确的是( )
A.始祖鸟烯与乙烯互为同系物
B.若R1=R2=甲基,则其化学
式为C12H16
C.若R1=R2=甲基,则始祖鸟烯
的一氯代物有3种
D.始祖鸟烯既能使酸性高锰酸钾
溶液褪色,也能使溴水褪色,
则两反应的反应类型是相同的
C
C12H14
课堂练习
6.桶烯结构简式如下图所示,有关说法不正确的是( )
A.桶烯分子中所有的原子在同一平面上
B.桶烯在一定条件下能发生加聚反应
C.桶烯与苯乙烯(C6H5CH=CH2)
互为同分异构体
D.桶烯中的一个氢原子被氯原子取代,
所得产物只有两种
A
C8H8
课堂练习
拓展提升
CH2
CH
|
CH
CH2
+
CH2
CH2
CH2
CH
‖
CH
CH2
CH2
CH2
双烯合成
+
环己烯
拓展提升
用键线式表示为:
CH2
CH
|
CH
CH2
+
CH-CH3
CH-CH3
CH2
CH
‖
CH
CH2
CH-CH3
CH-CH3
+
(1)
(2)
(3)
CH3 CH3
| |
CH2=C— C=CH2
CH2=CH—CHO
拓展提升
课堂练习
5.1mol某链烃最多能和2molHCl发生加成反应,生成1mol氯代烷,1mol该氯代烷能和6molCl2发生取代反应,生成只含有碳元素和氯元素的氯代烃,该烃可能是( )
A.CH3CH=CH2
B. CH3C≡CH
C.CH3CH2C≡CH
D. CH2=CHCH=CH2
B
谢谢欣赏
烃和卤代烃
2021.03: W
知识回顾
1.将烃根据碳的骨架分类该如何分?
链状烃
环状烃
烷烃 C-C-C-C
烯烃 C=C-C-C
炔烃 C≡C-C-C
脂环烃
芳香烃
脂肪烃
烃
2.什么是烃的衍生物?什么是卤代烃?
烃的衍生物:烃分子中的氢原子被其他原子或原子团取代的产物
卤代烃:烃分子中的氢原子被卤素原子取代后生成的化合物
学习
目标
第一节
脂肪烃
1.了解烷烃、烯烃的物理性质的变化与分子中碳原子数目的关系。
2.能以典型代表物为例,理解烷烃、烯烃的化学性质。
3.认识烷烃和烯烃的特征结构。
水果中的胡萝卜素
二十七烷
二十九烷
十一烷和十三烷
C10H16
自然界中存在的脂肪烃
1. 请根据表中给出的数据,以分子中碳原子数为横坐标,以沸点或相对密度为纵坐标,制作曲线图。通过所绘制的曲线图你能得到什么信息?
表2-1 部分烷烃的沸点和相对密度
名称
结构简式
沸点/℃
相对密度
甲烷
CH4
-161.5
0.466
乙烷
CH3CH3
-88.6
0.527
丁烷
CH3(CH2)2CH3
-0.5
0.5788
戊烷
CH3(CH2)3CH3
36.0
0.6262
壬烷
CH3(CH2)7CH3
150.8
0.718
十一烷
CH3(CH2)9CH3
194.5
0.741
思考交流
思考交流
名称
结构简式
沸点/℃
相对密度
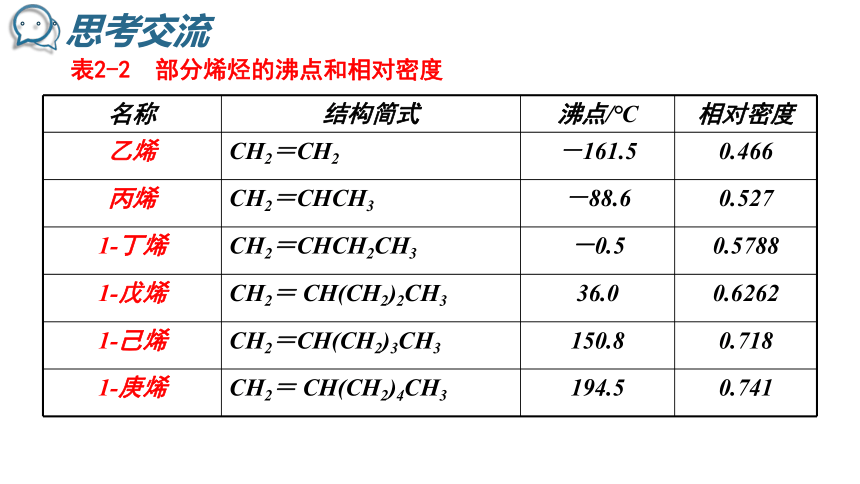
乙烯
CH2=CH2
-161.5
0.466
丙烯
CH2=CHCH3
-88.6
0.527
1-丁烯
CH2=CHCH2CH3
-0.5
0.5788
1-戊烯
CH2= CH(CH2)2CH3
36.0
0.6262
1-己烯
CH2=CH(CH2)3CH3
150.8
0.718
1-庚烯
CH2= CH(CH2)4CH3
194.5
0.741
表2-2 部分烯烃的沸点和相对密度
沸点℃
分子中碳原子数
2 4 6 8 10 12 14 16
200
100
50
0
-100
分子中碳原子数
相对密度
2 4 6 8 10 12 14 16
0.6
0.4
0.2
0
烷烃
烷烃
烯烃
烯烃
脂肪烃的物理性质
一.烷烃和烯烃
1、烷烃和烯烃的物理性质
烷烃和烯烃的物理性质随着分子中碳原子数的递增,呈现规律性的变化
(1)熔沸点:随碳原子数增多,熔沸点增大。
烷烃的同分异构体熔沸点如何比较?
烷烃的同分异构体是支链越多熔沸点越低,如:
正戊烷>异戊烷>新戊烷
(2)状态:气态——→液态——→固态
N(C) ≤ 4
与新戊烷
?
碳原子在5~16之间
N(C) ≥ 17
?
(3)相对密度:随碳原子数增多,相对密度增大。
(4)溶解性:均不溶于水,易溶于有机溶剂。
烃的密度都比水小,相混时浮在水面上。
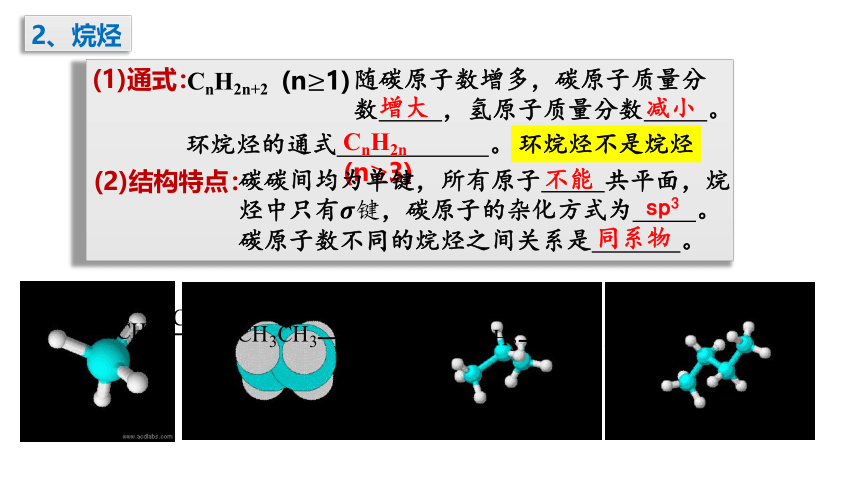
2、烷烃
(1)通式:
CnH2n+2 (n≥1)
?
(2)结构特点:
随碳原子数增多,碳原子质量分数 ,氢原子质量分数 。
增大
减小
环烷烃的通式 。
CnH2n (n≥3)
?
环烷烃不是烷烃
碳碳间均为单键,所有原子 共平面,烷烃中只有????键,碳原子的杂化方式为 。碳原子数不同的烷烃之间关系是 。
?
不能
sp3
同系物
2、烷烃
(3)化学性质:
①通常状况下,它们很稳定,不与酸、碱及氧化物反应,也难与其他物质化合。
不能使酸性高锰酸钾和溴水褪色
②氧化反应:
CH4 + 2O2 ? CO2 + 2H2O
点燃
火焰明亮,呈淡蓝色。
CnH2n+2 + 3????+????2O2 ? nCO2 + (n+1)H2O
?
点燃
③取代反应:
CH4
????????????
?
CH3Cl
????????????
?
CH2Cl2
????????????
?
CHCl3
????????????
?
CCl4
CH3CH3+Cl2 CH3CH2Cl+HCl
光
取代反应:有机物分子中某些原子或原子团被其它原子或原子团所代替的反应。
思考交流
2.如果1mol甲烷与氯气发生取代反应,生成等物质的量的四种有机物,则消耗氯气的物质的量为?若1mol甲烷与氯气全部生成CHCl3呢?
CH4
CH3Cl
CH2Cl2
CHCl3
CCl4
1mol
0.25mol
0.25mol
0.25mol
0.25mol
?(1+2+3+4)
?
0.25mol×
?
= 2.5mol
有多少物质的量的氢原子被取代,就消耗同样多物质的量的氯气。
消耗3mol氯气
1.下列反应中,属于 取代反应的是( )
①CH3CH=CH2+Br2 CH3CHBrCH2Br
②CH3CH2OH CH2=CH2↑ +H2O
③CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O
④C6H6 + HNO3 C6H5NO2+H2O
A. ①② B.③④
C.①③ D.②④
CCl4
浓硫酸
170℃
浓硫酸
△
浓硫酸
△
B
课堂练习
2、烷烃
(3)化学性质:
④热分解:
C4H10 C2H4+C2H6
△
C4H10 CH4+C3H6
△
石油的裂化:
石油的裂解:
得到更多更高质量的汽油
得到乙烯、丙烯等短链不饱和烃。
CH4 C +2H2
1000℃以上
3、烯烃
(1)通式:
CnH2n (n≥2)
?
随碳原子数增多,碳原子质量分数 ,氢原子质量分数 。
不变
不变
环烷烃:CnH2n (n≥3)
?
单烯烃与同碳原子数的环烷烃是同分异构体
二烯烃:CnH2n-2
(n≥4)
?
最简单的二烯烃:
CH2=CH—CH=CH2
二烯烃与同碳原子数的单炔烃是同分异构体
思考:C4H8的同分异构体有哪些?
3、烯烃
(2)结构特点:
含有碳碳双键,乙烯所有原子 共平面,键角约为 。烯烃中含有????键和 键,碳原子的杂化方式为 。碳原子数不同的单烯烃之间关系是 。
?
能
sp3和sp2
同系物
????
?
思考:(1)CH2=CH—CH3一定有 个原子共平面,最多有 个原子共平面。
(2)CH2=CH—CH=CH2一定有 个原子共平面。
120°
?
6
7
10
3、烯烃
(3)化学性质:
①氧化反应:
烯烃能使酸性高锰酸钾和溴水褪色
燃烧:
C2H4 + 3O2 ? 2CO2 + 2H2O
点燃
火焰明亮,伴有黑烟。
CnH2n + 3????2O2 ? nCO2 + nH2O
?
点燃
与酸性高锰酸钾反应:
5CH2=CH2 + 12KMnO4 +18H2SO4
10CO2 ↑ + 12MnSO4 + 6K2SO4 + 28H2O
CH2=CH2 + KMnO4 +H2SO4 →
②加成反应:
(与H2、Br2、HX、H2O等)
CH3-CH=CH2 + H2 CH3CH2CH3
催化剂
CH2=CH2+Br2 CH2BrCH2Br
1,2-二溴乙烷
3、烯烃
(3)化学性质:
②加成反应:
(与H2、Br2、HX、H2O等)
CH2=CH2+H2O CH3CH2OH
催化剂
加压、加热
CH2=CH2+HBr CH3CH2Br
CH2=CH-CH3
CH2-CH-CH3
| |
H Br
CH2-CH-CH3
| |
Br H
主要产物
+ HBr
马氏规则,即氢多加氢。
加成反应:有机物分子中未饱和的碳原子跟其它原子或原子团直接结合生成别的物质的反应。
思考交流
3.思考:(1)如想制备一氯乙烷,是采用乙烷与氯气的取代反应还是用乙烯与氯化氢的加成反应,为什么?
(2)乙烯能使溴的CCl4褪色,甲同学认为发生了取代反应,乙同学认为发生了加成反应,哪一位同学正确呢?试设计实验验证。
(1)乙烯与HCl的加成反应副反应更少,产物相对纯净。
(2)方法:向反应后溶液中加AgNO3溶液或石蕊
现象:若发生取代反应则生成HBr,则有淡黄色沉淀或加石蕊会变红;
若发生加成反应,则无此现象。
3、烯烃
(3)化学性质:
②加成反应:
(与H2、Br2、HX、H2O等)
共轭二烯烃和1molBr2的1,2加成与1,4加成:
CH2=CH—CH=CH2 + 2Br2 →
CH2 — CH—CH — CH2
Br Br Br Br
1,2,3,4 – 四溴丁烷
CH2=CH-CH=CH2+Br2
CH2-CH-CH=CH2
| |
Br Br
1,2 加成
1,4 加成
CH2-CH-CH-CH2
1,2 Br
1,4 Br
(中间体)
3,4-二溴-1-丁烯
1,4-二溴-2-丁烯
1 2 3 4
CH2-CH=CH-CH2
| |
Br Br
3、烯烃
(3)化学性质:
②加聚反应:
nCH2==CH2
催化剂
CH2 CH2
[
]
n
加聚反应:通过加成反应聚合成高分子化合物的反应(加成聚合反应)。
单体
链节
聚合度
CH2 CH2
由相对分子质量小的化合物分子互相结合成相对分子质量大的高分子的反应叫做聚合反应。
加聚反应的通式:
nR1-CH==CH-R2
一定条件
CH CH
[
]
n
R1 R2
高聚物都是混合物
思考交流
4.思考:(1)聚乙烯能使溴水褪色吗?
(2)2.8g乙烯和聚乙烯的混合物中含有 个碳原子。
(3)写出下列物质的加聚反应方程式:
丙烯 2-甲基丙烯 2-丁烯 2,3-二甲基-2-丁烯
0.2NA
nCH2==CH-CH3
一定条件
CH2 CH
[
]
n
CH3
nCH3-CH==CH-CH3
一定条件
CH CH
[
]
n
CH3 CH3
nCH2==C-CH3
一定条件
CH2 C
[
]
n
CH3
CH3
CH3
CH3
CH3
nCH3-C == C -CH3
一定条件
C C
[
]
n
CH3 CH3
CH3
CH3
3、烯烃
(3)化学性质:
②加聚反应:
n CH2=C—CH=CH2
CH3
[ CH2—C=CH—CH2 ]n
CH3
催化剂
n CH2=CH—CH=CH2
[ CH2—CH=CH—CH2 ]n
催化剂
思考交流
5.写出下列反应式:
[ CH2-CH2-CH2-CH=CH-CH2 ] n
nCH2=CH2 + nCH2=CH-CH3
[ CH2-CH2-CH2-CH ] n
催化剂
CH3
|
或 [ CH2-CH2-CH-CH2 ] n
CH3
|
nCH2=CH2 + nCH2=CH-CH=CH2
催化剂
分子式
C2H6
结构式
键的类别
键角
键长(10-10米)
键能(KJ/mol)
空间各原子的位置
C—C
109?28ˊ
1.54
120?
1.33
C2H4
乙烷与乙烯的对比
348
2C和6H不在同一平面上
615
2C和4H在同一平面上
课堂练习
2.由下列数据:可判断丙烷的沸点可能是( )
A.高于-0.5℃ B.约是+30℃
C.约是-40℃ D.低于-89℃
C
C
物质
甲烷
乙烷
丁烷
戊烷
沸点
-162?C
-89?C
-1?C
+36?C
3.下列烷烃沸点最高的是( )
A.CH3CH2CH3 B.CH3CH2CH2CH3
C.CH3(CH2)3CH3 D.(CH3)2CHCH2CH3
二.烯烃的顺反异构
1、概念
由于碳碳双键不能旋转而导致分子中原子或原子团在空间的排列方式不同所产生的异构现象,称为顺反异构。
2、产生顺反异构的条件
双键两端的同一个碳原子上不能连有相同基团只有这样才会产生顺反异构体
C=C
A B
B A
C=C
A A
B C
C=C
A C
B D
C=C
A B
B C
观察学习
【思考】下列结构是否为顺反异构体?
顺-2-丁烯
C
H
C
H3C
H
CH3
C
H
C
H3C
H
CH3
反-2-丁烯
课堂练习
4.下列物质中没有顺反异构的是哪些?
(1)、 1,2-二氯乙烯
(2)、 1,2-二氯丙烯
(3)、 2-甲基-2-丁烯
(4)、 2-氯-2-丁烯
×
√
√
√
CHCl=CHCl
C=C
H Cl
Cl H
C=C
Cl Cl
H H
CHCl=CCl-CH3
CH3
CH3-C = CH -CH3
C=C
H Cl
Cl CH3
C=C
Cl Cl
H CH3
Cl
CH3-C = CH -CH3
C=C
CH3 Cl
Cl CH3
C=C
Cl H
CH3 CH3
5.始祖鸟烯(Pterodactyladiene)形状宛如一只展翅飞翔的鸟,其键线式结构表示如下,其中R1、R2为烷烃基。则下列有关始祖鸟烯的说法中正确的是( )
A.始祖鸟烯与乙烯互为同系物
B.若R1=R2=甲基,则其化学
式为C12H16
C.若R1=R2=甲基,则始祖鸟烯
的一氯代物有3种
D.始祖鸟烯既能使酸性高锰酸钾
溶液褪色,也能使溴水褪色,
则两反应的反应类型是相同的
C
C12H14
课堂练习
6.桶烯结构简式如下图所示,有关说法不正确的是( )
A.桶烯分子中所有的原子在同一平面上
B.桶烯在一定条件下能发生加聚反应
C.桶烯与苯乙烯(C6H5CH=CH2)
互为同分异构体
D.桶烯中的一个氢原子被氯原子取代,
所得产物只有两种
A
C8H8
课堂练习
拓展提升
CH2
CH
|
CH
CH2
+
CH2
CH2
CH2
CH
‖
CH
CH2
CH2
CH2
双烯合成
+
环己烯
拓展提升
用键线式表示为:
CH2
CH
|
CH
CH2
+
CH-CH3
CH-CH3
CH2
CH
‖
CH
CH2
CH-CH3
CH-CH3
+
(1)
(2)
(3)
CH3 CH3
| |
CH2=C— C=CH2
CH2=CH—CHO
拓展提升
课堂练习
5.1mol某链烃最多能和2molHCl发生加成反应,生成1mol氯代烷,1mol该氯代烷能和6molCl2发生取代反应,生成只含有碳元素和氯元素的氯代烃,该烃可能是( )
A.CH3CH=CH2
B. CH3C≡CH
C.CH3CH2C≡CH
D. CH2=CHCH=CH2
B
谢谢欣赏
