四川省成都邛崃市高埂中学2020-2021学年高一下学期开学考试化学试卷 Word版含答案
文档属性
| 名称 | 四川省成都邛崃市高埂中学2020-2021学年高一下学期开学考试化学试卷 Word版含答案 |

|
|
| 格式 | doc | ||
| 文件大小 | 719.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-11 00:00:00 | ||
图片预览



文档简介
高埂中学2020-2021学年度下期高2023届收心考试
化学试卷
考试时间:(60分钟) 满分:(100分)
2021年3月4日
可能用到的原子量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 P-31 S-32 Cl-35.5 K-39
Ca-40 V-51 Cr-52 Mn-55 Fe-56 Cu-64 Zn-65 Br-80 Ba-137
第I卷(共45分)
一、选择题:本题共15小题,每小题3分。在每小题给出的四个选项中,只有一个选项是符合题目要求的。
1. 化学让生活更美好,下列说法正确的是( )
A. 84消毒液和医用酒精均可杀灭新型冠状病毒,二者消毒原理相同
B. 使用铝合金可实现航天航空器、高速列车轻量化
C. 碳酸氢钠和碳酸钠均可用作食用碱和膨松剂
D. 废弃医用外科口罩应投入可回收垃圾箱
2.我国发行的第五套人民币中的5角硬币,材质是钢芯镀铜合金。其与纯铜相比较有关性质不正确的是( )
A.合金的硬度更大 B.合金的耐腐蚀性能更好 C.合金不能导电 D.合金的熔点更低
3. 进入秋冬季节后,雾霾问题逐渐凸显,从物质分类来看雾霾属于胶体。下列有关胶体的说法不正确的是( )
A. 胶体粒子既能透过滤纸也能透过半透膜
B. 胶体与溶液的本质区别是分散质粒子直径大小
C. 在豆浆里加入盐卤做豆腐利用了胶体聚沉的原理
D. 当可见光束照射蛋白质溶液时,在侧面可看到光亮的“通路”
4.每做一次焰色反应实验,都要用一种试剂洗净铂丝,这种试剂是( )
A.Na2CO3溶液? B.NaOH溶液?? C.硫酸??? D.盐酸
5.下列各组离子能在溶液中大量共存的是( )
A.、、、 B.、、、
C.、、、 D.、H+、、
6 某同学欲用Na2CO3固体配制480mL 0.10mol/L Na2CO3溶液,过程如图所示。其中错误的操作有( )
A. ①⑤ B. ①⑥⑦ C. ②⑦ D. ⑤⑥⑦
7. 下列关于钠及其化合物性质的叙述中,正确的是( )
A. 钠金属性强于铜,故可用钠与硫酸铜溶液反应置换铜
B. Na2O和Na2O2都能与酸反应生成盐和水,故都属于碱性氧化物
C. Na2O2能与H2O、CO2反应放出氧气,故可用作潜水艇中的供氧剂
D. 侯德榜制碱法是利用了Na2CO3的溶解度小于NaHCO3,而制备Na2CO3晶体
8.下列解释事实的方程式错误的是( )
A.大理石溶于盐酸:
B.用溶液“腐蚀”覆铜板:
C.在空气中变色:
D.用铝与溶液反应疏通污水管道:
9. 设表示阿伏加德罗常数的值。下列叙述错误的是( )
A. 中含有电子的数目为
B. 一定条件下,与足量完全反应,失去的电子数为
C. 的溶液中,含有的数为
D. 中含数为,则的摩尔质量为
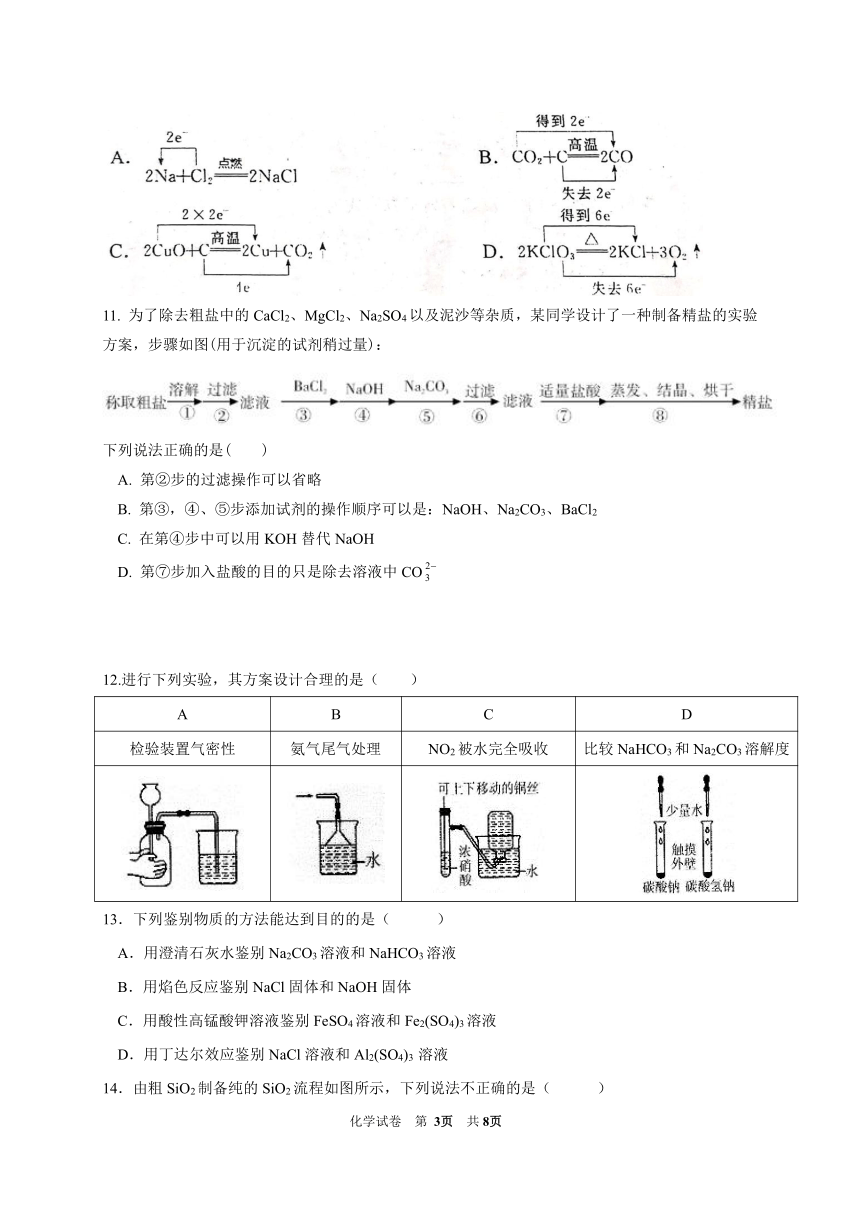
10.下列表示氧化还原反应中电子转移的方向和数目正确的是( )
11. 为了除去粗盐中的CaCl2、MgCl2、Na2SO4以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量):
下列说法正确的是( )
A. 第②步的过滤操作可以省略
B. 第③,④、⑤步添加试剂的操作顺序可以是:NaOH、Na2CO3、BaCl2
C. 在第④步中可以用KOH替代NaOH
D. 第⑦步加入盐酸的目的只是除去溶液中CO
12.进行下列实验,其方案设计合理的是( )
A B C D
检验装置气密性 氨气尾气处理 NO2被水完全吸收 比较NaHCO3和Na2CO3溶解度
13.下列鉴别物质的方法能达到目的的是( )
A.用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液
B.用焰色反应鉴别NaCl固体和NaOH固体
C.用酸性高锰酸钾溶液鉴别FeSO4溶液和Fe2(SO4)3溶液
D.用丁达尔效应鉴别NaCl溶液和Al2(SO4)3 溶液
由粗SiO2制备纯的SiO2流程如图所示,下列说法不正确的是( )
A.可用作木材防火剂
B.步骤Ⅱ的反应是Na2SiO3 + H2SO4 = H2SiO3 ↓+ Na2SO4
C.步骤Ⅱ中的稀硫酸可用CO2替代
D.若在实验室中完成步骤Ⅲ,一般在蒸发皿中进行
15. 某反应过程中存在、、、、和六种粒子,测得、的质量分数(w)随时间变化的曲线如图所示,下列判断错误的是( )
A. 被还原,发生还原反应
B. 还原性:
C. 被氧化为
D. 还原剂与氧化剂的物质的量之比为
第Ⅱ卷(共55分)
二、填空题。
16.(9分)下图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了、、、、KOH,图中相连的物质均可归为一类,相交部分A、B、C、D为相应的分类标准代号。
①相连的两种物质都是电解质的是 (填分类标准代号,下同),都是氧化物的是 。
②图中相连的两种物质能够相互反应的是 ,所属的基本反应类型是 反应。
③上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,则该反应的离子方程式为 。
④用洁净的烧杯取25mL蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热煮沸至液体呈红褐色,得到的分散系称为 ,要证明该分散系的实验方法是 。
17. (16分)从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物有重要用途,以下是氯元素的“价类二维图”的部分信息。请回答下列问题:
(1)根据图中信息写出Y、Z的化学式___________、___________。
(2)已知高氯酸()是强酸,写出高氯酸与氢氧化钠反应的离子方程式 。
(3)氯气既有氧化性又有还原性,结合上图说明理由______________________________________
(4)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。写出该反应的化学方程式____________________,
该反应中盐酸表现___________(填字母)。
A.酸性 B.氧化性 C.还原性
(5)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为,下列有关该反应说法不正确的是___________。
A.n(氧化剂):n(还原剂)=1:1 B.n(氧化剂):n(还原剂)=1:2
C.氧化性: D.既是氧化产物又是还原产物
(6)某游泳池常用来抑制藻类生长,工作人员一次错用消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了和,写出相应的化学方程式___________。
18. (16分)某废料铁泥主要成分为、FeO和Fe,其他杂质不与硫酸反应。现取wg废料铁泥提取,设计实验流程如下:
(1)写出步骤(I)中铁单质参与的有关反应的离子方程式 、 ,
分离溶液A和沉淀C的操作名称是___________。
(2)检验溶液A中含有应选用的试剂是___________
A.铁粉 B.溶液 C.酸性溶液 D.KSCN溶液
(3)步骤(Ⅱ)中加入溶液,在反应中作___________(填“氧化剂”或“还原剂”),反应的离子反应方程式为 。
(4)步骤(IV)中生成的固体的颜色是___________。
(5)若最终获得 ,则铁泥中铁元素的质量分数为___________。
19.(14分)工业上,向500℃左右的铁屑中通入Cl2生产无水氯化铁。已知:FeCl3熔点306℃、沸点316℃,易溶于水且有强烈的吸水性,能吸收空气里的水分而潮解。实验室模拟工业,制备无水FeCl3的装置如下图所示。请回答下列问题:
已知:高锰酸钾与盐酸在常温下反应能生成氯气和Mn2+。
(1)装置A中发生反应的离子方程式为 。
(2)装置B中的试剂是 。
(3)观察到 时(填实验现象),再点燃装置C处的酒精灯进行实验。
(4)装置C中玻璃丝的作用是 。
(5)装置E中发生反应的主要离子方程式为 。
(6)装置D和E可用装置F代替,则装置F中的试剂是 。
参考答案
BCADB BCBCB ABCDD
16.(9分)(1)①C、D (2分) B(1分) ② D(1分) 复分解(1分)
③(2分) ④胶体(1分) 丁达尔效应(1分)
17【答案】 (1). (2分) (2分) (2). (2分)
(3). 氯元素为0价,既有降低的趋势 ,又有升高的趋势。(或其他合理答案) (2分)
(4). (2分) AC (2分)
(5). B (2分) (6). (2分)
18【答案】 (1). (2分)、(2分) 过滤(2分)
(2) C(2分) (3)氧化性(2分) 2H++2Fe2++H2O2=2Fe3++2H2O (2分) (4). 红棕色(红色等) (2分)
(5). 或(或其他合理答案) (2分)
化学试卷 第 8页 共8页
化学试卷
考试时间:(60分钟) 满分:(100分)
2021年3月4日
可能用到的原子量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 P-31 S-32 Cl-35.5 K-39
Ca-40 V-51 Cr-52 Mn-55 Fe-56 Cu-64 Zn-65 Br-80 Ba-137
第I卷(共45分)
一、选择题:本题共15小题,每小题3分。在每小题给出的四个选项中,只有一个选项是符合题目要求的。
1. 化学让生活更美好,下列说法正确的是( )
A. 84消毒液和医用酒精均可杀灭新型冠状病毒,二者消毒原理相同
B. 使用铝合金可实现航天航空器、高速列车轻量化
C. 碳酸氢钠和碳酸钠均可用作食用碱和膨松剂
D. 废弃医用外科口罩应投入可回收垃圾箱
2.我国发行的第五套人民币中的5角硬币,材质是钢芯镀铜合金。其与纯铜相比较有关性质不正确的是( )
A.合金的硬度更大 B.合金的耐腐蚀性能更好 C.合金不能导电 D.合金的熔点更低
3. 进入秋冬季节后,雾霾问题逐渐凸显,从物质分类来看雾霾属于胶体。下列有关胶体的说法不正确的是( )
A. 胶体粒子既能透过滤纸也能透过半透膜
B. 胶体与溶液的本质区别是分散质粒子直径大小
C. 在豆浆里加入盐卤做豆腐利用了胶体聚沉的原理
D. 当可见光束照射蛋白质溶液时,在侧面可看到光亮的“通路”
4.每做一次焰色反应实验,都要用一种试剂洗净铂丝,这种试剂是( )
A.Na2CO3溶液? B.NaOH溶液?? C.硫酸??? D.盐酸
5.下列各组离子能在溶液中大量共存的是( )
A.、、、 B.、、、
C.、、、 D.、H+、、
6 某同学欲用Na2CO3固体配制480mL 0.10mol/L Na2CO3溶液,过程如图所示。其中错误的操作有( )
A. ①⑤ B. ①⑥⑦ C. ②⑦ D. ⑤⑥⑦
7. 下列关于钠及其化合物性质的叙述中,正确的是( )
A. 钠金属性强于铜,故可用钠与硫酸铜溶液反应置换铜
B. Na2O和Na2O2都能与酸反应生成盐和水,故都属于碱性氧化物
C. Na2O2能与H2O、CO2反应放出氧气,故可用作潜水艇中的供氧剂
D. 侯德榜制碱法是利用了Na2CO3的溶解度小于NaHCO3,而制备Na2CO3晶体
8.下列解释事实的方程式错误的是( )
A.大理石溶于盐酸:
B.用溶液“腐蚀”覆铜板:
C.在空气中变色:
D.用铝与溶液反应疏通污水管道:
9. 设表示阿伏加德罗常数的值。下列叙述错误的是( )
A. 中含有电子的数目为
B. 一定条件下,与足量完全反应,失去的电子数为
C. 的溶液中,含有的数为
D. 中含数为,则的摩尔质量为
10.下列表示氧化还原反应中电子转移的方向和数目正确的是( )
11. 为了除去粗盐中的CaCl2、MgCl2、Na2SO4以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量):
下列说法正确的是( )
A. 第②步的过滤操作可以省略
B. 第③,④、⑤步添加试剂的操作顺序可以是:NaOH、Na2CO3、BaCl2
C. 在第④步中可以用KOH替代NaOH
D. 第⑦步加入盐酸的目的只是除去溶液中CO
12.进行下列实验,其方案设计合理的是( )
A B C D
检验装置气密性 氨气尾气处理 NO2被水完全吸收 比较NaHCO3和Na2CO3溶解度
13.下列鉴别物质的方法能达到目的的是( )
A.用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液
B.用焰色反应鉴别NaCl固体和NaOH固体
C.用酸性高锰酸钾溶液鉴别FeSO4溶液和Fe2(SO4)3溶液
D.用丁达尔效应鉴别NaCl溶液和Al2(SO4)3 溶液
由粗SiO2制备纯的SiO2流程如图所示,下列说法不正确的是( )
A.可用作木材防火剂
B.步骤Ⅱ的反应是Na2SiO3 + H2SO4 = H2SiO3 ↓+ Na2SO4
C.步骤Ⅱ中的稀硫酸可用CO2替代
D.若在实验室中完成步骤Ⅲ,一般在蒸发皿中进行
15. 某反应过程中存在、、、、和六种粒子,测得、的质量分数(w)随时间变化的曲线如图所示,下列判断错误的是( )
A. 被还原,发生还原反应
B. 还原性:
C. 被氧化为
D. 还原剂与氧化剂的物质的量之比为
第Ⅱ卷(共55分)
二、填空题。
16.(9分)下图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了、、、、KOH,图中相连的物质均可归为一类,相交部分A、B、C、D为相应的分类标准代号。
①相连的两种物质都是电解质的是 (填分类标准代号,下同),都是氧化物的是 。
②图中相连的两种物质能够相互反应的是 ,所属的基本反应类型是 反应。
③上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,则该反应的离子方程式为 。
④用洁净的烧杯取25mL蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热煮沸至液体呈红褐色,得到的分散系称为 ,要证明该分散系的实验方法是 。
17. (16分)从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物有重要用途,以下是氯元素的“价类二维图”的部分信息。请回答下列问题:
(1)根据图中信息写出Y、Z的化学式___________、___________。
(2)已知高氯酸()是强酸,写出高氯酸与氢氧化钠反应的离子方程式 。
(3)氯气既有氧化性又有还原性,结合上图说明理由______________________________________
(4)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。写出该反应的化学方程式____________________,
该反应中盐酸表现___________(填字母)。
A.酸性 B.氧化性 C.还原性
(5)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为,下列有关该反应说法不正确的是___________。
A.n(氧化剂):n(还原剂)=1:1 B.n(氧化剂):n(还原剂)=1:2
C.氧化性: D.既是氧化产物又是还原产物
(6)某游泳池常用来抑制藻类生长,工作人员一次错用消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了和,写出相应的化学方程式___________。
18. (16分)某废料铁泥主要成分为、FeO和Fe,其他杂质不与硫酸反应。现取wg废料铁泥提取,设计实验流程如下:
(1)写出步骤(I)中铁单质参与的有关反应的离子方程式 、 ,
分离溶液A和沉淀C的操作名称是___________。
(2)检验溶液A中含有应选用的试剂是___________
A.铁粉 B.溶液 C.酸性溶液 D.KSCN溶液
(3)步骤(Ⅱ)中加入溶液,在反应中作___________(填“氧化剂”或“还原剂”),反应的离子反应方程式为 。
(4)步骤(IV)中生成的固体的颜色是___________。
(5)若最终获得 ,则铁泥中铁元素的质量分数为___________。
19.(14分)工业上,向500℃左右的铁屑中通入Cl2生产无水氯化铁。已知:FeCl3熔点306℃、沸点316℃,易溶于水且有强烈的吸水性,能吸收空气里的水分而潮解。实验室模拟工业,制备无水FeCl3的装置如下图所示。请回答下列问题:
已知:高锰酸钾与盐酸在常温下反应能生成氯气和Mn2+。
(1)装置A中发生反应的离子方程式为 。
(2)装置B中的试剂是 。
(3)观察到 时(填实验现象),再点燃装置C处的酒精灯进行实验。
(4)装置C中玻璃丝的作用是 。
(5)装置E中发生反应的主要离子方程式为 。
(6)装置D和E可用装置F代替,则装置F中的试剂是 。
参考答案
BCADB BCBCB ABCDD
16.(9分)(1)①C、D (2分) B(1分) ② D(1分) 复分解(1分)
③(2分) ④胶体(1分) 丁达尔效应(1分)
17【答案】 (1). (2分) (2分) (2). (2分)
(3). 氯元素为0价,既有降低的趋势 ,又有升高的趋势。(或其他合理答案) (2分)
(4). (2分) AC (2分)
(5). B (2分) (6). (2分)
18【答案】 (1). (2分)、(2分) 过滤(2分)
(2) C(2分) (3)氧化性(2分) 2H++2Fe2++H2O2=2Fe3++2H2O (2分) (4). 红棕色(红色等) (2分)
(5). 或(或其他合理答案) (2分)
化学试卷 第 8页 共8页
同课章节目录
