2020~2021学年鲁教版九年级下册 7.4酸碱中和反应基础训练(含答案)
文档属性
| 名称 | 2020~2021学年鲁教版九年级下册 7.4酸碱中和反应基础训练(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 105.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-12 00:00:00 | ||
图片预览

文档简介
鲁教版第7章7.4酸碱中和反应基础训练
一、选择题:
1、新鲜魔芋在去皮时出现的白色汁液内含有一种碱性物质--皂角甙,皮肤沾上它会奇痒难忍。下列厨房中的物质止痒效果最好的是( )
A.料酒 B.食醋 C.纯碱溶液 D.食盐水
2、如图是探究分子运动的实验。下列现象与结论错误的是( )
A.浓盐酸具有挥发性
B.分子在不断运动
C.乙烧杯溶液的颜色会改变
D.甲、乙、丙烧杯内溶液的颜色都会改变
3、从防止空气污染考虑,下列实验应在通风橱中进行的是( )
A.镁的燃烧 B.燃烧条件的探究
C.二氧化碳的实验室制取 D.酸碱中和实验
4、化学与生产、生活息息相关,以下对应物质及用途不正确的是( )
A.可用pH试纸测得食醋的pH=2.9
B.可用熟石灰改良酸性土壤
C.可利用洗洁精的乳化作用去除油污
D.可用氢氧化铝治疗胃酸过多
5、下列反应,属于中和反应的是( )
A.Zn+2HCl═ZnCl2+H2↑
B.CuO+2HCl═CuCl2+H2O
C.Cu(OH)2+H2SO4═CuSO4+2H2O
D.SO2+2NaOH═Na2SO3+H2O
6、下列生活经验没有应用酸碱反应原理的是( )
A.用熟石灰改良酸性土壤
B.用氢氧化钠溶液洗涤石油产品中的残留硫酸
C.用氢氧化铝治疗胃酸过多
D.用生石灰作干燥剂
7、向滴有酚酞的氢氧化钠溶液中,逐滴滴加稀盐酸至过量,下列有关说法正确的是( )
A.溶液由无色变为红色
B.溶液的pH先升高,后降低
C.氢氧化钠与盐酸的反应不是复分解反应
D.氯化钠的质量逐渐增加,最后保持不变
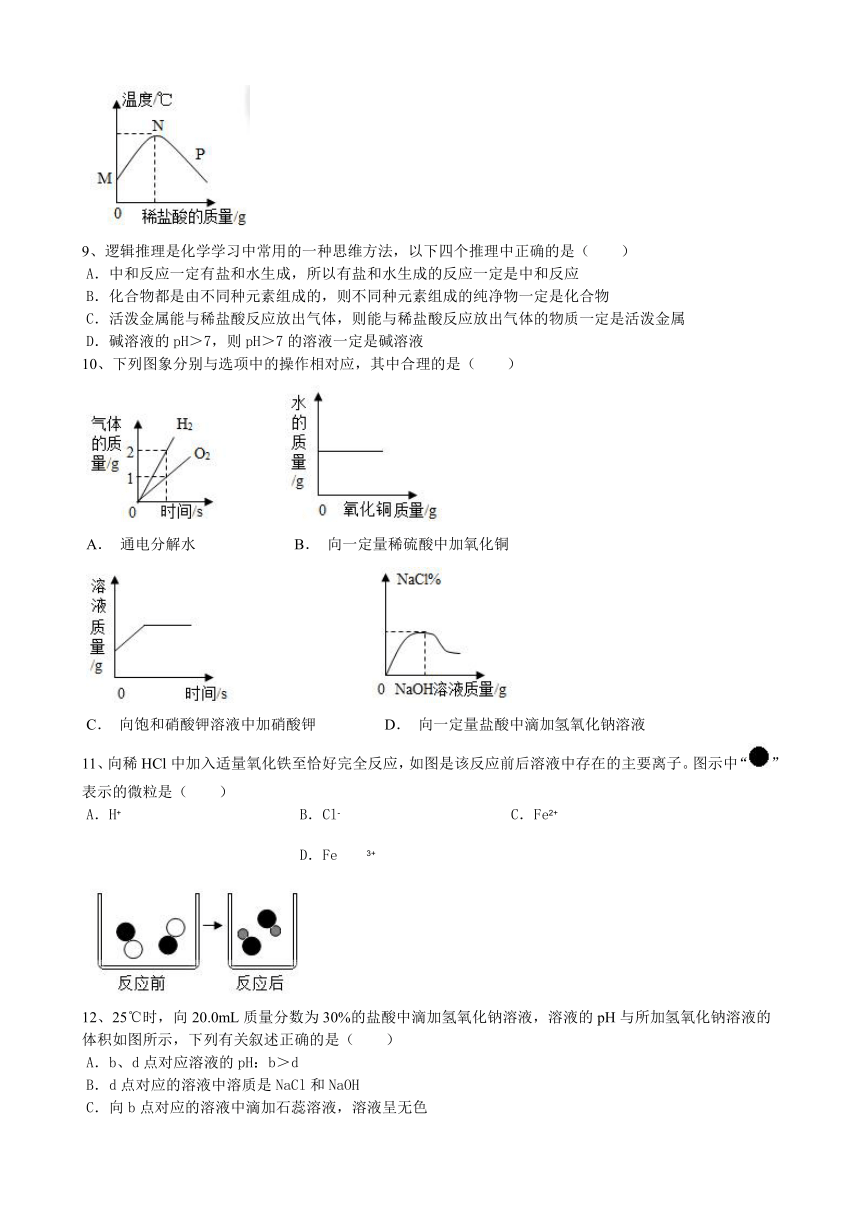
8、一定温度下,向含有适量酚酞溶液的氢氧化钠溶液中慢慢滴加稀盐酸,溶液温度随加入稀盐酸的质量如图所示。下列叙述不正确的是( )
A.N点时溶液的pH最大
B.N点表示氢氧化钠与稀盐酸恰好完全反应
C.M点时溶液呈红色
D.P点时,溶液中除酚酞外还含有两种溶质
9、逻辑推理是化学学习中常用的一种思维方法,以下四个推理中正确的是( )
A.中和反应一定有盐和水生成,所以有盐和水生成的反应一定是中和反应
B.化合物都是由不同种元素组成的,则不同种元素组成的纯净物一定是化合物
C.活泼金属能与稀盐酸反应放出气体,则能与稀盐酸反应放出气体的物质一定是活泼金属
D.碱溶液的pH>7,则pH>7的溶液一定是碱溶液
10、下列图象分别与选项中的操作相对应,其中合理的是( )
A. 通电分解水 B. 向一定量稀硫酸中加氧化铜
C. 向饱和硝酸钾溶液中加硝酸钾 D. 向一定量盐酸中滴加氢氧化钠溶液
11、向稀HCl中加入适量氧化铁至恰好完全反应,如图是该反应前后溶液中存在的主要离子。图示中“”表示的微粒是( )
A.H+ B.Cl- C.Fe2+ D.Fe3+
12、25℃时,向20.0mL质量分数为30%的盐酸中滴加氢氧化钠溶液,溶液的pH与所加氢氧化钠溶液的体积如图所示,下列有关叙述正确的是( )
A.b、d点对应溶液的pH:b>d
B.d点对应的溶液中溶质是NaCl和NaOH
C.向b点对应的溶液中滴加石蕊溶液,溶液呈无色
D.所用氢氧化钠溶液的质量分数一定为30%
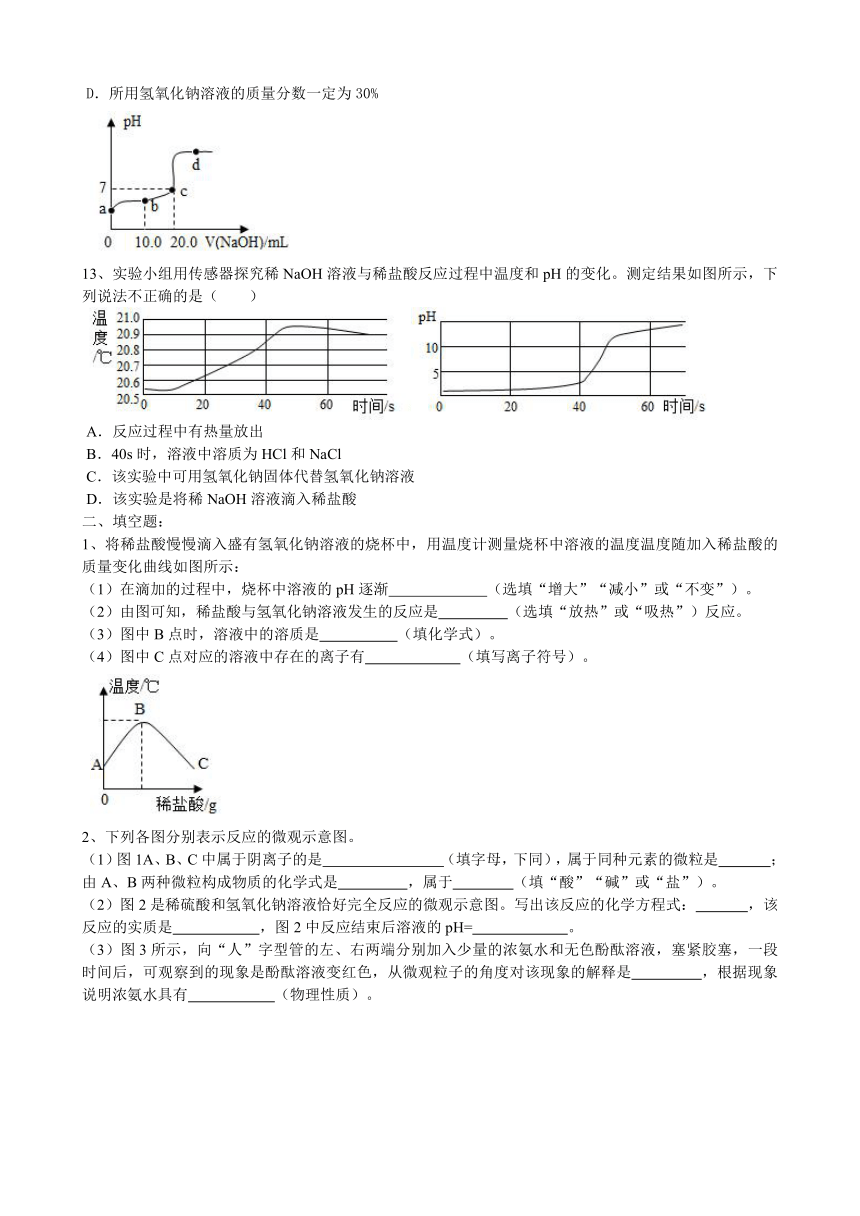
13、实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变化。测定结果如图所示,下列说法不正确的是( )
A.反应过程中有热量放出
B.40s时,溶液中溶质为HCl和NaCl
C.该实验中可用氢氧化钠固体代替氢氧化钠溶液
D.该实验是将稀NaOH溶液滴入稀盐酸
二、填空题:
1、将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度温度随加入稀盐酸的质量变化曲线如图所示:
(1)在滴加的过程中,烧杯中溶液的pH逐渐 (选填“增大”“减小”或“不变”)。
(2)由图可知,稀盐酸与氢氧化钠溶液发生的反应是 (选填“放热”或“吸热”)反应。
(3)图中B点时,溶液中的溶质是 (填化学式)。
(4)图中C点对应的溶液中存在的离子有 (填写离子符号)。
2、下列各图分别表示反应的微观示意图。
(1)图1A、B、C中属于阴离子的是 (填字母,下同),属于同种元素的微粒是 ;由?A、B?两种微粒构成物质的化学式是 ,属于 (填“酸”“碱”或“盐”)。
(2)图2是稀硫酸和氢氧化钠溶液恰好完全反应的微观示意图。写出该反应的化学方程式: ,该反应的实质是 ,图2中反应结束后溶液的pH= 。
(3)图3所示,向“人”字型管的左、右两端分别加入少量的浓氨水和无色酚酞溶液,塞紧胶塞,一段时间后,可观察到的现象是酚酞溶液变红色,从微观粒子的角度对该现象的解释是 ,根据现象说明浓氨水具有 (物理性质)。
3、中和反应是重要的化学反应。某同学利用图1装置研究稀盐酸与氢氧化钠溶液反应的过程,并用pH和温度传感器测量反应过程中相关物理量的变化情况,得到图2和图3。
(1)根据图2可知最后烧杯中的溶液的溶质是 (用化学式表示)。
(2)该实验操作是将 滴加到 中。图3中V的数值最接近 (填“6”、“12”或“16”)。
(3)下列说法错误的是 。
A.图2中b点所示溶液中的溶质是NaCl和NaOH
B.取图2中d点所示溶液加热蒸干所得固体为纯净物
C.图2中c→d所示溶液中NaCl的质量不断增加
D.图3中e→f变化趋势可说明该反应是放热反应
4、某实验小组的同学为了探究稀盐酸与NaOH能否发生化学反应,设计了如下的方案:
(1)方案一:测定溶液pH的变化证明二者发生化学反应
如图1为用pH传感器测定两溶液混合时pH的变化曲线,测定的pH值结果为 ,则能说明二者发生了化学反应。下列说法中不正确的是 。
A.该实验是将氢氧化钠溶液滴加到稀盐酸中
B.a点溶液中所含溶质为NaCl、HCl
C.b点溶液中所含溶质为NaCl、NaOH
D.从b点到c点的变化过程中,没有发生化学反应
(2)方案二:借助反应前后的温度变化证明二者发生化学反应
某同学在不使用温度计的情况下,通过如图2所示装置进行实验,观察到红色墨水向右移动。有的同学提出,该现象不足以证明NaOH与稀盐酸发生了化学反应,他的理由是: 。
(3)方案三:利用图3实验证明二者发生化学反应。
整个实验过程中无明显现象,请写出步骤Ⅱ中所加试剂为 。图4为整个反应过程中的微观实质,反应中数目减少的离子是 (填微粒符号,下同),生成的新微粒是 。
参考答案
一、选择题:
1、B 2、D 3、B 4、A 5、C 6、D 7、D 8、A 9、B 10、D
11、B 12、B 13、C
二、填空题:
1、答案:答案为:
(1)减小;
(2)放热;
(3)NaCl;
(4)H+、Na+、Cl-。
2、答案为:(1)B; BC; MgCl2; 盐;
(2)2NaOH+H2SO4=Na2SO4+2H2O; H++OH-=H2O;7;
(3)氨分子不断运动到酚酞试液中,氨分子溶于水显碱性,碱性溶液使酚酞变红; 挥发性。
3、解:(1)根据图2可知溶液显酸性,最后烧杯中的溶液的溶质是反应生成的氯化钠和过量的氯化氢。
故填:NaCl、HCl。
(2)反应前溶液pH大于7,显碱性,该实验操作是将盐酸滴加到氢氧化钠溶液中;
图3中V的数值最接近12,是因为加入12mL稀盐酸时,恰好完全反应,放热最多。
故填:盐酸;NaOH溶液;12。
(3)A.图2中b点所示溶液中的溶质是反应生成的NaCl和过量的NaOH,该选项说法正确;
B.取图2中d点所示溶液加热蒸干所得固体为纯净物,是因为氯化氢在蒸发过程中逸出,该选项说法正确;
C.图2中c→d所示溶液中,没有发生化学反应,只是不断加入稀盐酸,NaCl的质量不变,该选项说法不正确;
D.图3中e→f变化趋势可说明该反应是放热反应,该选项说法正确。
故填:C。
4、答案:(1)pH<7;ABC;
(2)氢氧化钠固体溶于水放热,也能使红色墨水向右移动;
(3)无色酚酞试液(或硫酸铜溶液);H+、OH-;H2O。
一、选择题:
1、新鲜魔芋在去皮时出现的白色汁液内含有一种碱性物质--皂角甙,皮肤沾上它会奇痒难忍。下列厨房中的物质止痒效果最好的是( )
A.料酒 B.食醋 C.纯碱溶液 D.食盐水
2、如图是探究分子运动的实验。下列现象与结论错误的是( )
A.浓盐酸具有挥发性
B.分子在不断运动
C.乙烧杯溶液的颜色会改变
D.甲、乙、丙烧杯内溶液的颜色都会改变
3、从防止空气污染考虑,下列实验应在通风橱中进行的是( )
A.镁的燃烧 B.燃烧条件的探究
C.二氧化碳的实验室制取 D.酸碱中和实验
4、化学与生产、生活息息相关,以下对应物质及用途不正确的是( )
A.可用pH试纸测得食醋的pH=2.9
B.可用熟石灰改良酸性土壤
C.可利用洗洁精的乳化作用去除油污
D.可用氢氧化铝治疗胃酸过多
5、下列反应,属于中和反应的是( )
A.Zn+2HCl═ZnCl2+H2↑
B.CuO+2HCl═CuCl2+H2O
C.Cu(OH)2+H2SO4═CuSO4+2H2O
D.SO2+2NaOH═Na2SO3+H2O
6、下列生活经验没有应用酸碱反应原理的是( )
A.用熟石灰改良酸性土壤
B.用氢氧化钠溶液洗涤石油产品中的残留硫酸
C.用氢氧化铝治疗胃酸过多
D.用生石灰作干燥剂
7、向滴有酚酞的氢氧化钠溶液中,逐滴滴加稀盐酸至过量,下列有关说法正确的是( )
A.溶液由无色变为红色
B.溶液的pH先升高,后降低
C.氢氧化钠与盐酸的反应不是复分解反应
D.氯化钠的质量逐渐增加,最后保持不变
8、一定温度下,向含有适量酚酞溶液的氢氧化钠溶液中慢慢滴加稀盐酸,溶液温度随加入稀盐酸的质量如图所示。下列叙述不正确的是( )
A.N点时溶液的pH最大
B.N点表示氢氧化钠与稀盐酸恰好完全反应
C.M点时溶液呈红色
D.P点时,溶液中除酚酞外还含有两种溶质
9、逻辑推理是化学学习中常用的一种思维方法,以下四个推理中正确的是( )
A.中和反应一定有盐和水生成,所以有盐和水生成的反应一定是中和反应
B.化合物都是由不同种元素组成的,则不同种元素组成的纯净物一定是化合物
C.活泼金属能与稀盐酸反应放出气体,则能与稀盐酸反应放出气体的物质一定是活泼金属
D.碱溶液的pH>7,则pH>7的溶液一定是碱溶液
10、下列图象分别与选项中的操作相对应,其中合理的是( )
A. 通电分解水 B. 向一定量稀硫酸中加氧化铜
C. 向饱和硝酸钾溶液中加硝酸钾 D. 向一定量盐酸中滴加氢氧化钠溶液
11、向稀HCl中加入适量氧化铁至恰好完全反应,如图是该反应前后溶液中存在的主要离子。图示中“”表示的微粒是( )
A.H+ B.Cl- C.Fe2+ D.Fe3+
12、25℃时,向20.0mL质量分数为30%的盐酸中滴加氢氧化钠溶液,溶液的pH与所加氢氧化钠溶液的体积如图所示,下列有关叙述正确的是( )
A.b、d点对应溶液的pH:b>d
B.d点对应的溶液中溶质是NaCl和NaOH
C.向b点对应的溶液中滴加石蕊溶液,溶液呈无色
D.所用氢氧化钠溶液的质量分数一定为30%
13、实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变化。测定结果如图所示,下列说法不正确的是( )
A.反应过程中有热量放出
B.40s时,溶液中溶质为HCl和NaCl
C.该实验中可用氢氧化钠固体代替氢氧化钠溶液
D.该实验是将稀NaOH溶液滴入稀盐酸
二、填空题:
1、将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度温度随加入稀盐酸的质量变化曲线如图所示:
(1)在滴加的过程中,烧杯中溶液的pH逐渐 (选填“增大”“减小”或“不变”)。
(2)由图可知,稀盐酸与氢氧化钠溶液发生的反应是 (选填“放热”或“吸热”)反应。
(3)图中B点时,溶液中的溶质是 (填化学式)。
(4)图中C点对应的溶液中存在的离子有 (填写离子符号)。
2、下列各图分别表示反应的微观示意图。
(1)图1A、B、C中属于阴离子的是 (填字母,下同),属于同种元素的微粒是 ;由?A、B?两种微粒构成物质的化学式是 ,属于 (填“酸”“碱”或“盐”)。
(2)图2是稀硫酸和氢氧化钠溶液恰好完全反应的微观示意图。写出该反应的化学方程式: ,该反应的实质是 ,图2中反应结束后溶液的pH= 。
(3)图3所示,向“人”字型管的左、右两端分别加入少量的浓氨水和无色酚酞溶液,塞紧胶塞,一段时间后,可观察到的现象是酚酞溶液变红色,从微观粒子的角度对该现象的解释是 ,根据现象说明浓氨水具有 (物理性质)。
3、中和反应是重要的化学反应。某同学利用图1装置研究稀盐酸与氢氧化钠溶液反应的过程,并用pH和温度传感器测量反应过程中相关物理量的变化情况,得到图2和图3。
(1)根据图2可知最后烧杯中的溶液的溶质是 (用化学式表示)。
(2)该实验操作是将 滴加到 中。图3中V的数值最接近 (填“6”、“12”或“16”)。
(3)下列说法错误的是 。
A.图2中b点所示溶液中的溶质是NaCl和NaOH
B.取图2中d点所示溶液加热蒸干所得固体为纯净物
C.图2中c→d所示溶液中NaCl的质量不断增加
D.图3中e→f变化趋势可说明该反应是放热反应
4、某实验小组的同学为了探究稀盐酸与NaOH能否发生化学反应,设计了如下的方案:
(1)方案一:测定溶液pH的变化证明二者发生化学反应
如图1为用pH传感器测定两溶液混合时pH的变化曲线,测定的pH值结果为 ,则能说明二者发生了化学反应。下列说法中不正确的是 。
A.该实验是将氢氧化钠溶液滴加到稀盐酸中
B.a点溶液中所含溶质为NaCl、HCl
C.b点溶液中所含溶质为NaCl、NaOH
D.从b点到c点的变化过程中,没有发生化学反应
(2)方案二:借助反应前后的温度变化证明二者发生化学反应
某同学在不使用温度计的情况下,通过如图2所示装置进行实验,观察到红色墨水向右移动。有的同学提出,该现象不足以证明NaOH与稀盐酸发生了化学反应,他的理由是: 。
(3)方案三:利用图3实验证明二者发生化学反应。
整个实验过程中无明显现象,请写出步骤Ⅱ中所加试剂为 。图4为整个反应过程中的微观实质,反应中数目减少的离子是 (填微粒符号,下同),生成的新微粒是 。
参考答案
一、选择题:
1、B 2、D 3、B 4、A 5、C 6、D 7、D 8、A 9、B 10、D
11、B 12、B 13、C
二、填空题:
1、答案:答案为:
(1)减小;
(2)放热;
(3)NaCl;
(4)H+、Na+、Cl-。
2、答案为:(1)B; BC; MgCl2; 盐;
(2)2NaOH+H2SO4=Na2SO4+2H2O; H++OH-=H2O;7;
(3)氨分子不断运动到酚酞试液中,氨分子溶于水显碱性,碱性溶液使酚酞变红; 挥发性。
3、解:(1)根据图2可知溶液显酸性,最后烧杯中的溶液的溶质是反应生成的氯化钠和过量的氯化氢。
故填:NaCl、HCl。
(2)反应前溶液pH大于7,显碱性,该实验操作是将盐酸滴加到氢氧化钠溶液中;
图3中V的数值最接近12,是因为加入12mL稀盐酸时,恰好完全反应,放热最多。
故填:盐酸;NaOH溶液;12。
(3)A.图2中b点所示溶液中的溶质是反应生成的NaCl和过量的NaOH,该选项说法正确;
B.取图2中d点所示溶液加热蒸干所得固体为纯净物,是因为氯化氢在蒸发过程中逸出,该选项说法正确;
C.图2中c→d所示溶液中,没有发生化学反应,只是不断加入稀盐酸,NaCl的质量不变,该选项说法不正确;
D.图3中e→f变化趋势可说明该反应是放热反应,该选项说法正确。
故填:C。
4、答案:(1)pH<7;ABC;
(2)氢氧化钠固体溶于水放热,也能使红色墨水向右移动;
(3)无色酚酞试液(或硫酸铜溶液);H+、OH-;H2O。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
