专题6 第1单元 第2课时 影响化学反应速率的因素
文档属性
| 名称 | 专题6 第1单元 第2课时 影响化学反应速率的因素 |
|
|
| 格式 | zip | ||
| 文件大小 | 906.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-13 00:00:00 | ||
图片预览




文档简介
(共18张PPT)
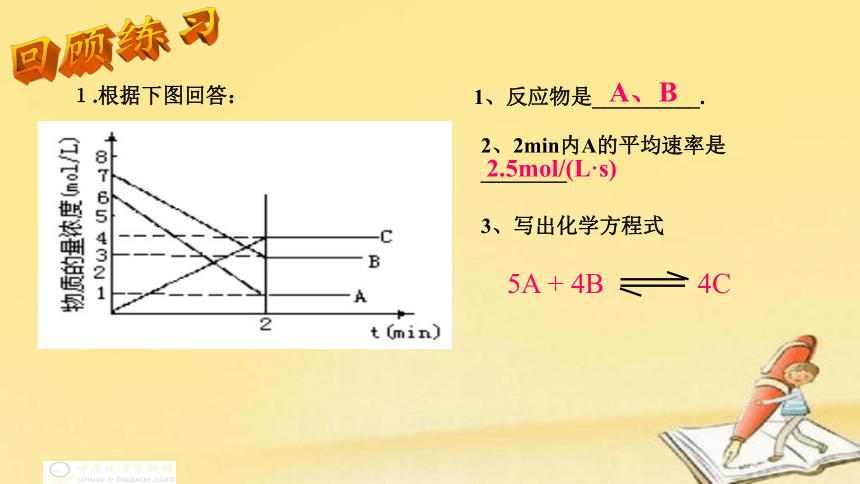
1.根据下图回答:
1、反应物是__________.
2、2min内A的平均速率是________
3、写出化学方程式
A、B
2.5mol/(L·s)
回顾练习
5A
+
4B
4C
有利的——越快越好!
有害的——越慢越好!
能否控制化学反应速率呢?
①一次性快餐盒、聚乙烯等塑料制品分解需要几百年。
②汽车尾气NO、CO反应能生成N2、CO2,但汽车尾气中仍有NO、CO排放,因为反应太慢了
①橡胶老化,钢铁腐蚀;
②“云龙陛石”近几十年腐蚀加快;
③乐山大佛近几十年腐蚀特别严重。
专题6
化学反应与能量变化
第一单元 化学反应速率与反应限度
第2课时 影响化学反应速率的因素
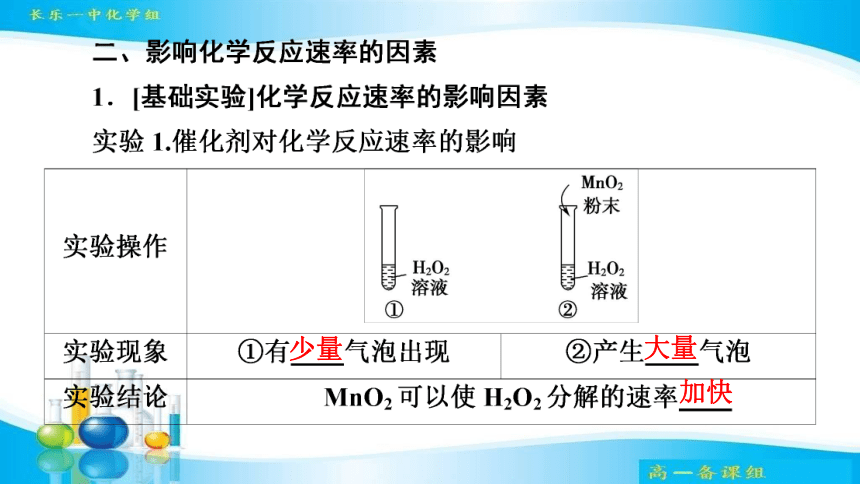
少量
大量
加快
减小
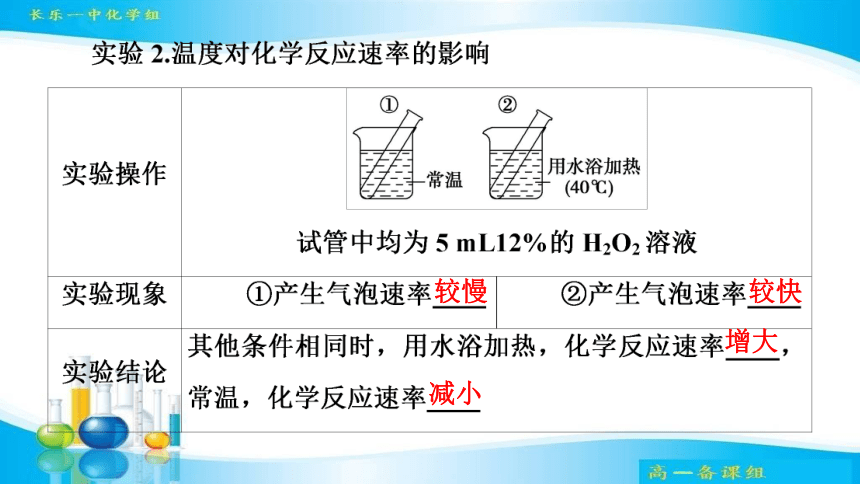
较慢
较快
增大
较慢
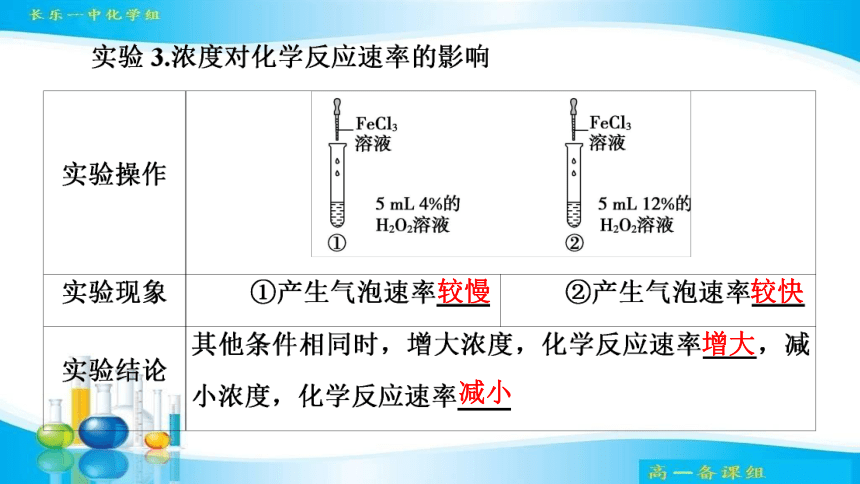
较快
增大
减小
增大
影响
外因
化学反应速率
增大反应物浓度
升高温度
使用正催化剂
增大反应物接触面积
加快
影响化学反应速率的因素
加快
加快
加快
原因:对气体来说,若其他条件不变,增大压强,就是增加单位体积的反应物的物质的量,即增加反应物的浓度,因而可以增大化学反应的速率。
请试根据浓度对化学反应速率的影响推出压强对化学反应速率的影响情况
结论:对于有气体参加的反应,若其他条件不变,增大压强,气体体积缩小,浓度增大,反应速率加快;减小压强,反应速率减慢。
压强对于反应速率的影响是通过对浓度的影响实现的
P增大→c成比例增大,P减小→c成比例减小
压强只对于有气体参加的反应的速率有影响
压强
对于气体有下列几种情况:
1、恒温时:增大压强→体积减少→反应物浓度c增大→反应速率增大
2、恒容时:
A、充入气体反应物→反应物浓度增大→总压增大→反应速率增大;
B、充入“无关气体”(如He)→引起总压增大,但各反应物的分压不变,各物质的浓度不变→反应速率不变
3、恒压时:充入“无关气体”(如He)→引起体积增大,
→各反应物浓度减少→反应速率减慢。
例:对于反应N2+O2=2NO在密闭容器中进行,下列条件哪些不能加快该反应的化学反应速率(
)
A、缩小体积使压强增大
B、体积不变充入
N2
使压强增大
C、体积不变充入
O2使压强增大
D、使体积增大到原来的2倍
E、体积不变充入氦气使压强增大
压强对反应速率的影响
DE
压强
影响
外因
化学反应速率
增大反应物浓度
升高温度
使用正催化剂
增大反应物接触面积
增大压强(有气体反应物,体积减小)
加快
加快
小结:影响化学反应速率的因素
加快
加快
加快
其他如光照、反应物固体的颗粒大小、电磁波、超声波、溶剂的性质等,也会对化学反应的速率产生影响。
a、对于固体或液体纯净物的反应物,一般情况下其浓度是常数,因此改变它们的量一般不会改变化学反应速率。
b、随着化学反应的进行,反应物的浓度会逐渐减小,因此一般反应速率也会逐渐减小。
注意!
?应用1:
一定条件下,在CaCO3(块状)+2HCl=CaCl2+H2O+CO2?
反应中,为了加快反应的速率,下列那些方法可行(
)
A、增加HCl的浓度
B、加水
C、增加同浓度盐酸的量
D、改加CaCO3粉末
AD
(P5)为了研究碳酸钙与稀盐酸的反应速率某同学根据反应中生成CO2
的体积随时间的变化情况,绘制出了右图所示的曲线。请分析讨论:
(1)在0
~
t1
、t1
~t2
、t2~t3
各相同的时间段里,反应速率最大的是
时间段,收集气体最多的是
时间段。
(2)试分析上述三个时间段里,反应速率不同的可能原因。
(3)在t4后,为什么收集到的气体的体积不再增加?
t1
~t2
t1
~t2
⑵开始时c(H+)较大,故此时反应的反应速率较大;
t1
~
t2由于反应放热、体系温度升高,所以速率迅速增大;最后是由于c(H+)减小,反应速率减慢。
⑶
c(H+)为0
学以致用
将一定浓度的盐酸倒入碳酸钙中,若作如下改变的情况,其中能使最初的化学反应速率增大的是
(
)
A、盐酸的浓度不变,而使盐酸的用量一倍
B、盐酸的浓度增大一倍,而使盐酸的用量减少到原来一半
C、盐酸的浓度和用量都不变,增加碳酸钙的量
D、盐酸和碳酸钙不变,增大压强一倍
E、加入CaCl2溶液
F、加入CaCl2固体
G、将CaCO3固体用CaCO3粉末代替
BG
作业:
1、课本P9第3题;
2、《名校学案》P3基础演练(一)化学反应速率
1.根据下图回答:
1、反应物是__________.
2、2min内A的平均速率是________
3、写出化学方程式
A、B
2.5mol/(L·s)
回顾练习
5A
+
4B
4C
有利的——越快越好!
有害的——越慢越好!
能否控制化学反应速率呢?
①一次性快餐盒、聚乙烯等塑料制品分解需要几百年。
②汽车尾气NO、CO反应能生成N2、CO2,但汽车尾气中仍有NO、CO排放,因为反应太慢了
①橡胶老化,钢铁腐蚀;
②“云龙陛石”近几十年腐蚀加快;
③乐山大佛近几十年腐蚀特别严重。
专题6
化学反应与能量变化
第一单元 化学反应速率与反应限度
第2课时 影响化学反应速率的因素
少量
大量
加快
减小
较慢
较快
增大
较慢
较快
增大
减小
增大
影响
外因
化学反应速率
增大反应物浓度
升高温度
使用正催化剂
增大反应物接触面积
加快
影响化学反应速率的因素
加快
加快
加快
原因:对气体来说,若其他条件不变,增大压强,就是增加单位体积的反应物的物质的量,即增加反应物的浓度,因而可以增大化学反应的速率。
请试根据浓度对化学反应速率的影响推出压强对化学反应速率的影响情况
结论:对于有气体参加的反应,若其他条件不变,增大压强,气体体积缩小,浓度增大,反应速率加快;减小压强,反应速率减慢。
压强对于反应速率的影响是通过对浓度的影响实现的
P增大→c成比例增大,P减小→c成比例减小
压强只对于有气体参加的反应的速率有影响
压强
对于气体有下列几种情况:
1、恒温时:增大压强→体积减少→反应物浓度c增大→反应速率增大
2、恒容时:
A、充入气体反应物→反应物浓度增大→总压增大→反应速率增大;
B、充入“无关气体”(如He)→引起总压增大,但各反应物的分压不变,各物质的浓度不变→反应速率不变
3、恒压时:充入“无关气体”(如He)→引起体积增大,
→各反应物浓度减少→反应速率减慢。
例:对于反应N2+O2=2NO在密闭容器中进行,下列条件哪些不能加快该反应的化学反应速率(
)
A、缩小体积使压强增大
B、体积不变充入
N2
使压强增大
C、体积不变充入
O2使压强增大
D、使体积增大到原来的2倍
E、体积不变充入氦气使压强增大
压强对反应速率的影响
DE
压强
影响
外因
化学反应速率
增大反应物浓度
升高温度
使用正催化剂
增大反应物接触面积
增大压强(有气体反应物,体积减小)
加快
加快
小结:影响化学反应速率的因素
加快
加快
加快
其他如光照、反应物固体的颗粒大小、电磁波、超声波、溶剂的性质等,也会对化学反应的速率产生影响。
a、对于固体或液体纯净物的反应物,一般情况下其浓度是常数,因此改变它们的量一般不会改变化学反应速率。
b、随着化学反应的进行,反应物的浓度会逐渐减小,因此一般反应速率也会逐渐减小。
注意!
?应用1:
一定条件下,在CaCO3(块状)+2HCl=CaCl2+H2O+CO2?
反应中,为了加快反应的速率,下列那些方法可行(
)
A、增加HCl的浓度
B、加水
C、增加同浓度盐酸的量
D、改加CaCO3粉末
AD
(P5)为了研究碳酸钙与稀盐酸的反应速率某同学根据反应中生成CO2
的体积随时间的变化情况,绘制出了右图所示的曲线。请分析讨论:
(1)在0
~
t1
、t1
~t2
、t2~t3
各相同的时间段里,反应速率最大的是
时间段,收集气体最多的是
时间段。
(2)试分析上述三个时间段里,反应速率不同的可能原因。
(3)在t4后,为什么收集到的气体的体积不再增加?
t1
~t2
t1
~t2
⑵开始时c(H+)较大,故此时反应的反应速率较大;
t1
~
t2由于反应放热、体系温度升高,所以速率迅速增大;最后是由于c(H+)减小,反应速率减慢。
⑶
c(H+)为0
学以致用
将一定浓度的盐酸倒入碳酸钙中,若作如下改变的情况,其中能使最初的化学反应速率增大的是
(
)
A、盐酸的浓度不变,而使盐酸的用量一倍
B、盐酸的浓度增大一倍,而使盐酸的用量减少到原来一半
C、盐酸的浓度和用量都不变,增加碳酸钙的量
D、盐酸和碳酸钙不变,增大压强一倍
E、加入CaCl2溶液
F、加入CaCl2固体
G、将CaCO3固体用CaCO3粉末代替
BG
作业:
1、课本P9第3题;
2、《名校学案》P3基础演练(一)化学反应速率
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
