鲁教版九年级下学期 7.2 碱及其性质 同步课时练(含解析)
文档属性
| 名称 | 鲁教版九年级下学期 7.2 碱及其性质 同步课时练(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-12 00:00:00 | ||
图片预览

文档简介
中小学教育资源及组卷应用平台
7.2 碱及其性质 同步练习
一、单选题
1.下列关于酸、碱的说法错误的是(?? )
A.?苛性钠、烧碱、火碱都是氢氧化钠??????????????????B.?氢氧化钙可以用来改良酸性土壤
C.?稀盐酸能够使酚酞溶液变红????????????????????????????D.?生活中许多常见的物质(如柠檬、柑橘)中含有酸
2.小深同学用思维导图梳理了Na2CO3的相关知识,其中描述错误的是(??? )
A.?俗称:烧碱、苏打???????????????????????????????????????????????????????????????B.?物理性质:白色固体
C.?化学性质:可与稀盐酸、Ca(OH)2溶液、CaCl2溶液反应?????D.?用途:用于玻璃、洗涤剂的产生
3.A~F为初中化学_???è§????è?¨??????_体A在空气中易潮解,B和C能参与光合作用,B和D组成元素相同。它们相互转化的关系如图所示(“→”表示反应能一步实现,“一”表示相连物质间能发生反应,部分反应物、生成物和反应条件已省略)。下列说法错误的是( ??) 21世纪教育网版权所有
A.?C和F组成元素可能相同???????????????????????????????????B.?固体B可用于人工降雨
C.?D和E在一定条件下反应生成B?????????????????????????D.?A~F属于酸、碱、盐、氧化物、单质中的四类物质
4.下列物质露置在空气中,质量会减少的是( ??)
A.?生石灰????????????????????????????????B.?苛性钠????????????????????????????????C.?浓硫酸????????????????????????????????D.?浓盐酸
5.下列关于Ca(OH)2的说法错误的是(? )
A.?微溶于水,水溶液呈碱性?????????????????????????????????????????B.?能与酸反应,可用于治疗胃酸过多
C.?与CuSO4溶液按一定比例混合,可配制波尔多液?????D.?澄清溶液可用来检验CO2
6.在100mL5%的硫酸中依次加入一定量的氧化铁和氢氧化钠溶液,有关说法一定正确的是( ??)
A.?有沉淀生成??????B.?溶液最终呈黄色??????C.?只发生两个反应??????D.?溶液中硫酸根的物质的量保持不变
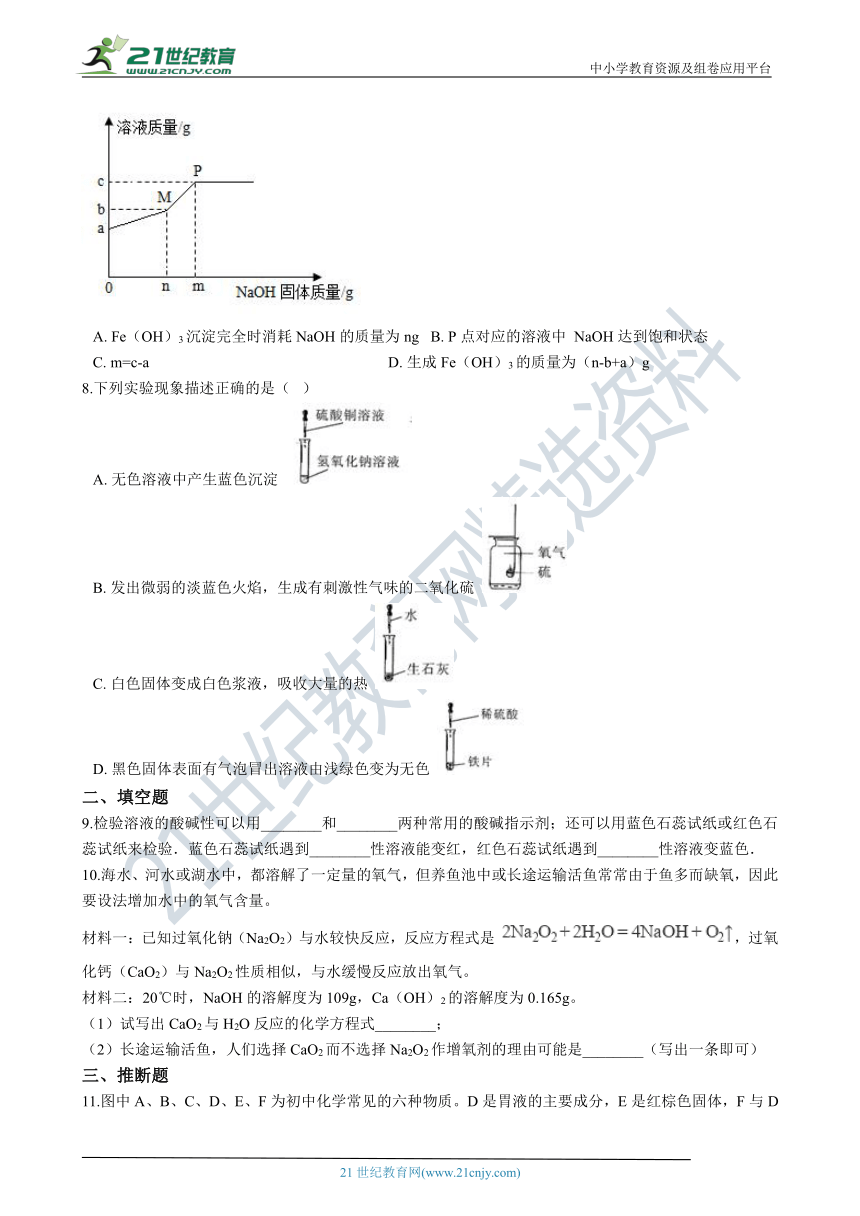
7.一定温度下,向a g _FeCl3???_液中加入NaOH固体,溶液的质量与加入NaOH固体的质量变化关系如下图所示。下列叙述错误的是(? ) 21·cn·jy·com
A.?Fe(OH)3沉淀完全时消耗NaOH的质量为ng???B.?P点对应的溶液中 NaOH达到饱和状态
C.?m=c-a???????????????????????????????????????????????????????????????D.?生成Fe(OH)3的质量为(n-b+a)g
8.下列实验现象描述正确的是(? )
A.?无色溶液中产生蓝色沉淀
B.?发出微弱的淡蓝色火焰,生成有刺激性气味的二氧化硫
C.?白色固体变成白色浆液,吸收大量的热
D.?黑色固体表面有气泡冒出溶液由浅绿色变为无色 www.21-cn-jy.com
二、填空题
9.检验溶液的酸碱性_????????¨_________和________两种常用的酸碱指示剂;还可以用蓝色石蕊试纸或红色石蕊试纸来检验.蓝色石蕊试纸遇到________性溶液能变红,红色石蕊试纸遇到________性溶液变蓝色.
10.海水、河水或湖水中,都溶解了一定量的氧气,但养鱼池中或长途运输活鱼常常由于鱼多而缺氧,因此要设法增加水中的氧气含量。 【来源:21·世纪·教育·网】
材料一:已知过氧化钠(Na2O2)与水较快反应,反应方程式是 ,过氧化钙(CaO2)与Na2O2性质相似,与水缓慢反应放出氧气。www-2-1-cnjy-com
材料二:20℃时,NaOH的溶解度为109g,Ca(OH)2的溶解度为0.165g。
(1)试写出CaO2与H2O反应的化学方程式________;
(2)长途运输活鱼,人们选择CaO2而不选择Na2O2作增氧剂的理由可能是________(写出一条即可)
三、推断题
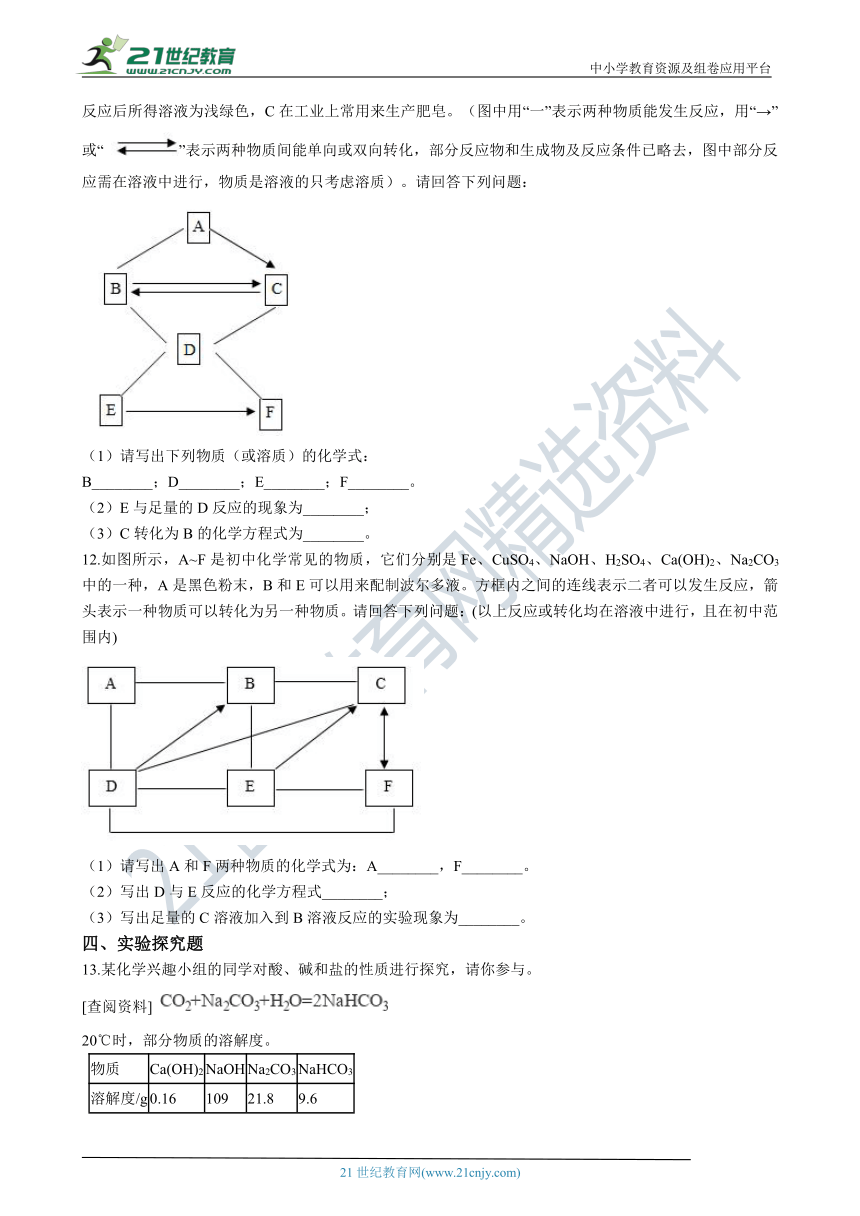
11.图中A、B、C、D、E、F为初中化学常见的六种物质。D是胃液的主要成分,E是红棕色固体,F与D反应后所得溶液为浅绿色,C在工业上常用来生产肥皂。(图中用“一”表示两种物质能发生反应,用“→”或“ ”表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。请回答下列问题: 2-1-c-n-j-y
(1)请写出下列物质(或溶质)的化学式:
B________;D________;E________;F________。
(2)E与足量的D反应的现象为________;
(3)C转化为B的化学方程式为________。
12.如图所示,A~F_??????????????????_见的物质,它们分别是Fe、CuSO4、NaOH、H2SO4、Ca(OH)2、Na2CO3中的一种,A是黑色粉末,B和E可以用来配制波尔多液。方框内之间的连线表示二者可以发生反应,箭头表示一种物质可以转化为另一种物质。请回答下列问题:(以上反应或转化均在溶液中进行,且在初中范围内) 【来源:21cnj*y.co*m】
(1)请写出A和F两种物质的化学式为:A________,F________。
(2)写出D与E反应的化学方程式________;
(3)写出足量的C溶液加入到B溶液反应的实验现象为________。
四、实验探究题
13.某化学兴趣小组的同学对酸、碱和盐的性质进行探究,请你参与。
[查阅资料]
20℃时,部分物质的溶解度。
物质 Ca(OH)2 NaOH Na2CO3 NaHCO3
溶解度/g 0.16 109 21.8 9.6
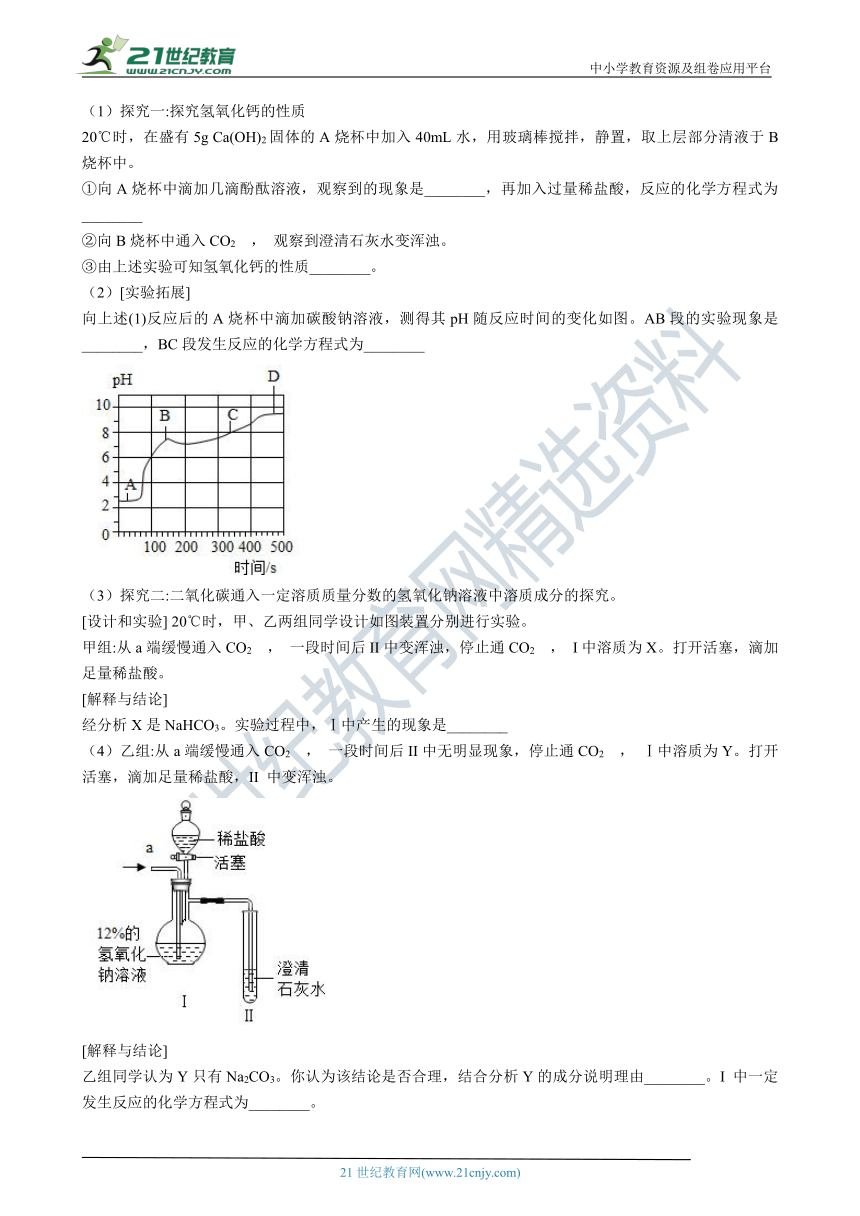
(1)探究一:探究氢氧化钙的性质
20℃时,在盛有5g Ca(OH)2固体的A烧杯中加入40mL水,用玻璃棒搅拌,静置,取上层部分清液于B烧杯中。【出处:21教育名师】
①向A烧杯中滴加几滴酚酞溶液,观察到的现象是________,再加入过量稀盐酸,反应的化学方程式为________21*cnjy*com
②向B烧杯中通入CO2 , 观察到澄清石灰水变浑浊。
③由上述实验可知氢氧化钙的性质________。
(2)[实验拓展]
向上述(1)反应后的A烧杯_????????????é??é??_溶液,测得其pH随反应时间的变化如图。AB段的实验现象是________,BC段发生反应的化学方程式为________
(3)探究二:二氧化碳通入一定溶质质量分数的氢氧化钠溶液中溶质成分的探究。
[设计和实验] 20℃时,甲、乙两组同学设计如图装置分别进行实验。
甲组:从a端缓慢通入CO2 , 一段时间后II中变浑浊,停止通CO2 , I中溶质为X。打开活塞,滴加足量稀盐酸。
[解释与结论]
经分析X是NaHCO3。实验过程中,Ⅰ中产生的现象是________
(4)乙组:从a端缓慢通_???CO2___, 一段时间后II中无明显现象,停止通CO2 , Ⅰ中溶质为Y。打开活塞,滴加足量稀盐酸,II 中变浑浊。
[解释与结论]
乙组同学认为Y只有_Na2CO3_。你认为该结论是否合理,结合分析Y的成分说明理由________。I 中一定发生反应的化学方程式为________。
五、综合题
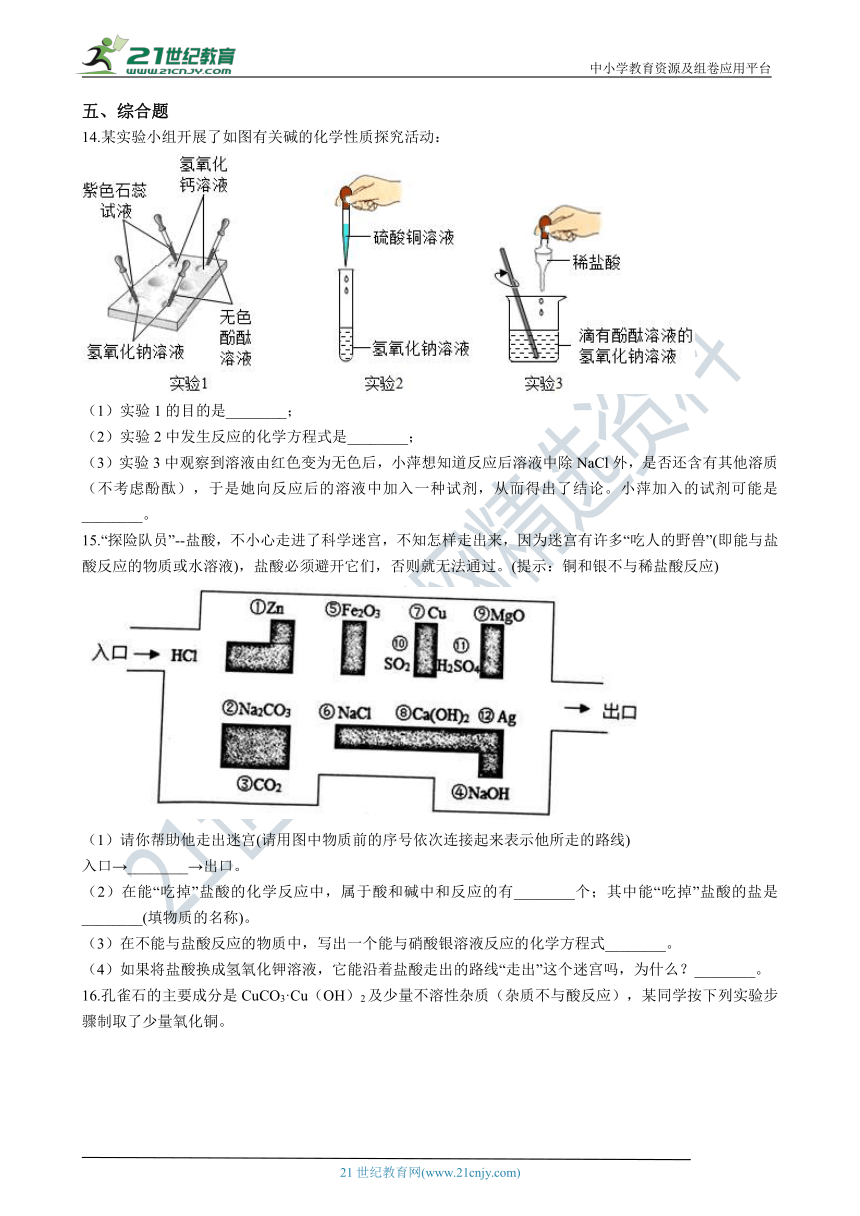
14.某实验小组开展了如图有关碱的化学性质探究活动:
(1)实验1的目的是________;
(2)实验2中发生反应的化学方程式是________;
(3)实验3中观_?????°????????±???_色变为无色后,小萍想知道反应后溶液中除NaCl外,是否还含有其他溶质(不考虑酚酞),于是她向反应后的溶液中加入一种试剂,从而得出了结论。小萍加入的试剂可能是________。
15.“探险队员”--盐酸,不小心走进了科学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或水溶液),盐酸必须避开它们,否则就无法通过。(提示:铜和银不与稀盐酸反应)
(1)请你帮助他走出迷宫(请用图中物质前的序号依次连接起来表示他所走的路线)
入口→________→出口。
(2)在能“吃掉”盐酸的化学反_??????????±????é??_和碱中和反应的有________个;其中能“吃掉”盐酸的盐是________(填物质的名称)。 21教育网
(3)在不能与盐酸反应的物质中,写出一个能与硝酸银溶液反应的化学方程式________。
(4)如果将盐酸换成氢氧化钾溶液,它能沿着盐酸走出的路线“走出”这个迷宫吗,为什么?________。
16.孔雀石的主要成分是CuCO3·Cu(OH)2及少量不溶性杂质(杂质不与酸反应),某同学按下列实验步骤制取了少量氧化铜。
(1)白色沉淀的化学式为________。
(2)写出步骤③中发生反应的化学方程式________。
(3)蓝色沉淀受热分解生成另一种氧化物的化学式是________。
(4)若向溶液A中逐滴加入NaOH溶液,其过程中溶质种数会发生变化,最多时可达________种。
答案解析部分
一、单选题
1. C
解答:A. 苛性钠、烧碱、火碱都是氢氧化钠的俗称,故说法正确,不符合题意;
B. 氢氧化钙显碱性,可用来改良酸性土壤,故说法正确,不符合题意;
C. 稀盐酸显酸性,不能使无色酚酞试液变色,故说法错误,符合题意;
D. 生活中很多物质中都含有酸,如柠檬含柠檬酸,故说法正确,不符合题意。
故答案为:C。
分析:A、根据氢氧化钠_???????§°???è??è??_分析。
B、根据氢氧化钙的性质,进行分析。
C、酸性溶液不能使无色酚酞试液变色。
D、根据生活中的酸,进行分析。【版权所有:21教育】
2. A
解答:A. 碳酸钠,俗称食碱、苏打,故描述错误,符合题意;
B. 碳酸钠是白色固体,故描述正确,不符合题意;
C. 碳酸钠与稀盐酸反应生成_????°§??????????°?_化钠和水,能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,能与氯化钙反应生成碳酸钙沉淀和氯化钠,故描述正确,不符合题意;
D. 碳酸钠广泛应用于生产玻璃,造纸,纺织,洗涤剂等,故描述正确,不符合题意;
故答案为:A。
分析:根据碳酸钠的俗称,性质,用途,进行分析。
3. D
解答:A、C是水,F是过氧化氢,都是由氢氧两种元素组成的,说法不符合题意;
B、B是二氧化碳,可用于人工降雨,说法不符合题意;
C、D是一氧化碳,E是氧气,一氧化碳在氧气中燃烧生成二氧化碳,说法不符合题意;
D、A是氢氧化钠属于碱,B是二氧化碳、D是一氧化碳、C是水、F是过氧化氢都属于氧化物,E是氧气属于单质,共三类物质,说法符合题意。21cnjy.com
故答案为:D。
分析:固体A在_????°??????????è§?_,所以A是氢氧化钠,B和C能参与光合作用,B和D组成元素相同,所以B是二氧化碳,D是一氧化碳,C是水,根据图中反应关系可推知:F是过氧化氢,E是氧气,代入验证,推理符合题意。21·世纪*教育网
4. D
解答:A. 生石灰氧化钙和空气中水蒸汽反应生成氢氧化钙,质量增大,故不符合题意。
B. 苛性钠吸水,还可以吸收空气中二氧化碳,质量增大,故不符合题意。
C. 浓硫酸具有吸水性,吸收空气中水蒸气质量增大,故不符合题意。
D. 浓盐酸具有挥发性,溶液质量减少,故符合题意。
故答案为:D。
分析: 浓盐酸具有挥发性,会挥发出氯化氢气体。
5. B
解答:A. 氢氧化钙微溶于水,且水溶液显碱性,故说法正确,不符合题意;
B. 氢氧化钙属于碱,能与酸反应,但是氢氧化钙腐蚀性较强,不能用于治疗胃酸过多,故说法错误,符合题意;2·1·c·n·j·y
C. 氢氧化钙与硫酸铜按照一定比例混合,可用于配制农药波尔多液,故说法正确,不符合题意;
D. 通常用澄清石灰水来检验二氧化碳,二氧化碳能使澄清石灰水变浑浊,故说法正确,不符合题意。
故答案为:B。
分析_????°??°§???é???±?_于碱,其水溶液显碱性,能与硫酸铜反应生成氢氧化铜沉淀和硫酸钙。
二氧化碳能使澄清石灰水变浑浊,氢氧化钙能中和酸性土壤。21*cnjy*com
6. D
解_??????A??????é??_能与氧化铁反应生成硫酸铁和水,硫酸能与氢氧化钠反应生成硫酸钠和水,若硫酸过量,是不会有沉淀生成的,说法不符合题意。
B、硫酸能与氧化铁反应生成硫酸_é??????°????è???°§_化铁过量,硫酸铁与氢氧化钠反应生成氢氧化铁沉淀和硫酸钠,硫酸铁可能完全被消耗,液最终可能显无色,说法不符合题意。
C、不一定只发生两个反应,可能_????????????é??è??_与氧化铁反应生成硫酸铁和水、硫酸能与氢氧化钠反应生成硫酸钠和水、硫酸铁能与氢氧化钠溶液反应生成氢氧化铁沉淀和硫酸钠三个反应,说法不符合题意。
D、硫酸能与氧化铁反_????????????é??é??_和水,硫酸能与氢氧化钠反应生成硫酸钠和水,硫酸铁能与氢氧化钠溶液反应生成氢氧化铁沉淀和硫酸钠,不论发生了上述几个反应,溶液中硫酸根的物质的量始终不变,说法符合题意。
故答案为:D。
分析:根据稀硫酸和氢氧化钠反应生成硫酸钠和水,稀硫酸和氧化铁反应生成硫酸铁和水,据此分析
7. C
解答:A、M点是氢氧化钠和氯化铁恰好完全反应,所以Fe(OH)3沉淀完全时消耗NaOH的质量为ng,故不符合题意;
B、P点溶液的质量不再增加,说明氢氧化钠不能继续溶解,说明溶液中 NaOH达到饱和状态,故不符合题意;
C、根据 可知,当Fe(OH)3沉淀完全时,得到氯化钠溶液的质量为bg,所以m-n=c-b,即m=c-b+n,故符合题意;
D、根据 可知,生成Fe(OH)3的质量为(n-b+a)g,故不符合题意。
故答案为:C。
分析:氯化铁和氢氧化钠反应生_????°??°§???é?????_淀和氯化钠,根据图像分析可知,M点是氢氧化钠和氯化铁恰好完全反应,M点后溶液增加的质量质量为加入氢氧化钠的质量,P点溶液的质量不再增加,说明氢氧化钠不能继续溶解。
8. A
解答:A、硫酸铜和氢氧化钠反应生成氢氧化铜蓝色沉淀和硫酸钠,无色溶液中产生蓝色沉淀,故A符合题意;
B、硫在氧气中燃烧发出蓝紫色火焰,生成有刺激性气味的二氧化硫属于实验结论,故B不符合题意;
C、生石灰与水反应生成氢氧化钙,生石灰中加入一定量的水,白色固体变成白色浆液,该反应放出大量的热,故C不符合题意;
D、铁和稀硫酸反应生成硫酸亚铁和氢气,银白色的固体表面有气泡生成,溶液变为浅绿色,故D不符合题意。
故答案为:A。
分析:A、根据氢氧化_é?????è??è??????·?_分析;
B、根据硫在氧气中燃烧及现象描述的要求分析,其中有生成物名称的描述为结论;
C、根据水和氧化钙反应生成氢氧化钙且放热分析;
D、根据铁与硫酸反应的现象分析。
二、填空题
9.石蕊试液;酚酞试液;酸;碱
解答:能检验_??????é????±??§???_试液,称为酸碱指示剂,常见的酸碱指示剂有:石蕊试液和酚酞试液. 除此之外还可用石蕊试纸,其规律是:用蓝色石蕊试纸可以检验酸性物质,如蓝色石蕊济纸变红,则显酸性;用红色石蕊试纸可以检验碱性物质,如红色石蕊试纸变蓝,则显碱性.
所以本题答案为:石蕊试液;酚酞试液;酸;碱.
分析:科学探究是重要的学习方式,本题是通过实验探究物质的性质或变化规律的基本题型,溶液酸碱性的探究常借助酸碱指示剂来检验其酸碱性,掌握指示剂和试纸的使用方法和规律.
10. (1)2CaO_2+2H2O_═2Ca(OH)2+O2↑
(2)过氧化钠与水反应生成的氢氧化钠具有强烈的腐蚀性(合理即可)
解答:(_1???è???°§???é??_与水反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑,过氧化钙(CaO2)与Na2O2性质相似,则过氧化钙与水反应生成氢氧化钙和氧气,反应的化学方程式为:2CaO2+2H2O═2Ca(OH)2+O2↑。
(2)过氧化钠与水反应生成的氢氧化钠具有强烈的腐蚀性,故人们选择CaO2而不选择Na2O2作增氧剂(合理即可)。
分析:(1)根据过氧化钙与水反应生成氢氧化钙和氧气,写出化学方程式。
(2)根据氢氧化钠具有强烈的腐蚀性,进行分析。
三、推断题
11. (1)Na2CO3;HCl;Fe2O3;Fe
(2)红棕色固体逐渐减少至消失,溶液由无色变为黄色
(3)
解答:(1)B为碳酸钠,化学式 ,D为盐酸,化学式HCl,E为氧化铁,化学式为 ,F为铁,化学式为Fe;(2)氧化铁和盐酸反应生成氯化铁和水,氯化铁溶液为黄色,现象是红棕色固体逐渐减少至消失,溶液由无色变为黄色;(3)氢氧化钠和二氧化碳反应生成碳酸钠和水,化学方程式为: 。
分析:推断题的关键是抓住题眼,本题的题眼是 D是胃液的主要成分,E是红棕色固体,F与D反应后所得溶液为浅绿色,C在工业上常用来生产肥皂。 结合题中的转化关系进行分析
12. (1)Fe;Na2CO3
(2)
(3)溶液中产生蓝色沉淀,蓝色溶液逐渐变为无色
解答:(1)由分析可知,A为铁,化学式为Fe;F为碳酸钠,化学式为Na2CO3;(2)D与E反应是稀硫酸与氢氧化钙反应生成硫酸钙和水,该反应的化学方程式为: ;(3)足量的C溶液加入到B溶液中,氢氧化钠与硫酸铜反应生成氢氧化铜和硫酸钠,氢氧化钠足量,故硫酸铜完全反应,故实验现象为:溶液中产生蓝色沉淀,蓝色溶液逐渐变为无色。
分析:推断题的关键是抓住题眼,本题的题眼是 A是黑色粉末,B和E可以用来配制波尔多液。 结合几种物质之间的反应进行分析
四、实验探究题
13. (1)溶液由无色变为红色;;固体;微溶于水,能与指示剂作用;能与某些非金属氧化物反应生成盐和水;能与酸反应生成盐和水
(2)产生大量气泡;
(3)无色溶液中逐渐有固体析出(变浑浊),滴盐酸后有气泡产生,固体逐渐溶解(消失)
(4)不合理,根据通入的CO2的量的不同情况,Y的溶质成分可能还有:NaOH和Na2CO3 , Na2CO3和NaHCO3 , NaHCO3这三种情况。三种情况均能与稀盐酸反应产生气体且使澄清石灰水变浑浊;
解答:(1)氢氧化钙溶液显碱性,向A烧杯中滴加几滴酚酞溶液,观察到的现象是溶液由无色变为红色,再加入过量稀盐酸,稀盐酸和氢氧化钙反应生成氯化钙和水,反应的化学方程式为 。由上述实验可知氢氧化钙的性质:固体;微溶于水(20℃时,溶解度0.16 g),能与指示剂作用;能与某些非金属氧化物反应生成盐和水;能与酸反应生成盐和水。
[实验拓展](2)向上述(1)反应后的A烧杯中滴加碳酸钠溶液,AB段是碳酸钠溶液先和上步过量的稀盐酸反应生成氯化钠、水、二氧化碳,pH上升;BC段是氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠;化学方程式为 。CD段是最后加入过量碳酸钠溶液。碳酸钠溶液显碱性。故AB段的实验现象是产生大量气泡,BC段发生反应的化学方程式为 。
[解释与结论](3)二氧化碳和氢氧化钠反应生成碳酸钠和水,二氧化碳和碳酸钠和水反应生成碳酸氢钠,盐酸和碳酸氢钠反应生成氯化钠、水和二氧化碳。经分析X是NaHCO3。所以实验过程中,Ⅰ中产生的现象是无色溶液中逐渐变浑浊,滴盐酸后有气泡产生,固体逐渐消失。
(4)乙组同学认为Y只有Na2CO3。不合理,根据通入的CO2的量的不同情况,Y的溶质成分可能还有:NaOH和Na2CO3(二氧化碳只够与部分氢氧化钠反应), Na2CO3和NaHCO3(二氧化碳将氢氧化钠反应全部反应完,且与部分碳酸钠反应),NaHCO3(二氧化碳将氢氧化钠反应全部反应完,且与将碳酸钠反应完)这三种情况。三种情况均能与稀盐酸反应产生气体且使澄清石灰水变浑浊。I 中一定发生反应为二氧化碳和氢氧化钠反应生成碳酸钠和水,化学方程式为 。
分析:(1)_??±??§??????è?????_无色酚酞试液变红色。
氢氧化钙与盐酸反应,生成氯化钙和水。
(2)碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳。
氯化钙和碳酸钠反应,生成碳酸钙沉淀和氯化钠。
(3)根据二氧化碳的化学性质,进行分析。
(4)二氧化碳和氢氧化钠反应生成碳酸钠和水。
五、综合题
14. (1)探究碱溶液_???????¤??????????_应
(2)2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
(3)紫色的石蕊试液(或锌粒或碳酸钠粉末等) 21教育名师原创作品
解答:(1)_???é??1??????é??_过氢氧化钠和氢氧化钙分别对石蕊试液和酚酞试液的作用,可以探究碱溶液与指示剂的反应;
(2)实验2中,氢氧化钠和硫酸铜反应生成蓝色氢氧化铜沉淀和硫酸钠,化学方程式为:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;
(3)实验3中观察到溶液由红色变为无色,氢氧化钠肯定全部被反应,此时溶液中除NaCl外(不考虑酚酞),溶液中可能存在的是盐酸。因此为了证明盐酸的存在与否,可以取适量的溶液滴加石蕊试液,若变成红色,或加入锌粒产生气泡等均可说明盐酸的存在。(合理即可)
分析:根据碱的性质,进行分析。
15. (1)③→⑥→⑩_??????????????????_
(2)2;碳酸钠
(3)NaCl+AgNO3=AgCl↓+NaNO3
(4)不能,氢氧化钾与二氧化碳反应,从而被“吃掉”。
解答:(1)根据图示的_???è?¨?????±??????_酸不能和二氧化碳、二氧化硫、不活泼金属铜和银、氯化钠、硫酸反应。
?故答案为:③→⑥→⑩→⑦→?→?
(2)中和反应是酸与碱反应,氢氧化钙、氢氧化钠为碱,所以碱有2种,故能发生中和反应有2个;
能与盐酸反应的盐只有碳酸钠。
(3)不能与盐酸反应的物质有:③⑥⑩?,氯化钠与硝酸银反应,生成氯化银沉淀和硝酸钠,其反应的化学方程式是:NaCl+AgNO3═AgCl↓+NaNO3 , 此反应是两种化合物相互交换成分生成两种新的化合物的反应类型,属于复分解反应。
(4)二氧化碳与氢氧化钾反应生成碳酸钾和水,
分析:(1)根据盐酸的性质,进行分析。
(2)根据中和反应的特点,进行分析。
(3)根据氯离子与银离子不共存,会生成氯化银沉淀,进行分析。
(4)根据氢氧化钾的性质,进行分析。
16. (1)CaCO3
(2),2NaOH+H2SO4=Na2SO4+2H2O
(3)H2O
(4)3
解答:CuCO3·Cu(OH)2与过量稀硫酸反应方程式为 ,因此气体是CO2 , 溶液A的溶质是CuSO4和H2SO4;
(1)CO2遇澄清石灰水生成H2O和CaCO3 , 故白色沉淀是CaCO3;
(2)溶液A的溶质是CuSO4和H2SO4 , CuSO4与NaOH反应生成硫酸钠和氢氧化铜,反应方程式为 ;硫酸与氢氧化钠反应生成硫酸钠和水,反应的化学方程式为: 2NaOH+H2SO4=Na2SO4+2H2O;
(3)经过③反应后,生成的蓝色沉淀是Cu(OH)2 , Cu(OH)2加热会产生两种氧化物CuO和H2O,故填H2O;
(4)因①的操作加入了过量的稀硫酸,因此溶液A中有两种溶质CuSO4和H2SO4;在滴加NaOH很少时,H2SO4未反应完,此时溶质有CuSO4、Na2SO4和H2SO4 , 溶质为3种;当H2SO4反应完全至生成蓝色沉淀最多之前,溶液中只有Na2SO4和CuSO4 , 溶质只有2种;当NaOH滴加生成沉淀最多时,溶液中只有1种溶质Na2SO4;当NaOH过量时,溶液中有2种溶质Na2SO4和NaOH;综上所述,向A中加入NaOH溶液,其溶质最多时可达3种,故填3。
分析:写出CuCO3·Cu(OH)2与过量稀硫酸反应的化学方程式。
(1)CO2与氢氧化钙反应生成CaCO3沉淀。
(2)根据CuSO4与NaOH反应生成硫酸钠和氢氧化铜,写出化学方程式;
根据硫酸与氢氧化钠反应生成硫酸钠和水,写出化学方程式。
(3)根据Cu(OH)2加热会生成CuO和H2O,进行分析。
(4)根据物质的性质,进行分析。
_21?????????è?????(www.21cnjy.com)_
7.2 碱及其性质 同步练习
一、单选题
1.下列关于酸、碱的说法错误的是(?? )
A.?苛性钠、烧碱、火碱都是氢氧化钠??????????????????B.?氢氧化钙可以用来改良酸性土壤
C.?稀盐酸能够使酚酞溶液变红????????????????????????????D.?生活中许多常见的物质(如柠檬、柑橘)中含有酸
2.小深同学用思维导图梳理了Na2CO3的相关知识,其中描述错误的是(??? )
A.?俗称:烧碱、苏打???????????????????????????????????????????????????????????????B.?物理性质:白色固体
C.?化学性质:可与稀盐酸、Ca(OH)2溶液、CaCl2溶液反应?????D.?用途:用于玻璃、洗涤剂的产生
3.A~F为初中化学_???è§????è?¨??????_体A在空气中易潮解,B和C能参与光合作用,B和D组成元素相同。它们相互转化的关系如图所示(“→”表示反应能一步实现,“一”表示相连物质间能发生反应,部分反应物、生成物和反应条件已省略)。下列说法错误的是( ??) 21世纪教育网版权所有
A.?C和F组成元素可能相同???????????????????????????????????B.?固体B可用于人工降雨
C.?D和E在一定条件下反应生成B?????????????????????????D.?A~F属于酸、碱、盐、氧化物、单质中的四类物质
4.下列物质露置在空气中,质量会减少的是( ??)
A.?生石灰????????????????????????????????B.?苛性钠????????????????????????????????C.?浓硫酸????????????????????????????????D.?浓盐酸
5.下列关于Ca(OH)2的说法错误的是(? )
A.?微溶于水,水溶液呈碱性?????????????????????????????????????????B.?能与酸反应,可用于治疗胃酸过多
C.?与CuSO4溶液按一定比例混合,可配制波尔多液?????D.?澄清溶液可用来检验CO2
6.在100mL5%的硫酸中依次加入一定量的氧化铁和氢氧化钠溶液,有关说法一定正确的是( ??)
A.?有沉淀生成??????B.?溶液最终呈黄色??????C.?只发生两个反应??????D.?溶液中硫酸根的物质的量保持不变
7.一定温度下,向a g _FeCl3???_液中加入NaOH固体,溶液的质量与加入NaOH固体的质量变化关系如下图所示。下列叙述错误的是(? ) 21·cn·jy·com
A.?Fe(OH)3沉淀完全时消耗NaOH的质量为ng???B.?P点对应的溶液中 NaOH达到饱和状态
C.?m=c-a???????????????????????????????????????????????????????????????D.?生成Fe(OH)3的质量为(n-b+a)g
8.下列实验现象描述正确的是(? )
A.?无色溶液中产生蓝色沉淀
B.?发出微弱的淡蓝色火焰,生成有刺激性气味的二氧化硫
C.?白色固体变成白色浆液,吸收大量的热
D.?黑色固体表面有气泡冒出溶液由浅绿色变为无色 www.21-cn-jy.com
二、填空题
9.检验溶液的酸碱性_????????¨_________和________两种常用的酸碱指示剂;还可以用蓝色石蕊试纸或红色石蕊试纸来检验.蓝色石蕊试纸遇到________性溶液能变红,红色石蕊试纸遇到________性溶液变蓝色.
10.海水、河水或湖水中,都溶解了一定量的氧气,但养鱼池中或长途运输活鱼常常由于鱼多而缺氧,因此要设法增加水中的氧气含量。 【来源:21·世纪·教育·网】
材料一:已知过氧化钠(Na2O2)与水较快反应,反应方程式是 ,过氧化钙(CaO2)与Na2O2性质相似,与水缓慢反应放出氧气。www-2-1-cnjy-com
材料二:20℃时,NaOH的溶解度为109g,Ca(OH)2的溶解度为0.165g。
(1)试写出CaO2与H2O反应的化学方程式________;
(2)长途运输活鱼,人们选择CaO2而不选择Na2O2作增氧剂的理由可能是________(写出一条即可)
三、推断题
11.图中A、B、C、D、E、F为初中化学常见的六种物质。D是胃液的主要成分,E是红棕色固体,F与D反应后所得溶液为浅绿色,C在工业上常用来生产肥皂。(图中用“一”表示两种物质能发生反应,用“→”或“ ”表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。请回答下列问题: 2-1-c-n-j-y
(1)请写出下列物质(或溶质)的化学式:
B________;D________;E________;F________。
(2)E与足量的D反应的现象为________;
(3)C转化为B的化学方程式为________。
12.如图所示,A~F_??????????????????_见的物质,它们分别是Fe、CuSO4、NaOH、H2SO4、Ca(OH)2、Na2CO3中的一种,A是黑色粉末,B和E可以用来配制波尔多液。方框内之间的连线表示二者可以发生反应,箭头表示一种物质可以转化为另一种物质。请回答下列问题:(以上反应或转化均在溶液中进行,且在初中范围内) 【来源:21cnj*y.co*m】
(1)请写出A和F两种物质的化学式为:A________,F________。
(2)写出D与E反应的化学方程式________;
(3)写出足量的C溶液加入到B溶液反应的实验现象为________。
四、实验探究题
13.某化学兴趣小组的同学对酸、碱和盐的性质进行探究,请你参与。
[查阅资料]
20℃时,部分物质的溶解度。
物质 Ca(OH)2 NaOH Na2CO3 NaHCO3
溶解度/g 0.16 109 21.8 9.6
(1)探究一:探究氢氧化钙的性质
20℃时,在盛有5g Ca(OH)2固体的A烧杯中加入40mL水,用玻璃棒搅拌,静置,取上层部分清液于B烧杯中。【出处:21教育名师】
①向A烧杯中滴加几滴酚酞溶液,观察到的现象是________,再加入过量稀盐酸,反应的化学方程式为________21*cnjy*com
②向B烧杯中通入CO2 , 观察到澄清石灰水变浑浊。
③由上述实验可知氢氧化钙的性质________。
(2)[实验拓展]
向上述(1)反应后的A烧杯_????????????é??é??_溶液,测得其pH随反应时间的变化如图。AB段的实验现象是________,BC段发生反应的化学方程式为________
(3)探究二:二氧化碳通入一定溶质质量分数的氢氧化钠溶液中溶质成分的探究。
[设计和实验] 20℃时,甲、乙两组同学设计如图装置分别进行实验。
甲组:从a端缓慢通入CO2 , 一段时间后II中变浑浊,停止通CO2 , I中溶质为X。打开活塞,滴加足量稀盐酸。
[解释与结论]
经分析X是NaHCO3。实验过程中,Ⅰ中产生的现象是________
(4)乙组:从a端缓慢通_???CO2___, 一段时间后II中无明显现象,停止通CO2 , Ⅰ中溶质为Y。打开活塞,滴加足量稀盐酸,II 中变浑浊。
[解释与结论]
乙组同学认为Y只有_Na2CO3_。你认为该结论是否合理,结合分析Y的成分说明理由________。I 中一定发生反应的化学方程式为________。
五、综合题
14.某实验小组开展了如图有关碱的化学性质探究活动:
(1)实验1的目的是________;
(2)实验2中发生反应的化学方程式是________;
(3)实验3中观_?????°????????±???_色变为无色后,小萍想知道反应后溶液中除NaCl外,是否还含有其他溶质(不考虑酚酞),于是她向反应后的溶液中加入一种试剂,从而得出了结论。小萍加入的试剂可能是________。
15.“探险队员”--盐酸,不小心走进了科学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或水溶液),盐酸必须避开它们,否则就无法通过。(提示:铜和银不与稀盐酸反应)
(1)请你帮助他走出迷宫(请用图中物质前的序号依次连接起来表示他所走的路线)
入口→________→出口。
(2)在能“吃掉”盐酸的化学反_??????????±????é??_和碱中和反应的有________个;其中能“吃掉”盐酸的盐是________(填物质的名称)。 21教育网
(3)在不能与盐酸反应的物质中,写出一个能与硝酸银溶液反应的化学方程式________。
(4)如果将盐酸换成氢氧化钾溶液,它能沿着盐酸走出的路线“走出”这个迷宫吗,为什么?________。
16.孔雀石的主要成分是CuCO3·Cu(OH)2及少量不溶性杂质(杂质不与酸反应),某同学按下列实验步骤制取了少量氧化铜。
(1)白色沉淀的化学式为________。
(2)写出步骤③中发生反应的化学方程式________。
(3)蓝色沉淀受热分解生成另一种氧化物的化学式是________。
(4)若向溶液A中逐滴加入NaOH溶液,其过程中溶质种数会发生变化,最多时可达________种。
答案解析部分
一、单选题
1. C
解答:A. 苛性钠、烧碱、火碱都是氢氧化钠的俗称,故说法正确,不符合题意;
B. 氢氧化钙显碱性,可用来改良酸性土壤,故说法正确,不符合题意;
C. 稀盐酸显酸性,不能使无色酚酞试液变色,故说法错误,符合题意;
D. 生活中很多物质中都含有酸,如柠檬含柠檬酸,故说法正确,不符合题意。
故答案为:C。
分析:A、根据氢氧化钠_???????§°???è??è??_分析。
B、根据氢氧化钙的性质,进行分析。
C、酸性溶液不能使无色酚酞试液变色。
D、根据生活中的酸,进行分析。【版权所有:21教育】
2. A
解答:A. 碳酸钠,俗称食碱、苏打,故描述错误,符合题意;
B. 碳酸钠是白色固体,故描述正确,不符合题意;
C. 碳酸钠与稀盐酸反应生成_????°§??????????°?_化钠和水,能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,能与氯化钙反应生成碳酸钙沉淀和氯化钠,故描述正确,不符合题意;
D. 碳酸钠广泛应用于生产玻璃,造纸,纺织,洗涤剂等,故描述正确,不符合题意;
故答案为:A。
分析:根据碳酸钠的俗称,性质,用途,进行分析。
3. D
解答:A、C是水,F是过氧化氢,都是由氢氧两种元素组成的,说法不符合题意;
B、B是二氧化碳,可用于人工降雨,说法不符合题意;
C、D是一氧化碳,E是氧气,一氧化碳在氧气中燃烧生成二氧化碳,说法不符合题意;
D、A是氢氧化钠属于碱,B是二氧化碳、D是一氧化碳、C是水、F是过氧化氢都属于氧化物,E是氧气属于单质,共三类物质,说法符合题意。21cnjy.com
故答案为:D。
分析:固体A在_????°??????????è§?_,所以A是氢氧化钠,B和C能参与光合作用,B和D组成元素相同,所以B是二氧化碳,D是一氧化碳,C是水,根据图中反应关系可推知:F是过氧化氢,E是氧气,代入验证,推理符合题意。21·世纪*教育网
4. D
解答:A. 生石灰氧化钙和空气中水蒸汽反应生成氢氧化钙,质量增大,故不符合题意。
B. 苛性钠吸水,还可以吸收空气中二氧化碳,质量增大,故不符合题意。
C. 浓硫酸具有吸水性,吸收空气中水蒸气质量增大,故不符合题意。
D. 浓盐酸具有挥发性,溶液质量减少,故符合题意。
故答案为:D。
分析: 浓盐酸具有挥发性,会挥发出氯化氢气体。
5. B
解答:A. 氢氧化钙微溶于水,且水溶液显碱性,故说法正确,不符合题意;
B. 氢氧化钙属于碱,能与酸反应,但是氢氧化钙腐蚀性较强,不能用于治疗胃酸过多,故说法错误,符合题意;2·1·c·n·j·y
C. 氢氧化钙与硫酸铜按照一定比例混合,可用于配制农药波尔多液,故说法正确,不符合题意;
D. 通常用澄清石灰水来检验二氧化碳,二氧化碳能使澄清石灰水变浑浊,故说法正确,不符合题意。
故答案为:B。
分析_????°??°§???é???±?_于碱,其水溶液显碱性,能与硫酸铜反应生成氢氧化铜沉淀和硫酸钙。
二氧化碳能使澄清石灰水变浑浊,氢氧化钙能中和酸性土壤。21*cnjy*com
6. D
解_??????A??????é??_能与氧化铁反应生成硫酸铁和水,硫酸能与氢氧化钠反应生成硫酸钠和水,若硫酸过量,是不会有沉淀生成的,说法不符合题意。
B、硫酸能与氧化铁反应生成硫酸_é??????°????è???°§_化铁过量,硫酸铁与氢氧化钠反应生成氢氧化铁沉淀和硫酸钠,硫酸铁可能完全被消耗,液最终可能显无色,说法不符合题意。
C、不一定只发生两个反应,可能_????????????é??è??_与氧化铁反应生成硫酸铁和水、硫酸能与氢氧化钠反应生成硫酸钠和水、硫酸铁能与氢氧化钠溶液反应生成氢氧化铁沉淀和硫酸钠三个反应,说法不符合题意。
D、硫酸能与氧化铁反_????????????é??é??_和水,硫酸能与氢氧化钠反应生成硫酸钠和水,硫酸铁能与氢氧化钠溶液反应生成氢氧化铁沉淀和硫酸钠,不论发生了上述几个反应,溶液中硫酸根的物质的量始终不变,说法符合题意。
故答案为:D。
分析:根据稀硫酸和氢氧化钠反应生成硫酸钠和水,稀硫酸和氧化铁反应生成硫酸铁和水,据此分析
7. C
解答:A、M点是氢氧化钠和氯化铁恰好完全反应,所以Fe(OH)3沉淀完全时消耗NaOH的质量为ng,故不符合题意;
B、P点溶液的质量不再增加,说明氢氧化钠不能继续溶解,说明溶液中 NaOH达到饱和状态,故不符合题意;
C、根据 可知,当Fe(OH)3沉淀完全时,得到氯化钠溶液的质量为bg,所以m-n=c-b,即m=c-b+n,故符合题意;
D、根据 可知,生成Fe(OH)3的质量为(n-b+a)g,故不符合题意。
故答案为:C。
分析:氯化铁和氢氧化钠反应生_????°??°§???é?????_淀和氯化钠,根据图像分析可知,M点是氢氧化钠和氯化铁恰好完全反应,M点后溶液增加的质量质量为加入氢氧化钠的质量,P点溶液的质量不再增加,说明氢氧化钠不能继续溶解。
8. A
解答:A、硫酸铜和氢氧化钠反应生成氢氧化铜蓝色沉淀和硫酸钠,无色溶液中产生蓝色沉淀,故A符合题意;
B、硫在氧气中燃烧发出蓝紫色火焰,生成有刺激性气味的二氧化硫属于实验结论,故B不符合题意;
C、生石灰与水反应生成氢氧化钙,生石灰中加入一定量的水,白色固体变成白色浆液,该反应放出大量的热,故C不符合题意;
D、铁和稀硫酸反应生成硫酸亚铁和氢气,银白色的固体表面有气泡生成,溶液变为浅绿色,故D不符合题意。
故答案为:A。
分析:A、根据氢氧化_é?????è??è??????·?_分析;
B、根据硫在氧气中燃烧及现象描述的要求分析,其中有生成物名称的描述为结论;
C、根据水和氧化钙反应生成氢氧化钙且放热分析;
D、根据铁与硫酸反应的现象分析。
二、填空题
9.石蕊试液;酚酞试液;酸;碱
解答:能检验_??????é????±??§???_试液,称为酸碱指示剂,常见的酸碱指示剂有:石蕊试液和酚酞试液. 除此之外还可用石蕊试纸,其规律是:用蓝色石蕊试纸可以检验酸性物质,如蓝色石蕊济纸变红,则显酸性;用红色石蕊试纸可以检验碱性物质,如红色石蕊试纸变蓝,则显碱性.
所以本题答案为:石蕊试液;酚酞试液;酸;碱.
分析:科学探究是重要的学习方式,本题是通过实验探究物质的性质或变化规律的基本题型,溶液酸碱性的探究常借助酸碱指示剂来检验其酸碱性,掌握指示剂和试纸的使用方法和规律.
10. (1)2CaO_2+2H2O_═2Ca(OH)2+O2↑
(2)过氧化钠与水反应生成的氢氧化钠具有强烈的腐蚀性(合理即可)
解答:(_1???è???°§???é??_与水反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑,过氧化钙(CaO2)与Na2O2性质相似,则过氧化钙与水反应生成氢氧化钙和氧气,反应的化学方程式为:2CaO2+2H2O═2Ca(OH)2+O2↑。
(2)过氧化钠与水反应生成的氢氧化钠具有强烈的腐蚀性,故人们选择CaO2而不选择Na2O2作增氧剂(合理即可)。
分析:(1)根据过氧化钙与水反应生成氢氧化钙和氧气,写出化学方程式。
(2)根据氢氧化钠具有强烈的腐蚀性,进行分析。
三、推断题
11. (1)Na2CO3;HCl;Fe2O3;Fe
(2)红棕色固体逐渐减少至消失,溶液由无色变为黄色
(3)
解答:(1)B为碳酸钠,化学式 ,D为盐酸,化学式HCl,E为氧化铁,化学式为 ,F为铁,化学式为Fe;(2)氧化铁和盐酸反应生成氯化铁和水,氯化铁溶液为黄色,现象是红棕色固体逐渐减少至消失,溶液由无色变为黄色;(3)氢氧化钠和二氧化碳反应生成碳酸钠和水,化学方程式为: 。
分析:推断题的关键是抓住题眼,本题的题眼是 D是胃液的主要成分,E是红棕色固体,F与D反应后所得溶液为浅绿色,C在工业上常用来生产肥皂。 结合题中的转化关系进行分析
12. (1)Fe;Na2CO3
(2)
(3)溶液中产生蓝色沉淀,蓝色溶液逐渐变为无色
解答:(1)由分析可知,A为铁,化学式为Fe;F为碳酸钠,化学式为Na2CO3;(2)D与E反应是稀硫酸与氢氧化钙反应生成硫酸钙和水,该反应的化学方程式为: ;(3)足量的C溶液加入到B溶液中,氢氧化钠与硫酸铜反应生成氢氧化铜和硫酸钠,氢氧化钠足量,故硫酸铜完全反应,故实验现象为:溶液中产生蓝色沉淀,蓝色溶液逐渐变为无色。
分析:推断题的关键是抓住题眼,本题的题眼是 A是黑色粉末,B和E可以用来配制波尔多液。 结合几种物质之间的反应进行分析
四、实验探究题
13. (1)溶液由无色变为红色;;固体;微溶于水,能与指示剂作用;能与某些非金属氧化物反应生成盐和水;能与酸反应生成盐和水
(2)产生大量气泡;
(3)无色溶液中逐渐有固体析出(变浑浊),滴盐酸后有气泡产生,固体逐渐溶解(消失)
(4)不合理,根据通入的CO2的量的不同情况,Y的溶质成分可能还有:NaOH和Na2CO3 , Na2CO3和NaHCO3 , NaHCO3这三种情况。三种情况均能与稀盐酸反应产生气体且使澄清石灰水变浑浊;
解答:(1)氢氧化钙溶液显碱性,向A烧杯中滴加几滴酚酞溶液,观察到的现象是溶液由无色变为红色,再加入过量稀盐酸,稀盐酸和氢氧化钙反应生成氯化钙和水,反应的化学方程式为 。由上述实验可知氢氧化钙的性质:固体;微溶于水(20℃时,溶解度0.16 g),能与指示剂作用;能与某些非金属氧化物反应生成盐和水;能与酸反应生成盐和水。
[实验拓展](2)向上述(1)反应后的A烧杯中滴加碳酸钠溶液,AB段是碳酸钠溶液先和上步过量的稀盐酸反应生成氯化钠、水、二氧化碳,pH上升;BC段是氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠;化学方程式为 。CD段是最后加入过量碳酸钠溶液。碳酸钠溶液显碱性。故AB段的实验现象是产生大量气泡,BC段发生反应的化学方程式为 。
[解释与结论](3)二氧化碳和氢氧化钠反应生成碳酸钠和水,二氧化碳和碳酸钠和水反应生成碳酸氢钠,盐酸和碳酸氢钠反应生成氯化钠、水和二氧化碳。经分析X是NaHCO3。所以实验过程中,Ⅰ中产生的现象是无色溶液中逐渐变浑浊,滴盐酸后有气泡产生,固体逐渐消失。
(4)乙组同学认为Y只有Na2CO3。不合理,根据通入的CO2的量的不同情况,Y的溶质成分可能还有:NaOH和Na2CO3(二氧化碳只够与部分氢氧化钠反应), Na2CO3和NaHCO3(二氧化碳将氢氧化钠反应全部反应完,且与部分碳酸钠反应),NaHCO3(二氧化碳将氢氧化钠反应全部反应完,且与将碳酸钠反应完)这三种情况。三种情况均能与稀盐酸反应产生气体且使澄清石灰水变浑浊。I 中一定发生反应为二氧化碳和氢氧化钠反应生成碳酸钠和水,化学方程式为 。
分析:(1)_??±??§??????è?????_无色酚酞试液变红色。
氢氧化钙与盐酸反应,生成氯化钙和水。
(2)碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳。
氯化钙和碳酸钠反应,生成碳酸钙沉淀和氯化钠。
(3)根据二氧化碳的化学性质,进行分析。
(4)二氧化碳和氢氧化钠反应生成碳酸钠和水。
五、综合题
14. (1)探究碱溶液_???????¤??????????_应
(2)2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
(3)紫色的石蕊试液(或锌粒或碳酸钠粉末等) 21教育名师原创作品
解答:(1)_???é??1??????é??_过氢氧化钠和氢氧化钙分别对石蕊试液和酚酞试液的作用,可以探究碱溶液与指示剂的反应;
(2)实验2中,氢氧化钠和硫酸铜反应生成蓝色氢氧化铜沉淀和硫酸钠,化学方程式为:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;
(3)实验3中观察到溶液由红色变为无色,氢氧化钠肯定全部被反应,此时溶液中除NaCl外(不考虑酚酞),溶液中可能存在的是盐酸。因此为了证明盐酸的存在与否,可以取适量的溶液滴加石蕊试液,若变成红色,或加入锌粒产生气泡等均可说明盐酸的存在。(合理即可)
分析:根据碱的性质,进行分析。
15. (1)③→⑥→⑩_??????????????????_
(2)2;碳酸钠
(3)NaCl+AgNO3=AgCl↓+NaNO3
(4)不能,氢氧化钾与二氧化碳反应,从而被“吃掉”。
解答:(1)根据图示的_???è?¨?????±??????_酸不能和二氧化碳、二氧化硫、不活泼金属铜和银、氯化钠、硫酸反应。
?故答案为:③→⑥→⑩→⑦→?→?
(2)中和反应是酸与碱反应,氢氧化钙、氢氧化钠为碱,所以碱有2种,故能发生中和反应有2个;
能与盐酸反应的盐只有碳酸钠。
(3)不能与盐酸反应的物质有:③⑥⑩?,氯化钠与硝酸银反应,生成氯化银沉淀和硝酸钠,其反应的化学方程式是:NaCl+AgNO3═AgCl↓+NaNO3 , 此反应是两种化合物相互交换成分生成两种新的化合物的反应类型,属于复分解反应。
(4)二氧化碳与氢氧化钾反应生成碳酸钾和水,
分析:(1)根据盐酸的性质,进行分析。
(2)根据中和反应的特点,进行分析。
(3)根据氯离子与银离子不共存,会生成氯化银沉淀,进行分析。
(4)根据氢氧化钾的性质,进行分析。
16. (1)CaCO3
(2),2NaOH+H2SO4=Na2SO4+2H2O
(3)H2O
(4)3
解答:CuCO3·Cu(OH)2与过量稀硫酸反应方程式为 ,因此气体是CO2 , 溶液A的溶质是CuSO4和H2SO4;
(1)CO2遇澄清石灰水生成H2O和CaCO3 , 故白色沉淀是CaCO3;
(2)溶液A的溶质是CuSO4和H2SO4 , CuSO4与NaOH反应生成硫酸钠和氢氧化铜,反应方程式为 ;硫酸与氢氧化钠反应生成硫酸钠和水,反应的化学方程式为: 2NaOH+H2SO4=Na2SO4+2H2O;
(3)经过③反应后,生成的蓝色沉淀是Cu(OH)2 , Cu(OH)2加热会产生两种氧化物CuO和H2O,故填H2O;
(4)因①的操作加入了过量的稀硫酸,因此溶液A中有两种溶质CuSO4和H2SO4;在滴加NaOH很少时,H2SO4未反应完,此时溶质有CuSO4、Na2SO4和H2SO4 , 溶质为3种;当H2SO4反应完全至生成蓝色沉淀最多之前,溶液中只有Na2SO4和CuSO4 , 溶质只有2种;当NaOH滴加生成沉淀最多时,溶液中只有1种溶质Na2SO4;当NaOH过量时,溶液中有2种溶质Na2SO4和NaOH;综上所述,向A中加入NaOH溶液,其溶质最多时可达3种,故填3。
分析:写出CuCO3·Cu(OH)2与过量稀硫酸反应的化学方程式。
(1)CO2与氢氧化钙反应生成CaCO3沉淀。
(2)根据CuSO4与NaOH反应生成硫酸钠和氢氧化铜,写出化学方程式;
根据硫酸与氢氧化钠反应生成硫酸钠和水,写出化学方程式。
(3)根据Cu(OH)2加热会生成CuO和H2O,进行分析。
(4)根据物质的性质,进行分析。
_21?????????è?????(www.21cnjy.com)_
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
