2020~2021学年人教版九年级下册 第09单元课题2溶解度(第2课时溶解度)学案
文档属性
| 名称 | 2020~2021学年人教版九年级下册 第09单元课题2溶解度(第2课时溶解度)学案 |

|
|
| 格式 | doc | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-12 00:00:00 | ||
图片预览

文档简介
第九单元 溶液
课题2溶解度
第2课时溶解度
一、溶解度
1、概念:固体的溶解度表示在一定温度下某物质(固态)
在100g溶剂中达到饱和状态所溶解的质量
通常溶剂指水
通常溶解度指物质在水中的溶解度
2、对概念的理解(溶解度四要素)
(1)明确温度
(2)溶剂的质量是100g(溶剂为水)
(3)溶液要达到饱和状态
(4)单位是g
【练习】20 ℃时,50 g水中溶解18 g食盐达到饱和,
则20 ℃时,NaCl的溶解度是( )
A.18 B.18 g C.36 D.36 g
3、影响固体物质溶解度的因素
溶质的种类,性质。
溶剂的种类,性质。 外界的温度
4、溶解度表示的意义
例:30℃KCl的溶解度为37.0g
表示的意义:在30℃时在100g水中最多溶解37.0gKCl,此时溶液达到饱和状态
【练习】60 ℃时,硝酸钾的溶解度为110 g。对这句话理解错误的是(B)
A.60 ℃时,100 g水中最多能溶解硝酸钾110 g
B.60 ℃时,100 g硝酸钾饱和溶液中含硝酸钾110 g
C.60 ℃时,硝酸钾饱和溶液中水与硝酸钾的质量比为100∶110
D.60 ℃时,将110 g硝酸钾溶解于100 g水中所得溶液为该温度下硝酸钾的饱和溶液
二、溶解性
1、概念:物质在20℃时溶解度的相对大小
绝对不溶于水的物质是没有的,
只说难溶
溶解性只能一般说明某种物质在水中溶解能力大小(物理性质)
溶解度是衡量溶解性大小的尺度,是物质溶解性的定量表示方法
【练习】将2.5 g硼酸在20 ℃时溶于50 g水中即达到饱和,
则一般把这种物质的溶解性划分为( )
A.易溶物质 B.可溶物质 C.微溶物质 D.难溶物质
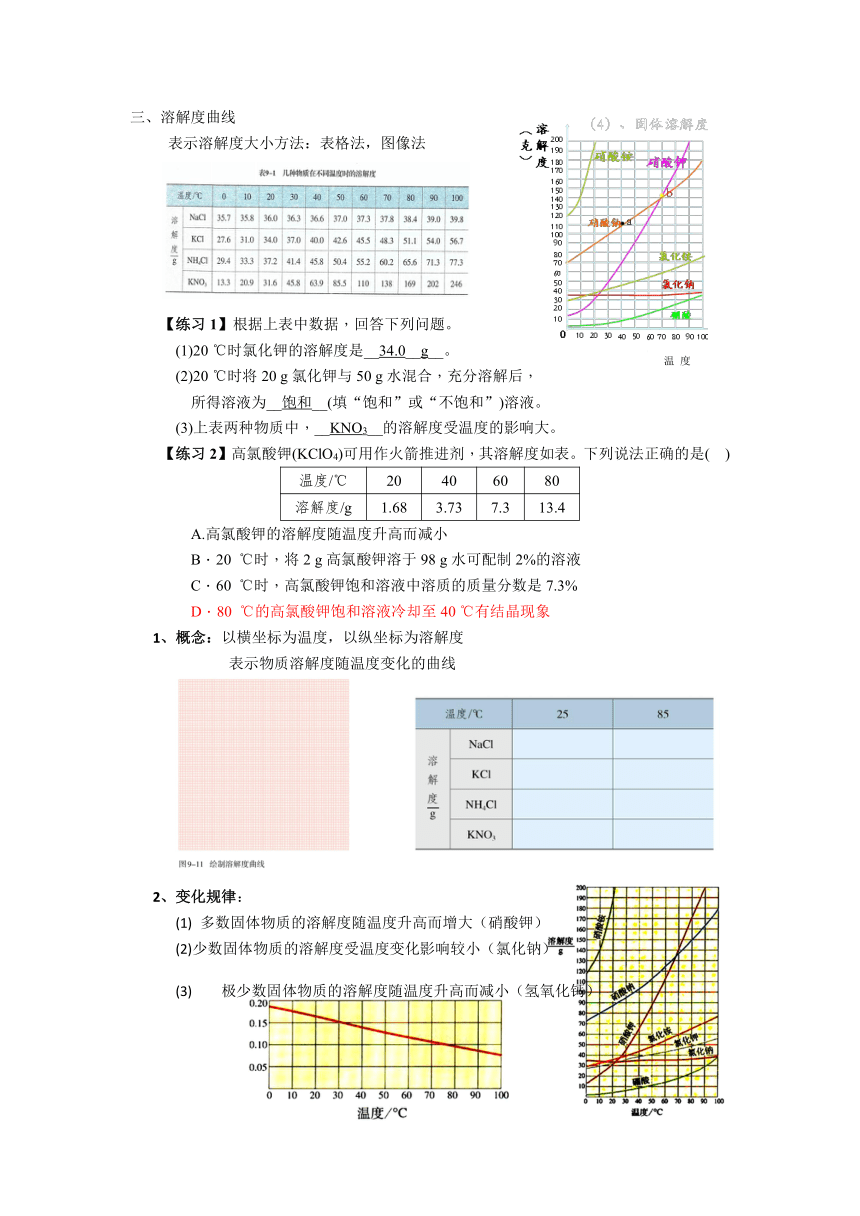
三、溶解度曲线
表示溶解度大小方法:表格法,图像法
【练习1】根据上表中数据,回答下列问题。
(1)20 ℃时氯化钾的溶解度是__34.0__g__。
(2)20 ℃时将20 g氯化钾与50 g水混合,充分溶解后,
所得溶液为__饱和__(填“饱和”或“不饱和”)溶液。
(3)上表两种物质中,__KNO3__的溶解度受温度的影响大。
【练习2】高氯酸钾(KClO4)可用作火箭推进剂,其溶解度如表。下列说法正确的是( )
温度/℃ 20 40 60 80
溶解度/g 1.68 3.73 7.3 13.4
A.高氯酸钾的溶解度随温度升高而减小
B.20 ℃时,将2 g高氯酸钾溶于98 g水可配制2%的溶液
C.60 ℃时,高氯酸钾饱和溶液中溶质的质量分数是7.3%
D.80 ℃的高氯酸钾饱和溶液冷却至40 ℃有结晶现象
1、概念:以横坐标为温度,以纵坐标为溶解度
表示物质溶解度随温度变化的曲线
2、变化规律:
(1) 多数固体物质的溶解度随温度升高而增大(硝酸钾)
(2)少数固体物质的溶解度受温度变化影响较小(氯化钠)
(3)极少数固体物质的溶解度随温度升高而减小(氢氧化钙)
3、运用
(1)可查出某物质在不同温度时的溶解度
(2)可比较不同物质在同一温度时溶解度的大小
(3)可比较不同物质的溶解度受温度变化影响的大小
(4)可看出物质的溶解度随温度变化的规律
(5)可以确定某种物质的饱和溶液(如何配制)
例: 水 20℃ NaCl 36g 溶 液
100g 36g 136g
50g 18g 68g
25g 9g 34g
(6)可以确定混合物分离的方法
【练习1】如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,
下列说法正确的是( )
A.t1 ℃时,丙的溶解度为70
B.乙中含有少量的甲,可用降温结晶的方法提纯乙
C.t2 ℃时,甲、乙两种物质的溶液分别降温到t1 ℃,
析出晶体的质量甲一定大于乙
D.丙中含有少量的甲,可用升高温度的方法提纯丙
【练习2】下图表示某物质在水(a)和酒精(b)中的溶解度曲线。下列有关该物质的说法
正确的是( )
A.在水和酒精中的溶解度相同
B.在水和酒精中的溶解度都随温度的升高而增大
C.20 ℃时,其水溶液比其酒精溶液的溶质质量分数大
D.40 ℃时,其水溶液的溶质质量分数为38%
4、溶解度曲线中交点意义
交点表示在t1℃时甲和乙溶解度相同,溶解度都为ag
A点表示在t2℃时丙的饱和溶液
C点表示在t2℃时丙的不饱和溶液
B点表示在t2℃时丙溶液不仅饱和
且溶液中有为溶解的丙
四、气体物质的溶解度
1、概念:指该气体的压强为101Kpa时和一定温度时,在1体积水里溶解达到饱和状态时气体体积。(在压强为101Kpa时,在一定温度下,在一个体积水里达到饱和状态时所溶解气体的体积。)
2、影响气体物质溶解度的因素
(1)气体种类
(2)气体性质
(3)溶剂种类
(4)溶剂性质
强调:(1)压强(压强增大溶解度增大)反之减小
(2)温度(温度升高,溶解度减小)反之增大
例题:(1)打开汽水瓶盖时,自动喷出汽水
(2)喝了汽水后会打嗝
【练习1】气体的溶解度与气体性质、溶剂有关,还与外界条件有关。“打开汽水瓶盖,汽水会自动喷出来”,这种现象与下列外界条件存在主要关系的是( )
A.压强 B.温度 C.汽水瓶 D.光照
【练习2】喝了汽水以后常常要打嗝,如图所示曲线中,能正确解释这一现象的是(B)
【练习3】压强为101 kPa时,硝酸钾和氨气在不同温度下的溶解度如下表。
下列说法正确的是(C)
温度/℃ 10 20 30 60
溶解度/g KNO3 20.9 31.6 45.8 110
NH3 70 56 44.5 20
A.两种物质的溶解度均随温度升高而增大
B.20 ℃时,KNO3饱和溶液中溶质的质量为31.6 g
C.60 ℃的KNO3饱和溶液降温至30 ℃,有晶体析出
D.NH3的溶解度与压强大小无关
3、如何增强养鱼池水中的含氧量:
(1)把水喷向空中。设置水泵。
(把水喷向空中可以增加水中氧气的溶解量)
(2)向鱼缸中通入空气。(可以增加水中的含氧量)
课题2溶解度
第2课时溶解度
一、溶解度
1、概念:固体的溶解度表示在一定温度下某物质(固态)
在100g溶剂中达到饱和状态所溶解的质量
通常溶剂指水
通常溶解度指物质在水中的溶解度
2、对概念的理解(溶解度四要素)
(1)明确温度
(2)溶剂的质量是100g(溶剂为水)
(3)溶液要达到饱和状态
(4)单位是g
【练习】20 ℃时,50 g水中溶解18 g食盐达到饱和,
则20 ℃时,NaCl的溶解度是( )
A.18 B.18 g C.36 D.36 g
3、影响固体物质溶解度的因素
溶质的种类,性质。
溶剂的种类,性质。 外界的温度
4、溶解度表示的意义
例:30℃KCl的溶解度为37.0g
表示的意义:在30℃时在100g水中最多溶解37.0gKCl,此时溶液达到饱和状态
【练习】60 ℃时,硝酸钾的溶解度为110 g。对这句话理解错误的是(B)
A.60 ℃时,100 g水中最多能溶解硝酸钾110 g
B.60 ℃时,100 g硝酸钾饱和溶液中含硝酸钾110 g
C.60 ℃时,硝酸钾饱和溶液中水与硝酸钾的质量比为100∶110
D.60 ℃时,将110 g硝酸钾溶解于100 g水中所得溶液为该温度下硝酸钾的饱和溶液
二、溶解性
1、概念:物质在20℃时溶解度的相对大小
绝对不溶于水的物质是没有的,
只说难溶
溶解性只能一般说明某种物质在水中溶解能力大小(物理性质)
溶解度是衡量溶解性大小的尺度,是物质溶解性的定量表示方法
【练习】将2.5 g硼酸在20 ℃时溶于50 g水中即达到饱和,
则一般把这种物质的溶解性划分为( )
A.易溶物质 B.可溶物质 C.微溶物质 D.难溶物质
三、溶解度曲线
表示溶解度大小方法:表格法,图像法
【练习1】根据上表中数据,回答下列问题。
(1)20 ℃时氯化钾的溶解度是__34.0__g__。
(2)20 ℃时将20 g氯化钾与50 g水混合,充分溶解后,
所得溶液为__饱和__(填“饱和”或“不饱和”)溶液。
(3)上表两种物质中,__KNO3__的溶解度受温度的影响大。
【练习2】高氯酸钾(KClO4)可用作火箭推进剂,其溶解度如表。下列说法正确的是( )
温度/℃ 20 40 60 80
溶解度/g 1.68 3.73 7.3 13.4
A.高氯酸钾的溶解度随温度升高而减小
B.20 ℃时,将2 g高氯酸钾溶于98 g水可配制2%的溶液
C.60 ℃时,高氯酸钾饱和溶液中溶质的质量分数是7.3%
D.80 ℃的高氯酸钾饱和溶液冷却至40 ℃有结晶现象
1、概念:以横坐标为温度,以纵坐标为溶解度
表示物质溶解度随温度变化的曲线
2、变化规律:
(1) 多数固体物质的溶解度随温度升高而增大(硝酸钾)
(2)少数固体物质的溶解度受温度变化影响较小(氯化钠)
(3)极少数固体物质的溶解度随温度升高而减小(氢氧化钙)
3、运用
(1)可查出某物质在不同温度时的溶解度
(2)可比较不同物质在同一温度时溶解度的大小
(3)可比较不同物质的溶解度受温度变化影响的大小
(4)可看出物质的溶解度随温度变化的规律
(5)可以确定某种物质的饱和溶液(如何配制)
例: 水 20℃ NaCl 36g 溶 液
100g 36g 136g
50g 18g 68g
25g 9g 34g
(6)可以确定混合物分离的方法
【练习1】如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,
下列说法正确的是( )
A.t1 ℃时,丙的溶解度为70
B.乙中含有少量的甲,可用降温结晶的方法提纯乙
C.t2 ℃时,甲、乙两种物质的溶液分别降温到t1 ℃,
析出晶体的质量甲一定大于乙
D.丙中含有少量的甲,可用升高温度的方法提纯丙
【练习2】下图表示某物质在水(a)和酒精(b)中的溶解度曲线。下列有关该物质的说法
正确的是( )
A.在水和酒精中的溶解度相同
B.在水和酒精中的溶解度都随温度的升高而增大
C.20 ℃时,其水溶液比其酒精溶液的溶质质量分数大
D.40 ℃时,其水溶液的溶质质量分数为38%
4、溶解度曲线中交点意义
交点表示在t1℃时甲和乙溶解度相同,溶解度都为ag
A点表示在t2℃时丙的饱和溶液
C点表示在t2℃时丙的不饱和溶液
B点表示在t2℃时丙溶液不仅饱和
且溶液中有为溶解的丙
四、气体物质的溶解度
1、概念:指该气体的压强为101Kpa时和一定温度时,在1体积水里溶解达到饱和状态时气体体积。(在压强为101Kpa时,在一定温度下,在一个体积水里达到饱和状态时所溶解气体的体积。)
2、影响气体物质溶解度的因素
(1)气体种类
(2)气体性质
(3)溶剂种类
(4)溶剂性质
强调:(1)压强(压强增大溶解度增大)反之减小
(2)温度(温度升高,溶解度减小)反之增大
例题:(1)打开汽水瓶盖时,自动喷出汽水
(2)喝了汽水后会打嗝
【练习1】气体的溶解度与气体性质、溶剂有关,还与外界条件有关。“打开汽水瓶盖,汽水会自动喷出来”,这种现象与下列外界条件存在主要关系的是( )
A.压强 B.温度 C.汽水瓶 D.光照
【练习2】喝了汽水以后常常要打嗝,如图所示曲线中,能正确解释这一现象的是(B)
【练习3】压强为101 kPa时,硝酸钾和氨气在不同温度下的溶解度如下表。
下列说法正确的是(C)
温度/℃ 10 20 30 60
溶解度/g KNO3 20.9 31.6 45.8 110
NH3 70 56 44.5 20
A.两种物质的溶解度均随温度升高而增大
B.20 ℃时,KNO3饱和溶液中溶质的质量为31.6 g
C.60 ℃的KNO3饱和溶液降温至30 ℃,有晶体析出
D.NH3的溶解度与压强大小无关
3、如何增强养鱼池水中的含氧量:
(1)把水喷向空中。设置水泵。
(把水喷向空中可以增加水中氧气的溶解量)
(2)向鱼缸中通入空气。(可以增加水中的含氧量)
同课章节目录
