2020-2021学年人教版初中化学九年级下册第九单元《溶液》测试题(含答案)
文档属性
| 名称 | 2020-2021学年人教版初中化学九年级下册第九单元《溶液》测试题(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 135.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-14 21:19:19 | ||
图片预览



文档简介
第九单元《溶液》测试题
一、单选题
1.下列说法中不正确的是( )
A.氧气在通常状况下是一种无色无味的气体
B.原子是化学变化中的最小粒子
C.浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液
D.水通电分解生成氢气和氧气,说明水中含有氢分子和氧分子
2.下列物质属于溶液的是
A.泥水
B.牛奶
C.碘酒
D.冰水
3.下列洗涤或除污过程应用乳化原理的是(
)
A.用钢丝球刷除炒菜锅上的污垢
B.用酒精除去衣服上的碘
C.用汽油除去衣服上的油污
D.用洗洁精洗去餐具上的油脂
4.下列说法正确的是()
A.均一稳定的液体一定是溶液
B.检测酒驾的重铬酸钾(K2Cr2O7)中铬元素的化合价为+7价
C.硫在氧气中燃烧产生明亮的蓝紫色火焰
D.厨房发生燃气泄漏应马上开灯检查
5.欲一次配制的氢氧化钠溶液,需要用到的一组仪器是(
)
A.量筒、天平、玻璃棒
B.量筒、烧杯、天平、玻璃棒
C.量筒、酒精灯、天平、玻璃棒
D.量筒、烧杯、天平、玻璃棒
6.甲、乙两种固体物质的溶解度曲线如图所示。下列说法正确的是( )
A.温度为时,100g甲、乙的饱和溶液,温度降到时,两溶液的质量仍然相等
B.温度为时,甲和乙各30g分别加入100g水中,均形成饱和溶液
C.温度为时,在100g水中加入50g乙,形成的是不饱和溶液
D.甲的溶解度大于乙
7.家用的碱面溶于水时温度会升高,原因是(
)
A.只发生水合过程
B.只发生扩散过程,并且放出热量
C.水合过程放出的热量大于扩散过程吸收的热量
D.扩散过程放出的热量大于水合过程吸收的热量
8.配制490g10%稀硫酸需要98%浓硫酸
(密度为1.84g/cm3)的体积为
A.29.4mL
B.27.2mL
C.30.8mL
D.25.3
mL
9.水与人们的生活息息相关,下列有关水的说法不正确的是( )
A.水是最常用的溶剂
B.过滤可除去水中所有杂质
C.用肥皂水可鉴别硬水和软水
D.将硬水加热煮沸能降低水的硬度
10.20℃时,NaCl
的溶解度为
36g。下列关于该温度下某
NaCl
饱和溶液的说法不正确的是(
)
A.该溶液中的微粒既有分子又有离子
B.该溶液的溶质质量分数一定比任意
NaCl
不饱和溶液的溶质质量分数大
C.将溶液升温至
30℃,其溶质质量分数不变
D.恒温蒸发
10g
水,会析出
3.6gNaCl
固体
11.如图是甲、乙、丙物质的溶解度曲线。下列说法正确的是
A.T1°C时,甲、丙饱和溶液的溶质质量分数相等
B.将甲溶液从T2°C降温至T1°C,一定有晶体析出
C.将甲、乙、丙的饱和溶液从T2°C降温至T1°C,所得溶液中溶质质量分数乙>甲=丙
D.T2°C时,在50g水中加入30g的甲,充分搅拌后得到80g溶液
12.下图是甲、乙两种不含结晶水的固体的溶解度曲线,下列说法正确的是
A.乙属于微溶物质
B.可用t1℃时20%的甲溶液配制10%的甲溶液
C.图中P点可以表示t3℃时甲的饱和溶液
D.分别将t3℃甲、乙饱和溶液降温至t2℃,所得溶液中溶质质量分数相等
13.下列有关溶液的说法正确的是(
)
A.将饱和澄清石灰水升温,可以观察到浑浊现象
B.配制溶液时,搅拌可以增大溶质的溶解度
C.将10%的KHNO3溶液倒出一半,剩余溶液中溶质的质量分数为20%
D.将高锰酸钾粉末与汽油混合,可以得到高锰酸钾的汽油溶液
14.甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示。下列说法正确的是(
)
A.甲物质的溶解度大于乙物质的溶解度
B.t1℃时甲、乙两物质的溶液溶质质量分数一定相等
C.t1℃时,甲、乙两物质各50
g分别加入100g水中,充分溶解,得到的溶液质量都是140g
D.t2℃时,等质量甲、乙两种固体配制成饱和溶液时甲比乙需要的水多
二、填空题
15.生命的孕育和维系需要水,人类的日常生活和工农业生产离不开水,水是最常用的溶剂。
(1)在水的净化中,活性炭表现出较强的吸附能力,是因为活性炭具有_______的结构。
(2)对水体取样,加入肥皂水后振荡,发现泡沫较多,浮渣较少,说明该水样为____(填“硬水”或“软水”)。
(3)电解水实验中得到的结论:水是由______组成。
(4)将少量下列物质分别放入水中,充分搅拌,可以得到无色溶液的是____(填字母)。
A
高锰酸钾
B
汽油
C
面粉
D
白糖
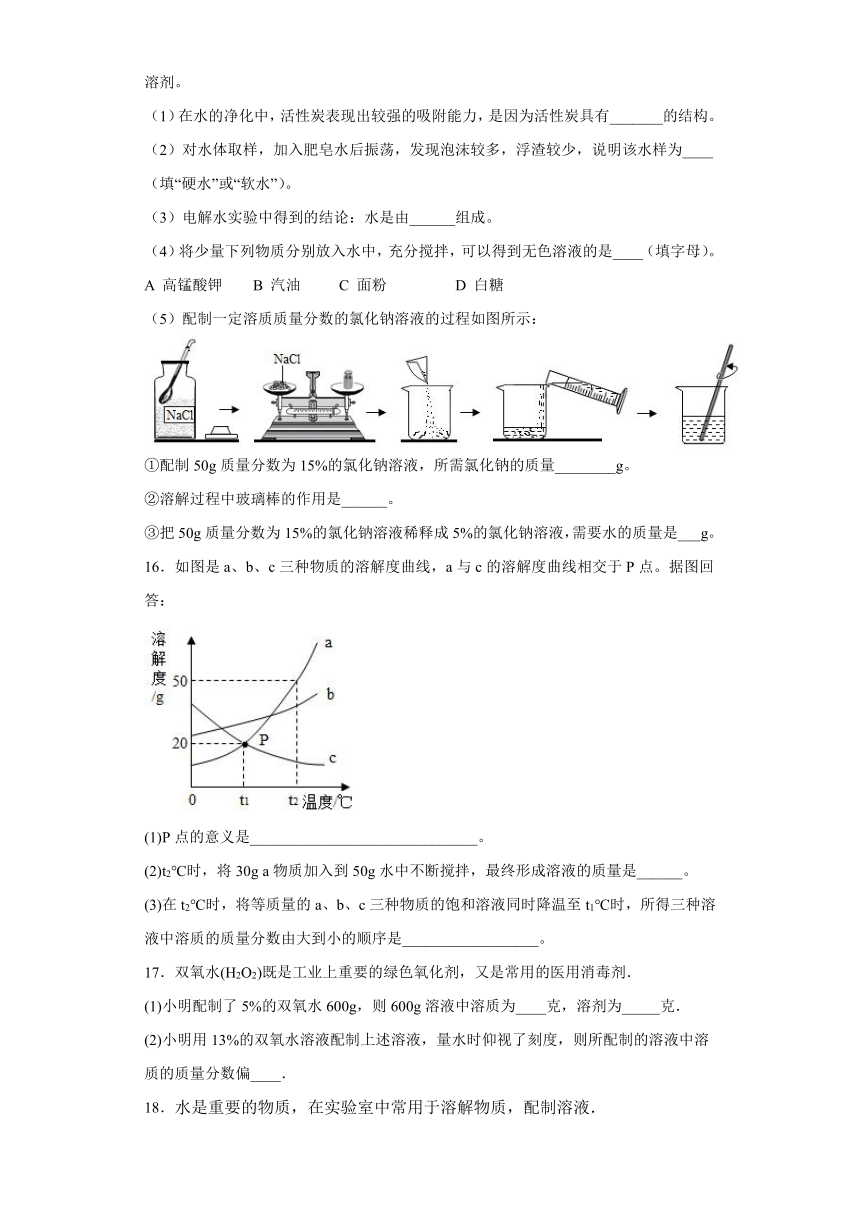
(5)配制一定溶质质量分数的氯化钠溶液的过程如图所示:
①配制50g质量分数为15%的氯化钠溶液,所需氯化钠的质量________g。
②溶解过程中玻璃棒的作用是______。
③把50g质量分数为15%的氯化钠溶液稀释成5%的氯化钠溶液,需要水的质量是___g。
16.如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:
(1)P点的意义是______________________________。
(2)t2℃时,将30g
a物质加入到50g水中不断搅拌,最终形成溶液的质量是______。
(3)在t2℃时,将等质量的a、b、c三种物质的饱和溶液同时降温至t1℃时,所得三种溶液中溶质的质量分数由大到小的顺序是__________________。
17.双氧水(H2O2)既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.
(1)小明配制了5%的双氧水600g,则600g溶液中溶质为____克,溶剂为_____克.
(2)小明用13%的双氧水溶液配制上述溶液,量水时仰视了刻度,则所配制的溶液中溶质的质量分数偏____.
18.水是重要的物质,在实验室中常用于溶解物质,配制溶液.
(1)水是最常见的溶剂,将少量下列物质分别加入水中,不能形成溶液的是______
A.面粉
B.白糖
C.冰块
D.植物油
E.硝酸钾
(2)含有较多可溶性钙、镁化合物的水叫做___________(填“软水”或“硬水”)。
加入___________可以区分硬水和软水。
(3)下列净化水的单一操作中,相对净化程度较高的是_____________(填字母)
A.静置沉淀
B.吸附沉淀
C.
蒸馏
(4)甲和乙两种固体物质的溶解度曲线如右下图所示,回答下列问题:
①在________℃时,甲和乙两种物质的溶解度相等。
②将t1℃时等质量的甲和乙两种物质的饱和溶液分别降温到0℃,析出固体质量较少的是______(填“甲”或“乙”)。
③t2℃时,将60
g甲物质放入100
g
水中,充分搅拌,所得溶液的溶质质量分数w(甲)与同温下乙物质的饱和溶液的溶质质量分数w(乙)大小关系为_______(填字母)。
A.
w(甲)<
w(乙)
B.w(甲)>
w(乙)
C.w(甲)=
w(乙)
D.无法确定
三、推断题
19.我国化工专家侯德榜创立了“侯氏制碱法”,促进了世界制碱技术的发展。其流程简图和部分物质的溶解度曲线如下:
已知:①母液中有一种铵态氮肥
②
请回答下列问题:
(1)操作a的名称是_____。
(2)结合图2分析,图1反应1中NaHCO3作为晶体析出的原因是_____,从图2中还能获得的一条信息是_____。
(3)图1中得到的母液中一定含有的阳离子是_____
(填离子符号),
流程中可以循环使用的物质是_____。
(4)从图2可以看出温度高于60°C,NaHCO3的溶解度曲线“消失”了,其原因可能是_____。
四、实验题
20.实验室有下列的仪器装置,请回答下列问题。
(1)配制50g质量分数5%的氯化钠溶液,不需要甲图中的仪器是
_______
(填名称),还缺少的仪器是
__________
;在量取水时,若仰视量筒凹液面的最低处,其他操作规范,则配制的溶液的质量分数
_____
(选填“大于”、“等于”或“小于”)5%。
(2)乙图A用于实验室制取氧气,请指出中的一处错误
____________________________
;若用乙图B来制取氧气,则反应的化学方程式是
________________________________________
。
(3)实验室用可图B或C来制取CO2,C装置相对于B操作上的优点是
_______________________
;用排空气法收集CO2,检验CO2集满的操作是
___________________________________
。
(4)下图是用排水法收集氧气的实验装置,请把下图补充完整。
________
(5)实验室用锌粒与稀硫酸反应制取氢气,发生装置如乙图图C所示。打开止水夹,若发现稀硫酸未能与有孔塑料板上锌粒接触,但此时已无稀硫酸可加,为不影响生成的气体量,则下列物质中,最适宜从长颈漏斗中添加的是
_______
(填字母)。
A.水
B.碳酸钠溶液
C.硫酸钠溶液
D.澄清石灰水
21.下表是硝酸钾和氯化铵在不同温度时的溶解度。分析表中数据,回答问题。
温度/℃
0
20
40
60
溶解度/g
KNO3
13.3
31.6
63.9
110
NH4Cl
29.4
37.2
45.8
55.2
(1)上述下图中,甲可表示________的溶解度曲线。
(2)60℃时,两种物质的饱和溶液中,溶质质量分数较小的是_____________。
(3)20℃时,按下图所示操作:B中的溶液是________(选填“饱和”或“不饱和”)溶液,C中溶液的溶质和溶剂质量比为_______。
五、计算题
22.200g15%的食盐溶液欲使其质量分数变为30%,若蒸发溶剂水,需要蒸发多少克水?若需要加入溶质食盐,需要加入多少克食盐?(写出计算步骤,如果结果出现小数,保留小数点后一位)
23.为测定某AgNO3溶液的溶质质量分数,用溶质质量分数为7.3%的稀盐酸进行滴定。现取待测液50.0g,滴定过程如图所示。
试计算恰好完全反应时,所得溶液的溶质质量分数(滴定反应为AgNO3+HCl=AgCl↓+HNO3,计算结果均保留1位小数)
参考答案
1.D
2.C
3.D
4.C
5.D
6.B
7.C
8.B
9.B
10.B
11.A
12.D
13.A
14.C
15.疏松多孔
软水
氢元素和氧元素
D
7.5
搅拌,加速溶解
100
16.t1℃时,a、c物质的溶解度相等,均为20g
75g
b>a>c
17.30
570
小
18.
ACD
硬水
肥皂水
C
20
乙
B
19.过滤
此温度下碳酸氢钠的溶解度较小
氯化铵的溶解度受温度的影响较大
Na+、NH4+
CO2
温度高于60℃时,碳酸氢钠开始分解
20.试管
托盘天平
小于
试管口没有略向下倾斜
2H2O2=
MnO2==2H2O+O2
↑
能使反应随时停止随时开始
把燃烧的木条放在集气瓶口
AC
21.KNO3或硝酸钾
NH4Cl或氯化铵
饱和
2:5
22.解:设需要蒸发水的质量是x,根据蒸发前后,溶质的质量不变,可得:200g×15%=(200g-x)×30%,x=100g;
解:设需要加入食盐的质量是y,则200g×15%+y=(200g+y)×30%,y≈42.9g。
23.解:由图像可知,滴加10.0g稀盐酸时恰好完全反应。
设恰好完全反应时生成HNO3的质量为x,
恰好完全反应时溶液的质量为
恰好完全反应时所得溶液溶质的质量分数
答:恰好完全反应时所得溶液溶质的质量分数为2.2%。
一、单选题
1.下列说法中不正确的是( )
A.氧气在通常状况下是一种无色无味的气体
B.原子是化学变化中的最小粒子
C.浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液
D.水通电分解生成氢气和氧气,说明水中含有氢分子和氧分子
2.下列物质属于溶液的是
A.泥水
B.牛奶
C.碘酒
D.冰水
3.下列洗涤或除污过程应用乳化原理的是(
)
A.用钢丝球刷除炒菜锅上的污垢
B.用酒精除去衣服上的碘
C.用汽油除去衣服上的油污
D.用洗洁精洗去餐具上的油脂
4.下列说法正确的是()
A.均一稳定的液体一定是溶液
B.检测酒驾的重铬酸钾(K2Cr2O7)中铬元素的化合价为+7价
C.硫在氧气中燃烧产生明亮的蓝紫色火焰
D.厨房发生燃气泄漏应马上开灯检查
5.欲一次配制的氢氧化钠溶液,需要用到的一组仪器是(
)
A.量筒、天平、玻璃棒
B.量筒、烧杯、天平、玻璃棒
C.量筒、酒精灯、天平、玻璃棒
D.量筒、烧杯、天平、玻璃棒
6.甲、乙两种固体物质的溶解度曲线如图所示。下列说法正确的是( )
A.温度为时,100g甲、乙的饱和溶液,温度降到时,两溶液的质量仍然相等
B.温度为时,甲和乙各30g分别加入100g水中,均形成饱和溶液
C.温度为时,在100g水中加入50g乙,形成的是不饱和溶液
D.甲的溶解度大于乙
7.家用的碱面溶于水时温度会升高,原因是(
)
A.只发生水合过程
B.只发生扩散过程,并且放出热量
C.水合过程放出的热量大于扩散过程吸收的热量
D.扩散过程放出的热量大于水合过程吸收的热量
8.配制490g10%稀硫酸需要98%浓硫酸
(密度为1.84g/cm3)的体积为
A.29.4mL
B.27.2mL
C.30.8mL
D.25.3
mL
9.水与人们的生活息息相关,下列有关水的说法不正确的是( )
A.水是最常用的溶剂
B.过滤可除去水中所有杂质
C.用肥皂水可鉴别硬水和软水
D.将硬水加热煮沸能降低水的硬度
10.20℃时,NaCl
的溶解度为
36g。下列关于该温度下某
NaCl
饱和溶液的说法不正确的是(
)
A.该溶液中的微粒既有分子又有离子
B.该溶液的溶质质量分数一定比任意
NaCl
不饱和溶液的溶质质量分数大
C.将溶液升温至
30℃,其溶质质量分数不变
D.恒温蒸发
10g
水,会析出
3.6gNaCl
固体
11.如图是甲、乙、丙物质的溶解度曲线。下列说法正确的是
A.T1°C时,甲、丙饱和溶液的溶质质量分数相等
B.将甲溶液从T2°C降温至T1°C,一定有晶体析出
C.将甲、乙、丙的饱和溶液从T2°C降温至T1°C,所得溶液中溶质质量分数乙>甲=丙
D.T2°C时,在50g水中加入30g的甲,充分搅拌后得到80g溶液
12.下图是甲、乙两种不含结晶水的固体的溶解度曲线,下列说法正确的是
A.乙属于微溶物质
B.可用t1℃时20%的甲溶液配制10%的甲溶液
C.图中P点可以表示t3℃时甲的饱和溶液
D.分别将t3℃甲、乙饱和溶液降温至t2℃,所得溶液中溶质质量分数相等
13.下列有关溶液的说法正确的是(
)
A.将饱和澄清石灰水升温,可以观察到浑浊现象
B.配制溶液时,搅拌可以增大溶质的溶解度
C.将10%的KHNO3溶液倒出一半,剩余溶液中溶质的质量分数为20%
D.将高锰酸钾粉末与汽油混合,可以得到高锰酸钾的汽油溶液
14.甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示。下列说法正确的是(
)
A.甲物质的溶解度大于乙物质的溶解度
B.t1℃时甲、乙两物质的溶液溶质质量分数一定相等
C.t1℃时,甲、乙两物质各50
g分别加入100g水中,充分溶解,得到的溶液质量都是140g
D.t2℃时,等质量甲、乙两种固体配制成饱和溶液时甲比乙需要的水多
二、填空题
15.生命的孕育和维系需要水,人类的日常生活和工农业生产离不开水,水是最常用的溶剂。
(1)在水的净化中,活性炭表现出较强的吸附能力,是因为活性炭具有_______的结构。
(2)对水体取样,加入肥皂水后振荡,发现泡沫较多,浮渣较少,说明该水样为____(填“硬水”或“软水”)。
(3)电解水实验中得到的结论:水是由______组成。
(4)将少量下列物质分别放入水中,充分搅拌,可以得到无色溶液的是____(填字母)。
A
高锰酸钾
B
汽油
C
面粉
D
白糖
(5)配制一定溶质质量分数的氯化钠溶液的过程如图所示:
①配制50g质量分数为15%的氯化钠溶液,所需氯化钠的质量________g。
②溶解过程中玻璃棒的作用是______。
③把50g质量分数为15%的氯化钠溶液稀释成5%的氯化钠溶液,需要水的质量是___g。
16.如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:
(1)P点的意义是______________________________。
(2)t2℃时,将30g
a物质加入到50g水中不断搅拌,最终形成溶液的质量是______。
(3)在t2℃时,将等质量的a、b、c三种物质的饱和溶液同时降温至t1℃时,所得三种溶液中溶质的质量分数由大到小的顺序是__________________。
17.双氧水(H2O2)既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.
(1)小明配制了5%的双氧水600g,则600g溶液中溶质为____克,溶剂为_____克.
(2)小明用13%的双氧水溶液配制上述溶液,量水时仰视了刻度,则所配制的溶液中溶质的质量分数偏____.
18.水是重要的物质,在实验室中常用于溶解物质,配制溶液.
(1)水是最常见的溶剂,将少量下列物质分别加入水中,不能形成溶液的是______
A.面粉
B.白糖
C.冰块
D.植物油
E.硝酸钾
(2)含有较多可溶性钙、镁化合物的水叫做___________(填“软水”或“硬水”)。
加入___________可以区分硬水和软水。
(3)下列净化水的单一操作中,相对净化程度较高的是_____________(填字母)
A.静置沉淀
B.吸附沉淀
C.
蒸馏
(4)甲和乙两种固体物质的溶解度曲线如右下图所示,回答下列问题:
①在________℃时,甲和乙两种物质的溶解度相等。
②将t1℃时等质量的甲和乙两种物质的饱和溶液分别降温到0℃,析出固体质量较少的是______(填“甲”或“乙”)。
③t2℃时,将60
g甲物质放入100
g
水中,充分搅拌,所得溶液的溶质质量分数w(甲)与同温下乙物质的饱和溶液的溶质质量分数w(乙)大小关系为_______(填字母)。
A.
w(甲)<
w(乙)
B.w(甲)>
w(乙)
C.w(甲)=
w(乙)
D.无法确定
三、推断题
19.我国化工专家侯德榜创立了“侯氏制碱法”,促进了世界制碱技术的发展。其流程简图和部分物质的溶解度曲线如下:
已知:①母液中有一种铵态氮肥
②
请回答下列问题:
(1)操作a的名称是_____。
(2)结合图2分析,图1反应1中NaHCO3作为晶体析出的原因是_____,从图2中还能获得的一条信息是_____。
(3)图1中得到的母液中一定含有的阳离子是_____
(填离子符号),
流程中可以循环使用的物质是_____。
(4)从图2可以看出温度高于60°C,NaHCO3的溶解度曲线“消失”了,其原因可能是_____。
四、实验题
20.实验室有下列的仪器装置,请回答下列问题。
(1)配制50g质量分数5%的氯化钠溶液,不需要甲图中的仪器是
_______
(填名称),还缺少的仪器是
__________
;在量取水时,若仰视量筒凹液面的最低处,其他操作规范,则配制的溶液的质量分数
_____
(选填“大于”、“等于”或“小于”)5%。
(2)乙图A用于实验室制取氧气,请指出中的一处错误
____________________________
;若用乙图B来制取氧气,则反应的化学方程式是
________________________________________
。
(3)实验室用可图B或C来制取CO2,C装置相对于B操作上的优点是
_______________________
;用排空气法收集CO2,检验CO2集满的操作是
___________________________________
。
(4)下图是用排水法收集氧气的实验装置,请把下图补充完整。
________
(5)实验室用锌粒与稀硫酸反应制取氢气,发生装置如乙图图C所示。打开止水夹,若发现稀硫酸未能与有孔塑料板上锌粒接触,但此时已无稀硫酸可加,为不影响生成的气体量,则下列物质中,最适宜从长颈漏斗中添加的是
_______
(填字母)。
A.水
B.碳酸钠溶液
C.硫酸钠溶液
D.澄清石灰水
21.下表是硝酸钾和氯化铵在不同温度时的溶解度。分析表中数据,回答问题。
温度/℃
0
20
40
60
溶解度/g
KNO3
13.3
31.6
63.9
110
NH4Cl
29.4
37.2
45.8
55.2
(1)上述下图中,甲可表示________的溶解度曲线。
(2)60℃时,两种物质的饱和溶液中,溶质质量分数较小的是_____________。
(3)20℃时,按下图所示操作:B中的溶液是________(选填“饱和”或“不饱和”)溶液,C中溶液的溶质和溶剂质量比为_______。
五、计算题
22.200g15%的食盐溶液欲使其质量分数变为30%,若蒸发溶剂水,需要蒸发多少克水?若需要加入溶质食盐,需要加入多少克食盐?(写出计算步骤,如果结果出现小数,保留小数点后一位)
23.为测定某AgNO3溶液的溶质质量分数,用溶质质量分数为7.3%的稀盐酸进行滴定。现取待测液50.0g,滴定过程如图所示。
试计算恰好完全反应时,所得溶液的溶质质量分数(滴定反应为AgNO3+HCl=AgCl↓+HNO3,计算结果均保留1位小数)
参考答案
1.D
2.C
3.D
4.C
5.D
6.B
7.C
8.B
9.B
10.B
11.A
12.D
13.A
14.C
15.疏松多孔
软水
氢元素和氧元素
D
7.5
搅拌,加速溶解
100
16.t1℃时,a、c物质的溶解度相等,均为20g
75g
b>a>c
17.30
570
小
18.
ACD
硬水
肥皂水
C
20
乙
B
19.过滤
此温度下碳酸氢钠的溶解度较小
氯化铵的溶解度受温度的影响较大
Na+、NH4+
CO2
温度高于60℃时,碳酸氢钠开始分解
20.试管
托盘天平
小于
试管口没有略向下倾斜
2H2O2=
MnO2==2H2O+O2
↑
能使反应随时停止随时开始
把燃烧的木条放在集气瓶口
AC
21.KNO3或硝酸钾
NH4Cl或氯化铵
饱和
2:5
22.解:设需要蒸发水的质量是x,根据蒸发前后,溶质的质量不变,可得:200g×15%=(200g-x)×30%,x=100g;
解:设需要加入食盐的质量是y,则200g×15%+y=(200g+y)×30%,y≈42.9g。
23.解:由图像可知,滴加10.0g稀盐酸时恰好完全反应。
设恰好完全反应时生成HNO3的质量为x,
恰好完全反应时溶液的质量为
恰好完全反应时所得溶液溶质的质量分数
答:恰好完全反应时所得溶液溶质的质量分数为2.2%。
同课章节目录
