2020-2021学年人教版化学九年级下册第九单元 溶液测试题(含答案)
文档属性
| 名称 | 2020-2021学年人教版化学九年级下册第九单元 溶液测试题(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 155.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-14 21:22:41 | ||
图片预览



文档简介
第9单元《溶液》测试题
一、单选题
1.下列物质不是溶液的是( )
A.食醋
B.泥浆
C.生理盐水
D.澄清石灰水
2.实验室配制50g溶质质量分数为6%的氯化钠溶液,下列做法正确的是(
)
A.用托盘天平称取5g氯化钠
B.用50mL量筒量取所需水的体积
C.溶解氯化钠时,使用的玻璃仪器有量筒、玻璃棒
D.将配制好的溶液装入广口瓶中,塞好瓶塞并贴上标签
3.MgSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示。下列说法正确的是( )
A.N点对应的MgSO4溶液升温或降温均都可能析出晶体
B.M点对应的MgSO4溶液是不饱和溶液
C.MgSO4饱和溶液的溶质质量分数随温度升高而增大
D.40℃时,MgSO4的溶解度为41g
4.有关溶液的说法中正确的是(
)
A.均一、稳定的液体一定是溶液
B.将面粉加入水中搅拌,可得到溶液
C.5%的酒精溶液中,酒精是溶质,水是溶剂
D.饱和溶液一定比不饱和溶液浓
5.下列叙述正确的是( )
A.用活性炭可将硬水软化
B.硝酸铵溶于水,溶液温度升高
C.用食盐水除去热水壶内壁的水垢
D.用汽油可除去衣服上的油污
6.甲、乙两种物质的溶解度曲线如图所示。下列叙述不正确的是(
)
A.t3℃时,将甲的饱和溶液变为不饱和溶液,可采取升温的方法
B.t1℃时,将甲、乙的饱和溶液各蒸发掉10g水,析出甲的质量大
C.t2℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等
D.分别将100g甲、乙的饱和溶液从t3℃降温到t1℃时,析出甲的质量大
7.下列成语所描述的过程,从化学的角度理解正确的是( )
A.点石成金:碳酸钙中含有金元素
B.釜底抽薪:木柴燃烧温度必须达到着火点
C.水乳交融:水和油混合物属于溶液
D.百炼成钢:发生的反应属于化合反应
8.在一定质量的某H2SO4溶液中加入足量的BaCl2溶液,所得沉淀质量等于原H2SO4溶液质量的1/2,则原H2SO4溶液中溶质的质量分数接近于(?
?)。
A.10.5%
B.21%
C.30%
D.42%
9.甲、乙两种固体物质的溶解度曲线如图所示。下列有关叙述中错误的是
A.t2℃时甲的溶解度比乙的大
B.将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大
C.升高温度可将甲的饱和溶液变成不饱和溶液
D.t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等
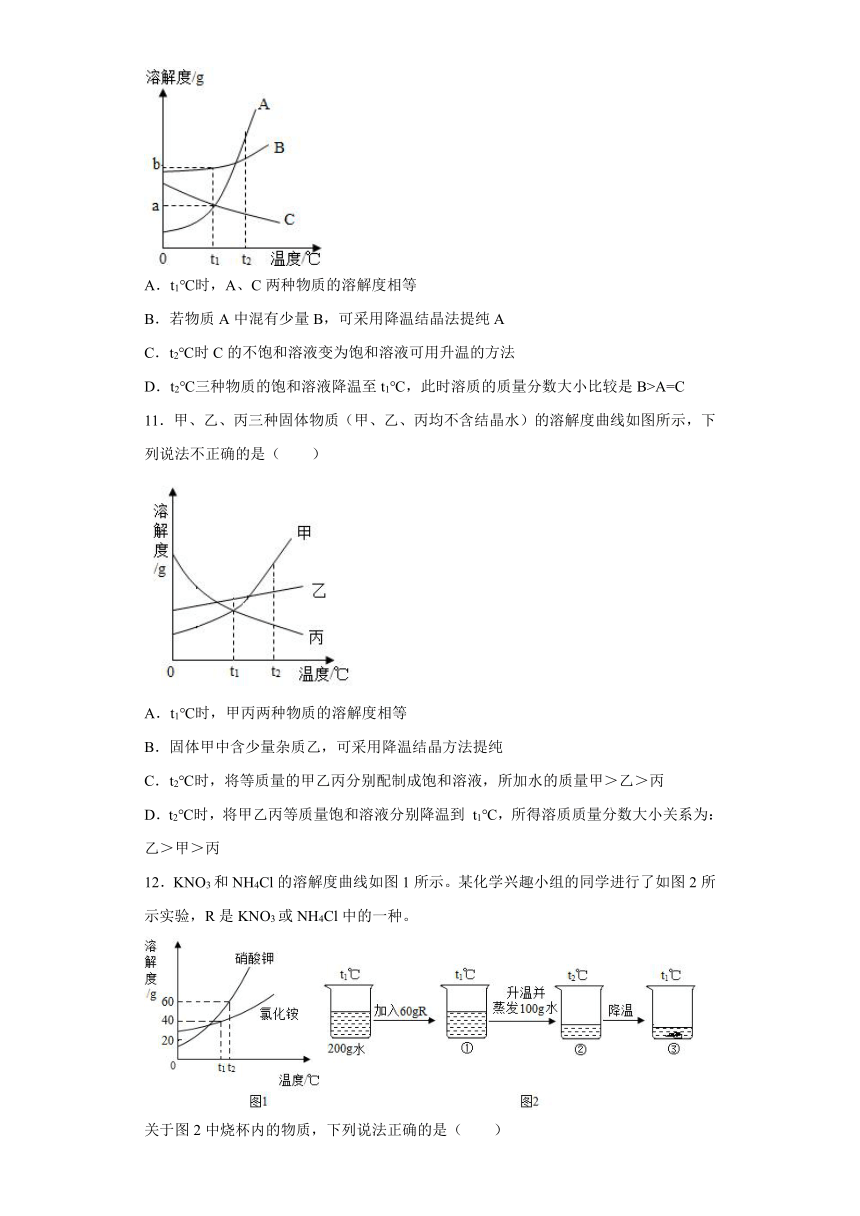
10.下图为A、B、C三种固体物质的溶解度曲线。下列有关说法错误的是
A.t1℃时,A、C两种物质的溶解度相等
B.若物质A中混有少量B,可采用降温结晶法提纯A
C.t2℃时C的不饱和溶液变为饱和溶液可用升温的方法
D.t2℃三种物质的饱和溶液降温至t1℃,此时溶质的质量分数大小比较是B>A=C
11.甲、乙、丙三种固体物质(甲、乙、丙均不含结晶水)的溶解度曲线如图所示,下列说法不正确的是( )
A.t1℃时,甲丙两种物质的溶解度相等
B.固体甲中含少量杂质乙,可采用降温结晶方法提纯
C.t2℃时,将等质量的甲乙丙分别配制成饱和溶液,所加水的质量甲>乙>丙
D.t2℃时,将甲乙丙等质量饱和溶液分别降温到
t1℃,所得溶质质量分数大小关系为:乙>甲>丙
12.KNO3和NH4Cl的溶解度曲线如图1所示。某化学兴趣小组的同学进行了如图2所示实验,R是KNO3或NH4Cl中的一种。
关于图2中烧杯内的物质,下列说法正确的是( )
A.R是
B.烧杯溶液的溶质质量分数小于烧杯
C.若使烧杯中的固体溶解,只能采用加水的方法
D.烧杯、、中,只有烧杯中上层清液是饱和溶液
13.小明同学梳理了以下知识:①有氧气参加的化合反应一定是氧化反应;②洗涤剂用来洗涤油污,是因为洗涤剂能溶解油污;③由同种元素组成的纯净物可能是单质;④最外层电子数为8的原子一定是稀有气体原子;⑤二氧化碳和氧气可以通过化学反应相互转化;⑥有单质参加或生成的反应中一定有化合价的改变;⑦溶液一定是澄清透明的、均一稳定的,但不一定是无色的;上面说法正确的是( )
A.①④⑤⑥⑦
B.③④⑤⑥⑦
C.①③④⑥⑦
D.①④⑤⑦
14.农业上常用质量分数为16%的氯化钠溶液来选种。下列方法能配制出该选种溶液的是
A.4g氯化钠和16g水
B.16g20%的氯化钠溶液和5g水
C.10g8%的氯化钠溶液蒸发4g水
D.14g10%的氯化钠溶液和1g氯化钠
15.类推是化学学习中常用的思维方法,以下结论中正确的是
A.由同种分子构成的物质是纯净物则纯净物都是由同种分子构成的
B.溶液具有均一稳定的特征.则均一稳定的物质一定是溶液
C.单质中只含有一种元素.所以含有一种元素的物质一定是单质
D.在同―化合物中金属元素显正价但非金属元素不一定显负价
二、填空题
16.晓楠在家里发现了许多有趣的化学问题请你帮助她解释或解决这些问题。
(1)妈妈做她最爱吃的“红烧肉”时加入了“加铁酱油”,其中“加铁酱油”中的“铁”指_____(填“元素”或“原子”),身体一旦缺铁可能贫血。
(2)她发现洗洁精能轻松除去碗碟上的油污,这是利用了洗洁精的______作用。
17.用化学用语填空
(1)标出过氧化氢中氧元素的化合价_________
(2)碘酒在医疗上常用来消炎,其溶剂是_____
(3)地壳中含量最多的金属元素和最多的非金属元素组成的物质_____
(4)写出符号中“2”的含义:Ca2+_____
(5)氯化铁中的阳离子_____.
18.如图为MgCl2和NaCl的溶解度曲线。
(1)t2℃时,MgC12饱和溶液的溶质质量分数_____NaC1饱和溶液的溶质质量分数(填“大于”“小于”“等于”“无法确定”之一)。
(2)t1℃时,一小试管内盛有MgCl2的饱和溶液,试管底部还存有少许MgCl2固体,将小试管放入盛有水的烧杯中,现将多量的氢氧化钠固体加入烧杯内的水中(如图所示),小试管内的固体物质逐渐溶解,原因是_____。
19.在一个温度不变的密闭容器内,放入一杯饱和的硫酸铜溶液,用细线吊住一块有缺口的硫酸铜晶体浸在溶液中(如右图)过几天后观察到:晶体上的缺口_____(填“有”或“没有”)了;晶体的质量____(填“减小”、“增大”或“没变”);此时的硫酸铜溶液是_____(填“饱和”或“不饱和”溶液)。
20.水和溶液对于人类的生产和生命活动有重大的意义。
(1)电解水的实验中,正负两极产生气体的体积比为___________,通过实验可以得出水是由___________组成的。
(2)用氯化钠固体和水配制6%的氯化钠溶液,如图正确的操作顺序是___________(填字母序号),若量取水时仰视读数,其它操作均正确,则配制的氯化钠溶液中溶质质量分数___________6%(填“>”“<”或“=”)。
三、推断题
21.柠檬酸亚铁是重要的含铁试剂,兴趣小组制取柠檬酸亚铁溶液的实验流程如图:
(1)写出反应1的化学方程式:__________;
(2)操作1的名称为__________;
(3)反应3中会有气体生成,该气体是_________;
(4)柠檬酸亚铁的化学式为FeC6H6O7,柠檬酸亚铁中铁元素和碳元素质量比为________;
(5)若选用的稀硫酸溶质的质量分数为12%,则用100mL98%的浓硫酸(密度为1.8g/cm3)配制该稀硫酸,需加水________g。
四、实验题
22.我县各学区都进行了部分学生化学实验操作竞赛,某学区竞赛题目之一是“配制70g20%的氯化钠溶液"。该实验的部分操作如下图所示。
(1)用托盘天平称量所需的氯化钠,托盘天平调节平衡后,接下来的操作应该是_____________(填字母)。
A
先在左盘纸片上加氯化钠,后在右盘纸片上加砝码
B
先在右盘纸片上加砝码,后在左盘纸片上加氯化钠
(2)称量时A出现了右盘低的现象,接下来的操作应该是______________;
①平衡螺母向左调
②移动游码
③右盘中减少砝码
④左盘中增加食盐
⑤左盘中减少食盐
(3)量取水时,如果按照图B的方法读数,会使配制的溶液溶质质量分数_______________________(填“偏大”或“偏小”)
(4)配制溶液时主要操作步骤是计算、称量、__________________
、装
瓶存放,
C操作中
用玻璃棒搅拌的作用是_______________________。
(5)
D中所贴标签有不妥之处,请在方框中写出你认为适合的内容_________________。
23.化学通过实验研究物质的组成、性质和变化规律。
甲
乙
丙
丁
?
?
?
?
探究影响物质溶解性的因素
探究水的组成
探究?CO2?性质
探究燃烧条件
①实验甲中,发现B中固体可溶,A中几乎不溶,说明影响物质溶解性的因素是______,补充C试管实验,想探究的影响因素是____。
②实验乙中,观察到集气瓶内壁有______产生。可以得出结论:水由______两种元素组成。
③实验丙中,观察到的现象是_______,体现了二氧化碳_______性质。
④实验丁中,磷燃烧的化学方程式_______,其中热水的作用是_______。
五、计算题
24.某同学用图甲气体发生装置来制取二氧化碳,在实验室里,他找到了石灰石、无标签的稀盐酸一瓶。该同学把部分石灰石和100g稀盐酸装入发生装置中,用天平称量发生装置里面物质的总质量,发现总质量的减小值m与反应时间t的关系如图乙所示,最后还有少量石灰石剩余。
(1)最终生成二氧化碳的质量为_______g。
(2)反应所用稀盐酸的溶质质量分数是多少?
25.某同学为了测定石灰石中碳酸钙的质量分数进行了如下实验。取12.5g的石灰石样品研碎和100g溶质质量分数为10%的稀盐酸放入烧杯中,石灰石中的碳酸钙与盐酸恰好完全反应(假设杂质不溶于水,也不与稀盐酸反应。),最终烧杯内物质的质量为108.1g。请计算:
(1)生成二氧化碳气体的质量是多少;
(2)反应后溶液中溶质的质量分数。(计算结果精确至0.1
%
)
参考答案
1.B
2.B
3.A
4.C
5.D
6.B
7.D
8.B
9.B
10.D
11.C
12.B
13.D
14.D
15.D
16.元素
乳化
17.H22
C2H5OH
Al2O3
一个钙离子带有两个单位的正电荷
Fe3+
18.大于
氢氧化钠固体溶于水使溶液温度升高,氯化镁的溶解度随温度升高而增大,所以小试管中的固体逐渐溶解
19.没有
没变
饱和
20.1:2
氢元素和氧元素
BCAED
<
21.Fe
+
H2SO4
=
Fe
SO4
+
H2↑
过滤
CO2
7
:
9
1290
22.B
④
偏小
溶解
加速溶解
23.溶剂种类
溶质种类
水珠
氢、氧
蜡烛由下而上先后熄灭
密度比空气大、不可燃、不助燃
4P+5O22P2O5
隔绝氧气、提供热量
24.(1)4.4
(2)设:生成4.4g二氧化碳气体需要氯化氢的质量为x
x=7.3g
所用稀盐酸的溶质质量分数是
答:所用稀盐酸的溶质质量分数是7.3%。
25.(1)4.4
(2)10.5%
一、单选题
1.下列物质不是溶液的是( )
A.食醋
B.泥浆
C.生理盐水
D.澄清石灰水
2.实验室配制50g溶质质量分数为6%的氯化钠溶液,下列做法正确的是(
)
A.用托盘天平称取5g氯化钠
B.用50mL量筒量取所需水的体积
C.溶解氯化钠时,使用的玻璃仪器有量筒、玻璃棒
D.将配制好的溶液装入广口瓶中,塞好瓶塞并贴上标签
3.MgSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示。下列说法正确的是( )
A.N点对应的MgSO4溶液升温或降温均都可能析出晶体
B.M点对应的MgSO4溶液是不饱和溶液
C.MgSO4饱和溶液的溶质质量分数随温度升高而增大
D.40℃时,MgSO4的溶解度为41g
4.有关溶液的说法中正确的是(
)
A.均一、稳定的液体一定是溶液
B.将面粉加入水中搅拌,可得到溶液
C.5%的酒精溶液中,酒精是溶质,水是溶剂
D.饱和溶液一定比不饱和溶液浓
5.下列叙述正确的是( )
A.用活性炭可将硬水软化
B.硝酸铵溶于水,溶液温度升高
C.用食盐水除去热水壶内壁的水垢
D.用汽油可除去衣服上的油污
6.甲、乙两种物质的溶解度曲线如图所示。下列叙述不正确的是(
)
A.t3℃时,将甲的饱和溶液变为不饱和溶液,可采取升温的方法
B.t1℃时,将甲、乙的饱和溶液各蒸发掉10g水,析出甲的质量大
C.t2℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等
D.分别将100g甲、乙的饱和溶液从t3℃降温到t1℃时,析出甲的质量大
7.下列成语所描述的过程,从化学的角度理解正确的是( )
A.点石成金:碳酸钙中含有金元素
B.釜底抽薪:木柴燃烧温度必须达到着火点
C.水乳交融:水和油混合物属于溶液
D.百炼成钢:发生的反应属于化合反应
8.在一定质量的某H2SO4溶液中加入足量的BaCl2溶液,所得沉淀质量等于原H2SO4溶液质量的1/2,则原H2SO4溶液中溶质的质量分数接近于(?
?)。
A.10.5%
B.21%
C.30%
D.42%
9.甲、乙两种固体物质的溶解度曲线如图所示。下列有关叙述中错误的是
A.t2℃时甲的溶解度比乙的大
B.将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大
C.升高温度可将甲的饱和溶液变成不饱和溶液
D.t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等
10.下图为A、B、C三种固体物质的溶解度曲线。下列有关说法错误的是
A.t1℃时,A、C两种物质的溶解度相等
B.若物质A中混有少量B,可采用降温结晶法提纯A
C.t2℃时C的不饱和溶液变为饱和溶液可用升温的方法
D.t2℃三种物质的饱和溶液降温至t1℃,此时溶质的质量分数大小比较是B>A=C
11.甲、乙、丙三种固体物质(甲、乙、丙均不含结晶水)的溶解度曲线如图所示,下列说法不正确的是( )
A.t1℃时,甲丙两种物质的溶解度相等
B.固体甲中含少量杂质乙,可采用降温结晶方法提纯
C.t2℃时,将等质量的甲乙丙分别配制成饱和溶液,所加水的质量甲>乙>丙
D.t2℃时,将甲乙丙等质量饱和溶液分别降温到
t1℃,所得溶质质量分数大小关系为:乙>甲>丙
12.KNO3和NH4Cl的溶解度曲线如图1所示。某化学兴趣小组的同学进行了如图2所示实验,R是KNO3或NH4Cl中的一种。
关于图2中烧杯内的物质,下列说法正确的是( )
A.R是
B.烧杯溶液的溶质质量分数小于烧杯
C.若使烧杯中的固体溶解,只能采用加水的方法
D.烧杯、、中,只有烧杯中上层清液是饱和溶液
13.小明同学梳理了以下知识:①有氧气参加的化合反应一定是氧化反应;②洗涤剂用来洗涤油污,是因为洗涤剂能溶解油污;③由同种元素组成的纯净物可能是单质;④最外层电子数为8的原子一定是稀有气体原子;⑤二氧化碳和氧气可以通过化学反应相互转化;⑥有单质参加或生成的反应中一定有化合价的改变;⑦溶液一定是澄清透明的、均一稳定的,但不一定是无色的;上面说法正确的是( )
A.①④⑤⑥⑦
B.③④⑤⑥⑦
C.①③④⑥⑦
D.①④⑤⑦
14.农业上常用质量分数为16%的氯化钠溶液来选种。下列方法能配制出该选种溶液的是
A.4g氯化钠和16g水
B.16g20%的氯化钠溶液和5g水
C.10g8%的氯化钠溶液蒸发4g水
D.14g10%的氯化钠溶液和1g氯化钠
15.类推是化学学习中常用的思维方法,以下结论中正确的是
A.由同种分子构成的物质是纯净物则纯净物都是由同种分子构成的
B.溶液具有均一稳定的特征.则均一稳定的物质一定是溶液
C.单质中只含有一种元素.所以含有一种元素的物质一定是单质
D.在同―化合物中金属元素显正价但非金属元素不一定显负价
二、填空题
16.晓楠在家里发现了许多有趣的化学问题请你帮助她解释或解决这些问题。
(1)妈妈做她最爱吃的“红烧肉”时加入了“加铁酱油”,其中“加铁酱油”中的“铁”指_____(填“元素”或“原子”),身体一旦缺铁可能贫血。
(2)她发现洗洁精能轻松除去碗碟上的油污,这是利用了洗洁精的______作用。
17.用化学用语填空
(1)标出过氧化氢中氧元素的化合价_________
(2)碘酒在医疗上常用来消炎,其溶剂是_____
(3)地壳中含量最多的金属元素和最多的非金属元素组成的物质_____
(4)写出符号中“2”的含义:Ca2+_____
(5)氯化铁中的阳离子_____.
18.如图为MgCl2和NaCl的溶解度曲线。
(1)t2℃时,MgC12饱和溶液的溶质质量分数_____NaC1饱和溶液的溶质质量分数(填“大于”“小于”“等于”“无法确定”之一)。
(2)t1℃时,一小试管内盛有MgCl2的饱和溶液,试管底部还存有少许MgCl2固体,将小试管放入盛有水的烧杯中,现将多量的氢氧化钠固体加入烧杯内的水中(如图所示),小试管内的固体物质逐渐溶解,原因是_____。
19.在一个温度不变的密闭容器内,放入一杯饱和的硫酸铜溶液,用细线吊住一块有缺口的硫酸铜晶体浸在溶液中(如右图)过几天后观察到:晶体上的缺口_____(填“有”或“没有”)了;晶体的质量____(填“减小”、“增大”或“没变”);此时的硫酸铜溶液是_____(填“饱和”或“不饱和”溶液)。
20.水和溶液对于人类的生产和生命活动有重大的意义。
(1)电解水的实验中,正负两极产生气体的体积比为___________,通过实验可以得出水是由___________组成的。
(2)用氯化钠固体和水配制6%的氯化钠溶液,如图正确的操作顺序是___________(填字母序号),若量取水时仰视读数,其它操作均正确,则配制的氯化钠溶液中溶质质量分数___________6%(填“>”“<”或“=”)。
三、推断题
21.柠檬酸亚铁是重要的含铁试剂,兴趣小组制取柠檬酸亚铁溶液的实验流程如图:
(1)写出反应1的化学方程式:__________;
(2)操作1的名称为__________;
(3)反应3中会有气体生成,该气体是_________;
(4)柠檬酸亚铁的化学式为FeC6H6O7,柠檬酸亚铁中铁元素和碳元素质量比为________;
(5)若选用的稀硫酸溶质的质量分数为12%,则用100mL98%的浓硫酸(密度为1.8g/cm3)配制该稀硫酸,需加水________g。
四、实验题
22.我县各学区都进行了部分学生化学实验操作竞赛,某学区竞赛题目之一是“配制70g20%的氯化钠溶液"。该实验的部分操作如下图所示。
(1)用托盘天平称量所需的氯化钠,托盘天平调节平衡后,接下来的操作应该是_____________(填字母)。
A
先在左盘纸片上加氯化钠,后在右盘纸片上加砝码
B
先在右盘纸片上加砝码,后在左盘纸片上加氯化钠
(2)称量时A出现了右盘低的现象,接下来的操作应该是______________;
①平衡螺母向左调
②移动游码
③右盘中减少砝码
④左盘中增加食盐
⑤左盘中减少食盐
(3)量取水时,如果按照图B的方法读数,会使配制的溶液溶质质量分数_______________________(填“偏大”或“偏小”)
(4)配制溶液时主要操作步骤是计算、称量、__________________
、装
瓶存放,
C操作中
用玻璃棒搅拌的作用是_______________________。
(5)
D中所贴标签有不妥之处,请在方框中写出你认为适合的内容_________________。
23.化学通过实验研究物质的组成、性质和变化规律。
甲
乙
丙
丁
?
?
?
?
探究影响物质溶解性的因素
探究水的组成
探究?CO2?性质
探究燃烧条件
①实验甲中,发现B中固体可溶,A中几乎不溶,说明影响物质溶解性的因素是______,补充C试管实验,想探究的影响因素是____。
②实验乙中,观察到集气瓶内壁有______产生。可以得出结论:水由______两种元素组成。
③实验丙中,观察到的现象是_______,体现了二氧化碳_______性质。
④实验丁中,磷燃烧的化学方程式_______,其中热水的作用是_______。
五、计算题
24.某同学用图甲气体发生装置来制取二氧化碳,在实验室里,他找到了石灰石、无标签的稀盐酸一瓶。该同学把部分石灰石和100g稀盐酸装入发生装置中,用天平称量发生装置里面物质的总质量,发现总质量的减小值m与反应时间t的关系如图乙所示,最后还有少量石灰石剩余。
(1)最终生成二氧化碳的质量为_______g。
(2)反应所用稀盐酸的溶质质量分数是多少?
25.某同学为了测定石灰石中碳酸钙的质量分数进行了如下实验。取12.5g的石灰石样品研碎和100g溶质质量分数为10%的稀盐酸放入烧杯中,石灰石中的碳酸钙与盐酸恰好完全反应(假设杂质不溶于水,也不与稀盐酸反应。),最终烧杯内物质的质量为108.1g。请计算:
(1)生成二氧化碳气体的质量是多少;
(2)反应后溶液中溶质的质量分数。(计算结果精确至0.1
%
)
参考答案
1.B
2.B
3.A
4.C
5.D
6.B
7.D
8.B
9.B
10.D
11.C
12.B
13.D
14.D
15.D
16.元素
乳化
17.H22
C2H5OH
Al2O3
一个钙离子带有两个单位的正电荷
Fe3+
18.大于
氢氧化钠固体溶于水使溶液温度升高,氯化镁的溶解度随温度升高而增大,所以小试管中的固体逐渐溶解
19.没有
没变
饱和
20.1:2
氢元素和氧元素
BCAED
<
21.Fe
+
H2SO4
=
Fe
SO4
+
H2↑
过滤
CO2
7
:
9
1290
22.B
④
偏小
溶解
加速溶解
23.溶剂种类
溶质种类
水珠
氢、氧
蜡烛由下而上先后熄灭
密度比空气大、不可燃、不助燃
4P+5O22P2O5
隔绝氧气、提供热量
24.(1)4.4
(2)设:生成4.4g二氧化碳气体需要氯化氢的质量为x
x=7.3g
所用稀盐酸的溶质质量分数是
答:所用稀盐酸的溶质质量分数是7.3%。
25.(1)4.4
(2)10.5%
同课章节目录
