2020-2021学年九年级化学鲁教版下册第八单元《海水中的化学》测试题(含答案)
文档属性
| 名称 | 2020-2021学年九年级化学鲁教版下册第八单元《海水中的化学》测试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 189.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-15 00:00:00 | ||
图片预览


文档简介
本卷由系统自动生成,请仔细校对后使用,答案仅供参考。
《海水中的化学》测试题
一、单选题
1.以下四个变化中,其中一个与其他三个有本质区别的是(
)
A.自来水厂在水中通入氯气进行消毒
B.点燃试管内的氢气产生尖锐的爆鸣声
C.用镶有金刚石的玻璃刀裁玻璃
D.往装有碳酸钠粉末的烧杯中加入稀盐酸产生大量气泡
2.下列各组离子在指定的溶液中能大量共存的一组是
A.在氯化铵溶液中:
Ag+
Cu2+
OH-
B.在稀盐酸中:
Zn2+
Mg2+
CO32-
C.在硝酸钠溶液中:
K+
Ca2+
Cl-
D.在氢氧化钡溶液中:
H+
Na+
SO42-
3.下列各组内物质间的转化关系中,不能一步转化的是(
)
A.Mg→MgO→MgSO4
B.H2O2→O2→H2O
C.KCl→KNO3→KOH
D.NaHCO3→Na2CO3→NaOH
4.下面是王华同学从“错题集”摘抄的部分内容,其中需加以改正的是( )
A.洗涤剂能除去油污,是因为它具有乳化作用
B.8gCaO溶于92g水中,所得溶液中溶质的质量分数为8%
C.喝下汽水后,常会打嗝,说明气体的溶解度随温度的升高而减小
D.配制100g
10%
的氯化钠溶液的主要步骤是:计算、称量、溶解、装瓶贴标签
5.将碳酸钙中的少量碳酸钠杂质除去,应该选用下列方法中的(
)
A.加入稀盐酸搅拌,过滤
B.加入足量水搅拌,过滤
C.高温加热固体
D.加入过量的石灰水,蒸发
6.下列各组离子能在pH=12的溶液中共存的一组是
A.H+、K+、CO
B.Ba2+、OH-、SO
C.Na+、Cl-、NO
D.Mg2+、NH、SO
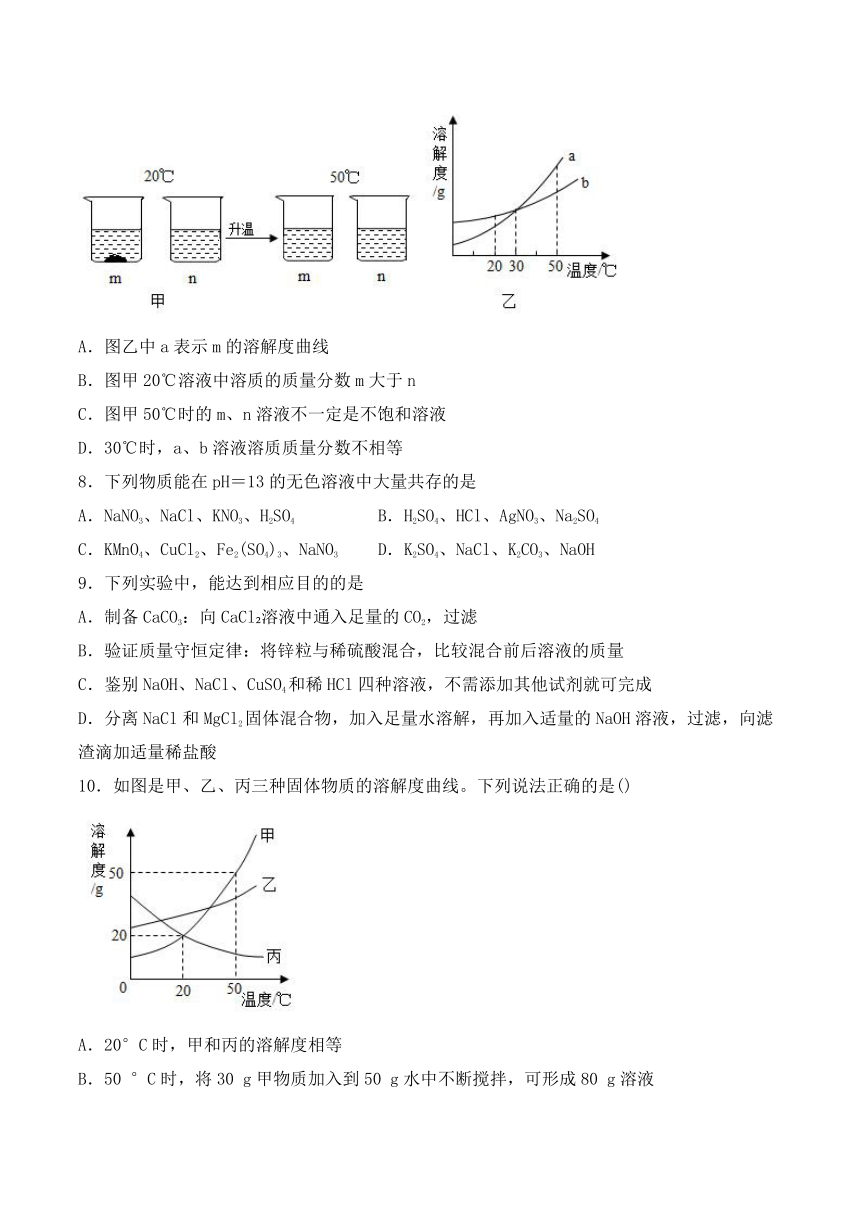
7.20℃时,将等质量的m、n两种固体,分别加入到盛有100g水的烧杯中,充分搅拌后,再升温到50℃时,现象如图甲,m、n两种固体的溶解度曲线如图乙。下列说法正确的是(
)
A.图乙中a表示m的溶解度曲线
B.图甲20℃溶液中溶质的质量分数m大于n
C.图甲50℃时的m、n溶液不一定是不饱和溶液
D.30℃时,a、b溶液溶质质量分数不相等
8.下列物质能在pH=13的无色溶液中大量共存的是
A.NaNO3、NaCl、KNO3、H2SO4
B.H2SO4、HCl、AgNO3、Na2SO4
C.KMnO4、CuCl2、Fe2(SO4)3、NaNO3
D.K2SO4、NaCl、K2CO3、NaOH
9.下列实验中,能达到相应目的的是
A.制备CaCO3:向CaCl?溶液中通入足量的CO2,过滤
B.验证质量守恒定律:将锌粒与稀硫酸混合,比较混合前后溶液的质量
C.鉴别NaOH、NaCl、CuSO4和稀HCl四种溶液,不需添加其他试剂就可完成
D.分离NaCl和MgCl2固体混合物,加入足量水溶解,再加入适量的NaOH溶液,过滤,向滤渣滴加适量稀盐酸
10.如图是甲、乙、丙三种固体物质的溶解度曲线。下列说法正确的是()
A.20°C时,甲和丙的溶解度相等
B.50
°C时,将30
g甲物质加入到50
g水中不断搅拌,可形成80
g溶液
C.甲中混有少量丙时,可用蒸发结晶的方法提纯甲
D.将三种物质的饱和溶液从50
°C降温至20
°C
,所得溶液溶质质量分数的大小关系是:乙>甲=丙
11.下列涉及学科观点的说法中正确的是
A.微粒观:氢气是由氢原子构成的
B.分类观:纯碱属于碱
C.转化观:CO2和CaCO3可以相互转化
D.守恒观:2mL一氧化碳和1mL氧气反应生成3mL二氧化碳
12.海水晒盐是(
)
A.利用日晒,使海水分解
B.利用日晒,使氯化钠的溶解度变小
C.利用阳光和风力,使海水中的水分蒸发
D.利用阳光和风力,使海水中的氯化钠蒸发
13.在含有大量H+、Na+、SO42-的溶液中,还可能大量存在的是
A.NH4+
B.Ba2+
C.OH-
D.HCO3-
14.对于反应:X+2NaOH→2Y+Cu(OH)2↓,下列分析中正确的是( )
A.Y一定是氯化钠
B.X和Y的相对分子质量之差为18
C.X可能是CuCl2或Cu(NO3)2
D.Y可能是Na2SO4
二、填空题
15.猜谜语
(1)组成半个圆,杀人不见血,追捕无踪影,点火冒蓝火焰。(打一化学物质化学式)_____。
(2)100%的氢氧化钠(打一化学物质俗名)_____。
16.甲乙两种固体物质溶解度曲线如下图所示。
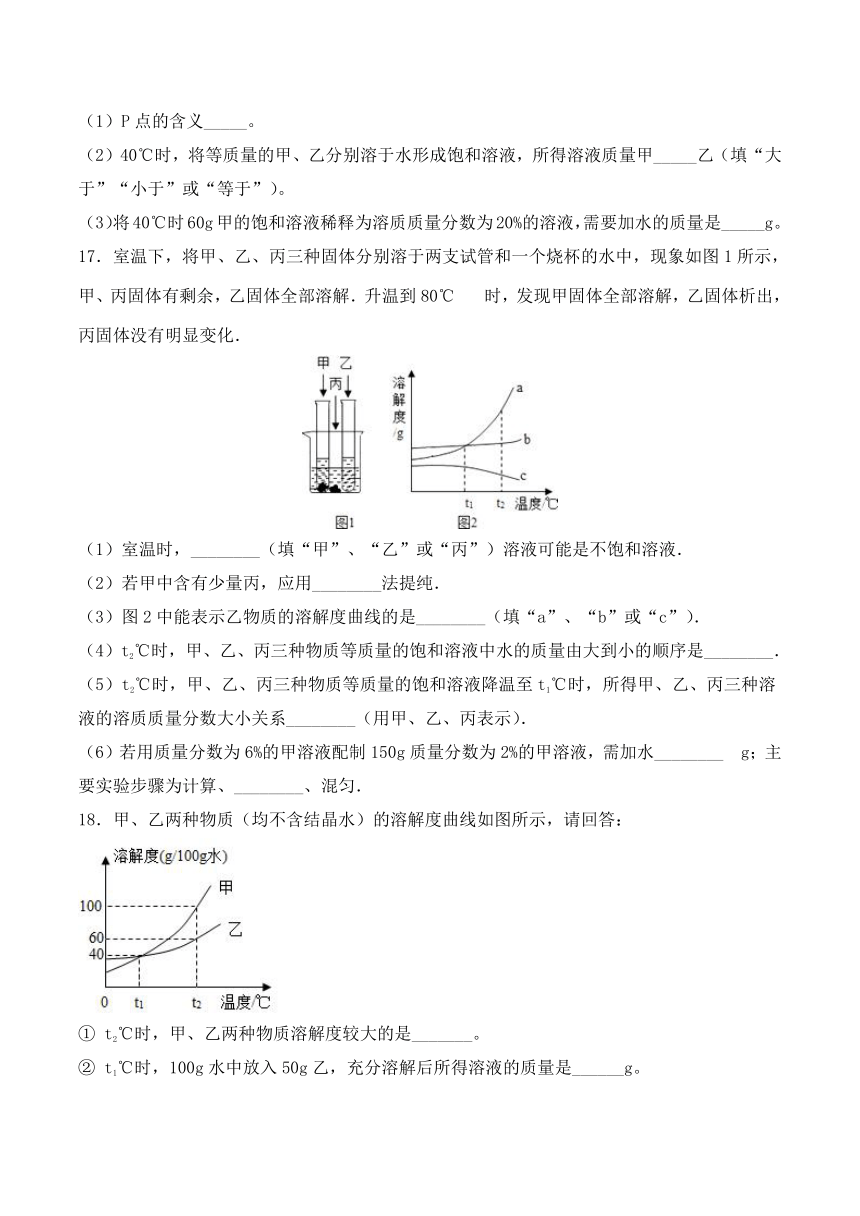
(1)P点的含义_____。
(2)40℃时,将等质量的甲、乙分别溶于水形成饱和溶液,所得溶液质量甲_____乙(填“大于”“小于”或“等于”)。
(3)将40℃时60g甲的饱和溶液稀释为溶质质量分数为20%的溶液,需要加水的质量是_____g。
17.室温下,将甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如图1所示,甲、丙固体有剩余,乙固体全部溶解.升温到80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化.
(1)室温时,________(填“甲”、“乙”或“丙”)溶液可能是不饱和溶液.
(2)若甲中含有少量丙,应用________法提纯.
(3)图2中能表示乙物质的溶解度曲线的是________(填“a”、“b”或“c”).
(4)t2℃时,甲、乙、丙三种物质等质量的饱和溶液中水的质量由大到小的顺序是________.
(5)t2℃时,甲、乙、丙三种物质等质量的饱和溶液降温至t1℃时,所得甲、乙、丙三种溶液的溶质质量分数大小关系________(用甲、乙、丙表示).
(6)若用质量分数为6%的甲溶液配制150g质量分数为2%的甲溶液,需加水________?g;主要实验步骤为计算、________、混匀.
18.甲、乙两种物质(均不含结晶水)的溶解度曲线如图所示,请回答:
①
t2℃时,甲、乙两种物质溶解度较大的是_______。
②
t1℃时,100g水中放入50g乙,充分溶解后所得溶液的质量是______g。
③
t2℃时,甲、乙溶液的溶质质量分数相等均为a%,其中一定是不饱和溶液的是________,a%的取值范围是_______。
④
将t2℃等质量的甲、乙饱和溶液分别降温到t1℃,下列说法正确的是_______。
A.t1℃时溶质质量分数:甲=乙
B.t1℃时溶质质量:甲=乙
C.t1℃时溶剂质量:甲>乙
D.析出晶体质量:甲>乙
19.写出下列溶液中的溶质的化学式:
(1)碳酸钠溶液:_____。
(2)高锰酸钾溶液:_____。
(3)食盐水:_____。
(4)澄清的石灰水:_____。
三、推断题
20.“烧碱同学”要穿过迷宫,从进口顺利地走到出口,途中遇到不反应的物质才能通过。
①请在答题卡中用“连续线”画出烧碱应行走的路线______。
②烧碱在刚进迷宫时,碰到了两种阻止他前进的物质,写出化学反应的方程式:_________、_________
③能用于鉴别烧碱溶液和稀盐酸的是________。
A.酚酞试液
B.CO2
C.Cu(OH)2
D.铜粉
21.甲、乙、丙、丁是初中化学常见的物质。图中“→”表示转化关系表示相互能反应。
(1)若甲、乙为氧化物,且乙为最常见的溶剂,丙、丁为单质。则丁的化学式为___________。甲→乙的化学方程式___________________________________。
(2)若甲、乙、丙中含有同一种金属元素,丁中不含乙中元素,丙通常作食品干燥剂。则丁的化学式为___________。丙→甲的反应属于__________(填“吸热”或“放热”)反应。
四、实验题
22.同学们在实验室用混合两种固体药品的办法自制“钾、氮复合肥料”,使用到的药品有KCl,K2SO4,NH4HCO3,NH4Cl。同学们制得了成分不同的“钾、氮复合肥料”,从中抽取一份作为样品探究其成分,请回答有关问题:
限选试剂:稀HCl,稀H2SO4,BaCl2溶液,AgNO3溶液,蒸馏水
(1)提出合理假设。所抽样品的成分有4种可能:
假设1:KCl和
NH4HCO3;假设2:KCl和NH4Cl;
假设3:K2SO4和
NH4HCO3;假设4:_____。
(2)形成设计思路。
①甲同学先提出先用AgNO3溶液确定是否含有KCl,你是否同意并说出理由:____。
②乙同学提出先确定是否含有NH4HCO3,则可以选择的试剂是_____。
(3)完成实验方案。请填写实验操作,与表中结论相符的预期现象。
实验操作
预期现象
结论
步骤1:____
_____
假设2成立
步骤2:_____
_____
23.某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50g
5%的氯化钠溶液。
实验一:下图是同学们做粗盐提纯实验的操作示意图。
请回答下列问题:
(1)操作③中用玻璃棒搅拌的作用是_____________________
。
(2)操作⑥中的错误是______________________。
(3)粗盐提纯实验的操作顺序为(填操作序号)___________________________________、称量精盐并计算产率。
实验二:
(4)用提纯得到的精盐配制了50
g
5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有____________________(填序号)。
①选择的氯化钠固体不纯
②游码未归零就调整天平平衡
③量好水倾倒时,洒出一部分
④配制好的溶液装瓶时,有少量溶液洒出
五、计算题
24.某纯碱样品中含有少量NaCl.小丽同学取该样品23g全部溶解于150g水中,再逐滴加入160g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。
计算当恰好完全反应时:
(1)产生的二氧化碳的质量是
克。
(2)求原稀盐酸中溶质的质量分数。
25.某课外小组的同学欲探究某石灰石样品(杂质不与酸反应)中碳酸钙的百分含量,他取样
品的质量
25克,再用
150g
的稀盐酸分五次加入样品中,实验结果如下表:
实验次数
第
1
次
第
2
次
第
3
次
第
4
次
第五次
加入稀盐酸质量/g
30
30
30
30
30
充分反应后剩余固体质量/g
20
15
10
5
2.4
根据上表中的数据分析,完成下列问题:
(1)样品中碳酸钙的质量是
克。
(2)所用稀盐酸的溶质质量分数是多少(计算结果精确到
0.1%)?
参考答案
1.C
2.C
3.C
4.B
5.B
6.C
7.A
8.D
9.C
10.A
11.C
12.C
13.A
14.C
15.CO
纯碱
16.在20℃时,甲和乙的溶解度相等
小于
40
17.乙冷却热饱和溶液C乙>丙>甲甲=丙>乙100g
量取
18.甲
140
甲
≤37.5%
AD
19.Na2CO3
KMnO4
NaCl
Ca(OH)2
20.略
2NaOH
+
CO2=
Na2CO3
+
H2O
2NaOH
+
CuSO4=
Na2SO4+
Cu(OH)2↓
A
C
21.C
HCl
放热
22.K2SO4和NH4Cl
不同意,因为AgNO3也可以与NH4Cl反应生成AgCl沉淀,不能确定是否有KCl
稀HCl(或稀H2SO4)
取少量样品放入试管中,加适量水溶解,加入足量稀盐酸
不产生气泡
向步骤1的试管中加入少量氯化钡溶液
不产生白色沉淀
23.加快氯化钠的溶解速率
没有用玻璃棒引流
①⑤②③⑥④
①②
24.(1)8.8;
(2)10%。
25.(1)22.6(2)12.2%
答案第2页,总2页
《海水中的化学》测试题
一、单选题
1.以下四个变化中,其中一个与其他三个有本质区别的是(
)
A.自来水厂在水中通入氯气进行消毒
B.点燃试管内的氢气产生尖锐的爆鸣声
C.用镶有金刚石的玻璃刀裁玻璃
D.往装有碳酸钠粉末的烧杯中加入稀盐酸产生大量气泡
2.下列各组离子在指定的溶液中能大量共存的一组是
A.在氯化铵溶液中:
Ag+
Cu2+
OH-
B.在稀盐酸中:
Zn2+
Mg2+
CO32-
C.在硝酸钠溶液中:
K+
Ca2+
Cl-
D.在氢氧化钡溶液中:
H+
Na+
SO42-
3.下列各组内物质间的转化关系中,不能一步转化的是(
)
A.Mg→MgO→MgSO4
B.H2O2→O2→H2O
C.KCl→KNO3→KOH
D.NaHCO3→Na2CO3→NaOH
4.下面是王华同学从“错题集”摘抄的部分内容,其中需加以改正的是( )
A.洗涤剂能除去油污,是因为它具有乳化作用
B.8gCaO溶于92g水中,所得溶液中溶质的质量分数为8%
C.喝下汽水后,常会打嗝,说明气体的溶解度随温度的升高而减小
D.配制100g
10%
的氯化钠溶液的主要步骤是:计算、称量、溶解、装瓶贴标签
5.将碳酸钙中的少量碳酸钠杂质除去,应该选用下列方法中的(
)
A.加入稀盐酸搅拌,过滤
B.加入足量水搅拌,过滤
C.高温加热固体
D.加入过量的石灰水,蒸发
6.下列各组离子能在pH=12的溶液中共存的一组是
A.H+、K+、CO
B.Ba2+、OH-、SO
C.Na+、Cl-、NO
D.Mg2+、NH、SO
7.20℃时,将等质量的m、n两种固体,分别加入到盛有100g水的烧杯中,充分搅拌后,再升温到50℃时,现象如图甲,m、n两种固体的溶解度曲线如图乙。下列说法正确的是(
)
A.图乙中a表示m的溶解度曲线
B.图甲20℃溶液中溶质的质量分数m大于n
C.图甲50℃时的m、n溶液不一定是不饱和溶液
D.30℃时,a、b溶液溶质质量分数不相等
8.下列物质能在pH=13的无色溶液中大量共存的是
A.NaNO3、NaCl、KNO3、H2SO4
B.H2SO4、HCl、AgNO3、Na2SO4
C.KMnO4、CuCl2、Fe2(SO4)3、NaNO3
D.K2SO4、NaCl、K2CO3、NaOH
9.下列实验中,能达到相应目的的是
A.制备CaCO3:向CaCl?溶液中通入足量的CO2,过滤
B.验证质量守恒定律:将锌粒与稀硫酸混合,比较混合前后溶液的质量
C.鉴别NaOH、NaCl、CuSO4和稀HCl四种溶液,不需添加其他试剂就可完成
D.分离NaCl和MgCl2固体混合物,加入足量水溶解,再加入适量的NaOH溶液,过滤,向滤渣滴加适量稀盐酸
10.如图是甲、乙、丙三种固体物质的溶解度曲线。下列说法正确的是()
A.20°C时,甲和丙的溶解度相等
B.50
°C时,将30
g甲物质加入到50
g水中不断搅拌,可形成80
g溶液
C.甲中混有少量丙时,可用蒸发结晶的方法提纯甲
D.将三种物质的饱和溶液从50
°C降温至20
°C
,所得溶液溶质质量分数的大小关系是:乙>甲=丙
11.下列涉及学科观点的说法中正确的是
A.微粒观:氢气是由氢原子构成的
B.分类观:纯碱属于碱
C.转化观:CO2和CaCO3可以相互转化
D.守恒观:2mL一氧化碳和1mL氧气反应生成3mL二氧化碳
12.海水晒盐是(
)
A.利用日晒,使海水分解
B.利用日晒,使氯化钠的溶解度变小
C.利用阳光和风力,使海水中的水分蒸发
D.利用阳光和风力,使海水中的氯化钠蒸发
13.在含有大量H+、Na+、SO42-的溶液中,还可能大量存在的是
A.NH4+
B.Ba2+
C.OH-
D.HCO3-
14.对于反应:X+2NaOH→2Y+Cu(OH)2↓,下列分析中正确的是( )
A.Y一定是氯化钠
B.X和Y的相对分子质量之差为18
C.X可能是CuCl2或Cu(NO3)2
D.Y可能是Na2SO4
二、填空题
15.猜谜语
(1)组成半个圆,杀人不见血,追捕无踪影,点火冒蓝火焰。(打一化学物质化学式)_____。
(2)100%的氢氧化钠(打一化学物质俗名)_____。
16.甲乙两种固体物质溶解度曲线如下图所示。
(1)P点的含义_____。
(2)40℃时,将等质量的甲、乙分别溶于水形成饱和溶液,所得溶液质量甲_____乙(填“大于”“小于”或“等于”)。
(3)将40℃时60g甲的饱和溶液稀释为溶质质量分数为20%的溶液,需要加水的质量是_____g。
17.室温下,将甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如图1所示,甲、丙固体有剩余,乙固体全部溶解.升温到80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化.
(1)室温时,________(填“甲”、“乙”或“丙”)溶液可能是不饱和溶液.
(2)若甲中含有少量丙,应用________法提纯.
(3)图2中能表示乙物质的溶解度曲线的是________(填“a”、“b”或“c”).
(4)t2℃时,甲、乙、丙三种物质等质量的饱和溶液中水的质量由大到小的顺序是________.
(5)t2℃时,甲、乙、丙三种物质等质量的饱和溶液降温至t1℃时,所得甲、乙、丙三种溶液的溶质质量分数大小关系________(用甲、乙、丙表示).
(6)若用质量分数为6%的甲溶液配制150g质量分数为2%的甲溶液,需加水________?g;主要实验步骤为计算、________、混匀.
18.甲、乙两种物质(均不含结晶水)的溶解度曲线如图所示,请回答:
①
t2℃时,甲、乙两种物质溶解度较大的是_______。
②
t1℃时,100g水中放入50g乙,充分溶解后所得溶液的质量是______g。
③
t2℃时,甲、乙溶液的溶质质量分数相等均为a%,其中一定是不饱和溶液的是________,a%的取值范围是_______。
④
将t2℃等质量的甲、乙饱和溶液分别降温到t1℃,下列说法正确的是_______。
A.t1℃时溶质质量分数:甲=乙
B.t1℃时溶质质量:甲=乙
C.t1℃时溶剂质量:甲>乙
D.析出晶体质量:甲>乙
19.写出下列溶液中的溶质的化学式:
(1)碳酸钠溶液:_____。
(2)高锰酸钾溶液:_____。
(3)食盐水:_____。
(4)澄清的石灰水:_____。
三、推断题
20.“烧碱同学”要穿过迷宫,从进口顺利地走到出口,途中遇到不反应的物质才能通过。
①请在答题卡中用“连续线”画出烧碱应行走的路线______。
②烧碱在刚进迷宫时,碰到了两种阻止他前进的物质,写出化学反应的方程式:_________、_________
③能用于鉴别烧碱溶液和稀盐酸的是________。
A.酚酞试液
B.CO2
C.Cu(OH)2
D.铜粉
21.甲、乙、丙、丁是初中化学常见的物质。图中“→”表示转化关系表示相互能反应。
(1)若甲、乙为氧化物,且乙为最常见的溶剂,丙、丁为单质。则丁的化学式为___________。甲→乙的化学方程式___________________________________。
(2)若甲、乙、丙中含有同一种金属元素,丁中不含乙中元素,丙通常作食品干燥剂。则丁的化学式为___________。丙→甲的反应属于__________(填“吸热”或“放热”)反应。
四、实验题
22.同学们在实验室用混合两种固体药品的办法自制“钾、氮复合肥料”,使用到的药品有KCl,K2SO4,NH4HCO3,NH4Cl。同学们制得了成分不同的“钾、氮复合肥料”,从中抽取一份作为样品探究其成分,请回答有关问题:
限选试剂:稀HCl,稀H2SO4,BaCl2溶液,AgNO3溶液,蒸馏水
(1)提出合理假设。所抽样品的成分有4种可能:
假设1:KCl和
NH4HCO3;假设2:KCl和NH4Cl;
假设3:K2SO4和
NH4HCO3;假设4:_____。
(2)形成设计思路。
①甲同学先提出先用AgNO3溶液确定是否含有KCl,你是否同意并说出理由:____。
②乙同学提出先确定是否含有NH4HCO3,则可以选择的试剂是_____。
(3)完成实验方案。请填写实验操作,与表中结论相符的预期现象。
实验操作
预期现象
结论
步骤1:____
_____
假设2成立
步骤2:_____
_____
23.某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50g
5%的氯化钠溶液。
实验一:下图是同学们做粗盐提纯实验的操作示意图。
请回答下列问题:
(1)操作③中用玻璃棒搅拌的作用是_____________________
。
(2)操作⑥中的错误是______________________。
(3)粗盐提纯实验的操作顺序为(填操作序号)___________________________________、称量精盐并计算产率。
实验二:
(4)用提纯得到的精盐配制了50
g
5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有____________________(填序号)。
①选择的氯化钠固体不纯
②游码未归零就调整天平平衡
③量好水倾倒时,洒出一部分
④配制好的溶液装瓶时,有少量溶液洒出
五、计算题
24.某纯碱样品中含有少量NaCl.小丽同学取该样品23g全部溶解于150g水中,再逐滴加入160g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。
计算当恰好完全反应时:
(1)产生的二氧化碳的质量是
克。
(2)求原稀盐酸中溶质的质量分数。
25.某课外小组的同学欲探究某石灰石样品(杂质不与酸反应)中碳酸钙的百分含量,他取样
品的质量
25克,再用
150g
的稀盐酸分五次加入样品中,实验结果如下表:
实验次数
第
1
次
第
2
次
第
3
次
第
4
次
第五次
加入稀盐酸质量/g
30
30
30
30
30
充分反应后剩余固体质量/g
20
15
10
5
2.4
根据上表中的数据分析,完成下列问题:
(1)样品中碳酸钙的质量是
克。
(2)所用稀盐酸的溶质质量分数是多少(计算结果精确到
0.1%)?
参考答案
1.C
2.C
3.C
4.B
5.B
6.C
7.A
8.D
9.C
10.A
11.C
12.C
13.A
14.C
15.CO
纯碱
16.在20℃时,甲和乙的溶解度相等
小于
40
17.乙冷却热饱和溶液C乙>丙>甲甲=丙>乙100g
量取
18.甲
140
甲
≤37.5%
AD
19.Na2CO3
KMnO4
NaCl
Ca(OH)2
20.略
2NaOH
+
CO2=
Na2CO3
+
H2O
2NaOH
+
CuSO4=
Na2SO4+
Cu(OH)2↓
A
C
21.C
HCl
放热
22.K2SO4和NH4Cl
不同意,因为AgNO3也可以与NH4Cl反应生成AgCl沉淀,不能确定是否有KCl
稀HCl(或稀H2SO4)
取少量样品放入试管中,加适量水溶解,加入足量稀盐酸
不产生气泡
向步骤1的试管中加入少量氯化钡溶液
不产生白色沉淀
23.加快氯化钠的溶解速率
没有用玻璃棒引流
①⑤②③⑥④
①②
24.(1)8.8;
(2)10%。
25.(1)22.6(2)12.2%
答案第2页,总2页
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
