2020-2021学年人教版初中化学九年级下册第九单元《溶液》检测题(含答案)
文档属性
| 名称 | 2020-2021学年人教版初中化学九年级下册第九单元《溶液》检测题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 136.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-15 00:00:00 | ||
图片预览


文档简介
本卷由系统自动生成,请仔细校对后使用,答案仅供参考。
《溶液》检测题
一、单选题
1.把20%的硝酸钾溶液加水稀释成10%的硝酸钾溶液,则所加水的质量为(
)
A.
B.
C.
D.
2.下列实验操作中(括号内为待检验物质或杂质)不能达到实验目的的是
选项
物质
目的
主要实验操作
A
NH4NO3和NaCl
鉴别
分别加水溶解,测温度变化
B
KNO3(NaCl)
提纯
加90℃水溶解,降温结晶、过滤
C
KClO3固体(KCl)
除杂
充分加热至固体质量不变
D
MnO2、KCl固体
分离
溶解、过滤、洗涤、烘干、蒸发
A.A
B.B
C.C
D.D
3.关于物质用途,下列解释正确的是(
)
A.氮气作为保护气是因为其化学性质很稳定
B.CO2
用于灭火只因其不可燃不助燃
C.汽油用于洗涤油污是因为发生乳化作用
D.焦炭用于冶炼金属是利用它的可燃性
4.对下列事实的微观解释错误的是( )
事实
解释
A
酒精溶液不能导电
溶液中没有自由移动的粒子
B
工业上用空气制取氧气的过程属于物理变化
分子的种类没有发生变化
C
金刚石、石墨性质存在明显差异
碳原子的排列方式不同
D
水蒸发为水蒸气,所占体积变大
分子间隔变大
A.A
B.B
C.C
D.D
5.下列家庭实验不会成功的是
A.用缝衣针淬火处理后制钓鱼钩
B.用6B铅笔芯做导电性实验
C.用等质量的同种白糖加入等量热水与冷水中,比较溶解速率
D.用冷碟子放在蜡烛火焰上制取炭黑
6.如图是A、B、C三种固体物质的溶解度曲线图,下列说法错误的是
A.t2℃时,A、B、C三种物质中,A物质的溶解度最大
B.P点表示t1℃时B、C两物质的溶解度大小相等
C.一定温度时,要将B物质的不饱和溶液转变成饱和溶液,可采取增加溶质的方法
D.20℃时,给A、B、C三种物质的饱和溶液加热(不考虑溶剂的蒸发),有晶体析出的是A物质
7.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是( )
A.t1℃时,丙的饱和溶液中溶质的质量分数为40%
B.t2℃时,甲、乙两饱和溶液的溶质质量相等
C.欲从含有少量乙的甲溶液中提纯甲,可采用降温结晶法
D.分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得三种溶液中溶质的质量分数大小关系是乙>丙>甲
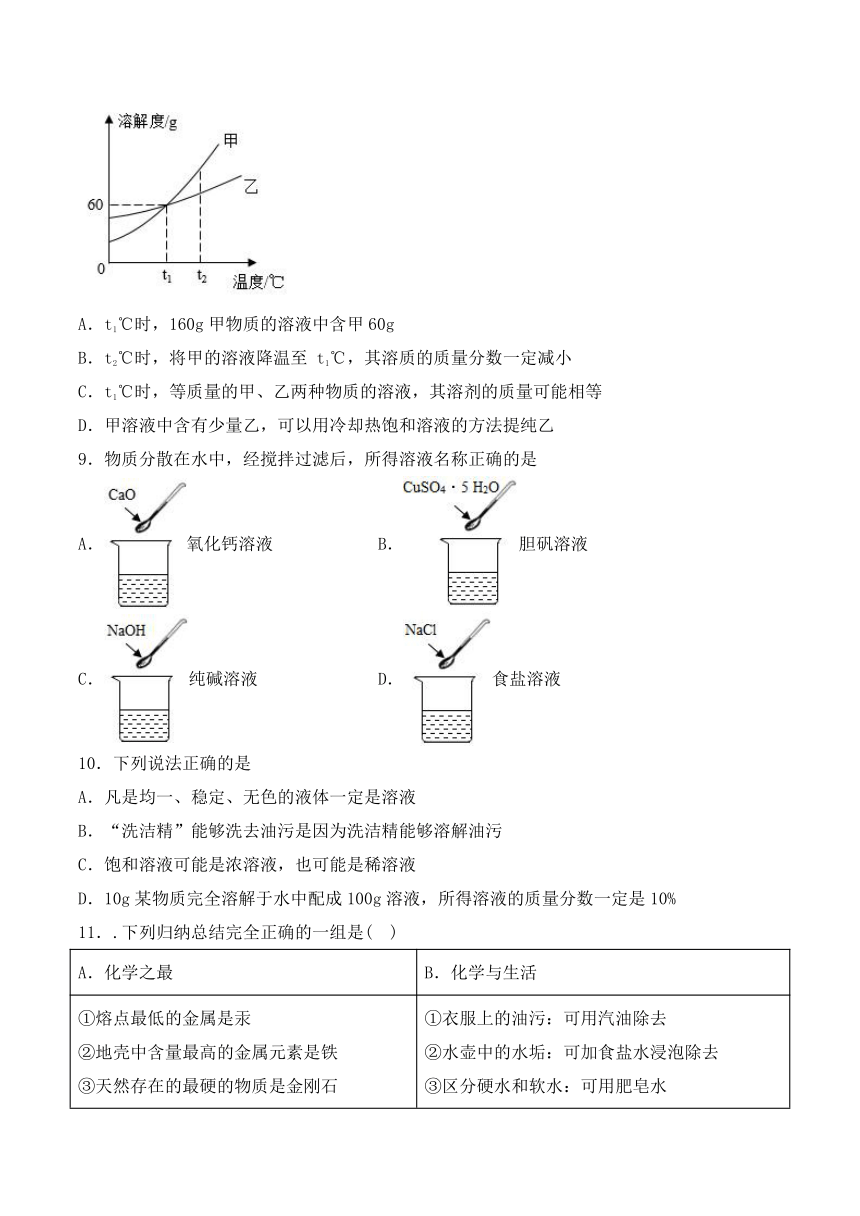
8.如图是甲、乙两种不含结晶水的固体物质的溶解度曲线。下列有关叙述正确的是(
)
A.t1℃时,160g甲物质的溶液中含甲60g
B.t2℃时,将甲的溶液降温至
t1℃,其溶质的质量分数一定减小
C.t1℃时,等质量的甲、乙两种物质的溶液,其溶剂的质量可能相等
D.甲溶液中含有少量乙,可以用冷却热饱和溶液的方法提纯乙
9.物质分散在水中,经搅拌过滤后,所得溶液名称正确的是
A.氧化钙溶液
B.胆矾溶液
C.纯碱溶液
D.食盐溶液
10.下列说法正确的是
A.凡是均一、稳定、无色的液体一定是溶液
B.“洗洁精”能够洗去油污是因为洗洁精能够溶解油污
C.饱和溶液可能是浓溶液,也可能是稀溶液
D.10g某物质完全溶解于水中配成100g溶液,所得溶液的质量分数一定是10%
11..下列归纳总结完全正确的一组是(
)
A.化学之最
B.化学与生活
①熔点最低的金属是汞
②地壳中含量最高的金属元素是铁
③天然存在的最硬的物质是金刚石
①衣服上的油污:可用汽油除去
②水壶中的水垢:可加食盐水浸泡除去
③区分硬水和软水:可用肥皂水
C.物质保存方法及解释
D.化学与工农业
①浓氨水密封保存:防止挥发
②白磷在煤油中保存:隔绝空气
③保持金属制品表面的洁净与干燥:防止锈蚀
①用焦炭和铁矿石炼铁
②将石油干馏生产航空煤油
③大水漫灌方式浇地
A.A
B.B
C.C
D.D
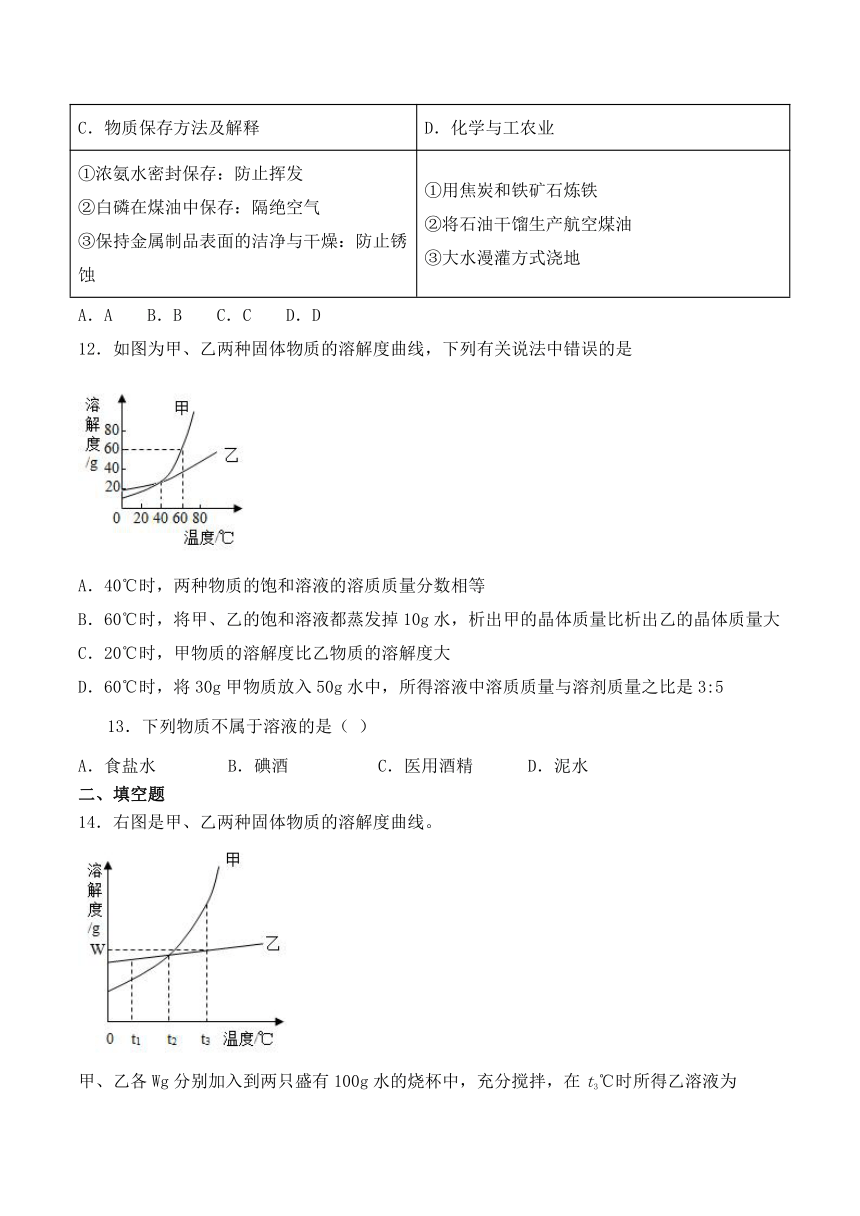
12.如图为甲、乙两种固体物质的溶解度曲线,下列有关说法中错误的是
A.40℃时,两种物质的饱和溶液的溶质质量分数相等
B.60℃时,将甲、乙的饱和溶液都蒸发掉10g水,析出甲的晶体质量比析出乙的晶体质量大
C.20℃时,甲物质的溶解度比乙物质的溶解度大
D.60℃时,将30g甲物质放入50g水中,所得溶液中溶质质量与溶剂质量之比是3:5
13.下列物质不属于溶液的是(
)
A.食盐水
B.碘酒
C.医用酒精
D.泥水
二、填空题
14.右图是甲、乙两种固体物质的溶解度曲线。
甲、乙各Wg分别加入到两只盛有100g水的烧杯中,充分搅拌,在t3℃时所得乙溶液为____________溶液(选填“饱和”
或“不饱和”);若将温度都降低到t2℃,甲溶液中溶质的质量分数__________乙溶液中溶质的质量分数(选填“大于”“等于”或“小于”)。
15.小盘同学配制质量分数为5%的氯化钠溶液100g,以备实验。
(1)通过计算,需称取氯化钠的质量为
g。
(2)配制该溶液所需要的玻璃仪器有:烧杯、量筒、胶头滴管和
(写仪器名称)。
(3)量取水的体积时,小盘同学仰视读数,则配制的氯化钠溶液的质量分数将
(填“偏小”、“不变”或“偏大”)。
三、实验题
16.如图是小梅配制100g溶质质量分数为12%的NaCl溶液的实验操作示意图:
(1)图中的玻璃仪器分别是广口瓶、量筒、烧杯和_____。
(2)指出图中的一处错误操作:_____。
(3)配制时应选择_____mL(10mL或50mL或100mL)的量筒量取所需要的水。
(4)用图示的序号表示配制溶液的操作顺序_____。
17.溶液在日常生活、工农业生产和科学研究中具有广泛的用途。
(1)生理盐水是医疗上常用的一种溶液,其溶质质量分数是_________________________。
A.10%
B.1%
C.9%
D.0.9%
(2)某兴趣小组同学为探究相同条件下碘在不同溶剂中的溶解性大小做以下实验。
①由图2所示现象可知:碘_________________________(填“不”、“微”或“易”)溶于水;
②图3所示试管中液体分层。上层紫红色溶液是碘溶解在汽油中形成的,该溶液的名称是_________________________。说明碘在汽油中的溶解性比在水中_________________________(填“大”或“小”)。
(3)在实验室配制一定溶质质量分数的氯化钠溶液,实验操作过程如图所示。
①正确的实验步骤顺序是_________________________(填字母),其中操作错误的是_________________________(填字母);
②下列操作会导致结果偏小的是_________________________(填字母)。
A.称量的氯化钠固体含有少量硝酸钠
B.用量筒量取水时仰视读数
C.往烧杯中加水时有水洒出
D.将配制好的溶液装入试剂瓶时溅出少许
四、推断题
18.同学们到实验室去进行“探究金属的性质”实验。将锌粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。请你填空。
(1)若将所得滤渣放入稀盐酸中,有气泡产生,则
①滤液里一定含有_____(填写化学式,下同),可能含有_____;
②滤渣中一定含有_____,可能含有_____。
(2)若反应后所得滤液呈无色,则滤渣中一定含有_____(填写化学式)。
(3)反应后所得滤液的溶质质量分数_____(选填“大于”、“等于”或“小于”)原硝酸银溶液的溶质质量分数。
五、计算题
19.试剂瓶中有1
000
g氯化钠溶液,瓶上的标签如图所示,计算其所含溶质的质量是________g;若将此溶液稀释为4%的稀溶液,需加水________g。
20.下图表示硝酸钾的溶解度曲线,10℃时,硝酸钾的溶解度是21克,50℃时硝酸钾的溶解度为86克,试问:
(1)A点表示的含义是__
(2)在50℃时93克硝酸钾饱和溶液冷却到10℃,有___硝酸钾晶体析出?
(3)如图中C点代表硝酸钾的不饱和溶液,如果使该点所表示的不饱和溶液变成饱和溶液;
①可加____克硝酸钾晶体?
②若仍维持原温度不变,应蒸发___水?
参考答案
1.A
2.C
3.A
4.A
5.A
6.D
7.C
8.C
9.D
10.C
11.C
12.C
13.D
14.不饱和
等于
15.(1)5
(2)玻璃棒
(3)偏小
16.玻璃棒
②中氯化钠与砝码的位置颠倒
100
④②①⑤③
17.D
微
碘的汽油溶液
大
baecd
a
AB
18.Zn(NO3)2
Fe(NO3)2
Ag、Fe
Zn
Ag、Fe
小于
19.100;1500
20.(1)50℃时硝酸甲的溶解度是86g;(2)32.5;(3)①65;②75.6g
答案第1页,总2页
《溶液》检测题
一、单选题
1.把20%的硝酸钾溶液加水稀释成10%的硝酸钾溶液,则所加水的质量为(
)
A.
B.
C.
D.
2.下列实验操作中(括号内为待检验物质或杂质)不能达到实验目的的是
选项
物质
目的
主要实验操作
A
NH4NO3和NaCl
鉴别
分别加水溶解,测温度变化
B
KNO3(NaCl)
提纯
加90℃水溶解,降温结晶、过滤
C
KClO3固体(KCl)
除杂
充分加热至固体质量不变
D
MnO2、KCl固体
分离
溶解、过滤、洗涤、烘干、蒸发
A.A
B.B
C.C
D.D
3.关于物质用途,下列解释正确的是(
)
A.氮气作为保护气是因为其化学性质很稳定
B.CO2
用于灭火只因其不可燃不助燃
C.汽油用于洗涤油污是因为发生乳化作用
D.焦炭用于冶炼金属是利用它的可燃性
4.对下列事实的微观解释错误的是( )
事实
解释
A
酒精溶液不能导电
溶液中没有自由移动的粒子
B
工业上用空气制取氧气的过程属于物理变化
分子的种类没有发生变化
C
金刚石、石墨性质存在明显差异
碳原子的排列方式不同
D
水蒸发为水蒸气,所占体积变大
分子间隔变大
A.A
B.B
C.C
D.D
5.下列家庭实验不会成功的是
A.用缝衣针淬火处理后制钓鱼钩
B.用6B铅笔芯做导电性实验
C.用等质量的同种白糖加入等量热水与冷水中,比较溶解速率
D.用冷碟子放在蜡烛火焰上制取炭黑
6.如图是A、B、C三种固体物质的溶解度曲线图,下列说法错误的是
A.t2℃时,A、B、C三种物质中,A物质的溶解度最大
B.P点表示t1℃时B、C两物质的溶解度大小相等
C.一定温度时,要将B物质的不饱和溶液转变成饱和溶液,可采取增加溶质的方法
D.20℃时,给A、B、C三种物质的饱和溶液加热(不考虑溶剂的蒸发),有晶体析出的是A物质
7.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是( )
A.t1℃时,丙的饱和溶液中溶质的质量分数为40%
B.t2℃时,甲、乙两饱和溶液的溶质质量相等
C.欲从含有少量乙的甲溶液中提纯甲,可采用降温结晶法
D.分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得三种溶液中溶质的质量分数大小关系是乙>丙>甲
8.如图是甲、乙两种不含结晶水的固体物质的溶解度曲线。下列有关叙述正确的是(
)
A.t1℃时,160g甲物质的溶液中含甲60g
B.t2℃时,将甲的溶液降温至
t1℃,其溶质的质量分数一定减小
C.t1℃时,等质量的甲、乙两种物质的溶液,其溶剂的质量可能相等
D.甲溶液中含有少量乙,可以用冷却热饱和溶液的方法提纯乙
9.物质分散在水中,经搅拌过滤后,所得溶液名称正确的是
A.氧化钙溶液
B.胆矾溶液
C.纯碱溶液
D.食盐溶液
10.下列说法正确的是
A.凡是均一、稳定、无色的液体一定是溶液
B.“洗洁精”能够洗去油污是因为洗洁精能够溶解油污
C.饱和溶液可能是浓溶液,也可能是稀溶液
D.10g某物质完全溶解于水中配成100g溶液,所得溶液的质量分数一定是10%
11..下列归纳总结完全正确的一组是(
)
A.化学之最
B.化学与生活
①熔点最低的金属是汞
②地壳中含量最高的金属元素是铁
③天然存在的最硬的物质是金刚石
①衣服上的油污:可用汽油除去
②水壶中的水垢:可加食盐水浸泡除去
③区分硬水和软水:可用肥皂水
C.物质保存方法及解释
D.化学与工农业
①浓氨水密封保存:防止挥发
②白磷在煤油中保存:隔绝空气
③保持金属制品表面的洁净与干燥:防止锈蚀
①用焦炭和铁矿石炼铁
②将石油干馏生产航空煤油
③大水漫灌方式浇地
A.A
B.B
C.C
D.D
12.如图为甲、乙两种固体物质的溶解度曲线,下列有关说法中错误的是
A.40℃时,两种物质的饱和溶液的溶质质量分数相等
B.60℃时,将甲、乙的饱和溶液都蒸发掉10g水,析出甲的晶体质量比析出乙的晶体质量大
C.20℃时,甲物质的溶解度比乙物质的溶解度大
D.60℃时,将30g甲物质放入50g水中,所得溶液中溶质质量与溶剂质量之比是3:5
13.下列物质不属于溶液的是(
)
A.食盐水
B.碘酒
C.医用酒精
D.泥水
二、填空题
14.右图是甲、乙两种固体物质的溶解度曲线。
甲、乙各Wg分别加入到两只盛有100g水的烧杯中,充分搅拌,在t3℃时所得乙溶液为____________溶液(选填“饱和”
或“不饱和”);若将温度都降低到t2℃,甲溶液中溶质的质量分数__________乙溶液中溶质的质量分数(选填“大于”“等于”或“小于”)。
15.小盘同学配制质量分数为5%的氯化钠溶液100g,以备实验。
(1)通过计算,需称取氯化钠的质量为
g。
(2)配制该溶液所需要的玻璃仪器有:烧杯、量筒、胶头滴管和
(写仪器名称)。
(3)量取水的体积时,小盘同学仰视读数,则配制的氯化钠溶液的质量分数将
(填“偏小”、“不变”或“偏大”)。
三、实验题
16.如图是小梅配制100g溶质质量分数为12%的NaCl溶液的实验操作示意图:
(1)图中的玻璃仪器分别是广口瓶、量筒、烧杯和_____。
(2)指出图中的一处错误操作:_____。
(3)配制时应选择_____mL(10mL或50mL或100mL)的量筒量取所需要的水。
(4)用图示的序号表示配制溶液的操作顺序_____。
17.溶液在日常生活、工农业生产和科学研究中具有广泛的用途。
(1)生理盐水是医疗上常用的一种溶液,其溶质质量分数是_________________________。
A.10%
B.1%
C.9%
D.0.9%
(2)某兴趣小组同学为探究相同条件下碘在不同溶剂中的溶解性大小做以下实验。
①由图2所示现象可知:碘_________________________(填“不”、“微”或“易”)溶于水;
②图3所示试管中液体分层。上层紫红色溶液是碘溶解在汽油中形成的,该溶液的名称是_________________________。说明碘在汽油中的溶解性比在水中_________________________(填“大”或“小”)。
(3)在实验室配制一定溶质质量分数的氯化钠溶液,实验操作过程如图所示。
①正确的实验步骤顺序是_________________________(填字母),其中操作错误的是_________________________(填字母);
②下列操作会导致结果偏小的是_________________________(填字母)。
A.称量的氯化钠固体含有少量硝酸钠
B.用量筒量取水时仰视读数
C.往烧杯中加水时有水洒出
D.将配制好的溶液装入试剂瓶时溅出少许
四、推断题
18.同学们到实验室去进行“探究金属的性质”实验。将锌粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。请你填空。
(1)若将所得滤渣放入稀盐酸中,有气泡产生,则
①滤液里一定含有_____(填写化学式,下同),可能含有_____;
②滤渣中一定含有_____,可能含有_____。
(2)若反应后所得滤液呈无色,则滤渣中一定含有_____(填写化学式)。
(3)反应后所得滤液的溶质质量分数_____(选填“大于”、“等于”或“小于”)原硝酸银溶液的溶质质量分数。
五、计算题
19.试剂瓶中有1
000
g氯化钠溶液,瓶上的标签如图所示,计算其所含溶质的质量是________g;若将此溶液稀释为4%的稀溶液,需加水________g。
20.下图表示硝酸钾的溶解度曲线,10℃时,硝酸钾的溶解度是21克,50℃时硝酸钾的溶解度为86克,试问:
(1)A点表示的含义是__
(2)在50℃时93克硝酸钾饱和溶液冷却到10℃,有___硝酸钾晶体析出?
(3)如图中C点代表硝酸钾的不饱和溶液,如果使该点所表示的不饱和溶液变成饱和溶液;
①可加____克硝酸钾晶体?
②若仍维持原温度不变,应蒸发___水?
参考答案
1.A
2.C
3.A
4.A
5.A
6.D
7.C
8.C
9.D
10.C
11.C
12.C
13.D
14.不饱和
等于
15.(1)5
(2)玻璃棒
(3)偏小
16.玻璃棒
②中氯化钠与砝码的位置颠倒
100
④②①⑤③
17.D
微
碘的汽油溶液
大
baecd
a
AB
18.Zn(NO3)2
Fe(NO3)2
Ag、Fe
Zn
Ag、Fe
小于
19.100;1500
20.(1)50℃时硝酸甲的溶解度是86g;(2)32.5;(3)①65;②75.6g
答案第1页,总2页
同课章节目录
