人教版高中化学必修二4.1开发利用金属矿物资源 课件(28张ppt)
文档属性
| 名称 | 人教版高中化学必修二4.1开发利用金属矿物资源 课件(28张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-22 00:00:00 | ||
图片预览








文档简介
(共28张PPT)
第四章
化学与自然资源的开发利用
人类使用的金属材料中金属的存在状态?
赤铁矿
蓝铜矿
萤石
Fe2O3
Cu3[CO3]2(OH)2
CaF2
矿物中的金属元素以什么形态存在?
铀矿石
镍矿石
矿物中的金属元素以阳离子形式存在
Rn+
R
+
ne-
金属的冶炼要使金属离子
得到电子
转化为金属原子
金属冶炼的实质:利用氧化还原反应,使金属化合物中的金属阳离子得到电子变成金属原子。
如何从矿物中提取金属单质
1、采矿
2、选矿
将矿物中的有效成分提取出来,以减少杂质、提高品位。
3、冶炼
将金属矿物中的金属从其化合物中还原出来
用于生产和制造各种金属材料
要从金属矿物得到金属单质经过
过程
还原
历史上金属被发现和冶炼利用的顺序
Au、
Fe、
Al、
Ti
原因:
越活泼的金属越难冶炼,
熔点越高的金属越难冶炼。
随着社会生产力和科学的发展,
难冶炼的金属才被冶炼出来
古代
现代
Ag、
Cu、
不活泼的金属
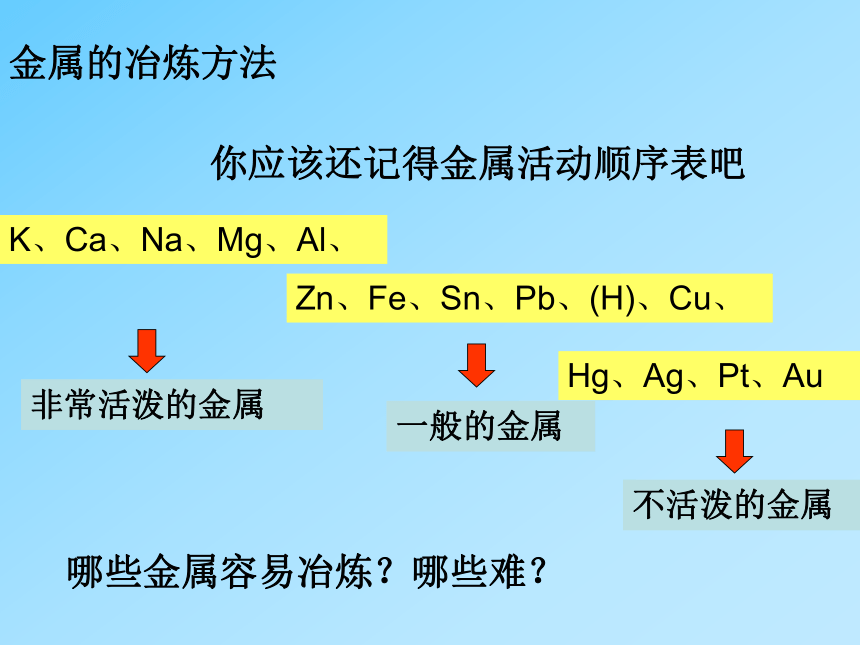
金属的冶炼方法
你应该还记得金属活动顺序表吧
K、Ca、Na、Mg、Al、
Zn、Fe、Sn、Pb、(H)、Cu、
Hg、Ag、Pt、Au
非常活泼的金属
一般的金属
哪些金属容易冶炼?哪些难?
不活泼的金属
采用加热分解法,
又叫做:热分解法
Hg、Ag、Pt、Au
你认为热分解反应方程式有什么特点?
得到对应的单质
AuCl4
加热
Au
+
2Cl2↑
非常活泼的金属的冶炼
使它们由化合物转化为单质难易:
K、Ca、Na、Mg、Al、
很困难
通常冶炼方法:
热电解法
高温下熔融金属化合物然后进行电解
--最强力的还原手段
电解氧化铝生产车间
2NaCl(熔融)
2Na
Cl2↑
电解
+
2Al2O3(熔融)
电解
冰晶石
4Al
+
3O2↑
离子交换膜电解槽
电解NaCl溶液
与电解熔融NaCl
不同
常温
高温
NaOH、H2、Cl2
Na、Cl2
产物:
原因:
水溶液中H+比Na+先电解出来
假如你是一个原始人,
打到一只兔子
你会考虑怎样吃?
点火烧烤
火焰烤过的有些石头上有发亮的物质
—— 铜
最早被人类发现、冶炼和利用的金属
一般的金属
Zn、Fe、Sn、Pb、(H)、Cu、
由化合物转化为单质难易:
比较容易
通常冶炼方法:
热还原法
加热或者高温下与还原剂反应
常用还原剂:
C、
CO、
H2、
活泼金属,如Na、Al
成本:
低
高
炼铁高炉
Fe2O3+3CO
2Fe+3CO2
高温
铝热反应
P83实验4-1
反应物:
铝粉、
氧化铁
镁条和氯酸钾的作用:
产生高温条件,引发反应
吸热反应还是放热反应:
放热反应
用途:
旧时用于缝合火车铁轨
现象:
火星四溅、纸漏斗被烧穿
有熔融物从纸漏斗中流出
高温下铝(粉)作还原剂
冶炼难熔金属,如钒、铬、锰
3MnO2+4Al
===
3Mn+
2Al2O3
高温
Cr2O3+2Al
===
2Cr
+
Al2O3
高温
3Co3O4+8Al
===
9Co
+
4Al2O3
高温
其它铝热反应
大气污染
太湖的蓝藻问题
水体污染
自然资源与可持续发展
自然资源定义:
一定时间、地点的条件下能够产生经济价值的以提高人类当前和将来福利的自然环境因素和条件的总称。
可持续发展:
尽可能地延长现有资源的可使用年限,
保护好自然环境,
使子孙后代也能够继续发展和安居乐业。
是指满足当前需要而又不剥削子孙后代
满足其需要之能力的发展
金属矿物资源有限
合理利用矿物资源
有效使用金属产品、材料
途径:
提高金属矿物的利用率
减少金属的使用量
加强金属资源的回收和再利用
使用其他材料代替金属材料
总结:
1、金属矿物中提取金属的过程叫做
冶炼
2、不同活动性的金属冶炼方式不同
非常活泼
一般活泼
不活泼
电解法
热还原法
热分解法
3、合理利用矿物资源,坚持可持续发展战略
练习:
1、无色气体A与红热的炭反应,得到另一种无色气体B,B与灼热的氧化铜反应,又得到A,则A、B分别是______,______。
2、铝热剂中铝作________。
CO
CO2
3、根据下表回答,工业生产电解镁应该选择
_______作原料,
原因是_______________________________。
还原剂
物质
MgCl2
MgO
沸点
714℃
2852℃
MgCl2
MgCl2的熔点低,电解工艺设备相对简单,成本低
第四章
化学与自然资源的开发利用
人类使用的金属材料中金属的存在状态?
赤铁矿
蓝铜矿
萤石
Fe2O3
Cu3[CO3]2(OH)2
CaF2
矿物中的金属元素以什么形态存在?
铀矿石
镍矿石
矿物中的金属元素以阳离子形式存在
Rn+
R
+
ne-
金属的冶炼要使金属离子
得到电子
转化为金属原子
金属冶炼的实质:利用氧化还原反应,使金属化合物中的金属阳离子得到电子变成金属原子。
如何从矿物中提取金属单质
1、采矿
2、选矿
将矿物中的有效成分提取出来,以减少杂质、提高品位。
3、冶炼
将金属矿物中的金属从其化合物中还原出来
用于生产和制造各种金属材料
要从金属矿物得到金属单质经过
过程
还原
历史上金属被发现和冶炼利用的顺序
Au、
Fe、
Al、
Ti
原因:
越活泼的金属越难冶炼,
熔点越高的金属越难冶炼。
随着社会生产力和科学的发展,
难冶炼的金属才被冶炼出来
古代
现代
Ag、
Cu、
不活泼的金属
金属的冶炼方法
你应该还记得金属活动顺序表吧
K、Ca、Na、Mg、Al、
Zn、Fe、Sn、Pb、(H)、Cu、
Hg、Ag、Pt、Au
非常活泼的金属
一般的金属
哪些金属容易冶炼?哪些难?
不活泼的金属
采用加热分解法,
又叫做:热分解法
Hg、Ag、Pt、Au
你认为热分解反应方程式有什么特点?
得到对应的单质
AuCl4
加热
Au
+
2Cl2↑
非常活泼的金属的冶炼
使它们由化合物转化为单质难易:
K、Ca、Na、Mg、Al、
很困难
通常冶炼方法:
热电解法
高温下熔融金属化合物然后进行电解
--最强力的还原手段
电解氧化铝生产车间
2NaCl(熔融)
2Na
Cl2↑
电解
+
2Al2O3(熔融)
电解
冰晶石
4Al
+
3O2↑
离子交换膜电解槽
电解NaCl溶液
与电解熔融NaCl
不同
常温
高温
NaOH、H2、Cl2
Na、Cl2
产物:
原因:
水溶液中H+比Na+先电解出来
假如你是一个原始人,
打到一只兔子
你会考虑怎样吃?
点火烧烤
火焰烤过的有些石头上有发亮的物质
—— 铜
最早被人类发现、冶炼和利用的金属
一般的金属
Zn、Fe、Sn、Pb、(H)、Cu、
由化合物转化为单质难易:
比较容易
通常冶炼方法:
热还原法
加热或者高温下与还原剂反应
常用还原剂:
C、
CO、
H2、
活泼金属,如Na、Al
成本:
低
高
炼铁高炉
Fe2O3+3CO
2Fe+3CO2
高温
铝热反应
P83实验4-1
反应物:
铝粉、
氧化铁
镁条和氯酸钾的作用:
产生高温条件,引发反应
吸热反应还是放热反应:
放热反应
用途:
旧时用于缝合火车铁轨
现象:
火星四溅、纸漏斗被烧穿
有熔融物从纸漏斗中流出
高温下铝(粉)作还原剂
冶炼难熔金属,如钒、铬、锰
3MnO2+4Al
===
3Mn+
2Al2O3
高温
Cr2O3+2Al
===
2Cr
+
Al2O3
高温
3Co3O4+8Al
===
9Co
+
4Al2O3
高温
其它铝热反应
大气污染
太湖的蓝藻问题
水体污染
自然资源与可持续发展
自然资源定义:
一定时间、地点的条件下能够产生经济价值的以提高人类当前和将来福利的自然环境因素和条件的总称。
可持续发展:
尽可能地延长现有资源的可使用年限,
保护好自然环境,
使子孙后代也能够继续发展和安居乐业。
是指满足当前需要而又不剥削子孙后代
满足其需要之能力的发展
金属矿物资源有限
合理利用矿物资源
有效使用金属产品、材料
途径:
提高金属矿物的利用率
减少金属的使用量
加强金属资源的回收和再利用
使用其他材料代替金属材料
总结:
1、金属矿物中提取金属的过程叫做
冶炼
2、不同活动性的金属冶炼方式不同
非常活泼
一般活泼
不活泼
电解法
热还原法
热分解法
3、合理利用矿物资源,坚持可持续发展战略
练习:
1、无色气体A与红热的炭反应,得到另一种无色气体B,B与灼热的氧化铜反应,又得到A,则A、B分别是______,______。
2、铝热剂中铝作________。
CO
CO2
3、根据下表回答,工业生产电解镁应该选择
_______作原料,
原因是_______________________________。
还原剂
物质
MgCl2
MgO
沸点
714℃
2852℃
MgCl2
MgCl2的熔点低,电解工艺设备相对简单,成本低
