人教版初中化学九年级下册 第九单元 溶液 单元测试卷
文档属性
| 名称 | 人教版初中化学九年级下册 第九单元 溶液 单元测试卷 |  | |
| 格式 | docx | ||
| 文件大小 | 139.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-22 09:34:12 | ||
图片预览


文档简介
人教版初中化学九年级下册 第九单元 溶液
一、单选题(共12题;共28分)
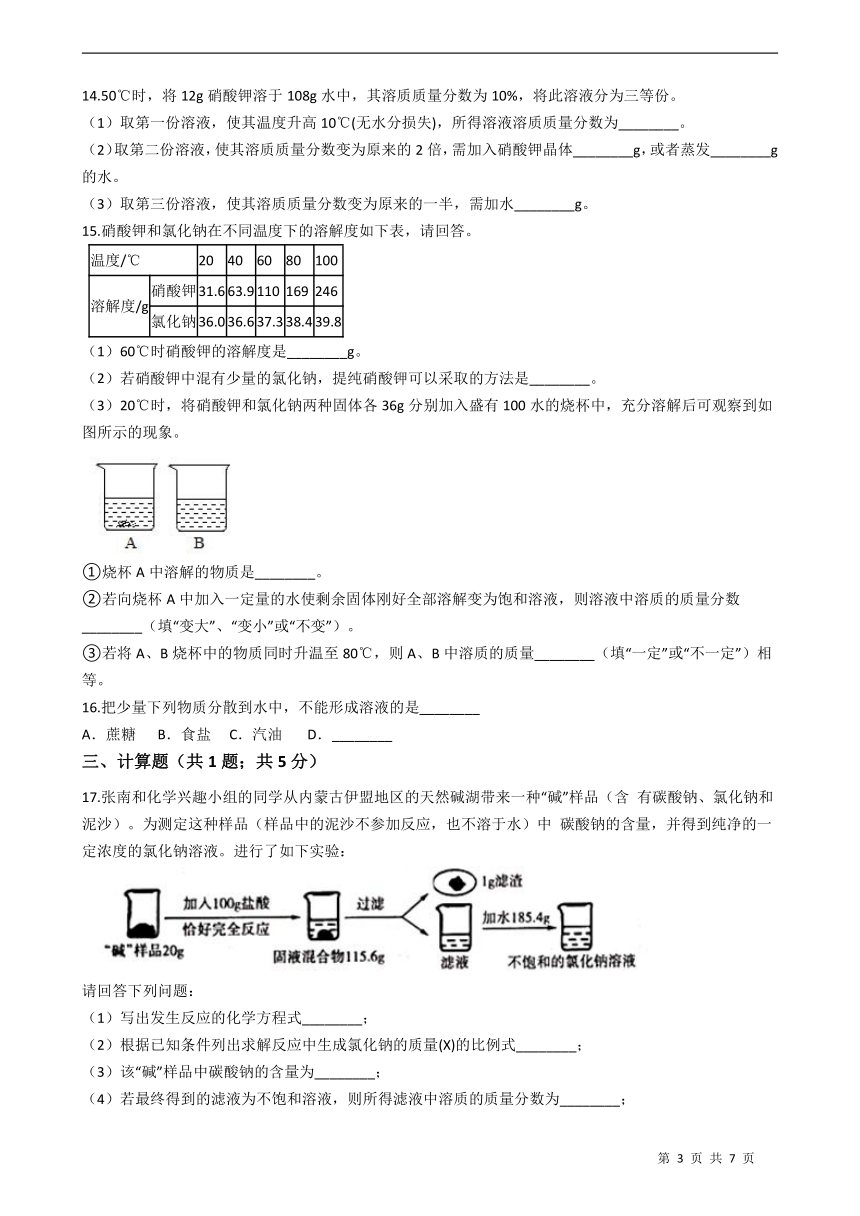
1.下列实验操作或记录正确的是(?? )
A.?稀释浓硫酸时,将水沿烧杯壁慢慢倒入浓硫酸中,并用玻璃棒不断搅拌??????????B.?打开装有浓盐酸的试剂瓶,可看到白烟
C.?用托盘天平称取5.4g氯化钠????????????????????????????????D.?测溶液pH值时,将待测液倾倒在pH试纸上,将pH试纸的颜色与标准比色卡比较即可
2.某物质的饱和溶液一定是 ( )
A.?浓溶液?????????B.?稀溶液?????????C.?含100克水的溶液?????????D.?在一定条件下,不能再溶解该物质的溶液
3.向接近饱和的氯化钠溶液中,逐渐加入氯化钠固体,边加边搅拌。下列图形中变化关系正确的是(??? )
A.???????B.?????????C.???????D.?
4.用溶质质量分数为36%的浓盐酸配制一定浓度的稀盐酸时,不会用到的仪器是(?? )
A.?????????????????????????B.????????????????????????C.?????????????????????????D.?
5.下列关于溶液的说法中,正确的是(?? ) ??
A.?溶液都是无色透明的??????????????????????????????????????????B.?凡是均一的、稳定的液体都是溶液
C.?蔗糖溶液上半部分溶液的甜度低于下半部分溶液的甜度?????????D.?氢氧化钠溶液能导电,因为溶液中有较多自由移动的离子
6.如图表示X、Y、Z三种固体物质的溶解度曲线,下列说法错误的是(?? )
A.?t3℃时,X的饱和溶液一定比Y的不饱和溶液浓
B.?t2℃时,等质量的X、Y的溶液中,含有相同质量的溶质
C.?将t1℃时的三种物质的饱和溶液升温到t2℃,溶液中溶质质量分数的大小关系是Y>X>Z
D.?将t3℃时的X的不饱和溶液降温至t1℃,其溶质的质量分数可能变小
7.下列各因素不会影响固体溶解度的是()
A.?溶质的种类???????????????????????B.?溶剂的种类???????????????????????C.?溶剂的质量???????????????????????D.?温度的变化
8.关于如图所示实验的相关判断错误的是(?? )
A.?固体X可能是NaOH????????????????????????????????????????????B.?固体X可能是NH4NO3
C.?Ca(OH)2溶解度:①>②???????????????????????????????D.?Ca(OH)2质量分数:①=③
9.向 100g 水中不断加入固体 A 或改变温度,得到相应的溶液①~⑤。下列说法正确的是(?? )
A.?A的溶液中②的质量分数最大? ???????
B.?③⑤中 A 的质量分数相等
C.?②④⑤的溶液为饱和溶液???????
D.?①③④⑤中没有固体存在
10.现有含金属元素的质量分数为75%的氧化铁和氧化铜组成的混合物6.4g,与200g硫酸溶液恰好完全反应,则所用硫酸溶液的溶质质量分数为(???? )
A.?9.8%???????????????????????????????????B.?4.9%???????????????????????????????????C.?19.6%???????????????????????????????????D.?10%
11.下列溶液中溶质是气体的是(?? )
A.?生理盐水????????????????????????B.?盐酸????????????????????????C.?75%的消毒酒精????????????????????????D.?澄清的石灰水
12.将80g质量分数为35%的浓盐酸,稀释成14%的稀盐酸,需加水的质量为( )
A.?80g???????????????????????????????????B.?100g???????????????????????????????????C.?120g???????????????????????????????????D.?200g
二、填空题(共4题;共16分)
13.如图所示,广口瓶中盛有少量饱和澄清石灰水,小试管和U形管中均有适量水,现向小试管中注入适量浓硫酸.
请回答:
(1)可观察到饱和澄清石灰水________;
(2)U形管中a、b液面变化情况是________?(选填序号).
A.a液面上升,b液面下降?? B.a液面下降,b液面上升.
14.50℃时,将12g硝酸钾溶于108g水中,其溶质质量分数为10%,将此溶液分为三等份。
(1)取第一份溶液,使其温度升高10℃(无水分损失),所得溶液溶质质量分数为________。
(2)取第二份溶液,使其溶质质量分数变为原来的2倍,需加入硝酸钾晶体________g,或者蒸发________g的水。
(3)取第三份溶液,使其溶质质量分数变为原来的一半,需加水________g。
15.硝酸钾和氯化钠在不同温度下的溶解度如下表,请回答。
温度/℃
20
40
60
80
100
溶解度/g
硝酸钾
31.6
63.9
110
169
246
氯化钠
36.0
36.6
37.3
38.4
39.8
(1)60℃时硝酸钾的溶解度是________g。
(2)若硝酸钾中混有少量的氯化钠,提纯硝酸钾可以采取的方法是________。
(3)20℃时,将硝酸钾和氯化钠两种固体各36g分别加入盛有100水的烧杯中,充分溶解后可观察到如图所示的现象。
①烧杯A中溶解的物质是________。
②若向烧杯A中加入一定量的水使剩余固体刚好全部溶解变为饱和溶液,则溶液中溶质的质量分数________(填“变大”、“变小”或“不变”)。
③若将A、B烧杯中的物质同时升温至80℃,则A、B中溶质的质量________(填“一定”或“不一定”)相等。
16.把少量下列物质分散到水中,不能形成溶液的是________
A.蔗糖? ???B.食盐??? C.汽油??? ??D.________
三、计算题(共1题;共5分)
17.张南和化学兴趣小组的同学从内蒙古伊盟地区的天然碱湖带来一种“碱”样品(含 有碳酸钠、氯化钠和泥沙)。为测定这种样品(样品中的泥沙不参加反应,也不溶于水)中 碳酸钠的含量,并得到纯净的一定浓度的氯化钠溶液。进行了如下实验:
请回答下列问题:
(1)写出发生反应的化学方程式________;
(2)根据已知条件列出求解反应中生成氯化钠的质量(X)的比例式________;
(3)该“碱”样品中碳酸钠的含量为________;
(4)若最终得到的滤液为不饱和溶液,则所得滤液中溶质的质量分数为________;
(5)若用36.5%的浓盐酸配制上述实验所用的稀盐酸,需浓盐酸的质量为________。
四、实验探究题(共4题;共44分)
18.某课外兴趣小组对一批铁样品(含有杂质,杂质不溶于水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中只有一位同学所取用的稀硫酸与铁样品恰好完全反应.实验数据如下表:
甲
乙
丙
烧杯+稀硫酸
200g
150g
150g
加入的铁样品
9g
9g
14g
充分反应后,烧杯+剩余物
208.7g
158.7g
163.7g
请你认真分析数据,回答下列问题:(烧杯的质量为25.4g,计算结果精确到1%)
(1)哪位同学所取用的稀硫酸与铁样品恰好完全应?
(2)计算样品中铁的质量分数?
(3)计算恰好完全反应后所得溶液中溶质的质量分数?
19.溶解度可表示物质溶解性的大小.
(1)如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.
①20℃时,甲的溶解度________(填“>”、“<”或“=”)乙的溶解度.
②40℃时,乙和丙________(填“能”或“不能”)形成溶质质量分数相同的饱和溶液.
③20℃时,烧杯中分别盛有相同质量甲、乙、丙的饱和溶液,各加入等质量的对应固体,并升温至50℃.请填写下表.
烧杯中的溶质
烧杯中固体的变化
甲
固体逐渐________
乙
固体逐渐________
丙
固体逐渐________
(2)气体的溶解度也有一定的变化规律:
打开可乐瓶,逸出大量气泡.由此可见,压强越小,CO2的溶解度越________.为增大CO2的溶解度,可采用的一种方法是________.
20.A,B,C三种物质的溶解度曲线如图所示,请回答下列问题:
(1)N点对应的是物质A的________(“饱和”或“不饱和”)溶液。
(2)t1℃时在50克水中加入10克A,充分搅拌,所得溶液的质量是________;要使该溶液中 A 的溶质质量分数变大,可进行的操作是________。
(3)除去A中少量的B的方法是________。
(4)t1℃时,将 A、B、C各8g分别加入盛有50g水的烧杯中,充分溶解,所得三种溶液中溶质的质量分数大小关系是________。
(5)用(3)提纯的A配制t1℃时50g质量分数为6%的A溶液。其操作步骤为:________、称量、量取、溶解装瓶贴标签。下列情况会导致上述所配制的溶液中溶质的质量分数偏大的是________(填字母序号)。
a.所用A仍然不纯
B.量取水所用量筒用蒸馏水润洗后有少量水残留在量筒中
C.用量筒量取水时,俯视读数
D.配好的溶液装瓶后,烧杯内有溶液残留
(6)t1℃时分别在100克水中配置成A,B,C的饱和溶液,升温到t2℃(不考虑水分蒸发),所得三种溶液溶质质量分数关系是________。
21.氯化钠是一种重要的资源,在海水中储量很丰富。
(1)海水晒盐是海水在常温下蒸发得到氯化钠的过程,实验室用氯化钠溶液模拟该过程(如图1)。已知B溶液恰好是氯化钠的饱和溶液,与B溶液中溶质质量相等的溶液是________(填字母,下同),与B溶液中溶质质量分数相等的溶液是________。
(2)氯化钠、硝酸钾、硒酸镉的溶解度曲线如图2所示。据图回答:
①溶解度变化受温度影响最大的是________,t℃时,溶解度最小的是________;
②t℃时,将25g硒酸镉加入________g水中,完全溶解后,恰好得到饱和溶液。要进一步提高该溶液的溶质质量分数,可进行的操作是________;
③硝酸钾溶液中含有少量氯化钠杂质,提纯的方法是________。
答案部分
一、单选题
1.【答案】 C
2.【答案】 D
3.【答案】 D
4.【答案】 D
5.【答案】 D
6.【答案】 B
7.【答案】 C
8.【答案】 B
9.【答案】D
10.【答案】 B
11.【答案】B
12.【答案】 C
二、填空题
13.【答案】 变浑浊;B
14.【答案】 (1)10%
(2)5;20
(3)40
15.【答案】 (1)110
(2)降温结晶
(3)硝酸钾;不变;一定
16.【答案】 C;面粉(或植物油等,其他合理答案也可)
三、计算题
17.【答案】 (1)Na2CO3+2HCl=2NaCl+H2O+CO2↑
(2)
(3)53%
(4)6.7%
(5)20g
四、实验探究题
18.【答案】 (1)解:甲、乙比较说明9g铁样品完全反应能产生0.3g氢气;乙、丙比较说明150g稀硫酸完全反应生成0.3g氢气,因此可以判断乙同学所取用的稀硫酸与铁样品恰好完全反应
答:乙同学所取用的稀硫酸与铁样品恰好完全应
(2)解:生成氢气的质量为:150g+9g﹣158.7g=0.3g
设Fe的质量为x,FeSO4的质量为y
Fe+H2SO4═
FeSO4+
H2↑
56
152
2
x
y
0.3g
?? 56x=152y=20.3g
解得:x═8.4g,y=22.8g
样品中铁的质量分数为: 8.4g9g ×100%=93%
答:样品中铁的质量分数为93%
(3)解:所得溶液中溶质的质量分数为: 22.8g150g+8.4g?0.3g?25.4g ×100%═17%
答:恰好完全反应后所得溶液中溶质的质量分数为17%
19.【答案】 (1)<;能;全部溶解;部分溶解;固体不溶解,反而增多
(2)小;增大压强或降低温度
20.【答案】 (1)不饱和
(2)60g;升高温度蒸发溶剂或升高温度增加溶质
(3)降温结晶
(4)A=B>C
(5)计算;C
(6)A=B>C
21.【答案】 (1)A;C、D
(2)硝酸钾;氯化钠;50;降低温度并加入硒酸镉;降温结晶法(或冷却热饱和溶液)
一、单选题(共12题;共28分)
1.下列实验操作或记录正确的是(?? )
A.?稀释浓硫酸时,将水沿烧杯壁慢慢倒入浓硫酸中,并用玻璃棒不断搅拌??????????B.?打开装有浓盐酸的试剂瓶,可看到白烟
C.?用托盘天平称取5.4g氯化钠????????????????????????????????D.?测溶液pH值时,将待测液倾倒在pH试纸上,将pH试纸的颜色与标准比色卡比较即可
2.某物质的饱和溶液一定是 ( )
A.?浓溶液?????????B.?稀溶液?????????C.?含100克水的溶液?????????D.?在一定条件下,不能再溶解该物质的溶液
3.向接近饱和的氯化钠溶液中,逐渐加入氯化钠固体,边加边搅拌。下列图形中变化关系正确的是(??? )
A.???????B.?????????C.???????D.?
4.用溶质质量分数为36%的浓盐酸配制一定浓度的稀盐酸时,不会用到的仪器是(?? )
A.?????????????????????????B.????????????????????????C.?????????????????????????D.?
5.下列关于溶液的说法中,正确的是(?? ) ??
A.?溶液都是无色透明的??????????????????????????????????????????B.?凡是均一的、稳定的液体都是溶液
C.?蔗糖溶液上半部分溶液的甜度低于下半部分溶液的甜度?????????D.?氢氧化钠溶液能导电,因为溶液中有较多自由移动的离子
6.如图表示X、Y、Z三种固体物质的溶解度曲线,下列说法错误的是(?? )
A.?t3℃时,X的饱和溶液一定比Y的不饱和溶液浓
B.?t2℃时,等质量的X、Y的溶液中,含有相同质量的溶质
C.?将t1℃时的三种物质的饱和溶液升温到t2℃,溶液中溶质质量分数的大小关系是Y>X>Z
D.?将t3℃时的X的不饱和溶液降温至t1℃,其溶质的质量分数可能变小
7.下列各因素不会影响固体溶解度的是()
A.?溶质的种类???????????????????????B.?溶剂的种类???????????????????????C.?溶剂的质量???????????????????????D.?温度的变化
8.关于如图所示实验的相关判断错误的是(?? )
A.?固体X可能是NaOH????????????????????????????????????????????B.?固体X可能是NH4NO3
C.?Ca(OH)2溶解度:①>②???????????????????????????????D.?Ca(OH)2质量分数:①=③
9.向 100g 水中不断加入固体 A 或改变温度,得到相应的溶液①~⑤。下列说法正确的是(?? )
A.?A的溶液中②的质量分数最大? ???????
B.?③⑤中 A 的质量分数相等
C.?②④⑤的溶液为饱和溶液???????
D.?①③④⑤中没有固体存在
10.现有含金属元素的质量分数为75%的氧化铁和氧化铜组成的混合物6.4g,与200g硫酸溶液恰好完全反应,则所用硫酸溶液的溶质质量分数为(???? )
A.?9.8%???????????????????????????????????B.?4.9%???????????????????????????????????C.?19.6%???????????????????????????????????D.?10%
11.下列溶液中溶质是气体的是(?? )
A.?生理盐水????????????????????????B.?盐酸????????????????????????C.?75%的消毒酒精????????????????????????D.?澄清的石灰水
12.将80g质量分数为35%的浓盐酸,稀释成14%的稀盐酸,需加水的质量为( )
A.?80g???????????????????????????????????B.?100g???????????????????????????????????C.?120g???????????????????????????????????D.?200g
二、填空题(共4题;共16分)
13.如图所示,广口瓶中盛有少量饱和澄清石灰水,小试管和U形管中均有适量水,现向小试管中注入适量浓硫酸.
请回答:
(1)可观察到饱和澄清石灰水________;
(2)U形管中a、b液面变化情况是________?(选填序号).
A.a液面上升,b液面下降?? B.a液面下降,b液面上升.
14.50℃时,将12g硝酸钾溶于108g水中,其溶质质量分数为10%,将此溶液分为三等份。
(1)取第一份溶液,使其温度升高10℃(无水分损失),所得溶液溶质质量分数为________。
(2)取第二份溶液,使其溶质质量分数变为原来的2倍,需加入硝酸钾晶体________g,或者蒸发________g的水。
(3)取第三份溶液,使其溶质质量分数变为原来的一半,需加水________g。
15.硝酸钾和氯化钠在不同温度下的溶解度如下表,请回答。
温度/℃
20
40
60
80
100
溶解度/g
硝酸钾
31.6
63.9
110
169
246
氯化钠
36.0
36.6
37.3
38.4
39.8
(1)60℃时硝酸钾的溶解度是________g。
(2)若硝酸钾中混有少量的氯化钠,提纯硝酸钾可以采取的方法是________。
(3)20℃时,将硝酸钾和氯化钠两种固体各36g分别加入盛有100水的烧杯中,充分溶解后可观察到如图所示的现象。
①烧杯A中溶解的物质是________。
②若向烧杯A中加入一定量的水使剩余固体刚好全部溶解变为饱和溶液,则溶液中溶质的质量分数________(填“变大”、“变小”或“不变”)。
③若将A、B烧杯中的物质同时升温至80℃,则A、B中溶质的质量________(填“一定”或“不一定”)相等。
16.把少量下列物质分散到水中,不能形成溶液的是________
A.蔗糖? ???B.食盐??? C.汽油??? ??D.________
三、计算题(共1题;共5分)
17.张南和化学兴趣小组的同学从内蒙古伊盟地区的天然碱湖带来一种“碱”样品(含 有碳酸钠、氯化钠和泥沙)。为测定这种样品(样品中的泥沙不参加反应,也不溶于水)中 碳酸钠的含量,并得到纯净的一定浓度的氯化钠溶液。进行了如下实验:
请回答下列问题:
(1)写出发生反应的化学方程式________;
(2)根据已知条件列出求解反应中生成氯化钠的质量(X)的比例式________;
(3)该“碱”样品中碳酸钠的含量为________;
(4)若最终得到的滤液为不饱和溶液,则所得滤液中溶质的质量分数为________;
(5)若用36.5%的浓盐酸配制上述实验所用的稀盐酸,需浓盐酸的质量为________。
四、实验探究题(共4题;共44分)
18.某课外兴趣小组对一批铁样品(含有杂质,杂质不溶于水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中只有一位同学所取用的稀硫酸与铁样品恰好完全反应.实验数据如下表:
甲
乙
丙
烧杯+稀硫酸
200g
150g
150g
加入的铁样品
9g
9g
14g
充分反应后,烧杯+剩余物
208.7g
158.7g
163.7g
请你认真分析数据,回答下列问题:(烧杯的质量为25.4g,计算结果精确到1%)
(1)哪位同学所取用的稀硫酸与铁样品恰好完全应?
(2)计算样品中铁的质量分数?
(3)计算恰好完全反应后所得溶液中溶质的质量分数?
19.溶解度可表示物质溶解性的大小.
(1)如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.
①20℃时,甲的溶解度________(填“>”、“<”或“=”)乙的溶解度.
②40℃时,乙和丙________(填“能”或“不能”)形成溶质质量分数相同的饱和溶液.
③20℃时,烧杯中分别盛有相同质量甲、乙、丙的饱和溶液,各加入等质量的对应固体,并升温至50℃.请填写下表.
烧杯中的溶质
烧杯中固体的变化
甲
固体逐渐________
乙
固体逐渐________
丙
固体逐渐________
(2)气体的溶解度也有一定的变化规律:
打开可乐瓶,逸出大量气泡.由此可见,压强越小,CO2的溶解度越________.为增大CO2的溶解度,可采用的一种方法是________.
20.A,B,C三种物质的溶解度曲线如图所示,请回答下列问题:
(1)N点对应的是物质A的________(“饱和”或“不饱和”)溶液。
(2)t1℃时在50克水中加入10克A,充分搅拌,所得溶液的质量是________;要使该溶液中 A 的溶质质量分数变大,可进行的操作是________。
(3)除去A中少量的B的方法是________。
(4)t1℃时,将 A、B、C各8g分别加入盛有50g水的烧杯中,充分溶解,所得三种溶液中溶质的质量分数大小关系是________。
(5)用(3)提纯的A配制t1℃时50g质量分数为6%的A溶液。其操作步骤为:________、称量、量取、溶解装瓶贴标签。下列情况会导致上述所配制的溶液中溶质的质量分数偏大的是________(填字母序号)。
a.所用A仍然不纯
B.量取水所用量筒用蒸馏水润洗后有少量水残留在量筒中
C.用量筒量取水时,俯视读数
D.配好的溶液装瓶后,烧杯内有溶液残留
(6)t1℃时分别在100克水中配置成A,B,C的饱和溶液,升温到t2℃(不考虑水分蒸发),所得三种溶液溶质质量分数关系是________。
21.氯化钠是一种重要的资源,在海水中储量很丰富。
(1)海水晒盐是海水在常温下蒸发得到氯化钠的过程,实验室用氯化钠溶液模拟该过程(如图1)。已知B溶液恰好是氯化钠的饱和溶液,与B溶液中溶质质量相等的溶液是________(填字母,下同),与B溶液中溶质质量分数相等的溶液是________。
(2)氯化钠、硝酸钾、硒酸镉的溶解度曲线如图2所示。据图回答:
①溶解度变化受温度影响最大的是________,t℃时,溶解度最小的是________;
②t℃时,将25g硒酸镉加入________g水中,完全溶解后,恰好得到饱和溶液。要进一步提高该溶液的溶质质量分数,可进行的操作是________;
③硝酸钾溶液中含有少量氯化钠杂质,提纯的方法是________。
答案部分
一、单选题
1.【答案】 C
2.【答案】 D
3.【答案】 D
4.【答案】 D
5.【答案】 D
6.【答案】 B
7.【答案】 C
8.【答案】 B
9.【答案】D
10.【答案】 B
11.【答案】B
12.【答案】 C
二、填空题
13.【答案】 变浑浊;B
14.【答案】 (1)10%
(2)5;20
(3)40
15.【答案】 (1)110
(2)降温结晶
(3)硝酸钾;不变;一定
16.【答案】 C;面粉(或植物油等,其他合理答案也可)
三、计算题
17.【答案】 (1)Na2CO3+2HCl=2NaCl+H2O+CO2↑
(2)
(3)53%
(4)6.7%
(5)20g
四、实验探究题
18.【答案】 (1)解:甲、乙比较说明9g铁样品完全反应能产生0.3g氢气;乙、丙比较说明150g稀硫酸完全反应生成0.3g氢气,因此可以判断乙同学所取用的稀硫酸与铁样品恰好完全反应
答:乙同学所取用的稀硫酸与铁样品恰好完全应
(2)解:生成氢气的质量为:150g+9g﹣158.7g=0.3g
设Fe的质量为x,FeSO4的质量为y
Fe+H2SO4═
FeSO4+
H2↑
56
152
2
x
y
0.3g
?? 56x=152y=20.3g
解得:x═8.4g,y=22.8g
样品中铁的质量分数为: 8.4g9g ×100%=93%
答:样品中铁的质量分数为93%
(3)解:所得溶液中溶质的质量分数为: 22.8g150g+8.4g?0.3g?25.4g ×100%═17%
答:恰好完全反应后所得溶液中溶质的质量分数为17%
19.【答案】 (1)<;能;全部溶解;部分溶解;固体不溶解,反而增多
(2)小;增大压强或降低温度
20.【答案】 (1)不饱和
(2)60g;升高温度蒸发溶剂或升高温度增加溶质
(3)降温结晶
(4)A=B>C
(5)计算;C
(6)A=B>C
21.【答案】 (1)A;C、D
(2)硝酸钾;氯化钠;50;降低温度并加入硒酸镉;降温结晶法(或冷却热饱和溶液)
同课章节目录
