第11单元 课题1 生活中常见的盐 第3课时-人教版九年级下册化学课件(共19张PPT含内嵌视频)
文档属性
| 名称 | 第11单元 课题1 生活中常见的盐 第3课时-人教版九年级下册化学课件(共19张PPT含内嵌视频) |
|
|
| 格式 | pptx | ||
| 文件大小 | 9.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-24 00:00:00 | ||
图片预览




文档简介
复分解反应之美丽化学
生活中常见的盐(第三课时)
复分解反应的应用
学习目标
1、巩固酸碱盐的性质及复分解反应发生的条件
2、掌握复分解反应的实质
3、会运用复分解反应条件解决物质的转化、共存、鉴别、除杂等问题。
明确目标
对照学案P25 【应用1】,回顾酸碱盐的化学性质,同桌之间相互说一说。
知识回顾
金属单质
金属氧化物
非金属氧化物
酸
碱
盐
指示剂
盐
?
?
③
⑤
⑥
⑦
⑧
④
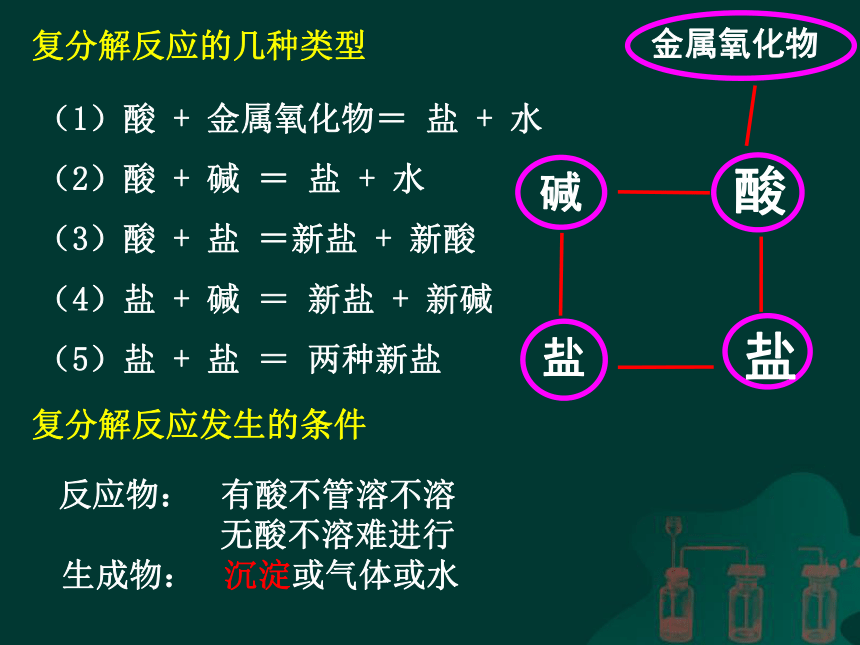
构建知识网络
(1)酸 + 金属氧化物= 盐 + 水
(2)酸 + 碱 = 盐 + 水
(3)酸 + 盐 =新盐 + 新酸
(4)盐 + 碱 = 新盐 + 新碱
(5)盐 + 盐 = 两种新盐
复分解反应的几种类型
复分解反应发生的条件
反应物: 有酸不管溶不溶
无酸不溶难进行
生成物: 沉淀或气体或水
酸
盐
碱
盐
金属氧化物
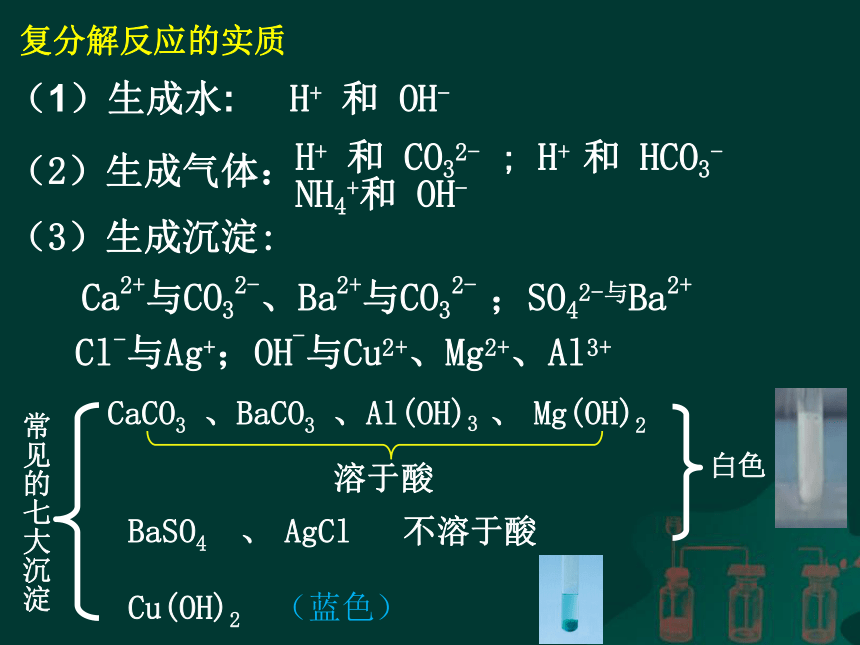
复分解反应的实质
(2)生成气体:
(1)生成水:
H+ 和 OH-
H+ 和 CO32- ; H+ 和 HCO3-
NH4+和 OH-
(3)生成沉淀:
Ca2+与CO32-、Ba2+与CO32- ;SO42-与Ba2+ Cl-与Ag+;OH-与Cu2+、Mg2+、Al3+
常见的七大沉淀
CaCO3 、BaCO3 、Al(OH)3 、 Mg(OH)2
Cu(OH)2 (蓝色)
BaSO4 、 AgCl 不溶于酸
白色
溶于酸
3.现有 Fe、CuO、MgCl2 、Ca(OH)2 、稀H 2 SO 4 等
五种物质,在常温下它们两两相互发生的化学反应有( )
A.7个 B.6个 C.5个 D.4个
应用1:物质转化
D
应用2、离子共存
4.下列各组物质能在pH=1的无色溶液中大量共存的是 ( )
A.K2SO4、Ba(OH)2、KCl
B.Cu(NO3)2、NaCl、KNO3
C.Na2CO3、KNO3、NH4Cl
D.MgSO4、NaNO3、KCl
D
H+
H+
H+
H+
H+
OH-
CO32-
构建知识网络
我们可以把11对不能共存的离子用自己喜欢的方式整理出来。
NH4+
Cu2+
Mg2+
Al3+
HCO3-
Ca2+
Ag+
Ba2+
SO42-
Cl-
方法总结
常见有颜色的离子:Fe2+ 浅绿色
Fe3+ 黄
Cu2+ 蓝色
(1)溶液无色透明时,则不含有色离子
(2)PH > 7 的溶液中不存在与 OH- 起反应的离子
PH < 7 的溶液中不存在与 H+ 起反应的离子
熟练掌握11对常考的不能共存的离子对,是解这类题的关键
注意题干中的隐含条件
应用3:鉴别
B
完成鉴别题时,首先考虑物质本身的颜色,其次考虑发生化学反应时出现的特殊现象,如产生气体、沉淀、指示剂颜色变化等。
方法总结
8、下列各组溶液,只用一种试剂不能鉴别的是( )
A.Na2SO4、CuSO4、NaCl
B.NaCl、Na2CO3、Na2SO4
C.FeCl2、NaNO3、Na2SO4
D. H2SO4、Ca(OH)2、NaCl
应用4:除杂
选项
物质
所含杂质
除杂质试剂及方法
A
硝酸钠
氯化钾
适量的水
B
KCl溶液
K2CO3
加入过量氯化钙溶液充分反应后过滤
C
硫酸亚铁溶液
硫酸铜溶液
过量的铁粉
D
氯化钾溶液
稀盐酸
过量的碳酸钠溶液
C
11.除去下列物质中所含的少量杂质,所选试剂正确的是( )
方法总结
除杂原则:
1.所加试剂只与杂质反应,不与被提纯物反应;
2.不引入新的杂质;
3.注意所加试剂的量是适量还是过量。
除杂方法:物理方法:过滤、蒸发、磁铁吸引等;
化学方法,将杂质转变成沉淀、气体或
水等便于分离的物质而除去。
学以致用
我能行
完成学案P25~26剩下的练习并展示。
1.D 2.B 5.C 6.C 7.B
9.C 11.C 12.D
交换批改,组内交流订正。
错题讲解。
应用5:综合题
13.一包固体粉末,由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的两种或两种以上的物质混合而成.为探究其组成(硫酸钡是不溶于水,也不溶于酸的白色固体),进行如下实验:
(1)取少量固体粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液.则原白色粉末中一定不含有 .
(2)取实验(1)滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体.则原白色粉末中一定含有 .
根据上述实验可推断:原白色粉末的组成有 种可能.
为进一步探究原白色粉末的组成,取实验(1)得到的滤液,向其中通入二氧化碳,产生白色沉淀,则原白色粉末中组成物质有 .
CaCO3
CuSO4
5
CaCO3、BaCl2、NaOH
(1)CuO 复分解反应
(2)硫酸
(3)CuSO4 + Fe = FeSO4 + Cu
CuSO4 + BaCl2 = BaSO4 ↓+ CuCl2
14.
本节课你收获了什么?
巩固成果
谢谢大家!
Good bye !
2018年3月
生活中常见的盐(第三课时)
复分解反应的应用
学习目标
1、巩固酸碱盐的性质及复分解反应发生的条件
2、掌握复分解反应的实质
3、会运用复分解反应条件解决物质的转化、共存、鉴别、除杂等问题。
明确目标
对照学案P25 【应用1】,回顾酸碱盐的化学性质,同桌之间相互说一说。
知识回顾
金属单质
金属氧化物
非金属氧化物
酸
碱
盐
指示剂
盐
?
?
③
⑤
⑥
⑦
⑧
④
构建知识网络
(1)酸 + 金属氧化物= 盐 + 水
(2)酸 + 碱 = 盐 + 水
(3)酸 + 盐 =新盐 + 新酸
(4)盐 + 碱 = 新盐 + 新碱
(5)盐 + 盐 = 两种新盐
复分解反应的几种类型
复分解反应发生的条件
反应物: 有酸不管溶不溶
无酸不溶难进行
生成物: 沉淀或气体或水
酸
盐
碱
盐
金属氧化物
复分解反应的实质
(2)生成气体:
(1)生成水:
H+ 和 OH-
H+ 和 CO32- ; H+ 和 HCO3-
NH4+和 OH-
(3)生成沉淀:
Ca2+与CO32-、Ba2+与CO32- ;SO42-与Ba2+ Cl-与Ag+;OH-与Cu2+、Mg2+、Al3+
常见的七大沉淀
CaCO3 、BaCO3 、Al(OH)3 、 Mg(OH)2
Cu(OH)2 (蓝色)
BaSO4 、 AgCl 不溶于酸
白色
溶于酸
3.现有 Fe、CuO、MgCl2 、Ca(OH)2 、稀H 2 SO 4 等
五种物质,在常温下它们两两相互发生的化学反应有( )
A.7个 B.6个 C.5个 D.4个
应用1:物质转化
D
应用2、离子共存
4.下列各组物质能在pH=1的无色溶液中大量共存的是 ( )
A.K2SO4、Ba(OH)2、KCl
B.Cu(NO3)2、NaCl、KNO3
C.Na2CO3、KNO3、NH4Cl
D.MgSO4、NaNO3、KCl
D
H+
H+
H+
H+
H+
OH-
CO32-
构建知识网络
我们可以把11对不能共存的离子用自己喜欢的方式整理出来。
NH4+
Cu2+
Mg2+
Al3+
HCO3-
Ca2+
Ag+
Ba2+
SO42-
Cl-
方法总结
常见有颜色的离子:Fe2+ 浅绿色
Fe3+ 黄
Cu2+ 蓝色
(1)溶液无色透明时,则不含有色离子
(2)PH > 7 的溶液中不存在与 OH- 起反应的离子
PH < 7 的溶液中不存在与 H+ 起反应的离子
熟练掌握11对常考的不能共存的离子对,是解这类题的关键
注意题干中的隐含条件
应用3:鉴别
B
完成鉴别题时,首先考虑物质本身的颜色,其次考虑发生化学反应时出现的特殊现象,如产生气体、沉淀、指示剂颜色变化等。
方法总结
8、下列各组溶液,只用一种试剂不能鉴别的是( )
A.Na2SO4、CuSO4、NaCl
B.NaCl、Na2CO3、Na2SO4
C.FeCl2、NaNO3、Na2SO4
D. H2SO4、Ca(OH)2、NaCl
应用4:除杂
选项
物质
所含杂质
除杂质试剂及方法
A
硝酸钠
氯化钾
适量的水
B
KCl溶液
K2CO3
加入过量氯化钙溶液充分反应后过滤
C
硫酸亚铁溶液
硫酸铜溶液
过量的铁粉
D
氯化钾溶液
稀盐酸
过量的碳酸钠溶液
C
11.除去下列物质中所含的少量杂质,所选试剂正确的是( )
方法总结
除杂原则:
1.所加试剂只与杂质反应,不与被提纯物反应;
2.不引入新的杂质;
3.注意所加试剂的量是适量还是过量。
除杂方法:物理方法:过滤、蒸发、磁铁吸引等;
化学方法,将杂质转变成沉淀、气体或
水等便于分离的物质而除去。
学以致用
我能行
完成学案P25~26剩下的练习并展示。
1.D 2.B 5.C 6.C 7.B
9.C 11.C 12.D
交换批改,组内交流订正。
错题讲解。
应用5:综合题
13.一包固体粉末,由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的两种或两种以上的物质混合而成.为探究其组成(硫酸钡是不溶于水,也不溶于酸的白色固体),进行如下实验:
(1)取少量固体粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液.则原白色粉末中一定不含有 .
(2)取实验(1)滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体.则原白色粉末中一定含有 .
根据上述实验可推断:原白色粉末的组成有 种可能.
为进一步探究原白色粉末的组成,取实验(1)得到的滤液,向其中通入二氧化碳,产生白色沉淀,则原白色粉末中组成物质有 .
CaCO3
CuSO4
5
CaCO3、BaCl2、NaOH
(1)CuO 复分解反应
(2)硫酸
(3)CuSO4 + Fe = FeSO4 + Cu
CuSO4 + BaCl2 = BaSO4 ↓+ CuCl2
14.
本节课你收获了什么?
巩固成果
谢谢大家!
Good bye !
2018年3月
同课章节目录
