鲁教版九年级下册化学 7.2碱及其性质 课件(14张PPT)
文档属性
| 名称 | 鲁教版九年级下册化学 7.2碱及其性质 课件(14张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 361.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-28 00:00:00 | ||
图片预览



文档简介
第二章 常见的酸和碱
碱及其性质
一、常见的碱
(一)物理性质
1、NaOH固体的物理性质
颜色
状态
露置在空气中的变化
溶解
情况
其他
氢氧
化钠
白色
固体
吸收水蒸气
而逐渐溶解,
NaOH固体
可作干燥剂
易溶
于水,
溶解时
放热
腐蚀性
俗称火碱、
烧碱、
苛性钠
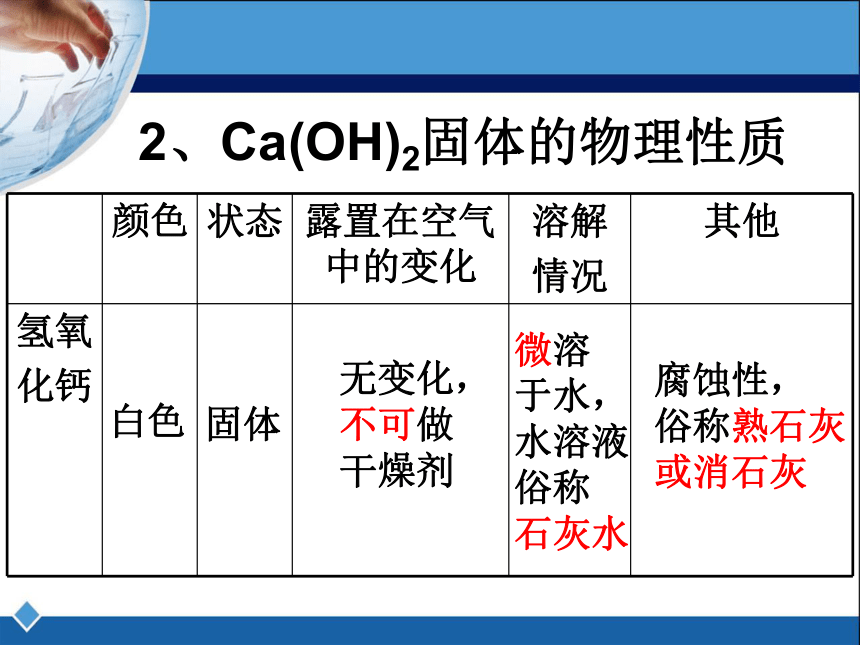
2、Ca(OH)2固体的物理性质
颜色
状态
露置在空气中的变化
溶解
情况
其他
氢氧
化钙
白色
固体
微溶
于水,
水溶液
俗称
石灰水
腐蚀性,
俗称熟石灰
或消石灰
无变化,
不可做
干燥剂
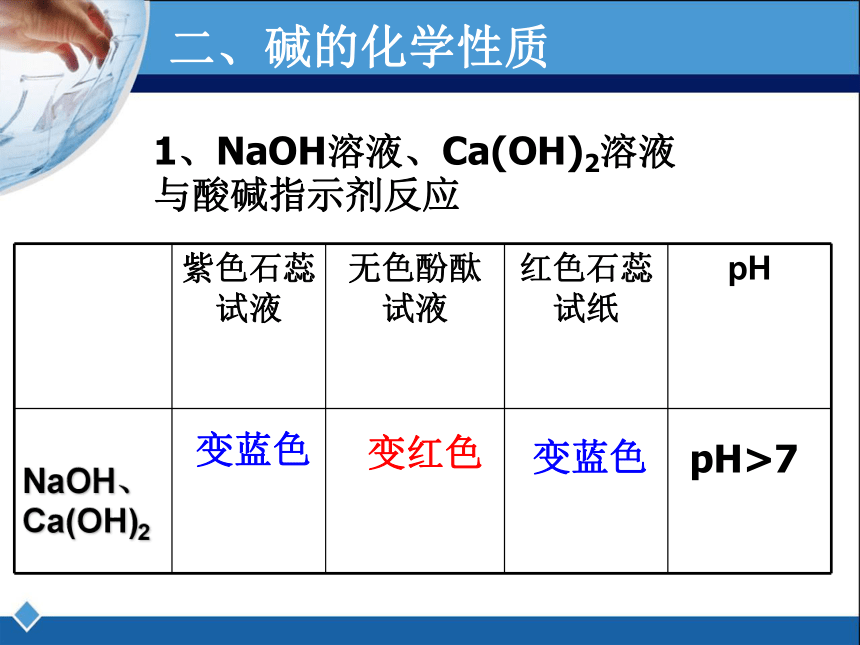
二、碱的化学性质
1、NaOH溶液、Ca(OH)2溶液
与酸碱指示剂反应
紫色石蕊试液
无色酚酞试液
红色石蕊试纸
pH
NaOH、Ca(OH)2
变蓝色
变红色
变蓝色
pH>7
2、 NaOH溶液、Ca(OH)2溶液
与非金属氧化物反应
CO2+Ca(OH)2==CaCO3 +H2O
CO2+2NaOH==Na2CO3+H2O
NaOH固体不仅吸收空气中的( )而
( ),而且与空气中的( )反应而( )
水蒸气
溶解
CO2
变质
因此, NaOH固体必须密封保存
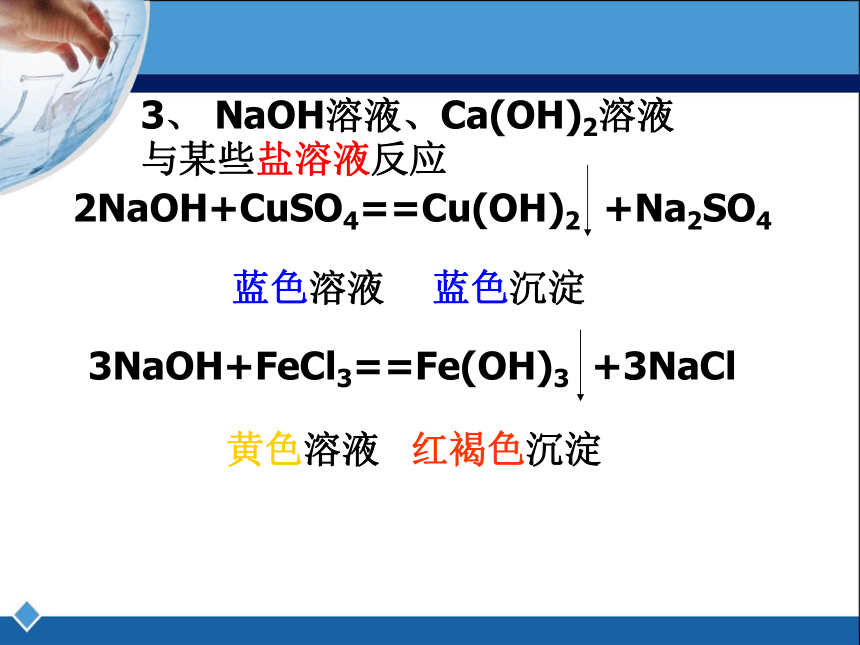
3、 NaOH溶液、Ca(OH)2溶液
与某些盐溶液反应
2NaOH+CuSO4==Cu(OH)2 +Na2SO4
蓝色沉淀
3NaOH+FeCl3==Fe(OH)3 +3NaCl
蓝色溶液
黄色溶液
红褐色沉淀
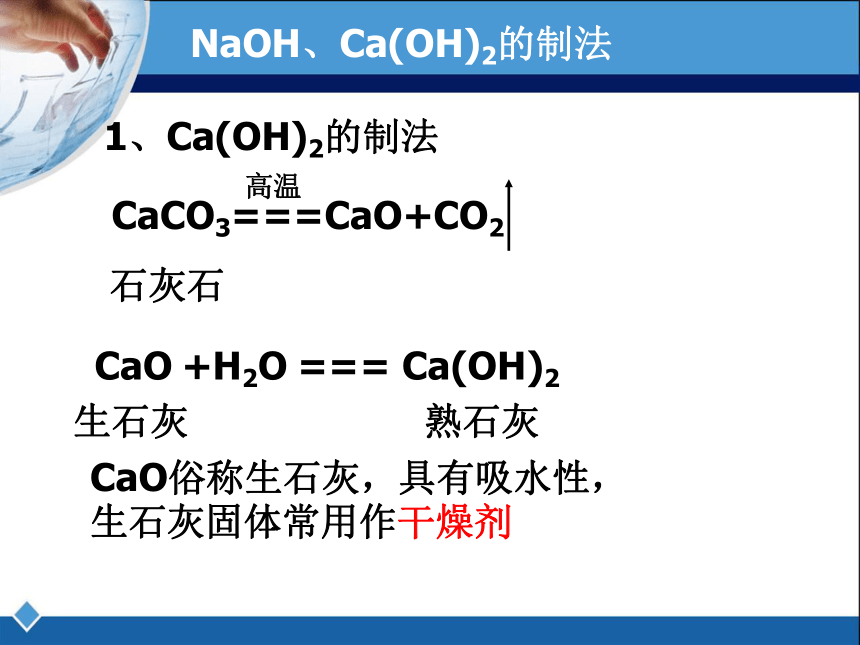
NaOH、Ca(OH)2的制法
1、Ca(OH)2的制法
生石灰
=== Ca(OH)2
熟石灰
CaO
石灰石
CaCO3===CaO+CO2
高温
+H2O
CaO俗称生石灰,具有吸水性,
生石灰固体常用作干燥剂
2、NaOH的制法
Na2CO3+Ca(OH)2==CaCO3 +2NaOH
CaCO3===CaO+CO2
高温
=== Ca(OH)2
CaO+H2O
工业上用此反应制烧碱
小结:NaOH溶液、Ca(OH)2溶液的化学
性质
1、NaOH溶液、Ca(OH)2溶液与酸碱指示剂反应
2、 NaOH溶液、Ca(OH)2溶液和酸反应,生成盐和水
3、 NaOH溶液、Ca(OH)2溶液与非金属氧化物反应
4、 NaOH溶液、Ca(OH)2溶液与盐溶液反应
多识一点
与酸不同,氢氧化钠和氢氧化钙不能与生锈
铁钉以及铁反应。
工业上,常用铁桶来储运烧碱,就是利用了
碱与铁不反应的性质。
3NaOH+FeCl3==Fe(OH)3 +3NaCl
Na2CO3+Ca(OH)2==CaCO3 +2NaOH
2NaOH+CuCl2==Cu(OH)2 +2NaCl
3、复分解反应
(1)定义:如果两种化合物互相交换成分,
生成另外两种新的化合物,那么这样的反应
就叫做复分解反应。
练习:写出下列反应的化学方程式
氢氧化钠与二氧化碳
盐酸与硝酸银
氢氧化钠与硫酸铜
氯化钠与硫酸
(2)复分解反应的条件:
有气体放出,
或有沉淀析出,
或有水生成。
(3)溶解性口诀:
钾钠铵盐硝酸盐,
氯化物难溶氯化银,
溶碱只有钾钠钙和钡,
均能溶于水中间,
硫酸盐难溶硫酸钡,
碳酸盐只溶钾钠铵。
碱及其性质
一、常见的碱
(一)物理性质
1、NaOH固体的物理性质
颜色
状态
露置在空气中的变化
溶解
情况
其他
氢氧
化钠
白色
固体
吸收水蒸气
而逐渐溶解,
NaOH固体
可作干燥剂
易溶
于水,
溶解时
放热
腐蚀性
俗称火碱、
烧碱、
苛性钠
2、Ca(OH)2固体的物理性质
颜色
状态
露置在空气中的变化
溶解
情况
其他
氢氧
化钙
白色
固体
微溶
于水,
水溶液
俗称
石灰水
腐蚀性,
俗称熟石灰
或消石灰
无变化,
不可做
干燥剂
二、碱的化学性质
1、NaOH溶液、Ca(OH)2溶液
与酸碱指示剂反应
紫色石蕊试液
无色酚酞试液
红色石蕊试纸
pH
NaOH、Ca(OH)2
变蓝色
变红色
变蓝色
pH>7
2、 NaOH溶液、Ca(OH)2溶液
与非金属氧化物反应
CO2+Ca(OH)2==CaCO3 +H2O
CO2+2NaOH==Na2CO3+H2O
NaOH固体不仅吸收空气中的( )而
( ),而且与空气中的( )反应而( )
水蒸气
溶解
CO2
变质
因此, NaOH固体必须密封保存
3、 NaOH溶液、Ca(OH)2溶液
与某些盐溶液反应
2NaOH+CuSO4==Cu(OH)2 +Na2SO4
蓝色沉淀
3NaOH+FeCl3==Fe(OH)3 +3NaCl
蓝色溶液
黄色溶液
红褐色沉淀
NaOH、Ca(OH)2的制法
1、Ca(OH)2的制法
生石灰
=== Ca(OH)2
熟石灰
CaO
石灰石
CaCO3===CaO+CO2
高温
+H2O
CaO俗称生石灰,具有吸水性,
生石灰固体常用作干燥剂
2、NaOH的制法
Na2CO3+Ca(OH)2==CaCO3 +2NaOH
CaCO3===CaO+CO2
高温
=== Ca(OH)2
CaO+H2O
工业上用此反应制烧碱
小结:NaOH溶液、Ca(OH)2溶液的化学
性质
1、NaOH溶液、Ca(OH)2溶液与酸碱指示剂反应
2、 NaOH溶液、Ca(OH)2溶液和酸反应,生成盐和水
3、 NaOH溶液、Ca(OH)2溶液与非金属氧化物反应
4、 NaOH溶液、Ca(OH)2溶液与盐溶液反应
多识一点
与酸不同,氢氧化钠和氢氧化钙不能与生锈
铁钉以及铁反应。
工业上,常用铁桶来储运烧碱,就是利用了
碱与铁不反应的性质。
3NaOH+FeCl3==Fe(OH)3 +3NaCl
Na2CO3+Ca(OH)2==CaCO3 +2NaOH
2NaOH+CuCl2==Cu(OH)2 +2NaCl
3、复分解反应
(1)定义:如果两种化合物互相交换成分,
生成另外两种新的化合物,那么这样的反应
就叫做复分解反应。
练习:写出下列反应的化学方程式
氢氧化钠与二氧化碳
盐酸与硝酸银
氢氧化钠与硫酸铜
氯化钠与硫酸
(2)复分解反应的条件:
有气体放出,
或有沉淀析出,
或有水生成。
(3)溶解性口诀:
钾钠铵盐硝酸盐,
氯化物难溶氯化银,
溶碱只有钾钠钙和钡,
均能溶于水中间,
硫酸盐难溶硫酸钡,
碳酸盐只溶钾钠铵。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
