5-3-3 羧酸 酯(2)酯 课件(24张ppt) 2020-2021学年人教版高二化学选修5有机化学基础
文档属性
| 名称 | 5-3-3 羧酸 酯(2)酯 课件(24张ppt) 2020-2021学年人教版高二化学选修5有机化学基础 |

|
|
| 格式 | pptx | ||
| 文件大小 | 43.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-03-31 00:00:00 | ||
图片预览







文档简介
第三章
烃的含氧衍生物
2021.04: W
学习
目标
第三节
羧酸 酯
1. 了解酯类化合物的结构特点。
2. 掌握酯类化合物的化学性质。
3.酯的组成及结构特点、水解反应。
在酒的商标里,常见到有XO、VOSP等符号,你知道它们代表什么意义呢?
储存了50年的酒。
储存了30年的酒。
XO
VOSP
生活小知识
为什么说“陈年老酒格外香?”
储存过程中生成了有香味的酯 。
含有:丁酸乙酯
含有:戊酸戊酯
含有:乙酸异戊酯
自然界中的有机酯
三.酯
1、概念
酯是羧酸分子羧基中的-OH被-OR′取代后的产物。
2、结构通式
R1 :只能是烃基
R(H)
C
O
R1
O
饱和一元酯的分子通式为:
由饱和一元羧酸与饱和一元醇反应生成的酯
CnH2nO2 (n≥2)
与饱和一元羧酸互为同分异构体
3、酯的命名
根据生成酯的酸和醇命名:
“某酸某酯”
(1)CH3COOCH2CH3
(2)HCOOCH2CH3
(3)CH3CH2O—NO2
乙酸乙酯
甲酸乙酯
硝酸乙酯
4、物理性质
(1)低级酯一般为无色有芳香气味的液体;
(2)高级酯中,饱和酯通常为固体,不饱和酯通常为液体。
(3)酯密度一般比水小,都难溶于水,易溶于有机溶剂。
阅读教材62页第一段,了解酯的物理性质。
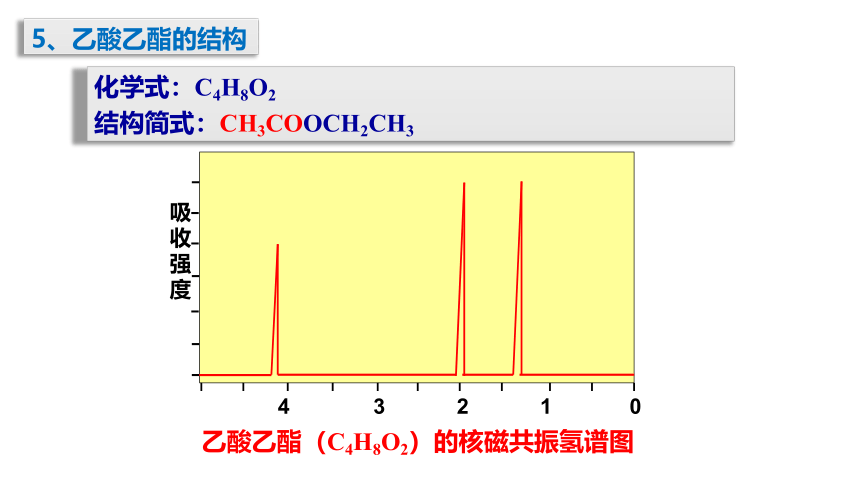
5、乙酸乙酯的结构
结构简式:CH3COOCH2CH3
化学式:C4H8O2
乙酸乙酯(C4H8O2)的核磁共振氢谱图
吸收强度
4 3 2 1 0
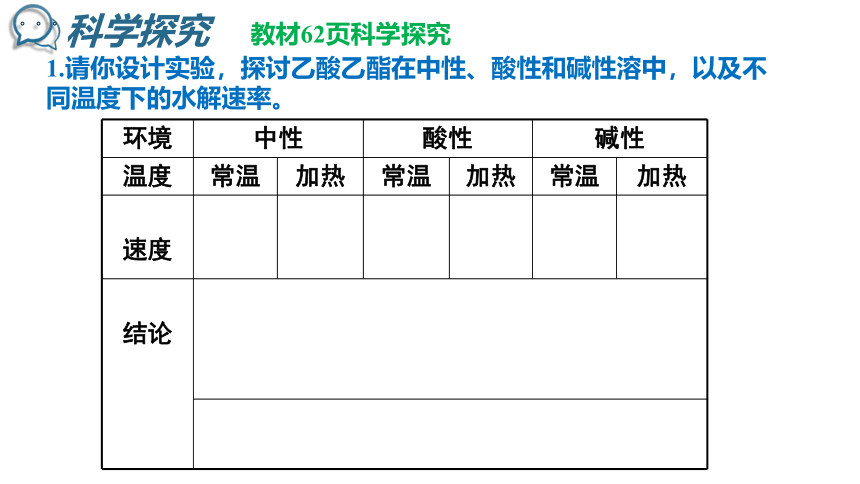
科学探究
教材62页科学探究
1.请你设计实验,探讨乙酸乙酯在中性、酸性和碱性溶中,以及不同温度下的水解速率。
环境
中性
酸性
碱性
温度
常温
加热
常温
加热
常温
加热
速度
结论
观察学习
科学探究
教材62页科学探究
1.请你设计实验,探讨乙酸乙酯在中性、酸性和碱性溶中,以及不同温度下的水解速率。
环境
中性
酸性
碱性
温度
常温
加热
常温
加热
常温
加热
速度
结论
无变化
无变
化
酯减少
较慢
酯减少
较快
酯层消失较快
酯层消失,快
1、酯在碱性条件下水解速率最快,其次是酸性条件,中性条件下几乎不水解; 在强碱的溶液中酯水解趋于完全。
2、温度越高,酯水解程度越大。
(水解反应是吸热反应)
6、酯的化学性质
(2)水解反应
(1)易燃
取代反应
无机酸或碱催化作用下能发生水解反应生成相应的酸与醇。
CH3COOC2H5 +H2O
稀H2SO4
△
CH3COOH + C2H5OH
NaOH
△
CH3COOC2H5 +H2O
CH3COOH + C2H5OH
O
CH3C-O-C2H5 + NaOH
=
△
O
CH3C-ONa + C2H5OH
=
注
意
1、无机酸只起催化作用。
2、无机碱不仅起催化作用,而且还能促使水解程度增大,直至完全。
3、酯类的水解与酯化反应互为可逆反应。
酯 化
水 解
反应关系
催 化 剂
催化剂的
其他作用
加热方式
反应类型
NaOH中和酯水解生成的CH3COOH,提高酯的水解率
CH3COOH+C2H5OH CH3COOC2H5+H2O
浓 硫 酸
稀H2SO4或NaOH
吸水,提高反应物的转化率
酒精灯火焰加热
水浴加热
酯化反应
取代反应
水解反应
取代反应
酯化反应与酯水解的比较
1.某酯A水解后生成B和C,其B经两步氧化后生成C,这种酯的结构简式可能是( )
A、CH3COOCH3
B、HCOOCH3
C、HCOOC2H5
D、CH3COOC2H5
课堂练习
D
2.某中性有机物,在酸性条件下可以发生水解,生成相对分子质量相同的A和B,A是中性物质,B可以与碳酸钠反应放出气体,该有机物是( )
A.CH3COOC3H7 B.CH3COOC2H5
C.CH3COONa D.CH3CH2Br
A
3.某有机物的结构简式是
关于它的性质描述正确的是( )
①能发生加成反应 ②能溶解于NaOH溶液中,且消耗NaOH 3 mol ③能水解生成两种酸 ④不能使溴水褪色 ⑤能发生酯化反应 ⑥有酸性
A.①②③ B.②③⑤ C.仅⑥ D.全部正确
课堂练习
D
7、同分异构体
(2)书写方法
(1)同分异构体
②碳链异构
①官能团异构(同碳原子数的酸和酯互为同分异构体)
③官能团位置异构
a、羧酸:取代法或插入法
b、酯:分配法或插入法
例1:(1) C3H6O2属于酸的同分异构有 种,C4H8O2属于酸的同分异构有 种, C5H10O2属于酸的同分异构有 种。
1
2
4
例2
(1)写出C3H6O2属于羧酸和酯的同分异构体.
(2)写出C4H8O2属于羧酸和酯的同分异构体。
CH3CH2
COOH
酸
酯
O
—C—O—
=
O
H-C-O-CH2CH3
=
O
CH3-C-O-CH3
=
C3H6O2共三种同分异构体,一种酸,两种酯。
左边为酸的部分,已含有一个碳
右边为醇的部分,最简单的是甲醇。
分子式除酯基还剩C2H6,可将碳依次分配到左右。
1.左边H—,右边—C2H5:
2.左边CH3—,右边—CH3:
思考:可以左边左边C2H5—,右边—H吗?
例2
(1)写出C3H6O2属于羧酸和酯的同分异构体.
(2)写出C4H8O2属于羧酸和酯的同分异构体。
CH3CH2CH2
COOH
酸
酯
O
—C—O—
=
O
H-C-O-CH2CH2CH3
=
O
CH3-C-O-CH2CH3
=
C3H6O2共六种同分异构体,两种酸,四种酯。
1.左边H—,右边—C3H7:
2.左边CH3—,右边—C2H5:
COOH
CH3CH—
CH3
O
H-C-O-CHCH3
CH3
=
3.左边C2H5—,右边—CH3:
O
CH3CH2-C-O-CH3
=
丙基有二种,所以酸有二种。
丙基有二种,所以酯有二种。
例3
写出C5H10O2属于羧酸和酯的同分异构体.
O
H-C-O-C4H9
=
O
CH3-C-O-C3H7
=
C4H9—
COOH
酸
酯
O
—C—O—
=
丁基有四种,所以酸有4种。
丁基有四种,所以酯有4种。
丙基有二种,所以酯有2种。
O
C2H5-C-O-C2H5
=
乙基只有一种,所以酯有1种。
O
C3H7-C-O-CH3
=
丙基有二种,所以酯有2种。
C5H10O2共13种同分异构体,四种酸,九种酯。
4、邻甲基苯甲酸( )有多种同分异构体,其中属于酯类,但分子结构中含有甲基和苯环的异构体有( )
A.2种 B.3种 C.4种 D.5种
课堂练习
D
C
5.由—CH3、—OH、 、—COOH四种基团两两组合而成的化合物中,其水溶液能使紫色石蕊试液变红的有( )
A.1种 B.2种 C.3种 D.4种
6.现有分子式为C3H6O2的四种有机物A、B、C、D,且分子内均含有甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
则A、B、C、D的结构简式分别为:
A: B:
C: D:
NaOH溶液
银氨溶液
新制Cu(OH)2
金属钠
A
中和反应
——
溶解
产生氢气
B
——
有银镜
产生红色沉淀
产生氢气
C
水解反应
有银镜
产生红色沉淀
——
D
水解反应
——
——
——
CH3CH2COOH
HCOOCH2CH3
CH3COOCH3
CH3CH(OH)CHO
课堂练习
7、某有机化合物X(C7H8O)与另一有机化合物Y发生如下反应
生成化合物Z(C11H14O2)。
(1)X是下列化合物之一,已知X不能与FeCl3溶液发生显色反应,则X是________(填标号字母)。
(2)Y的分子式是________,可能的结构简式是_____________________和__________________。
(3)Y有多种同分异构体,其中一种同分异构体E发生银镜反应后,其产物经氧化可得到F(C4H8O3)。F可发生如下反应:
该反应的类型是________,E的结构简式是________。
(4)若Y与E具有相同的碳链,则Z的结构简式为_____________。
课堂练习
D
C4H8O2
CH3CH2CH2COOH
CH3CHCOOH
CH3
取代反应
CH2CH2CH2CHO
OH
CH2OOCCH2CH2CH3
8、下图中A、B、C、D、E、F、G均为有机化合物。
(3)A的结构简式是___,1 mol A最多与_____mol NaOH溶液反应。
(4)符合下列3个条件的B的同分异构体的数目有______个。
①含有邻二取代苯环结构②与B有相同官能团③不与FeCl3溶液发生显色反应
根据上图回答问题:
(1)D、F的化学名称是________、________。
(2)写出反应②、 ④的化学方程式,并注明反应类型。
课堂练习
—CH2OH
—CH2COOH
CH2=CH2
CH3CH2OH
CH3COOH
CH3COOC2H5
—CH2OOCCH3
—CH2COOC2H5
乙醇
乙酸乙酯
2
4
—CH3
—CH2COOH
—CH2CH3
—COOH
9.请写出以水、空气、乙烯为原料制取乙酸乙酯的相关化学方程式:
CH2=CH2 + H2O CH3CH2OH
高温、高压
催化剂
CH3COOC2H5 +H2O
浓H2SO4
△
CH3COOH + C2H5OH
Cu或Ag
2CH3CHO +2H2O
2CH3CH2OH + O2
催化剂
△
2CH3COOH
2CH3CHO + O2
课堂练习
谢谢欣赏
烃的含氧衍生物
2021.04: W
学习
目标
第三节
羧酸 酯
1. 了解酯类化合物的结构特点。
2. 掌握酯类化合物的化学性质。
3.酯的组成及结构特点、水解反应。
在酒的商标里,常见到有XO、VOSP等符号,你知道它们代表什么意义呢?
储存了50年的酒。
储存了30年的酒。
XO
VOSP
生活小知识
为什么说“陈年老酒格外香?”
储存过程中生成了有香味的酯 。
含有:丁酸乙酯
含有:戊酸戊酯
含有:乙酸异戊酯
自然界中的有机酯
三.酯
1、概念
酯是羧酸分子羧基中的-OH被-OR′取代后的产物。
2、结构通式
R1 :只能是烃基
R(H)
C
O
R1
O
饱和一元酯的分子通式为:
由饱和一元羧酸与饱和一元醇反应生成的酯
CnH2nO2 (n≥2)
与饱和一元羧酸互为同分异构体
3、酯的命名
根据生成酯的酸和醇命名:
“某酸某酯”
(1)CH3COOCH2CH3
(2)HCOOCH2CH3
(3)CH3CH2O—NO2
乙酸乙酯
甲酸乙酯
硝酸乙酯
4、物理性质
(1)低级酯一般为无色有芳香气味的液体;
(2)高级酯中,饱和酯通常为固体,不饱和酯通常为液体。
(3)酯密度一般比水小,都难溶于水,易溶于有机溶剂。
阅读教材62页第一段,了解酯的物理性质。
5、乙酸乙酯的结构
结构简式:CH3COOCH2CH3
化学式:C4H8O2
乙酸乙酯(C4H8O2)的核磁共振氢谱图
吸收强度
4 3 2 1 0
科学探究
教材62页科学探究
1.请你设计实验,探讨乙酸乙酯在中性、酸性和碱性溶中,以及不同温度下的水解速率。
环境
中性
酸性
碱性
温度
常温
加热
常温
加热
常温
加热
速度
结论
观察学习
科学探究
教材62页科学探究
1.请你设计实验,探讨乙酸乙酯在中性、酸性和碱性溶中,以及不同温度下的水解速率。
环境
中性
酸性
碱性
温度
常温
加热
常温
加热
常温
加热
速度
结论
无变化
无变
化
酯减少
较慢
酯减少
较快
酯层消失较快
酯层消失,快
1、酯在碱性条件下水解速率最快,其次是酸性条件,中性条件下几乎不水解; 在强碱的溶液中酯水解趋于完全。
2、温度越高,酯水解程度越大。
(水解反应是吸热反应)
6、酯的化学性质
(2)水解反应
(1)易燃
取代反应
无机酸或碱催化作用下能发生水解反应生成相应的酸与醇。
CH3COOC2H5 +H2O
稀H2SO4
△
CH3COOH + C2H5OH
NaOH
△
CH3COOC2H5 +H2O
CH3COOH + C2H5OH
O
CH3C-O-C2H5 + NaOH
=
△
O
CH3C-ONa + C2H5OH
=
注
意
1、无机酸只起催化作用。
2、无机碱不仅起催化作用,而且还能促使水解程度增大,直至完全。
3、酯类的水解与酯化反应互为可逆反应。
酯 化
水 解
反应关系
催 化 剂
催化剂的
其他作用
加热方式
反应类型
NaOH中和酯水解生成的CH3COOH,提高酯的水解率
CH3COOH+C2H5OH CH3COOC2H5+H2O
浓 硫 酸
稀H2SO4或NaOH
吸水,提高反应物的转化率
酒精灯火焰加热
水浴加热
酯化反应
取代反应
水解反应
取代反应
酯化反应与酯水解的比较
1.某酯A水解后生成B和C,其B经两步氧化后生成C,这种酯的结构简式可能是( )
A、CH3COOCH3
B、HCOOCH3
C、HCOOC2H5
D、CH3COOC2H5
课堂练习
D
2.某中性有机物,在酸性条件下可以发生水解,生成相对分子质量相同的A和B,A是中性物质,B可以与碳酸钠反应放出气体,该有机物是( )
A.CH3COOC3H7 B.CH3COOC2H5
C.CH3COONa D.CH3CH2Br
A
3.某有机物的结构简式是
关于它的性质描述正确的是( )
①能发生加成反应 ②能溶解于NaOH溶液中,且消耗NaOH 3 mol ③能水解生成两种酸 ④不能使溴水褪色 ⑤能发生酯化反应 ⑥有酸性
A.①②③ B.②③⑤ C.仅⑥ D.全部正确
课堂练习
D
7、同分异构体
(2)书写方法
(1)同分异构体
②碳链异构
①官能团异构(同碳原子数的酸和酯互为同分异构体)
③官能团位置异构
a、羧酸:取代法或插入法
b、酯:分配法或插入法
例1:(1) C3H6O2属于酸的同分异构有 种,C4H8O2属于酸的同分异构有 种, C5H10O2属于酸的同分异构有 种。
1
2
4
例2
(1)写出C3H6O2属于羧酸和酯的同分异构体.
(2)写出C4H8O2属于羧酸和酯的同分异构体。
CH3CH2
COOH
酸
酯
O
—C—O—
=
O
H-C-O-CH2CH3
=
O
CH3-C-O-CH3
=
C3H6O2共三种同分异构体,一种酸,两种酯。
左边为酸的部分,已含有一个碳
右边为醇的部分,最简单的是甲醇。
分子式除酯基还剩C2H6,可将碳依次分配到左右。
1.左边H—,右边—C2H5:
2.左边CH3—,右边—CH3:
思考:可以左边左边C2H5—,右边—H吗?
例2
(1)写出C3H6O2属于羧酸和酯的同分异构体.
(2)写出C4H8O2属于羧酸和酯的同分异构体。
CH3CH2CH2
COOH
酸
酯
O
—C—O—
=
O
H-C-O-CH2CH2CH3
=
O
CH3-C-O-CH2CH3
=
C3H6O2共六种同分异构体,两种酸,四种酯。
1.左边H—,右边—C3H7:
2.左边CH3—,右边—C2H5:
COOH
CH3CH—
CH3
O
H-C-O-CHCH3
CH3
=
3.左边C2H5—,右边—CH3:
O
CH3CH2-C-O-CH3
=
丙基有二种,所以酸有二种。
丙基有二种,所以酯有二种。
例3
写出C5H10O2属于羧酸和酯的同分异构体.
O
H-C-O-C4H9
=
O
CH3-C-O-C3H7
=
C4H9—
COOH
酸
酯
O
—C—O—
=
丁基有四种,所以酸有4种。
丁基有四种,所以酯有4种。
丙基有二种,所以酯有2种。
O
C2H5-C-O-C2H5
=
乙基只有一种,所以酯有1种。
O
C3H7-C-O-CH3
=
丙基有二种,所以酯有2种。
C5H10O2共13种同分异构体,四种酸,九种酯。
4、邻甲基苯甲酸( )有多种同分异构体,其中属于酯类,但分子结构中含有甲基和苯环的异构体有( )
A.2种 B.3种 C.4种 D.5种
课堂练习
D
C
5.由—CH3、—OH、 、—COOH四种基团两两组合而成的化合物中,其水溶液能使紫色石蕊试液变红的有( )
A.1种 B.2种 C.3种 D.4种
6.现有分子式为C3H6O2的四种有机物A、B、C、D,且分子内均含有甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
则A、B、C、D的结构简式分别为:
A: B:
C: D:
NaOH溶液
银氨溶液
新制Cu(OH)2
金属钠
A
中和反应
——
溶解
产生氢气
B
——
有银镜
产生红色沉淀
产生氢气
C
水解反应
有银镜
产生红色沉淀
——
D
水解反应
——
——
——
CH3CH2COOH
HCOOCH2CH3
CH3COOCH3
CH3CH(OH)CHO
课堂练习
7、某有机化合物X(C7H8O)与另一有机化合物Y发生如下反应
生成化合物Z(C11H14O2)。
(1)X是下列化合物之一,已知X不能与FeCl3溶液发生显色反应,则X是________(填标号字母)。
(2)Y的分子式是________,可能的结构简式是_____________________和__________________。
(3)Y有多种同分异构体,其中一种同分异构体E发生银镜反应后,其产物经氧化可得到F(C4H8O3)。F可发生如下反应:
该反应的类型是________,E的结构简式是________。
(4)若Y与E具有相同的碳链,则Z的结构简式为_____________。
课堂练习
D
C4H8O2
CH3CH2CH2COOH
CH3CHCOOH
CH3
取代反应
CH2CH2CH2CHO
OH
CH2OOCCH2CH2CH3
8、下图中A、B、C、D、E、F、G均为有机化合物。
(3)A的结构简式是___,1 mol A最多与_____mol NaOH溶液反应。
(4)符合下列3个条件的B的同分异构体的数目有______个。
①含有邻二取代苯环结构②与B有相同官能团③不与FeCl3溶液发生显色反应
根据上图回答问题:
(1)D、F的化学名称是________、________。
(2)写出反应②、 ④的化学方程式,并注明反应类型。
课堂练习
—CH2OH
—CH2COOH
CH2=CH2
CH3CH2OH
CH3COOH
CH3COOC2H5
—CH2OOCCH3
—CH2COOC2H5
乙醇
乙酸乙酯
2
4
—CH3
—CH2COOH
—CH2CH3
—COOH
9.请写出以水、空气、乙烯为原料制取乙酸乙酯的相关化学方程式:
CH2=CH2 + H2O CH3CH2OH
高温、高压
催化剂
CH3COOC2H5 +H2O
浓H2SO4
△
CH3COOH + C2H5OH
Cu或Ag
2CH3CHO +2H2O
2CH3CH2OH + O2
催化剂
△
2CH3COOH
2CH3CHO + O2
课堂练习
谢谢欣赏
