2021浙教版科学中考第一轮复习--理化生学科综合(三)【word,含答案】
文档属性
| 名称 | 2021浙教版科学中考第一轮复习--理化生学科综合(三)【word,含答案】 |  | |
| 格式 | doc | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-03-31 21:20:12 | ||
图片预览


文档简介
例1.科学是一门基于实验的学科,以下研究的实验中,方法或实验目的不合理的是( )
A.“串、并联电路电流特点”:换不同的定值电阻多次测量,为了减小实验误差
B.“影响酶的催化作用”:将每组控制在不同的温度中,为了研究温度对酶的作用
C.“通电导体周围是否存在磁场”:往往用小磁针来观察,运用了转换法
D.“揭示原子结构的奥秘”:不同时期模型的建立,运用了模型法
例2.自2019年1月1日起《杭州市公共场所控制吸烟条例》施行,为加强公共场所控烟管理提供了强有力的法制保障。学校的科学探索小队想通过探究被动吸烟对小白鼠活动行为的影响,来告诉同学们公共场所禁烟的好处。
(1)组员们通过查阅资料得知:一氧化碳是香烟中的主要有害成分之一,请写出一氧化碳在空气中燃烧的化学方程式____________________________;
(2)该小组共准备了56只小白鼠,进行了下列实验:①方法步骤
组别
第一组 第二组 第三组
1 2 3 4 5 6 7 8 9
小白鼠数量 6 6 6 6 6 6 6 6 6
实验条件 每次点燃2支烟,每小时1次,每天10次 每次点燃4支烟,每小时1次,每天10次 不点烟
这样分组的目的是________________________(请写出两点);
②实验观察结果记录
每点燃一次烟,观察小白鼠5-10分钟,记录在_____________环境下,他们的活动行为:
组别 第一组 第二组 第三组
上午不点烟嗜睡的小白鼠数 10 16 无
点烟后12-16点活动加强的小白鼠数 18 18 无
不明原因死亡数 0 2 无
产仔后亲鼠咬死吃食幼鼠数 1 6 无
③实验分析:由以上的实验数据,可能得到的结论是_____________________。
例3.福建圣农集团为解决养殖过程中产生的大量鸡粪污染问题,发明利用鸡粪燃烧发电,某校科学兴趣小组的同学,根据所学的知识,用如图所示的装置,对“鸡粪发电”和“煤炭发电”的产热效率进行研究,测得的数据如表,请根据表中数据回答下列问题:
1克标准煤炭燃烧放出的能量(单位:焦) 1克干鸡粪燃烧放出的能量(单位:焦)
1 12843 4301
2 12390 4128
3 13860 4622
4 12582 4155
(1)以传统的处理方法:鸡粪(适量)能够作为天然的农家肥,从生态系统的成分看,鸡粪属于__________________;
(2)从能量转化的角度看,“鸡粪发电”是将鸡粪中的____________能转化成电能;
(3)你认为应该____________处理表中的数据,得出的结果才更可靠;
(4)1克标准煤炭完全燃烧放出的能量实际约为33600焦,与实验测得的各组数据相比较有较大差异,请解释原因______________________________________;
(5)实践生产中,每燃烧3吨鸡粪的热量相当于1吨标准煤,若燃烧产生的能量全部转化为电能,则每千克鸡粪的热值相当于_______________度电(小数点后保留一位)。
1.科学史上中国有很多科学发明,以下属于中国为世界现代物质文明做出重大贡献的发明的是( )
①造纸 ②元素周期律的发现 ③火药和中药学 ④指南针 ⑤湿法炼铜 ⑥陶瓷 ⑦第一台发电机⑧首次人工合成蛋白质(胰岛素)
A.①②③④⑥ B.①③⑤⑥⑦⑧
C.①③④⑤⑦⑧ D.①③④⑤⑥⑧
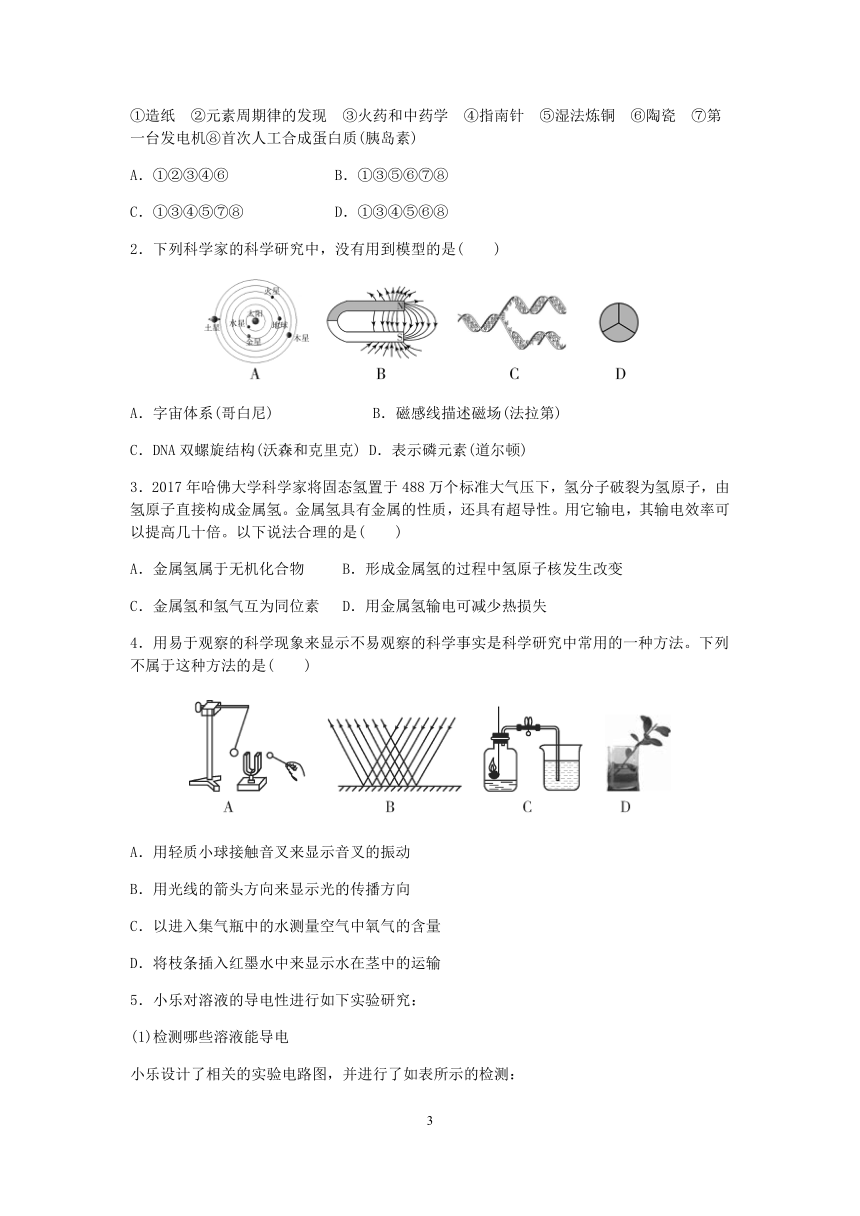
2.下列科学家的科学研究中,没有用到模型的是( )
A.字宙体系(哥白尼) B.磁感线描述磁场(法拉第)
C.DNA双螺旋结构(沃森和克里克) D.表示磷元素(道尔顿)
3.2017年哈佛大学科学家将固态氢置于488万个标准大气压下,氢分子破裂为氢原子,由氢原子直接构成金属氢。金属氢具有金属的性质,还具有超导性。用它输电,其输电效率可以提高几十倍。以下说法合理的是( )
A.金属氢属于无机化合物 B.形成金属氢的过程中氢原子核发生改变
C.金属氢和氢气互为同位素 D.用金属氢输电可减少热损失
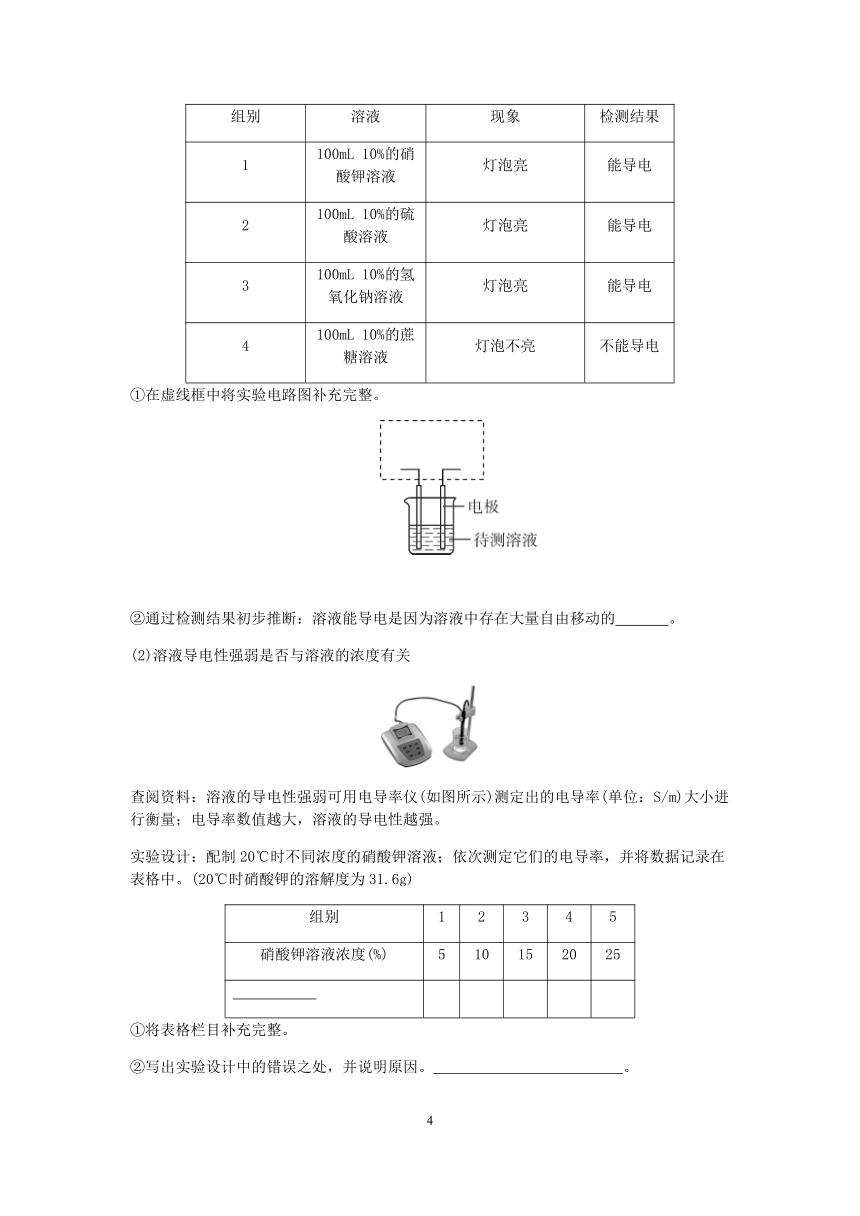
4.用易于观察的科学现象来显示不易观察的科学事实是科学研究中常用的一种方法。下列不属于这种方法的是( )
A.用轻质小球接触音叉来显示音叉的振动
B.用光线的箭头方向来显示光的传播方向
C.以进入集气瓶中的水测量空气中氧气的含量
D.将枝条插入红墨水中来显示水在茎中的运输
5.小乐对溶液的导电性进行如下实验研究:
(1)检测哪些溶液能导电
小乐设计了相关的实验电路图,并进行了如表所示的检测:
组别 溶液 现象 检测结果
1 100mL 10%的硝酸钾溶液 灯泡亮 能导电
2 100mL 10%的硫酸溶液 灯泡亮 能导电
3 100mL 10%的氢氧化钠溶液 灯泡亮 能导电
4 100mL 10%的蔗糖溶液 灯泡不亮 不能导电
①在虚线框中将实验电路图补充完整。
②通过检测结果初步推断:溶液能导电是因为溶液中存在大量自由移动的 。
(2)溶液导电性强弱是否与溶液的浓度有关
查阅资料:溶液的导电性强弱可用电导率仪(如图所示)测定出的电导率(单位:S/m)大小进行衡量;电导率数值越大,溶液的导电性越强。
实验设计:配制20℃时不同浓度的硝酸钾溶液;依次测定它们的电导率,并将数据记录在表格中。(20℃时硝酸钾的溶解度为31.6g)
组别 1 2 3 4 5
硝酸钾溶液浓度(%) 5 10 15 20 25
①将表格栏目补充完整。
②写出实验设计中的错误之处,并说明原因。 。
6.小徐为研究肝脏、胰腺对哺乳动物血液成分的影响,在8:00时同时切除某哺乳动物的肝脏和胰腺,并测量了7:00~20:00此动物血液中尿素和血糖浓度,测得实验结果如表所示。
当日时间 血液中尿素浓度(mg/100mL) 血液中葡萄糖浓度(mg/100mL)
7:00 7.0 90
8:00 7.0 90
11:00 6.0 97
14:00 4.6 112
17:00 3.2 127
20:00 2.7 138
请回答:
(1)8:00后,血糖浓度偏高的一种原因是 。
(2)通过口服胰岛素(一种蛋白质类的激素)来帮助降低血糖浓度是否合理?请说明理由 。
(3)11:00时,由尿素[CO(NH2)2]推知血液中氮元素的浓度是 mg/100mL。
(4)本实验能得出的一个结论是 __。
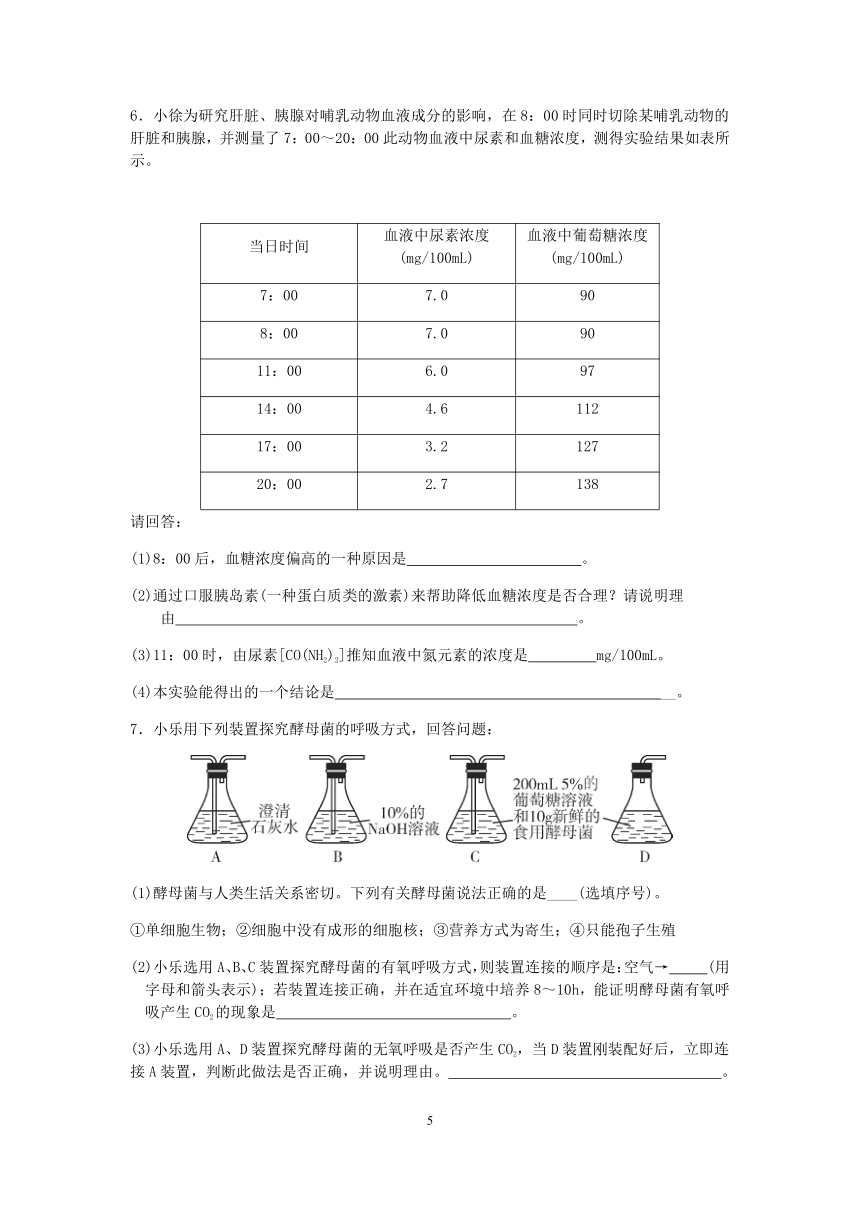
7.小乐用下列装置探究酵母菌的呼吸方式,回答问题:
(1)酵母菌与人类生活关系密切。下列有关酵母菌说法正确的是____(选填序号)。
①单细胞生物;②细胞中没有成形的细胞核;③营养方式为寄生;④只能孢子生殖
(2)小乐选用A、B、C装置探究酵母菌的有氧呼吸方式,则装置连接的顺序是:空气→ (用字母和箭头表示);若装置连接正确,并在适宜环境中培养8~10h,能证明酵母菌有氧呼吸产生CO2的现象是 。
(3)小乐选用A、D装置探究酵母菌的无氧呼吸是否产生CO2,当D装置刚装配好后,立即连接A装置,判断此做法是否正确,并说明理由。 。
8.“智能手环”是一种穿戴式智能设备,具有计步统计、能量消耗统计和心率监测等功能,业已成为许多运动人士的专属运动助理产品。
(1)如图甲所示,小乐在跑步时,以佩戴智能手环的手腕为参照物,智能手环是____(选填“运动”或“静止”)的。
(2)小乐跑步10min后,智能手环显示步数是1500步(一步距离约为1m),消耗能量是100千卡(1千卡=4200J),此时的心率为130次/min。
①若小乐跑步的平均作用力为40N,则她跑步时做功的功率大约是____W;
②假设跑步消耗的能量全部由糖类物质提供,则本次运动至少消耗了____g糖类物质(已知1g糖类物质在体内完全氧化释放的能量为16.8kJ);
③智能手环是根据手腕处桡动脉的跳动情况来测心率的,图乙中,a、b、c、d表示循环系统中心脏的四个腔,Ⅰ、Ⅱ、Ⅲ、Ⅳ表示与心脏相连的不同血管,则桡动脉与图中____(选填序号)血管直接相连。
(3)图丙所示为我国研发的“柔性、可裁剪碲化铋(Bi2Te3)/纤维素复合热点薄膜电池”,它能充分贴合人体体表,实现利用体表散热为智能手环供电。在碲化铋(Bi2Te3)中,碲元素的化合价为-2价,则铋元素的化合价为____价,此电池的能量转化是 。
9.运用“蓝鲸一号”钻探平台,我国南海实现可燃冰试采成功。
材料一:可燃冰,学名天然气水化合物,其化学式为CH4·8H2O。它是天然气的固体状态(因海底高压)。埋于海底地层深处的大量有机质在细菌的分解作用下,最后形成石油和天然气(石油气),其中许多天然气被包进水分子中,在海底的低温(2~5℃)与压力下结晶,形成“可燃冰”。
材料二:“蓝鲸一号”钻探平台设计和建造过程刷新了多项世界纪录,它长117米,宽92.7米,高118米,质量为42000吨。
请根据上述材料回答:
(1)形成可燃冰需要一定的生态环境。
①海底地层深处,这些分解有机质的细菌能很好的生存,体现了生物对环境的________。这些细菌分解有机质________(填“需要”或“不需要”)氧气,这些细菌与真菌在细胞结构上的主要区别是________?。
②在开采过程中,极少量的垃圾废弃物没有对海洋环境造成破环,这主要是因为海洋生态系统有 ________?的能力。
(2)形成可燃冰的其中一个条件是有甲烷气源。
①可燃冰(CH4·8H2O)中C:H:O的元素质量比是________,甲烷属于________(填“有机物”或“无机物”)。
②与石油、煤等化石燃料相比较,开采可燃冰的积极意义有________(写一条)。
(3)如果南海海水的密度是1.03×103千克/米3 , “蓝鲸一号”钻探平台漂浮海面受到海水浮力是 ________牛,开采出的可燃冰可以直接在管口广燃,说已经成为气体,从固体变成气体的原因可能是________?。
10.“道路千万条,安全第一条”。良好车况和遵规驾驶是确保驾乘人员安全的重要保障。
(1)车况良好的汽车有相应的安全系统确保驾乘人员安全。如图甲所示为汽车安全气囊,其内主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,产气药剂会产生大量气体使气囊迅速膨胀,从而起到保护作用。其中部分物质的作用及应用原理如下:①NaN3是气体发生剂,受热分解生成N2和Na;②KClO4是氧化剂,其中氯元素的化合价为____。③NaHCO3是冷却剂,它在受热分解生成Na2CO3、CO2和H2O时,____(选填“吸收”或“放出”)热量。如图乙所示为安全带,当紧急制动、碰撞或车辆行驶状态急剧变化时,系上安全带可有效防止驾乘人员由于____而造成伤害。
(2)遵规驾驶同样是确保驾乘人员安全的重要保障。“红灯停,绿灯行”,看到红灯变亮立即刹车,属于____(选填“非条件”或“条件”)反射;“开车不喝酒,喝酒不开车”,这是因为酒精会麻痹驾驶人员的____,常表现为思维混乱、反应迟钝、动作不协调等,难以安全驾驶汽车。
11.1928年9月,弗莱明在一次实验中把所有的细菌培养基一股脑堆在了实验室角落的长椅上,结果发现其中一个培养基不慎被青霉菌污染了,青霉菌周围一圈的葡萄球菌都被杀死了(如图)。就这样在一次偶然的实验中他发现了青霉素。
(1)根据弗莱明当时发现的这种现象,他提出了怎样的猜想 。
江干区某校开展探究青霉素作用的实验:将6.6g营养琼脂放在200mL蒸馏水中配制成固体培养基(营养琼脂),放入杀菌后的培养皿中,分别将0.96g青霉素放入5mL、20mL、80mL、320mL蒸馏水中配制成不同浓度的青霉素溶液,把几滴土壤细菌培养液均匀涂抹在营养琼脂上,将浸有不同浓度青霉素的圆纸片和浸在蒸馏水中的圆纸片(均为直径0.8cm的同种滤纸)放在琼脂表面,将培养皿放在30~32℃恒温箱(额定功率1kW)内24h,结果如图。分析并回答下列问题:
(2)为了配制一定浓度的青霉素溶液,需用到的玻璃仪器有 。
(3)实验需用到营养琼脂的原因是 。
(4)实验中为什么要有两片浸有蒸馏水的圆纸片 。
(5)青霉素的研制成功大大增强了人类抵抗细菌性感染的能力,带动了抗生素家族的诞生。但与此同时,部分病菌的抗药性也在逐渐增强,这种抗药性的产生就是长期 的结果。
(6)额定功率1kW恒温箱连续工作24h消耗的电能为 。
12.小徐在登山的过程中,注意到路边一处岩石有特殊的纹理,如图甲,此处的地面非常潮湿、植被低矮。
(1)小徐认为,形成图甲这样的地貌是地壳运动的结果,地壳运动主要的表现形式是 。
(2)小徐发现,这里有一种植物,有根、茎、叶,叶背面有一个个褐色的囊状结构,如图乙,该植物属于____类。
(3)通过进一步观察,小徐发现此处还生活着葫芦藓。它植株矮小,与(2)中植物在结构上最根本的区别是 。
(4)小徐还发现此处有地衣,我们实验室用到的石蕊试剂,就是取自这种生物。石蕊试剂可用于检验物质的 性,查阅资料,小徐知道石蕊的化学式为(C7H7O4N)n,则石蕊中碳元素和氧元素的质量比为____。
参考答案
例1.B
例2.(1)2CO+O2点 燃 2CO2;(2)①每组进行多次实验,减小实验偶然性;通过改变点燃烟的数量,比较被动吸烟对小白鼠行为影响;②条件适宜且相同;③点燃烟的支数越多(被动吸烟越多),对小白鼠行为影响越大。
例3.(1)非生物物质和能量;(2)化学;(3)去除第3组数据,求平均值;
(4)大量的光和热辐射在环境中散失或燃烧不充分;(5)3.1
1.D
2.D
3.D
4.B
5.(1)
②离子
(2)①电导率(S/m)
②第5组硝酸钾溶液的浓度设置错误,在20℃时硝酸钾溶液的最高浓度为24%__。
6.(1)切除胰腺后动物体内胰岛素分泌减少,不能正常降低血糖浓度。
(2)不合理,胰岛素是蛋白质,会被消化系统中的蛋白酶消化分解。
(3)2.8。
(4)切除肝脏和胰腺后,哺乳动物血液中尿素浓度会降低,葡萄糖浓度会上升。
7.(1)①。
(2)B→C→A A装置中的石灰水变浑浊。
(3)不正确,D装置刚装配好后,装置内存在一定量的氧气,可供酵母菌进行有氧呼吸;若此时立即连接A装置,对实验结果会产生干扰(合理即可)。
8.(1)静止。
(2)①100;
②25;
③Ⅰ。
(3)+3,内能转化为电能。
9.(1)适应;不需要; 细菌没有成形的细胞核 ; 自我修复 ;(2) 3:5:32 ; 有机物 ; 几乎不会对环境造成污染 ;(3) 4.116×108 ; 压强变小、温度升高
10.(1)+7 吸收 惯性。(2)条件 大脑和小脑。
11.(1)青霉菌对葡萄球菌的生长有影响。
(2)烧杯、玻璃棒、量筒、胶头滴管。
(3)为细菌的生长繁殖提供营养物质。
(4)形成对照,说明清水对细菌的生长不会产生影响。
(5)自然选择。
(6)8.64×107J(或24kW·h)。
12.(1)火山和地震。
(2)蕨。
(3)_葫芦藓没有根的分化。
(4)酸碱 21∶16。
A.“串、并联电路电流特点”:换不同的定值电阻多次测量,为了减小实验误差
B.“影响酶的催化作用”:将每组控制在不同的温度中,为了研究温度对酶的作用
C.“通电导体周围是否存在磁场”:往往用小磁针来观察,运用了转换法
D.“揭示原子结构的奥秘”:不同时期模型的建立,运用了模型法
例2.自2019年1月1日起《杭州市公共场所控制吸烟条例》施行,为加强公共场所控烟管理提供了强有力的法制保障。学校的科学探索小队想通过探究被动吸烟对小白鼠活动行为的影响,来告诉同学们公共场所禁烟的好处。
(1)组员们通过查阅资料得知:一氧化碳是香烟中的主要有害成分之一,请写出一氧化碳在空气中燃烧的化学方程式____________________________;
(2)该小组共准备了56只小白鼠,进行了下列实验:①方法步骤
组别
第一组 第二组 第三组
1 2 3 4 5 6 7 8 9
小白鼠数量 6 6 6 6 6 6 6 6 6
实验条件 每次点燃2支烟,每小时1次,每天10次 每次点燃4支烟,每小时1次,每天10次 不点烟
这样分组的目的是________________________(请写出两点);
②实验观察结果记录
每点燃一次烟,观察小白鼠5-10分钟,记录在_____________环境下,他们的活动行为:
组别 第一组 第二组 第三组
上午不点烟嗜睡的小白鼠数 10 16 无
点烟后12-16点活动加强的小白鼠数 18 18 无
不明原因死亡数 0 2 无
产仔后亲鼠咬死吃食幼鼠数 1 6 无
③实验分析:由以上的实验数据,可能得到的结论是_____________________。
例3.福建圣农集团为解决养殖过程中产生的大量鸡粪污染问题,发明利用鸡粪燃烧发电,某校科学兴趣小组的同学,根据所学的知识,用如图所示的装置,对“鸡粪发电”和“煤炭发电”的产热效率进行研究,测得的数据如表,请根据表中数据回答下列问题:
1克标准煤炭燃烧放出的能量(单位:焦) 1克干鸡粪燃烧放出的能量(单位:焦)
1 12843 4301
2 12390 4128
3 13860 4622
4 12582 4155
(1)以传统的处理方法:鸡粪(适量)能够作为天然的农家肥,从生态系统的成分看,鸡粪属于__________________;
(2)从能量转化的角度看,“鸡粪发电”是将鸡粪中的____________能转化成电能;
(3)你认为应该____________处理表中的数据,得出的结果才更可靠;
(4)1克标准煤炭完全燃烧放出的能量实际约为33600焦,与实验测得的各组数据相比较有较大差异,请解释原因______________________________________;
(5)实践生产中,每燃烧3吨鸡粪的热量相当于1吨标准煤,若燃烧产生的能量全部转化为电能,则每千克鸡粪的热值相当于_______________度电(小数点后保留一位)。
1.科学史上中国有很多科学发明,以下属于中国为世界现代物质文明做出重大贡献的发明的是( )
①造纸 ②元素周期律的发现 ③火药和中药学 ④指南针 ⑤湿法炼铜 ⑥陶瓷 ⑦第一台发电机⑧首次人工合成蛋白质(胰岛素)
A.①②③④⑥ B.①③⑤⑥⑦⑧
C.①③④⑤⑦⑧ D.①③④⑤⑥⑧
2.下列科学家的科学研究中,没有用到模型的是( )
A.字宙体系(哥白尼) B.磁感线描述磁场(法拉第)
C.DNA双螺旋结构(沃森和克里克) D.表示磷元素(道尔顿)
3.2017年哈佛大学科学家将固态氢置于488万个标准大气压下,氢分子破裂为氢原子,由氢原子直接构成金属氢。金属氢具有金属的性质,还具有超导性。用它输电,其输电效率可以提高几十倍。以下说法合理的是( )
A.金属氢属于无机化合物 B.形成金属氢的过程中氢原子核发生改变
C.金属氢和氢气互为同位素 D.用金属氢输电可减少热损失
4.用易于观察的科学现象来显示不易观察的科学事实是科学研究中常用的一种方法。下列不属于这种方法的是( )
A.用轻质小球接触音叉来显示音叉的振动
B.用光线的箭头方向来显示光的传播方向
C.以进入集气瓶中的水测量空气中氧气的含量
D.将枝条插入红墨水中来显示水在茎中的运输
5.小乐对溶液的导电性进行如下实验研究:
(1)检测哪些溶液能导电
小乐设计了相关的实验电路图,并进行了如表所示的检测:
组别 溶液 现象 检测结果
1 100mL 10%的硝酸钾溶液 灯泡亮 能导电
2 100mL 10%的硫酸溶液 灯泡亮 能导电
3 100mL 10%的氢氧化钠溶液 灯泡亮 能导电
4 100mL 10%的蔗糖溶液 灯泡不亮 不能导电
①在虚线框中将实验电路图补充完整。
②通过检测结果初步推断:溶液能导电是因为溶液中存在大量自由移动的 。
(2)溶液导电性强弱是否与溶液的浓度有关
查阅资料:溶液的导电性强弱可用电导率仪(如图所示)测定出的电导率(单位:S/m)大小进行衡量;电导率数值越大,溶液的导电性越强。
实验设计:配制20℃时不同浓度的硝酸钾溶液;依次测定它们的电导率,并将数据记录在表格中。(20℃时硝酸钾的溶解度为31.6g)
组别 1 2 3 4 5
硝酸钾溶液浓度(%) 5 10 15 20 25
①将表格栏目补充完整。
②写出实验设计中的错误之处,并说明原因。 。
6.小徐为研究肝脏、胰腺对哺乳动物血液成分的影响,在8:00时同时切除某哺乳动物的肝脏和胰腺,并测量了7:00~20:00此动物血液中尿素和血糖浓度,测得实验结果如表所示。
当日时间 血液中尿素浓度(mg/100mL) 血液中葡萄糖浓度(mg/100mL)
7:00 7.0 90
8:00 7.0 90
11:00 6.0 97
14:00 4.6 112
17:00 3.2 127
20:00 2.7 138
请回答:
(1)8:00后,血糖浓度偏高的一种原因是 。
(2)通过口服胰岛素(一种蛋白质类的激素)来帮助降低血糖浓度是否合理?请说明理由 。
(3)11:00时,由尿素[CO(NH2)2]推知血液中氮元素的浓度是 mg/100mL。
(4)本实验能得出的一个结论是 __。
7.小乐用下列装置探究酵母菌的呼吸方式,回答问题:
(1)酵母菌与人类生活关系密切。下列有关酵母菌说法正确的是____(选填序号)。
①单细胞生物;②细胞中没有成形的细胞核;③营养方式为寄生;④只能孢子生殖
(2)小乐选用A、B、C装置探究酵母菌的有氧呼吸方式,则装置连接的顺序是:空气→ (用字母和箭头表示);若装置连接正确,并在适宜环境中培养8~10h,能证明酵母菌有氧呼吸产生CO2的现象是 。
(3)小乐选用A、D装置探究酵母菌的无氧呼吸是否产生CO2,当D装置刚装配好后,立即连接A装置,判断此做法是否正确,并说明理由。 。
8.“智能手环”是一种穿戴式智能设备,具有计步统计、能量消耗统计和心率监测等功能,业已成为许多运动人士的专属运动助理产品。
(1)如图甲所示,小乐在跑步时,以佩戴智能手环的手腕为参照物,智能手环是____(选填“运动”或“静止”)的。
(2)小乐跑步10min后,智能手环显示步数是1500步(一步距离约为1m),消耗能量是100千卡(1千卡=4200J),此时的心率为130次/min。
①若小乐跑步的平均作用力为40N,则她跑步时做功的功率大约是____W;
②假设跑步消耗的能量全部由糖类物质提供,则本次运动至少消耗了____g糖类物质(已知1g糖类物质在体内完全氧化释放的能量为16.8kJ);
③智能手环是根据手腕处桡动脉的跳动情况来测心率的,图乙中,a、b、c、d表示循环系统中心脏的四个腔,Ⅰ、Ⅱ、Ⅲ、Ⅳ表示与心脏相连的不同血管,则桡动脉与图中____(选填序号)血管直接相连。
(3)图丙所示为我国研发的“柔性、可裁剪碲化铋(Bi2Te3)/纤维素复合热点薄膜电池”,它能充分贴合人体体表,实现利用体表散热为智能手环供电。在碲化铋(Bi2Te3)中,碲元素的化合价为-2价,则铋元素的化合价为____价,此电池的能量转化是 。
9.运用“蓝鲸一号”钻探平台,我国南海实现可燃冰试采成功。
材料一:可燃冰,学名天然气水化合物,其化学式为CH4·8H2O。它是天然气的固体状态(因海底高压)。埋于海底地层深处的大量有机质在细菌的分解作用下,最后形成石油和天然气(石油气),其中许多天然气被包进水分子中,在海底的低温(2~5℃)与压力下结晶,形成“可燃冰”。
材料二:“蓝鲸一号”钻探平台设计和建造过程刷新了多项世界纪录,它长117米,宽92.7米,高118米,质量为42000吨。
请根据上述材料回答:
(1)形成可燃冰需要一定的生态环境。
①海底地层深处,这些分解有机质的细菌能很好的生存,体现了生物对环境的________。这些细菌分解有机质________(填“需要”或“不需要”)氧气,这些细菌与真菌在细胞结构上的主要区别是________?。
②在开采过程中,极少量的垃圾废弃物没有对海洋环境造成破环,这主要是因为海洋生态系统有 ________?的能力。
(2)形成可燃冰的其中一个条件是有甲烷气源。
①可燃冰(CH4·8H2O)中C:H:O的元素质量比是________,甲烷属于________(填“有机物”或“无机物”)。
②与石油、煤等化石燃料相比较,开采可燃冰的积极意义有________(写一条)。
(3)如果南海海水的密度是1.03×103千克/米3 , “蓝鲸一号”钻探平台漂浮海面受到海水浮力是 ________牛,开采出的可燃冰可以直接在管口广燃,说已经成为气体,从固体变成气体的原因可能是________?。
10.“道路千万条,安全第一条”。良好车况和遵规驾驶是确保驾乘人员安全的重要保障。
(1)车况良好的汽车有相应的安全系统确保驾乘人员安全。如图甲所示为汽车安全气囊,其内主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,产气药剂会产生大量气体使气囊迅速膨胀,从而起到保护作用。其中部分物质的作用及应用原理如下:①NaN3是气体发生剂,受热分解生成N2和Na;②KClO4是氧化剂,其中氯元素的化合价为____。③NaHCO3是冷却剂,它在受热分解生成Na2CO3、CO2和H2O时,____(选填“吸收”或“放出”)热量。如图乙所示为安全带,当紧急制动、碰撞或车辆行驶状态急剧变化时,系上安全带可有效防止驾乘人员由于____而造成伤害。
(2)遵规驾驶同样是确保驾乘人员安全的重要保障。“红灯停,绿灯行”,看到红灯变亮立即刹车,属于____(选填“非条件”或“条件”)反射;“开车不喝酒,喝酒不开车”,这是因为酒精会麻痹驾驶人员的____,常表现为思维混乱、反应迟钝、动作不协调等,难以安全驾驶汽车。
11.1928年9月,弗莱明在一次实验中把所有的细菌培养基一股脑堆在了实验室角落的长椅上,结果发现其中一个培养基不慎被青霉菌污染了,青霉菌周围一圈的葡萄球菌都被杀死了(如图)。就这样在一次偶然的实验中他发现了青霉素。
(1)根据弗莱明当时发现的这种现象,他提出了怎样的猜想 。
江干区某校开展探究青霉素作用的实验:将6.6g营养琼脂放在200mL蒸馏水中配制成固体培养基(营养琼脂),放入杀菌后的培养皿中,分别将0.96g青霉素放入5mL、20mL、80mL、320mL蒸馏水中配制成不同浓度的青霉素溶液,把几滴土壤细菌培养液均匀涂抹在营养琼脂上,将浸有不同浓度青霉素的圆纸片和浸在蒸馏水中的圆纸片(均为直径0.8cm的同种滤纸)放在琼脂表面,将培养皿放在30~32℃恒温箱(额定功率1kW)内24h,结果如图。分析并回答下列问题:
(2)为了配制一定浓度的青霉素溶液,需用到的玻璃仪器有 。
(3)实验需用到营养琼脂的原因是 。
(4)实验中为什么要有两片浸有蒸馏水的圆纸片 。
(5)青霉素的研制成功大大增强了人类抵抗细菌性感染的能力,带动了抗生素家族的诞生。但与此同时,部分病菌的抗药性也在逐渐增强,这种抗药性的产生就是长期 的结果。
(6)额定功率1kW恒温箱连续工作24h消耗的电能为 。
12.小徐在登山的过程中,注意到路边一处岩石有特殊的纹理,如图甲,此处的地面非常潮湿、植被低矮。
(1)小徐认为,形成图甲这样的地貌是地壳运动的结果,地壳运动主要的表现形式是 。
(2)小徐发现,这里有一种植物,有根、茎、叶,叶背面有一个个褐色的囊状结构,如图乙,该植物属于____类。
(3)通过进一步观察,小徐发现此处还生活着葫芦藓。它植株矮小,与(2)中植物在结构上最根本的区别是 。
(4)小徐还发现此处有地衣,我们实验室用到的石蕊试剂,就是取自这种生物。石蕊试剂可用于检验物质的 性,查阅资料,小徐知道石蕊的化学式为(C7H7O4N)n,则石蕊中碳元素和氧元素的质量比为____。
参考答案
例1.B
例2.(1)2CO+O2点 燃 2CO2;(2)①每组进行多次实验,减小实验偶然性;通过改变点燃烟的数量,比较被动吸烟对小白鼠行为影响;②条件适宜且相同;③点燃烟的支数越多(被动吸烟越多),对小白鼠行为影响越大。
例3.(1)非生物物质和能量;(2)化学;(3)去除第3组数据,求平均值;
(4)大量的光和热辐射在环境中散失或燃烧不充分;(5)3.1
1.D
2.D
3.D
4.B
5.(1)
②离子
(2)①电导率(S/m)
②第5组硝酸钾溶液的浓度设置错误,在20℃时硝酸钾溶液的最高浓度为24%__。
6.(1)切除胰腺后动物体内胰岛素分泌减少,不能正常降低血糖浓度。
(2)不合理,胰岛素是蛋白质,会被消化系统中的蛋白酶消化分解。
(3)2.8。
(4)切除肝脏和胰腺后,哺乳动物血液中尿素浓度会降低,葡萄糖浓度会上升。
7.(1)①。
(2)B→C→A A装置中的石灰水变浑浊。
(3)不正确,D装置刚装配好后,装置内存在一定量的氧气,可供酵母菌进行有氧呼吸;若此时立即连接A装置,对实验结果会产生干扰(合理即可)。
8.(1)静止。
(2)①100;
②25;
③Ⅰ。
(3)+3,内能转化为电能。
9.(1)适应;不需要; 细菌没有成形的细胞核 ; 自我修复 ;(2) 3:5:32 ; 有机物 ; 几乎不会对环境造成污染 ;(3) 4.116×108 ; 压强变小、温度升高
10.(1)+7 吸收 惯性。(2)条件 大脑和小脑。
11.(1)青霉菌对葡萄球菌的生长有影响。
(2)烧杯、玻璃棒、量筒、胶头滴管。
(3)为细菌的生长繁殖提供营养物质。
(4)形成对照,说明清水对细菌的生长不会产生影响。
(5)自然选择。
(6)8.64×107J(或24kW·h)。
12.(1)火山和地震。
(2)蕨。
(3)_葫芦藓没有根的分化。
(4)酸碱 21∶16。
同课章节目录
