2020-2021学年人教版 九年级下册 第九单元 课题2 溶解度 练习(带解析答案)
文档属性
| 名称 | 2020-2021学年人教版 九年级下册 第九单元 课题2 溶解度 练习(带解析答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 143.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-01 00:00:00 | ||
图片预览


文档简介
溶解度练习
一、单选题
在一定温度下,某物质的饱和溶液一定是
A.
非常浓的溶液
B.
很稀的溶液
C.
增加该溶质,还能继续溶解的溶液
D.
增加该溶质,不能继续溶解的溶液
闻名中外的青岛啤酒内溶有一定量的气体,打开瓶盖时,你会发现啤酒会自动喷出来。喝了啤酒后又常常会打嗝,这说明气体在水中的溶解度与压强和温度有关。下列有关气体的溶解度说法正确是???
A.
压强减小,气体溶解度增大
B.
压强减小,气体溶解度减小
C.
温度升高,气体溶解度增大
D.
温度降低,气体溶解度减小
恒温条件下,盛放在敞口容器中的饱和食盐水久置后会有少量晶体析出,这是因为
A.
溶剂量减少
B.
溶质量减少
C.
溶液不稳定
D.
生成了新物质
从海水中提取食盐的流程如下,下列说法错误的是?
?
A.
经过第步操作,海水中的成分基本不变
B.
蒸发池中,氯化钠溶液逐渐变浓
C.
经过第步的操作,进入结晶池后,继续蒸发水,有氯化钠晶体析出
D.
析出食盐晶体后的母液是氯化钠的不饱和溶液
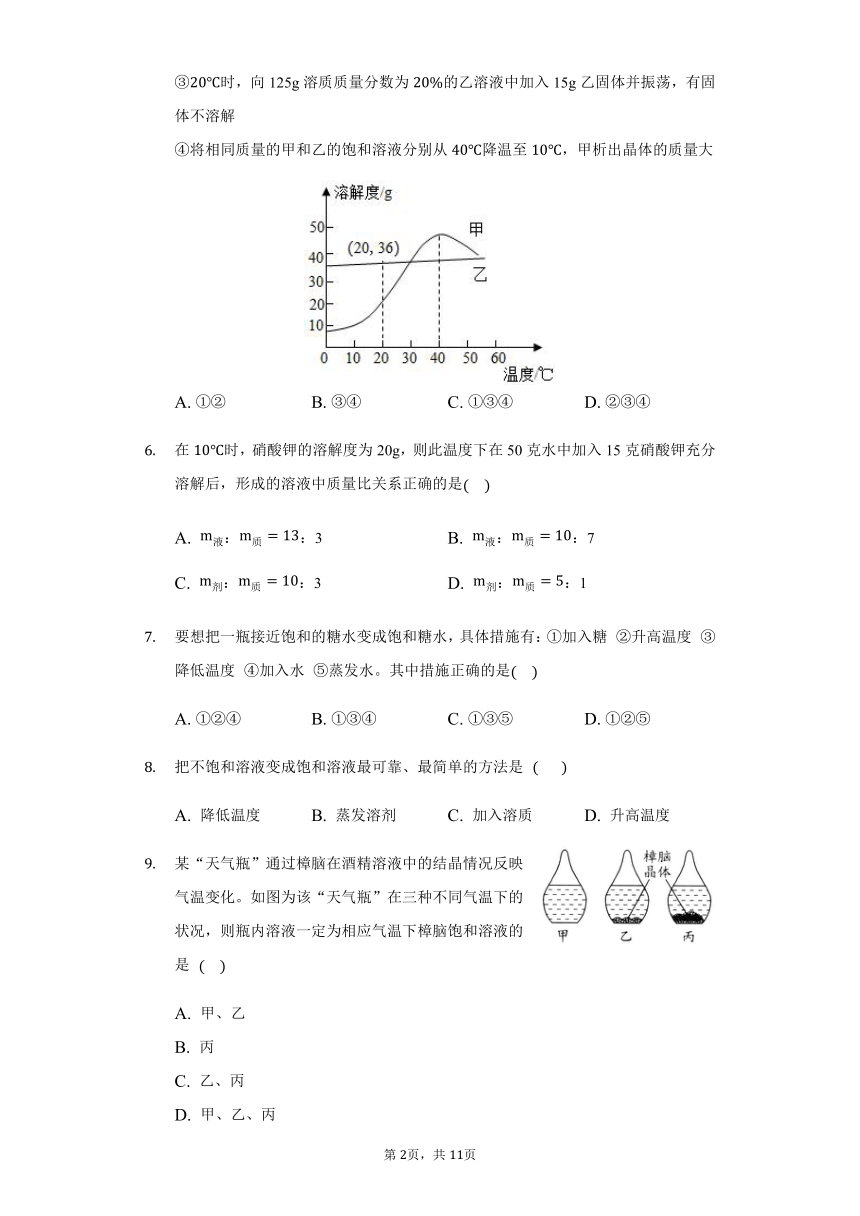
甲和乙两种物质的溶解度曲线如图所示。下列叙述正确的是
甲的溶解度随温度的升高而增大
时,使甲的饱和溶液析出晶体可用加热升温、冷却降温和蒸发溶剂三种方法
时,向125g溶质质量分数为的乙溶液中加入15g乙固体并振荡,有固体不溶解
将相同质量的甲和乙的饱和溶液分别从降温至,甲析出晶体的质量大
A.
B.
C.
D.
在时,硝酸钾的溶解度为20g,则此温度下在50克水中加入15克硝酸钾充分溶解后,形成的溶液中质量比关系正确的是
A.
::3
B.
::7
C.
::3
D.
::1
要想把一瓶接近饱和的糖水变成饱和糖水,具体措施有:加入糖
升高温度
降低温度
加入水
蒸发水。其中措施正确的是
A.
B.
C.
D.
把不饱和溶液变成饱和溶液最可靠、最简单的方法是
?
?
A.
降低温度
B.
蒸发溶剂
C.
加入溶质
D.
升高温度
某“天气瓶”通过樟脑在酒精溶液中的结晶情况反映气温变化。如图为该“天气瓶”在三种不同气温下的状况,则瓶内溶液一定为相应气温下樟脑饱和溶液的是
A.
甲、乙
B.
丙
C.
乙、丙
D.
甲、乙、丙
小明泡了一杯白糖开水,他用筷子充分搅拌杯中的白糖后,将杯子放在一边等待糖水变凉,喝糖水时,发现杯底有少量未溶解的白糖。下列操作或现象能说明糖水一定属于饱和溶液的是
?
?
A.
泡糖水时进行了充分搅拌
B.
糖水热的时候白糖全部溶解
C.
凉的糖水底部有剩余的白糖
D.
喝糖水时感到很甜
室温下,向一定质量的氯化钠溶液中加入氯化钠固体,充分搅拌后,尚有部分未溶解,加入水后,固体全部溶解。下列判断正确的是
?
?
A.
加水前一定是饱和溶液
B.
加水前可能是不饱和溶液
C.
加水后一定是饱和溶液
D.
加水后一定是不饱和溶液
某兴趣小组分别用加溶质和恒温蒸发溶剂的方法,将一定质量的硝酸钾不饱和溶液转化为饱和溶液。实验过程中,硝酸钾溶解度的变化情况分别是
A.
变大?
不变
B.
变大变小
C.
不变变大
D.
不变不变
将的硝酸钠饱和溶液降温到,有晶体析出晶体中不含水,下列各量没有发生变化的是
A.
溶液的质量
B.
溶质的质量
C.
溶剂的质量
D.
溶液的浓度
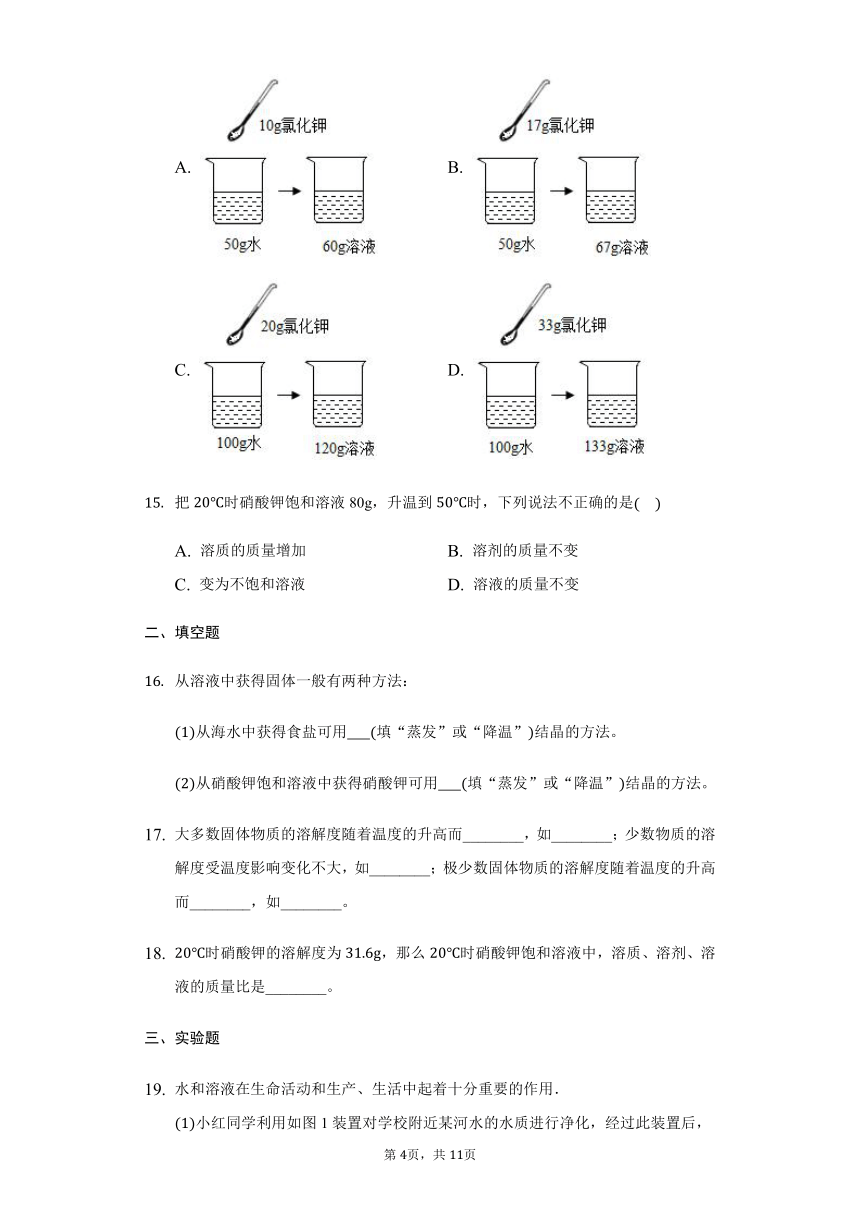
时氯化钾的溶解度为34g。下列是四位同学在时配制的氯化钾溶液,其中一定达到饱和的是
A.
B.
C.
D.
把时硝酸钾饱和溶液80g,升温到时,下列说法不正确的是
A.
溶质的质量增加
B.
溶剂的质量不变
C.
变为不饱和溶液
D.
溶液的质量不变
二、填空题
从溶液中获得固体一般有两种方法:
从海水中获得食盐可用??????填“蒸发”或“降温”结晶的方法。
从硝酸钾饱和溶液中获得硝酸钾可用??????填“蒸发”或“降温”结晶的方法。
大多数固体物质的溶解度随着温度的升高而________,如________;少数物质的溶解度受温度影响变化不大,如________;极少数固体物质的溶解度随着温度的升高而________,如________。
时硝酸钾的溶解度为,那么时硝酸钾饱和溶液中,溶质、溶剂、溶液的质量比是________。
三、实验题
水和溶液在生命活动和生产、生活中起着十分重要的作用.
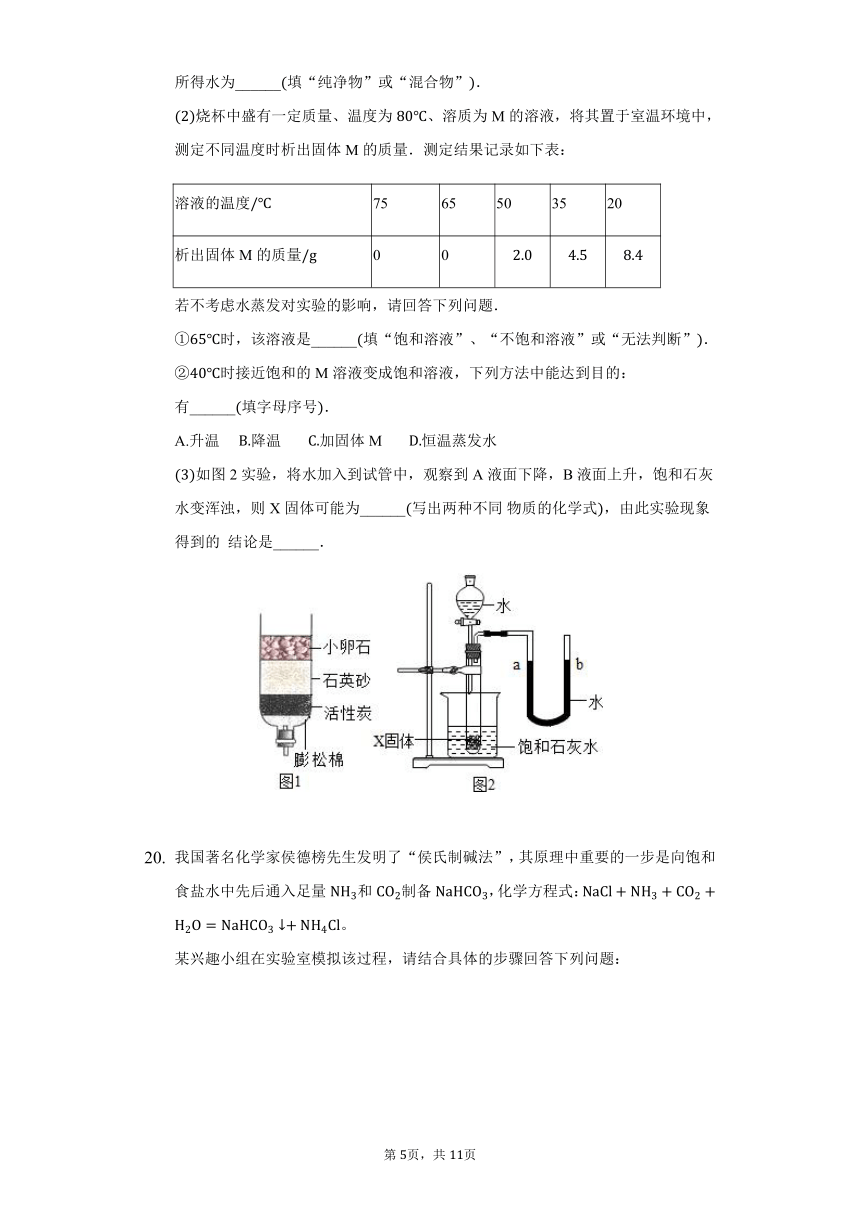
小红同学利用如图1装置对学校附近某河水的水质进行净化,经过此装置后,所得水为______填“纯净物”或“混合物”.
烧杯中盛有一定质量、温度为、溶质为M的溶液,将其置于室温环境中,测定不同温度时析出固体M的质量.测定结果记录如下表:
溶液的温度
75
65
50
35
20
析出固体M的质量
0
0
若不考虑水蒸发对实验的影响,请回答下列问题.
时,该溶液是______填“饱和溶液”、“不饱和溶液”或“无法判断”.
时接近饱和的M溶液变成饱和溶液,下列方法中能达到目的:
有______填字母序号.
A.升温?????降温???????加固体M???????恒温蒸发水
如图2实验,将水加入到试管中,观察到A液面下降,B液面上升,饱和石灰水变浑浊,则X固体可能为______写出两种不同?物质的化学式,由此实验现象得到的??结论是______.
我国著名化学家侯德榜先生发明了“侯氏制碱法”,其原理中重要的一步是向饱和食盐水中先后通入足量和制备,化学方程式:。
某兴趣小组在实验室模拟该过程,请结合具体的步骤回答下列问题:
I.气体制备
二氧化碳气体制备
实验室常采用石灰石与稀盐酸反应制备,其化学方程式为______。应选择的气体收集装置为______选填装置对应的字母。
氨气制备
实验室常用硫酸吸收氨气,防止污染空气,实验室制备的反应原理为:固固现要制备并干燥,所选装置的正确连接顺序为____________选择装置对应的字母。实验室制备也可用上述制备的发生装置,写出用该发生装置制备的化学方程式______。
制备
物质
溶解度
根据表格中的溶解度数据,解释产物中能够先从溶液中结晶析出的原因______。
该过程中另一产物在农业生产中常被用作______。
答案和解析
1.【答案】D
【解析】解:A、在一定温度下,某物质的饱和溶液不一定是非常浓的溶液,也可能为稀溶液,如氢氧化钙的饱和溶液,故选项说法错误。
B、浓稀溶液是溶液中所含溶质质量分数的大小,溶液是否饱和与溶液的浓稀没有必然联系,在一定温度下,某物质的饱和溶液不一定是很稀的溶液,故选项说法错误。
C、在一定温度下,增加该溶质,还能继续溶解的溶液,为该溶质的不饱和溶液,故选项错误。
D、在一定温度下,增加该溶质,不能继续溶解的溶液,为该溶质的饱和溶液,故选项正确。
2.【答案】B
【解答】
气体的溶解度随温度升高而降低,随压强升高而升高。
A.压强减小,气体溶解度会减小,故此选项错误。
B.压强越小,气体溶解度变小,故此选项正确。
C.温度升高,气体溶解度减小,故此选项错误。
D.温度降低,气体溶解度增大,故此选项错误。
3.【答案】A
【解答】
由于析出晶体需通过温度改变或减少溶剂两种方式的一种,由于是恒温状态下完成,故温度不变,析出晶体只能通过减小溶剂的方式完成,由题干知因是敞口水分会不断蒸发减小。
4.【答案】D
【解析】A.第步操作是将海水引入贮水池,经过第步操作,海水中的成分基本不变,故A说法正确;
B.蒸发池中,水分蒸发,氯化钠溶液逐渐变浓,故B说法正确;
C.经过第步的操作,进入结晶池后,继续蒸发水,溶液达到饱和状态后,继续蒸发,有氯化钠晶体析出,故C说法正确;
D.析出食盐晶体后的母液不能继续溶解氯化钠,是氯化钠的饱和溶液,故D说法错误;
故选D。
5.【答案】D
【解答】
通过分析溶解度曲线可知,小于时,甲的溶解度随温度的升高而增大,故错误;
小于时或大于时,甲物质的溶解度随温度的降低、升高时,溶解度都会减少,所以时,使甲的饱和溶液析出晶体可用加热升温、冷却降温和蒸发溶剂三种方法,故正确;
时,乙物质的溶解度是36g,向125g溶质质量分数为的乙溶液中含有溶质质量为:,加入15g乙固体并振荡,有固体不溶解,故正确;
将相同质量的甲和乙的饱和溶液分别从降温至,甲物质的溶解度变化最大,所以甲析出晶体的质量大,故正确。
故选:D。
6.【答案】D
【解答】
时,的溶解度为20g,则时50g水最多溶解溶质10g,所得溶液质量为60g;
A、:::1,错;
B、:::1,错;
C、:::1,错;
D、:::1,正确。
故选:D。
7.【答案】C
【解答】
向接近饱和的溶液中增加溶质或蒸发溶剂都可以使溶液变成饱和溶液,故把一瓶接近饱和的糖水变成饱和糖水,可以采取:加入糖、蒸发水的方法;?由于糖的溶解度随温度升高而增大,降低温度后糖的溶解度变小,故把一瓶接近饱和的糖水变成饱和,还可以采取降低温度的方法,符合题意,选项C正确。
故选C。
8.【答案】C
9.【答案】C
10.【答案】C
11.【答案】A
12.【答案】D
【解答】
由题意可知,某兴趣小组分别用加溶质和恒温蒸发溶剂的方法,将一定质量的硝酸钾不饱和溶液转化为饱和溶液。由于溶解度只随温度变化而变化,该兴趣小组实验过程中没有改变温度,故溶解度不会发生改变。
13.【答案】C
【解答】
将的硝酸钠饱和溶液降温到,有晶体析出晶体中不含水,溶质的质量减少,溶剂的质量不变,则溶液的质量减少。
14.【答案】B
【解答】
A、时氯化钾的溶解度为34g,含义是时,100g水中最多能溶解氯化钾34g,溶液达到饱和状态,则时,50g水中最多能溶解氯化钾17g,溶液达到饱和状态,向50g水中加入10g氯化钾,所得溶液是不饱和溶液,故选项错误。
B、向50g水中加入17g氯化钾,所得溶液恰好是饱和溶液,故选项正确。
C、时,100g水中最多能溶解氯化钾34g,时,向100g水中加入20g氯化钾,所得溶液是不饱和溶液,故选项错误。
D、时,向100g水中加入33g氯化钾,所得溶液是不饱和溶液,故选项错误。
15.【答案】A
【解答】
由于硝酸钾溶解度随着温度升高而增大,所以把时硝酸钾饱和溶液80g,升温到时,溶液变为不饱和溶液,溶液中溶质质量、溶剂质量都不变,溶液质量也不变,故A符合题意。
16.【答案】蒸发
?降温
17.【答案】升高;硝酸钾;氯化钠;降低;氢氧化钙
【解答】
大多数固体物质的溶解度随着温度的升高而升高,如硝酸钾;少数物质的溶解度受温度影响变化不大,如氯化钠;极少数固体物质的溶解度随着温度的升高而降低,如氢氧化钙。
18.【答案】
【解答】
时硝酸钾的溶解度为,那么时硝酸钾饱和溶液中,溶质质量为、溶剂质量为100g、溶液的质量为,其质量比是。
19.【答案】混合物
?
无法判断
?
BCD
?
NaOH和CaO
?
X固体遇水放热;氢氧化钙溶解度随温度升高而降低
【解析】解:将浑浊的河水通过简易净水器进行净化,其中活性炭的作用是吸附水中的色素和异味,用此装置净化后得到的水中仍然含有一些溶于水的物质,属于混合物.故填:混合物;
饱和溶液比较明确的表象是溶质与溶液共存,温度降到时无晶体析出,因此无法判断溶液是否饱和;
不饱和溶液变成饱和溶液通常可采用蒸发溶剂、加入溶质的方法完成,观察图表可知:M的溶解度随温度降低而减小,故也可采用降温的方法使其变为饱和溶液;
故答案为:无法判断;BCD;
观察到A液面下降,B液面上升,饱和石灰水变浑浊,说明试管内的气压增大,溶液的温度升高,因此加入的物质应该是溶于水的放热变化,使瓶内压强大于大气压,a端液面会下降,氢氧化钙的饱和溶液随着温度的升高溶解度变小,故符合条件的可以是氧化钙、氢氧化钠固体;由此实验现象得到的??结论是:X固体遇水放热;氢氧化钙溶解度随温度升高而降低;
20.【答案】;C;
;F;;
时碳酸氢钠的溶解度小于氯化铵的溶解度;
氮肥。
【解析】解:实验室常采用石灰石与稀盐酸反应制备,石灰石中的碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳,其化学方程式为:;
因为二氧化碳密度比空气大,可以用向上排空气法收集,即可以用C装置收集。
故填:;C。
实验室利用氢氧化钙和氯化铵制取氨气,是固固加热型,应该用B装置作为发生装置;
因为碱石灰中的氧化钙和氢氧化钠都不能和氨气反应,并且能够吸收水蒸气,因此可以用F装置对氨气进行干燥;
实验室制备用上述制备的发生装置时,应该是利用氯酸钾和二氧化锰制取,氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,反应的化学方程式为:。
故填:B;F;。
产物中能够先从溶液中结晶析出的原因是时碳酸氢钠的溶解度小于氯化铵的溶解度。
故填:时碳酸氢钠的溶解度小于氯化铵的溶解度。
该过程中另一产物在农业生产中常被用作氮肥。
故填:氮肥。
第2页,共2页
第1页,共1页
一、单选题
在一定温度下,某物质的饱和溶液一定是
A.
非常浓的溶液
B.
很稀的溶液
C.
增加该溶质,还能继续溶解的溶液
D.
增加该溶质,不能继续溶解的溶液
闻名中外的青岛啤酒内溶有一定量的气体,打开瓶盖时,你会发现啤酒会自动喷出来。喝了啤酒后又常常会打嗝,这说明气体在水中的溶解度与压强和温度有关。下列有关气体的溶解度说法正确是???
A.
压强减小,气体溶解度增大
B.
压强减小,气体溶解度减小
C.
温度升高,气体溶解度增大
D.
温度降低,气体溶解度减小
恒温条件下,盛放在敞口容器中的饱和食盐水久置后会有少量晶体析出,这是因为
A.
溶剂量减少
B.
溶质量减少
C.
溶液不稳定
D.
生成了新物质
从海水中提取食盐的流程如下,下列说法错误的是?
?
A.
经过第步操作,海水中的成分基本不变
B.
蒸发池中,氯化钠溶液逐渐变浓
C.
经过第步的操作,进入结晶池后,继续蒸发水,有氯化钠晶体析出
D.
析出食盐晶体后的母液是氯化钠的不饱和溶液
甲和乙两种物质的溶解度曲线如图所示。下列叙述正确的是
甲的溶解度随温度的升高而增大
时,使甲的饱和溶液析出晶体可用加热升温、冷却降温和蒸发溶剂三种方法
时,向125g溶质质量分数为的乙溶液中加入15g乙固体并振荡,有固体不溶解
将相同质量的甲和乙的饱和溶液分别从降温至,甲析出晶体的质量大
A.
B.
C.
D.
在时,硝酸钾的溶解度为20g,则此温度下在50克水中加入15克硝酸钾充分溶解后,形成的溶液中质量比关系正确的是
A.
::3
B.
::7
C.
::3
D.
::1
要想把一瓶接近饱和的糖水变成饱和糖水,具体措施有:加入糖
升高温度
降低温度
加入水
蒸发水。其中措施正确的是
A.
B.
C.
D.
把不饱和溶液变成饱和溶液最可靠、最简单的方法是
?
?
A.
降低温度
B.
蒸发溶剂
C.
加入溶质
D.
升高温度
某“天气瓶”通过樟脑在酒精溶液中的结晶情况反映气温变化。如图为该“天气瓶”在三种不同气温下的状况,则瓶内溶液一定为相应气温下樟脑饱和溶液的是
A.
甲、乙
B.
丙
C.
乙、丙
D.
甲、乙、丙
小明泡了一杯白糖开水,他用筷子充分搅拌杯中的白糖后,将杯子放在一边等待糖水变凉,喝糖水时,发现杯底有少量未溶解的白糖。下列操作或现象能说明糖水一定属于饱和溶液的是
?
?
A.
泡糖水时进行了充分搅拌
B.
糖水热的时候白糖全部溶解
C.
凉的糖水底部有剩余的白糖
D.
喝糖水时感到很甜
室温下,向一定质量的氯化钠溶液中加入氯化钠固体,充分搅拌后,尚有部分未溶解,加入水后,固体全部溶解。下列判断正确的是
?
?
A.
加水前一定是饱和溶液
B.
加水前可能是不饱和溶液
C.
加水后一定是饱和溶液
D.
加水后一定是不饱和溶液
某兴趣小组分别用加溶质和恒温蒸发溶剂的方法,将一定质量的硝酸钾不饱和溶液转化为饱和溶液。实验过程中,硝酸钾溶解度的变化情况分别是
A.
变大?
不变
B.
变大变小
C.
不变变大
D.
不变不变
将的硝酸钠饱和溶液降温到,有晶体析出晶体中不含水,下列各量没有发生变化的是
A.
溶液的质量
B.
溶质的质量
C.
溶剂的质量
D.
溶液的浓度
时氯化钾的溶解度为34g。下列是四位同学在时配制的氯化钾溶液,其中一定达到饱和的是
A.
B.
C.
D.
把时硝酸钾饱和溶液80g,升温到时,下列说法不正确的是
A.
溶质的质量增加
B.
溶剂的质量不变
C.
变为不饱和溶液
D.
溶液的质量不变
二、填空题
从溶液中获得固体一般有两种方法:
从海水中获得食盐可用??????填“蒸发”或“降温”结晶的方法。
从硝酸钾饱和溶液中获得硝酸钾可用??????填“蒸发”或“降温”结晶的方法。
大多数固体物质的溶解度随着温度的升高而________,如________;少数物质的溶解度受温度影响变化不大,如________;极少数固体物质的溶解度随着温度的升高而________,如________。
时硝酸钾的溶解度为,那么时硝酸钾饱和溶液中,溶质、溶剂、溶液的质量比是________。
三、实验题
水和溶液在生命活动和生产、生活中起着十分重要的作用.
小红同学利用如图1装置对学校附近某河水的水质进行净化,经过此装置后,所得水为______填“纯净物”或“混合物”.
烧杯中盛有一定质量、温度为、溶质为M的溶液,将其置于室温环境中,测定不同温度时析出固体M的质量.测定结果记录如下表:
溶液的温度
75
65
50
35
20
析出固体M的质量
0
0
若不考虑水蒸发对实验的影响,请回答下列问题.
时,该溶液是______填“饱和溶液”、“不饱和溶液”或“无法判断”.
时接近饱和的M溶液变成饱和溶液,下列方法中能达到目的:
有______填字母序号.
A.升温?????降温???????加固体M???????恒温蒸发水
如图2实验,将水加入到试管中,观察到A液面下降,B液面上升,饱和石灰水变浑浊,则X固体可能为______写出两种不同?物质的化学式,由此实验现象得到的??结论是______.
我国著名化学家侯德榜先生发明了“侯氏制碱法”,其原理中重要的一步是向饱和食盐水中先后通入足量和制备,化学方程式:。
某兴趣小组在实验室模拟该过程,请结合具体的步骤回答下列问题:
I.气体制备
二氧化碳气体制备
实验室常采用石灰石与稀盐酸反应制备,其化学方程式为______。应选择的气体收集装置为______选填装置对应的字母。
氨气制备
实验室常用硫酸吸收氨气,防止污染空气,实验室制备的反应原理为:固固现要制备并干燥,所选装置的正确连接顺序为____________选择装置对应的字母。实验室制备也可用上述制备的发生装置,写出用该发生装置制备的化学方程式______。
制备
物质
溶解度
根据表格中的溶解度数据,解释产物中能够先从溶液中结晶析出的原因______。
该过程中另一产物在农业生产中常被用作______。
答案和解析
1.【答案】D
【解析】解:A、在一定温度下,某物质的饱和溶液不一定是非常浓的溶液,也可能为稀溶液,如氢氧化钙的饱和溶液,故选项说法错误。
B、浓稀溶液是溶液中所含溶质质量分数的大小,溶液是否饱和与溶液的浓稀没有必然联系,在一定温度下,某物质的饱和溶液不一定是很稀的溶液,故选项说法错误。
C、在一定温度下,增加该溶质,还能继续溶解的溶液,为该溶质的不饱和溶液,故选项错误。
D、在一定温度下,增加该溶质,不能继续溶解的溶液,为该溶质的饱和溶液,故选项正确。
2.【答案】B
【解答】
气体的溶解度随温度升高而降低,随压强升高而升高。
A.压强减小,气体溶解度会减小,故此选项错误。
B.压强越小,气体溶解度变小,故此选项正确。
C.温度升高,气体溶解度减小,故此选项错误。
D.温度降低,气体溶解度增大,故此选项错误。
3.【答案】A
【解答】
由于析出晶体需通过温度改变或减少溶剂两种方式的一种,由于是恒温状态下完成,故温度不变,析出晶体只能通过减小溶剂的方式完成,由题干知因是敞口水分会不断蒸发减小。
4.【答案】D
【解析】A.第步操作是将海水引入贮水池,经过第步操作,海水中的成分基本不变,故A说法正确;
B.蒸发池中,水分蒸发,氯化钠溶液逐渐变浓,故B说法正确;
C.经过第步的操作,进入结晶池后,继续蒸发水,溶液达到饱和状态后,继续蒸发,有氯化钠晶体析出,故C说法正确;
D.析出食盐晶体后的母液不能继续溶解氯化钠,是氯化钠的饱和溶液,故D说法错误;
故选D。
5.【答案】D
【解答】
通过分析溶解度曲线可知,小于时,甲的溶解度随温度的升高而增大,故错误;
小于时或大于时,甲物质的溶解度随温度的降低、升高时,溶解度都会减少,所以时,使甲的饱和溶液析出晶体可用加热升温、冷却降温和蒸发溶剂三种方法,故正确;
时,乙物质的溶解度是36g,向125g溶质质量分数为的乙溶液中含有溶质质量为:,加入15g乙固体并振荡,有固体不溶解,故正确;
将相同质量的甲和乙的饱和溶液分别从降温至,甲物质的溶解度变化最大,所以甲析出晶体的质量大,故正确。
故选:D。
6.【答案】D
【解答】
时,的溶解度为20g,则时50g水最多溶解溶质10g,所得溶液质量为60g;
A、:::1,错;
B、:::1,错;
C、:::1,错;
D、:::1,正确。
故选:D。
7.【答案】C
【解答】
向接近饱和的溶液中增加溶质或蒸发溶剂都可以使溶液变成饱和溶液,故把一瓶接近饱和的糖水变成饱和糖水,可以采取:加入糖、蒸发水的方法;?由于糖的溶解度随温度升高而增大,降低温度后糖的溶解度变小,故把一瓶接近饱和的糖水变成饱和,还可以采取降低温度的方法,符合题意,选项C正确。
故选C。
8.【答案】C
9.【答案】C
10.【答案】C
11.【答案】A
12.【答案】D
【解答】
由题意可知,某兴趣小组分别用加溶质和恒温蒸发溶剂的方法,将一定质量的硝酸钾不饱和溶液转化为饱和溶液。由于溶解度只随温度变化而变化,该兴趣小组实验过程中没有改变温度,故溶解度不会发生改变。
13.【答案】C
【解答】
将的硝酸钠饱和溶液降温到,有晶体析出晶体中不含水,溶质的质量减少,溶剂的质量不变,则溶液的质量减少。
14.【答案】B
【解答】
A、时氯化钾的溶解度为34g,含义是时,100g水中最多能溶解氯化钾34g,溶液达到饱和状态,则时,50g水中最多能溶解氯化钾17g,溶液达到饱和状态,向50g水中加入10g氯化钾,所得溶液是不饱和溶液,故选项错误。
B、向50g水中加入17g氯化钾,所得溶液恰好是饱和溶液,故选项正确。
C、时,100g水中最多能溶解氯化钾34g,时,向100g水中加入20g氯化钾,所得溶液是不饱和溶液,故选项错误。
D、时,向100g水中加入33g氯化钾,所得溶液是不饱和溶液,故选项错误。
15.【答案】A
【解答】
由于硝酸钾溶解度随着温度升高而增大,所以把时硝酸钾饱和溶液80g,升温到时,溶液变为不饱和溶液,溶液中溶质质量、溶剂质量都不变,溶液质量也不变,故A符合题意。
16.【答案】蒸发
?降温
17.【答案】升高;硝酸钾;氯化钠;降低;氢氧化钙
【解答】
大多数固体物质的溶解度随着温度的升高而升高,如硝酸钾;少数物质的溶解度受温度影响变化不大,如氯化钠;极少数固体物质的溶解度随着温度的升高而降低,如氢氧化钙。
18.【答案】
【解答】
时硝酸钾的溶解度为,那么时硝酸钾饱和溶液中,溶质质量为、溶剂质量为100g、溶液的质量为,其质量比是。
19.【答案】混合物
?
无法判断
?
BCD
?
NaOH和CaO
?
X固体遇水放热;氢氧化钙溶解度随温度升高而降低
【解析】解:将浑浊的河水通过简易净水器进行净化,其中活性炭的作用是吸附水中的色素和异味,用此装置净化后得到的水中仍然含有一些溶于水的物质,属于混合物.故填:混合物;
饱和溶液比较明确的表象是溶质与溶液共存,温度降到时无晶体析出,因此无法判断溶液是否饱和;
不饱和溶液变成饱和溶液通常可采用蒸发溶剂、加入溶质的方法完成,观察图表可知:M的溶解度随温度降低而减小,故也可采用降温的方法使其变为饱和溶液;
故答案为:无法判断;BCD;
观察到A液面下降,B液面上升,饱和石灰水变浑浊,说明试管内的气压增大,溶液的温度升高,因此加入的物质应该是溶于水的放热变化,使瓶内压强大于大气压,a端液面会下降,氢氧化钙的饱和溶液随着温度的升高溶解度变小,故符合条件的可以是氧化钙、氢氧化钠固体;由此实验现象得到的??结论是:X固体遇水放热;氢氧化钙溶解度随温度升高而降低;
20.【答案】;C;
;F;;
时碳酸氢钠的溶解度小于氯化铵的溶解度;
氮肥。
【解析】解:实验室常采用石灰石与稀盐酸反应制备,石灰石中的碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳,其化学方程式为:;
因为二氧化碳密度比空气大,可以用向上排空气法收集,即可以用C装置收集。
故填:;C。
实验室利用氢氧化钙和氯化铵制取氨气,是固固加热型,应该用B装置作为发生装置;
因为碱石灰中的氧化钙和氢氧化钠都不能和氨气反应,并且能够吸收水蒸气,因此可以用F装置对氨气进行干燥;
实验室制备用上述制备的发生装置时,应该是利用氯酸钾和二氧化锰制取,氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,反应的化学方程式为:。
故填:B;F;。
产物中能够先从溶液中结晶析出的原因是时碳酸氢钠的溶解度小于氯化铵的溶解度。
故填:时碳酸氢钠的溶解度小于氯化铵的溶解度。
该过程中另一产物在农业生产中常被用作氮肥。
故填:氮肥。
第2页,共2页
第1页,共1页
同课章节目录
