2021届高中化学考前三个月专项复习课件(44张ppt) 命题区间九 角度二 实验装置图的辨识
文档属性
| 名称 | 2021届高中化学考前三个月专项复习课件(44张ppt) 命题区间九 角度二 实验装置图的辨识 |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-03 00:00:00 | ||
图片预览

文档简介
实验装置图的辨识
角度二
规范示意图再现
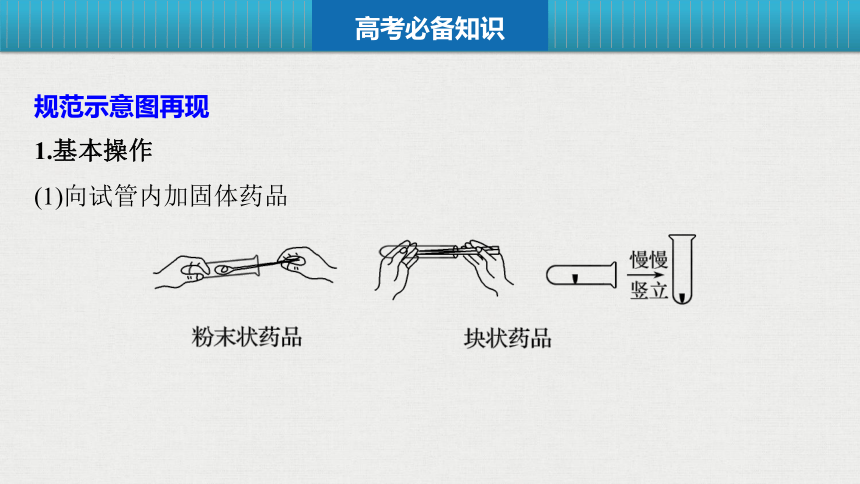
1.基本操作
(1)向试管内加固体药品
高考必备知识
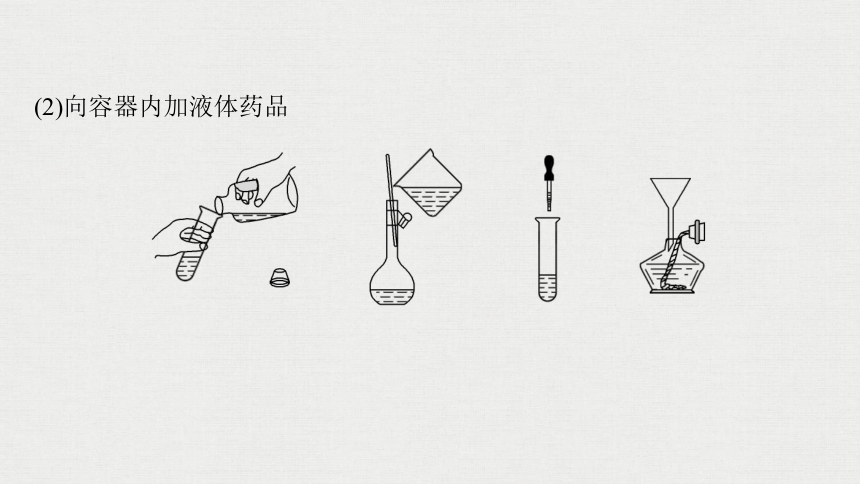
(2)向容器内加液体药品
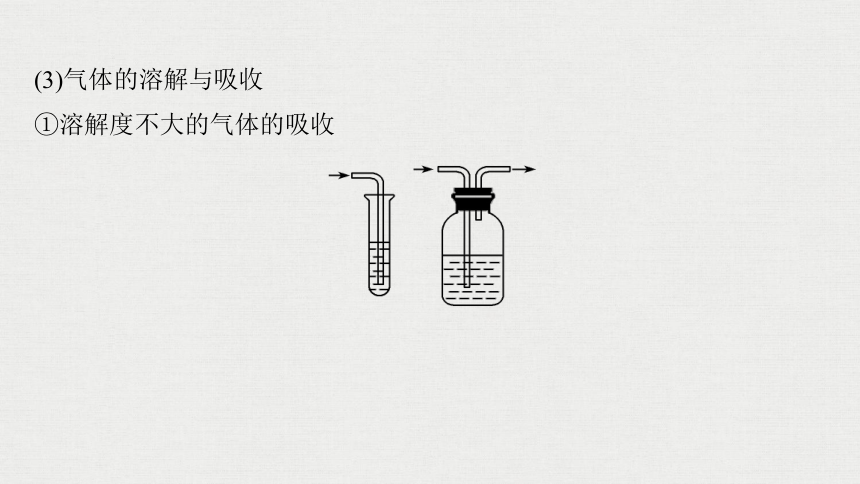
(3)气体的溶解与吸收
①溶解度不大的气体的吸收
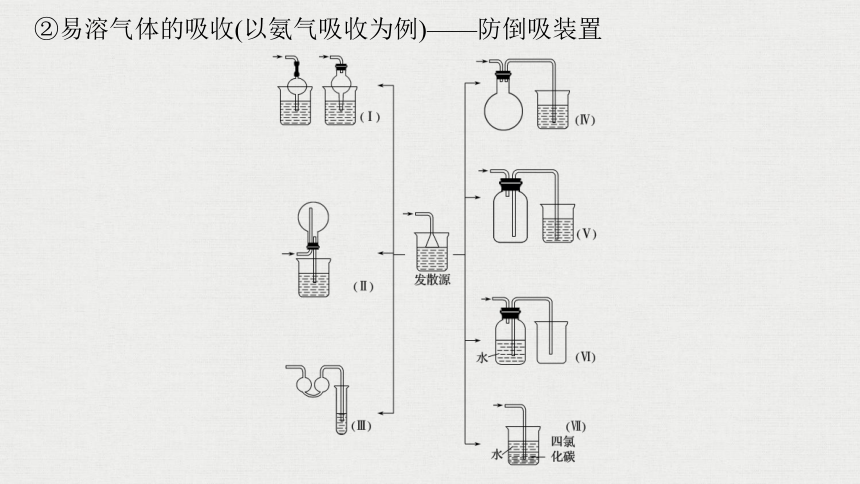
②易溶气体的吸收(以氨气吸收为例)——防倒吸装置
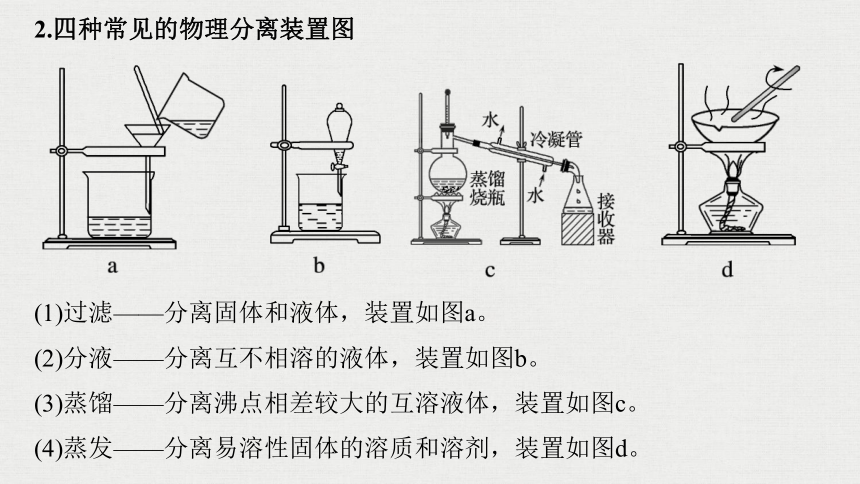
2.四种常见的物理分离装置图
(1)过滤——分离固体和液体,装置如图a。
(2)分液——分离互不相溶的液体,装置如图b。
(3)蒸馏——分离沸点相差较大的互溶液体,装置如图c。
(4)蒸发——分离易溶性固体的溶质和溶剂,装置如图d。
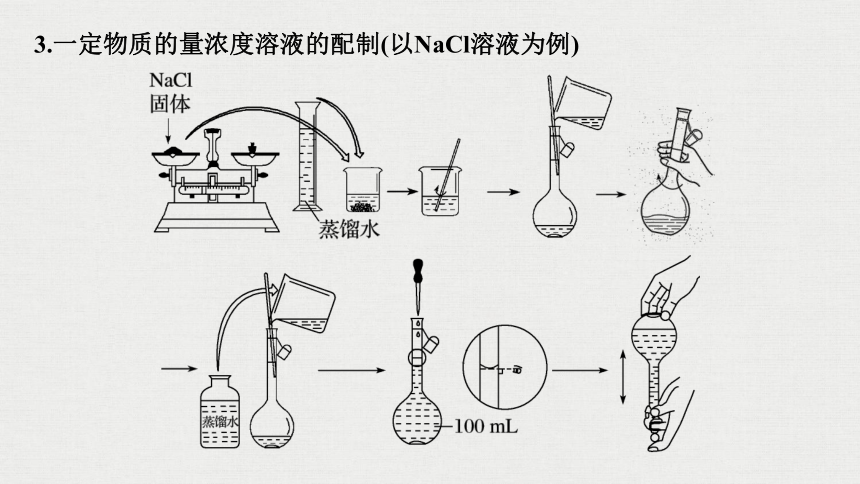
3.一定物质的量浓度溶液的配制(以NaCl溶液为例)
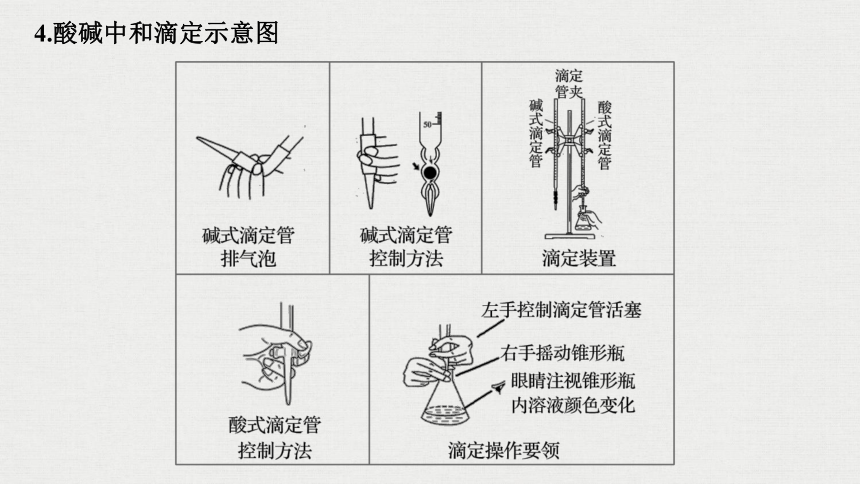
4.酸碱中和滴定示意图
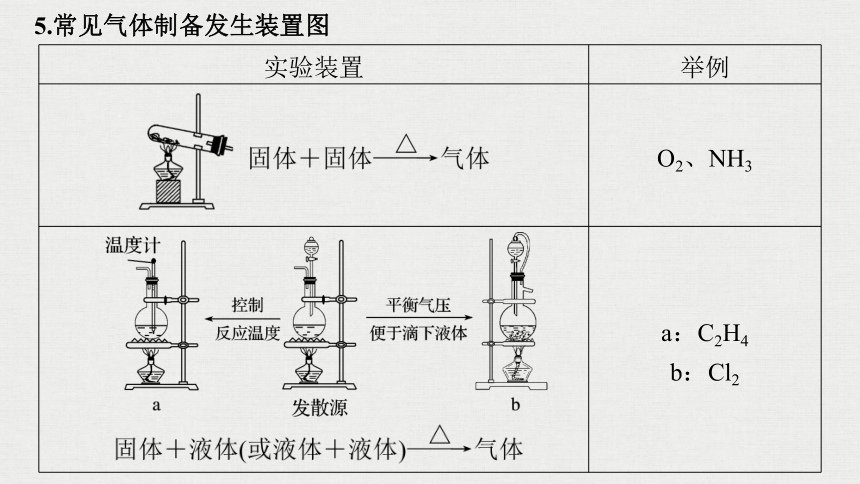
实验装置
举例
?
O2、NH3
?
?
a:C2H4
b:Cl2
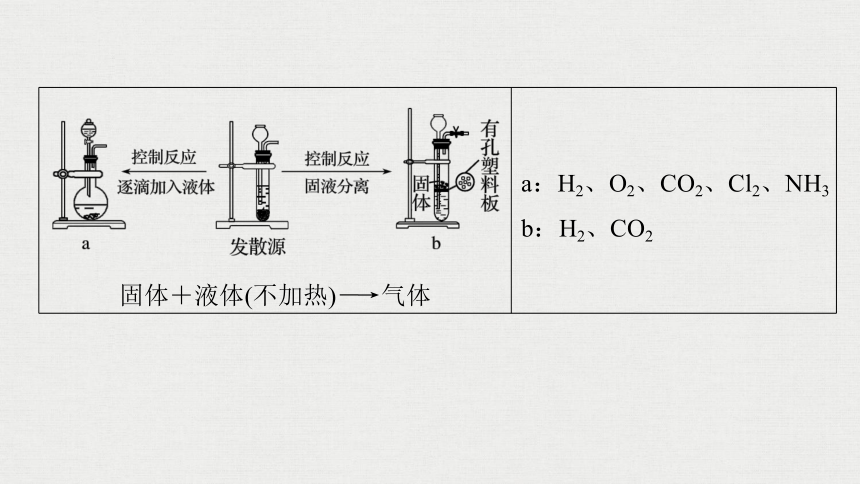
5.常见气体制备发生装置图
?
固体+液体(不加热)―→气体
a:H2、O2、CO2、Cl2、NH3
b:H2、CO2
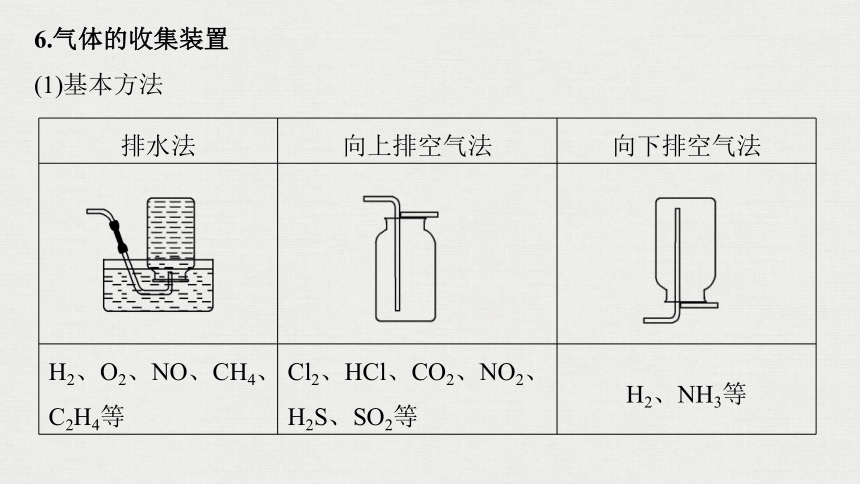
排水法
向上排空气法
向下排空气法
?
?
?
H2、O2、NO、CH4、C2H4等
Cl2、HCl、CO2、NO2、H2S、SO2等
H2、NH3等
6.气体的收集装置
(1)基本方法
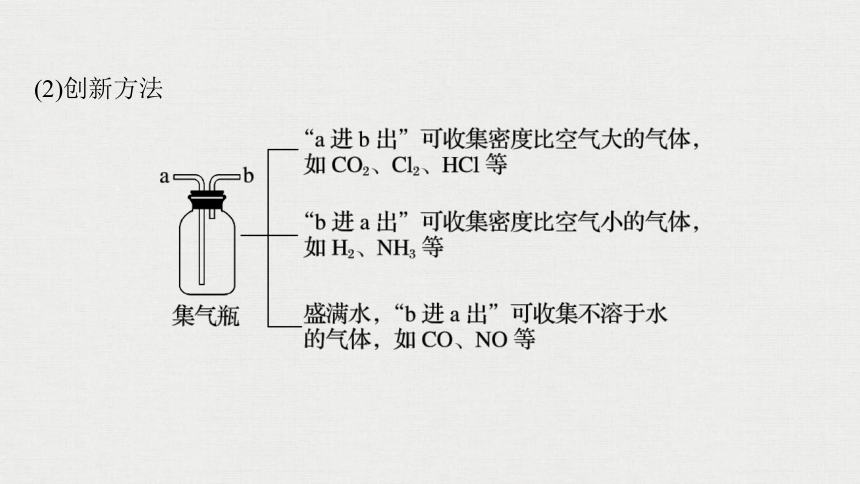
(2)创新方法
1.[2020·新高考全国卷Ⅰ(山东),5]利用下列装置(夹持装置略)进行实验,能达到实验目的的是
A.用甲装置制备并收集CO2
B.用乙装置制备溴苯并验证有HBr产生
C.用丙装置制备无水MgCl2
D.用丁装置在铁上镀铜
1
2
3
4
5
√
重练高考真题
解析 CO2密度比空气大,应该用向上排空气法收集,A项错误;
溴蒸气易挥发,挥发出的溴也能与硝酸银溶液反应生成淡黄色沉淀,B项错误;
氯化镁易水解,故需要在氯化氢气流中加热脱去结晶水,C项正确;
铁上镀铜需要铜作阳极,铁作阴极,D项错误。
1
2
3
4
5
2.(2020·江苏,5)实验室以CaCO3为原料,制备CO2并获得CaCl2·6H2O晶体。下列图示装置和原理不能达到实验目的的是
1
2
3
4
5
√
解析 A对,碳酸钙与稀盐酸反应可制备CO2,且为固液常温型反应,装置也正确;
B对,CO2密度比空气大,可以用向上排空气法收集;
C对,分离固体与液体,可采用过滤的方法;
D错,CaCl2·6H2O晶体可以通过蒸发浓缩、冷却结晶、过滤的方法制得,采用蒸发结晶法易导致CaCl2·6H2O失去结晶水。
1
2
3
4
5
A
B
C
D
?
?
?
?
配制50.00 mL 0.100 0 mol·L-1 Na2CO3溶液
除去Cl2中的HCl
蒸馏用冷凝管
盛装Na2SiO3溶液的试剂瓶
3.(2020·天津,5)下列实验仪器或装置的选择正确的是
1
2
3
4
5
√
解析 除去氯气中的氯化氢,可使用洗气法,通入饱和的氯化钠溶液中,导管长进短出,B项正确;
球形冷凝管用于冷凝回流,蒸馏时冷凝生成物,应使用直形冷凝管,C项错误;
盛放硅酸钠溶液的试剂瓶不可使用玻璃塞,否则会导致瓶口和瓶塞黏在一起,D项错误。
1
2
3
4
5
A
B
C
D
?
?
?
?
混合浓硫酸和乙醇
配制一定浓度的溶液
收集NO2气体
证明乙炔可使溴水褪色
4.(2019·天津,4)下列实验操作或装置能达到目的的是
1
2
3
4
5
√
1
2
3
4
5
解析 混合浓硫酸和乙醇时,应将浓硫酸沿着烧杯内壁缓缓注入乙醇中,并不断搅拌,A项错误;
配制一定浓度的溶液,定容时视线与容量瓶的刻度线相平,B项正确;
NO2的密度比空气的密度大,应用向上排空气法收集,C项错误;
电石与水反应制得的乙炔中含有H2S等杂质,H2S也能使溴水褪色,用溴水检验乙炔前,要先通过硫酸铜溶液除去H2S等杂质,D项错误。
1
2
3
4
5
5.(2019·全国卷Ⅰ,9)实验室制备溴苯的反应装置如图所示,关于实验操作或叙述错误的是
A.向圆底烧瓶中滴加苯和溴的混合
液前需先打开K
B.实验中装置b中的液体逐渐变为浅
红色
C.装置c中碳酸钠溶液的作用是吸收溴化氢
D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
√
1
2
3
4
5
解析 苯和溴均易挥发,苯与液溴在溴化铁作用下发生剧烈的放热反应,释放出溴化氢气体(含少量苯和溴蒸气),先打开K,后加入苯和液溴,避免因装置内气体压强过大而发生危险,A项正确;
四氯化碳用于吸收溴化氢气体中混有的溴单质,防止溴单质与碳酸钠溶液反应,四氯化碳呈无色,吸收红棕色溴蒸气后,液体呈浅红色,B项正确;
溴化氢极易溶于水,倒置漏斗防倒吸,碳酸钠溶液呈碱性,易吸收溴化氢,发生反应为Na2CO3+HBr===NaHCO3+NaBr,NaHCO3+HBr===
NaBr+CO2↑+H2O,C项正确;
1
2
3
4
5
反应后的混合液中混有苯、液溴、溴化铁和少量溴化氢等,提纯溴苯的正确操作是①用大量水洗涤,除去可溶性的溴化铁、溴化氢和少量溴;②用氢氧化钠溶液洗涤,除去剩余的溴等物质;③用水洗涤,除去残留的氢氧化钠;④加入干燥剂除去水,过滤;⑤对有机物进行蒸馏,除去杂质苯,从而提纯溴苯,分离溴苯不用“结晶”的方法,D项错误。
A
B
C
D
?
?
?
?
加热熔融的氢氧化钠固体
吸收CO2中的HCl杂质
蒸馏时的接收装置
吸收尾气中的Cl2
1
2
3
4
5
6
7
8
9
题组一 基本操作示意图的评价
1.下列选用的仪器和药品能达到实验目的的是
精练预测押题
√
解析 A项,瓷坩埚中含有SiO2,加热能与NaOH反应,错误;
B项,洗气瓶中气体流向应该从长导管进入,经溶液吸收杂质后气体从短导管导出,错误;
C项,尾部接收产品时应使用牛角管导流,以避免液体溅落到锥形瓶外部,错误。
1
2
3
4
5
6
7
8
9
2.下列实验操作正确的是
1
2
3
4
5
6
7
8
9
√
解析 氯化铁水解生成氢氧化铁和氯化氢,水解吸热且生成的氯化氢易挥发,所以直接加热不能得到氯化铁晶体,A项错误;
浓硫酸溶于水放热,需要在烧杯中稀释并冷却后才可以转移至容量瓶中,B项错误;
浓氨水中存在平衡 ,加入CaO,使平衡逆向移动,同时反应放热,促进NH3·H2O的分解,可以利用该装置制备少量氨气,C项正确;
碳酸氢钠受热易分解,要比较碳酸氢钠和碳酸钠的热稳定性大小,需要把碳酸钠放在大试管中,碳酸氢钠放在小试管中,D项错误。
1
2
3
4
5
6
7
8
9
3.(2020·河北4月联考)利用废蚀刻液(含FeCl2、CuCl2及FeCl3)制备碱性蚀刻液[Cu(NH3)4Cl2溶液]和FeCl3·6H2O的主要步骤:用H2O2氧化废蚀刻液,制备氨气,制备碱性蚀刻液[CuCl2+4NH3===Cu(NH3)4Cl2],固液分离,用盐酸溶解沉淀并制备FeCl3·6H2O,下列实验装置和操作不能达到实验目的的是
1
2
3
4
5
6
7
8
9
√
1
2
3
4
5
6
7
8
9
解析 实验室用Ca(OH)2和NH4Cl共热制备氨气,利用A项装置能够制备氨气,能达到实验目的,故A不符合题意;
B项装置制备碱性蚀刻液Cu(NH3)4Cl2,然后Fe3+与NH3·H2O反应生成Fe(OH)3沉淀,能达到实验目的,故B不符合题意;
C项装置用过滤的方法分离固液混合物,能达到实验目的,故C不符合题意;
由FeCl3溶液制备FeCl3·6H2O,应在HCl气流中蒸发浓缩、冷却结晶,所用仪器为蒸发皿,D项装置不能达到实验目的,故D符合题意。
题组二 无机物制备装置图的分析
4.(2019·江苏高三高考模拟)实验室用Ca与H2反应制取氢化钙(CaH2)。下列实验装置和原理不能达到实验目的的是
A.装置甲制取H2
B.装置乙净化干燥H2
C.装置丙制取CaH2
D.装置丁吸收尾气
1
2
3
4
5
6
7
8
9
√
解析 装置甲利用稀盐酸与锌在简易装置中制取H2,实验装置和原理能达到实验目的,选项A不选;
装置乙利用氢氧化钠溶液吸收
氢气中的氯化氢气体、利用浓
硫酸干燥氢气,起到净化干燥
H2的作用,实验装置和原理能达到实验目的,选项B不选;
装置丙利用纯净的氢气在高温条件下与钙反应制取CaH2,实验装置和原理能达到实验目的,选项C不选;
装置丁是防止空气中的水蒸气及氧气进入丙装置与钙或CaH2反应,故选D。
1
2
3
4
5
6
7
8
9
5.硫代硫酸钠(Na2S2O3)可作为鞣革时重铬酸盐的还原剂。纯碱与硫化钠的混合溶液与二氧化硫气体反应可生成Na2S2O3和CO2,实验室利用如图所示实验装置制备硫代硫酸钠
(夹持装置已略去)。
下列说法不正确的是
A.装置①也可用于实验室制备
氧气
B.装置②中虚线处表示的进气导管应伸至瓶底
C.实验时,应先打开活塞K1,再打开活塞K2
D.装置④中应盛装的试剂为NaOH溶液
1
2
3
4
5
6
7
8
9
√
解析 A项,①为固液不加热制气装置,MnO2催化分解H2O2制O2可用该装置;
B项,②应为防倒吸装置,两管均为短管;
C项,应先打开活塞K1,用SO2排尽装置中的空气,防止生成的Na2S2O3被氧化;
D项,尾气用碱液吸收。
1
2
3
4
5
6
7
8
9
题组三 探究反应产物与性质实验装置图的分析
6.一氧化铅(PbO)是黄或黄红色固体。实验室用草酸在浓硫酸作用下分解制备CO,其原理为H2C2O4 CO↑+CO2↑+H2O。某课题组同学设计实验探究CO还原一氧化铅并检验氧化产物(已知CO能使银氨溶液产生黑色沉淀)的装置如图所示。下列说法正确的是
1
2
3
4
5
6
7
8
9
A.装置②④⑤中的试剂依次为碱石灰、银氨溶液、澄清石灰水
B.实验时,先点燃装置①处酒精灯,当装置⑤中产生连续气泡且有明显
现象后再点燃装置③处酒精灯
C.实验完毕时,先熄灭装置①处酒精灯,再熄灭装置③处酒精灯
D.尾气处理可选用点燃、气袋收集、NaOH溶液吸收等方法
√
1
2
3
4
5
6
7
8
9
解析 装置①中发生反应生成CO、H2O和CO2,装置②中用碱石灰除去H2O和CO2,装置③中发生反应:CO+PbO Pb+CO2,装置④中用澄清石灰水检验并除去反应中产生的CO2,装置⑤中用银氨溶液检验反应前CO是否将装置中的空气排尽,尾气处理装置用于处理未反应的CO。装置②④⑤中的试剂依次为碱石灰、澄清石灰水、银氨溶液,A项错误;
1
2
3
4
5
6
7
8
9
实验时,先点燃装置①处酒精灯,当装置⑤中产生连续气泡且有明显现象后,即装置中的空气已被排尽,再点燃装置③处酒精灯,开始反应,B项正确;
实验完毕时,先熄灭装置③处酒精灯,再熄灭装置①处酒精灯,否则易发生倒吸,造成危险,C项错误;
尾气处理装置用于处理未反应的CO,可选用点燃、气袋收集,不能用NaOH溶液吸收,D项错误。
1
2
3
4
5
6
7
8
9
7.如图所示装置用于FeSO4受热分解实验及产品检验,已知亚硝酸铵受热易分解,下列相关说法正确的是
A.装置甲是N2的制备装置,实验时采用酒精灯直接加热至85 ℃
B.点燃装置乙处酒精喷灯前应先通入一段时间N2
C.装置丙依次装入品红溶液和BaCl2溶液用以检验产生的气体
D.采用装置丁,可更好地吸收尾气且避免了尾气外逸污染环境
1
2
3
4
5
6
7
8
9
√
解析 装置甲是N2的制备装置,实验时采用水浴加热才能控制温度在85 ℃,而酒精灯直接加热很难控制温度到85 ℃,A项错误;
亚铁盐易被氧气氧化,因此点燃装置乙处酒精喷灯前应先通入一段时间N2,排尽装置内的空气,B项正确;
1
2
3
4
5
6
7
8
9
FeSO4受热分解为氧化铁、二氧化硫、三氧化硫,品红溶液褪色,能够检验反应生成的二氧化硫气体,而三氧化硫与品红溶液中的水反应生成了硫酸,无法再用BaCl2溶液检验产生的三氧化硫气体,C项错误;
由于整个装置为密闭体系,多余的气体很难进入丁装置内被碱液吸收,D项错误。
1
2
3
4
5
6
7
8
9
题组四 实验方案的设计、装置的评价
8.利用如图所示实验装置进行相应实验
(部分夹持装置已略),不能达到实验目
的的是?
A.图1装置可用于实验室分离CO和CO2
B.用图2所示装置制取少量H2
C.用图3所示装置可制取并收集干燥纯
净的NH3
D.用图4所示装置可制取乙烯并验证其
易被氧化
1
2
3
4
5
6
7
8
9
√
解析 CO2能与NaOH溶液反应生成碳酸钠和水,而CO不能,因此可以先用氢氧化钠溶液吸收CO2,分离出CO,然后再向生成的碳酸钠溶液中加入过量的稀硫酸即可重新得到CO2,能达到实验目的,A项正确;
装置和原理均正确且能起到随关随停的效果,B项正确;
用图3所示装置制取的氨气中混有水蒸气,缺少干燥装置,
且收集氨气的试管口应塞一团棉花,防止氨气与空气对
流而使NH3不纯,C项错误;
乙醇与浓硫酸加热可制取乙烯,由于乙烯中混有乙醇和SO2,故可用KOH溶液除杂后再用酸性高锰酸钾溶液氧化乙烯,故可用图4所示装置制取乙烯并验证其易被氧化,D项正确。
1
2
3
4
5
6
7
8
9
9.下列装置应用于实验室制NO2并回收硝酸铜,能达到实验目的的是
A.用装置甲制取NO2
B.用装置乙除去NO2中的少量HNO3
C.用装置丙收集NO2
D.用装置丁蒸干Cu(NO3)2溶液制Cu(NO3)2·6H2O
1
2
3
4
5
6
7
8
9
√
解析 稀硝酸与铜反应生成一氧化氮,A项错误;
二氧化氮能与水反应生成硝酸且硝酸与碳酸氢钠反应生成二氧化碳,会引入新的杂质,B项错误;
用装置丙采用向上排空气法收集NO2,能达到实验目的,C项正确;
Cu(NO3)2水解产生氢氧化铜和硝酸,硝酸易挥发,用装置丁蒸干Cu(NO3)2溶液得到氢氧化铜而得不到Cu(NO3)2·6H2O,D项错误。
1
2
3
4
5
6
7
8
9
角度二
规范示意图再现
1.基本操作
(1)向试管内加固体药品
高考必备知识
(2)向容器内加液体药品
(3)气体的溶解与吸收
①溶解度不大的气体的吸收
②易溶气体的吸收(以氨气吸收为例)——防倒吸装置
2.四种常见的物理分离装置图
(1)过滤——分离固体和液体,装置如图a。
(2)分液——分离互不相溶的液体,装置如图b。
(3)蒸馏——分离沸点相差较大的互溶液体,装置如图c。
(4)蒸发——分离易溶性固体的溶质和溶剂,装置如图d。
3.一定物质的量浓度溶液的配制(以NaCl溶液为例)
4.酸碱中和滴定示意图
实验装置
举例
?
O2、NH3
?
?
a:C2H4
b:Cl2
5.常见气体制备发生装置图
?
固体+液体(不加热)―→气体
a:H2、O2、CO2、Cl2、NH3
b:H2、CO2
排水法
向上排空气法
向下排空气法
?
?
?
H2、O2、NO、CH4、C2H4等
Cl2、HCl、CO2、NO2、H2S、SO2等
H2、NH3等
6.气体的收集装置
(1)基本方法
(2)创新方法
1.[2020·新高考全国卷Ⅰ(山东),5]利用下列装置(夹持装置略)进行实验,能达到实验目的的是
A.用甲装置制备并收集CO2
B.用乙装置制备溴苯并验证有HBr产生
C.用丙装置制备无水MgCl2
D.用丁装置在铁上镀铜
1
2
3
4
5
√
重练高考真题
解析 CO2密度比空气大,应该用向上排空气法收集,A项错误;
溴蒸气易挥发,挥发出的溴也能与硝酸银溶液反应生成淡黄色沉淀,B项错误;
氯化镁易水解,故需要在氯化氢气流中加热脱去结晶水,C项正确;
铁上镀铜需要铜作阳极,铁作阴极,D项错误。
1
2
3
4
5
2.(2020·江苏,5)实验室以CaCO3为原料,制备CO2并获得CaCl2·6H2O晶体。下列图示装置和原理不能达到实验目的的是
1
2
3
4
5
√
解析 A对,碳酸钙与稀盐酸反应可制备CO2,且为固液常温型反应,装置也正确;
B对,CO2密度比空气大,可以用向上排空气法收集;
C对,分离固体与液体,可采用过滤的方法;
D错,CaCl2·6H2O晶体可以通过蒸发浓缩、冷却结晶、过滤的方法制得,采用蒸发结晶法易导致CaCl2·6H2O失去结晶水。
1
2
3
4
5
A
B
C
D
?
?
?
?
配制50.00 mL 0.100 0 mol·L-1 Na2CO3溶液
除去Cl2中的HCl
蒸馏用冷凝管
盛装Na2SiO3溶液的试剂瓶
3.(2020·天津,5)下列实验仪器或装置的选择正确的是
1
2
3
4
5
√
解析 除去氯气中的氯化氢,可使用洗气法,通入饱和的氯化钠溶液中,导管长进短出,B项正确;
球形冷凝管用于冷凝回流,蒸馏时冷凝生成物,应使用直形冷凝管,C项错误;
盛放硅酸钠溶液的试剂瓶不可使用玻璃塞,否则会导致瓶口和瓶塞黏在一起,D项错误。
1
2
3
4
5
A
B
C
D
?
?
?
?
混合浓硫酸和乙醇
配制一定浓度的溶液
收集NO2气体
证明乙炔可使溴水褪色
4.(2019·天津,4)下列实验操作或装置能达到目的的是
1
2
3
4
5
√
1
2
3
4
5
解析 混合浓硫酸和乙醇时,应将浓硫酸沿着烧杯内壁缓缓注入乙醇中,并不断搅拌,A项错误;
配制一定浓度的溶液,定容时视线与容量瓶的刻度线相平,B项正确;
NO2的密度比空气的密度大,应用向上排空气法收集,C项错误;
电石与水反应制得的乙炔中含有H2S等杂质,H2S也能使溴水褪色,用溴水检验乙炔前,要先通过硫酸铜溶液除去H2S等杂质,D项错误。
1
2
3
4
5
5.(2019·全国卷Ⅰ,9)实验室制备溴苯的反应装置如图所示,关于实验操作或叙述错误的是
A.向圆底烧瓶中滴加苯和溴的混合
液前需先打开K
B.实验中装置b中的液体逐渐变为浅
红色
C.装置c中碳酸钠溶液的作用是吸收溴化氢
D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
√
1
2
3
4
5
解析 苯和溴均易挥发,苯与液溴在溴化铁作用下发生剧烈的放热反应,释放出溴化氢气体(含少量苯和溴蒸气),先打开K,后加入苯和液溴,避免因装置内气体压强过大而发生危险,A项正确;
四氯化碳用于吸收溴化氢气体中混有的溴单质,防止溴单质与碳酸钠溶液反应,四氯化碳呈无色,吸收红棕色溴蒸气后,液体呈浅红色,B项正确;
溴化氢极易溶于水,倒置漏斗防倒吸,碳酸钠溶液呈碱性,易吸收溴化氢,发生反应为Na2CO3+HBr===NaHCO3+NaBr,NaHCO3+HBr===
NaBr+CO2↑+H2O,C项正确;
1
2
3
4
5
反应后的混合液中混有苯、液溴、溴化铁和少量溴化氢等,提纯溴苯的正确操作是①用大量水洗涤,除去可溶性的溴化铁、溴化氢和少量溴;②用氢氧化钠溶液洗涤,除去剩余的溴等物质;③用水洗涤,除去残留的氢氧化钠;④加入干燥剂除去水,过滤;⑤对有机物进行蒸馏,除去杂质苯,从而提纯溴苯,分离溴苯不用“结晶”的方法,D项错误。
A
B
C
D
?
?
?
?
加热熔融的氢氧化钠固体
吸收CO2中的HCl杂质
蒸馏时的接收装置
吸收尾气中的Cl2
1
2
3
4
5
6
7
8
9
题组一 基本操作示意图的评价
1.下列选用的仪器和药品能达到实验目的的是
精练预测押题
√
解析 A项,瓷坩埚中含有SiO2,加热能与NaOH反应,错误;
B项,洗气瓶中气体流向应该从长导管进入,经溶液吸收杂质后气体从短导管导出,错误;
C项,尾部接收产品时应使用牛角管导流,以避免液体溅落到锥形瓶外部,错误。
1
2
3
4
5
6
7
8
9
2.下列实验操作正确的是
1
2
3
4
5
6
7
8
9
√
解析 氯化铁水解生成氢氧化铁和氯化氢,水解吸热且生成的氯化氢易挥发,所以直接加热不能得到氯化铁晶体,A项错误;
浓硫酸溶于水放热,需要在烧杯中稀释并冷却后才可以转移至容量瓶中,B项错误;
浓氨水中存在平衡 ,加入CaO,使平衡逆向移动,同时反应放热,促进NH3·H2O的分解,可以利用该装置制备少量氨气,C项正确;
碳酸氢钠受热易分解,要比较碳酸氢钠和碳酸钠的热稳定性大小,需要把碳酸钠放在大试管中,碳酸氢钠放在小试管中,D项错误。
1
2
3
4
5
6
7
8
9
3.(2020·河北4月联考)利用废蚀刻液(含FeCl2、CuCl2及FeCl3)制备碱性蚀刻液[Cu(NH3)4Cl2溶液]和FeCl3·6H2O的主要步骤:用H2O2氧化废蚀刻液,制备氨气,制备碱性蚀刻液[CuCl2+4NH3===Cu(NH3)4Cl2],固液分离,用盐酸溶解沉淀并制备FeCl3·6H2O,下列实验装置和操作不能达到实验目的的是
1
2
3
4
5
6
7
8
9
√
1
2
3
4
5
6
7
8
9
解析 实验室用Ca(OH)2和NH4Cl共热制备氨气,利用A项装置能够制备氨气,能达到实验目的,故A不符合题意;
B项装置制备碱性蚀刻液Cu(NH3)4Cl2,然后Fe3+与NH3·H2O反应生成Fe(OH)3沉淀,能达到实验目的,故B不符合题意;
C项装置用过滤的方法分离固液混合物,能达到实验目的,故C不符合题意;
由FeCl3溶液制备FeCl3·6H2O,应在HCl气流中蒸发浓缩、冷却结晶,所用仪器为蒸发皿,D项装置不能达到实验目的,故D符合题意。
题组二 无机物制备装置图的分析
4.(2019·江苏高三高考模拟)实验室用Ca与H2反应制取氢化钙(CaH2)。下列实验装置和原理不能达到实验目的的是
A.装置甲制取H2
B.装置乙净化干燥H2
C.装置丙制取CaH2
D.装置丁吸收尾气
1
2
3
4
5
6
7
8
9
√
解析 装置甲利用稀盐酸与锌在简易装置中制取H2,实验装置和原理能达到实验目的,选项A不选;
装置乙利用氢氧化钠溶液吸收
氢气中的氯化氢气体、利用浓
硫酸干燥氢气,起到净化干燥
H2的作用,实验装置和原理能达到实验目的,选项B不选;
装置丙利用纯净的氢气在高温条件下与钙反应制取CaH2,实验装置和原理能达到实验目的,选项C不选;
装置丁是防止空气中的水蒸气及氧气进入丙装置与钙或CaH2反应,故选D。
1
2
3
4
5
6
7
8
9
5.硫代硫酸钠(Na2S2O3)可作为鞣革时重铬酸盐的还原剂。纯碱与硫化钠的混合溶液与二氧化硫气体反应可生成Na2S2O3和CO2,实验室利用如图所示实验装置制备硫代硫酸钠
(夹持装置已略去)。
下列说法不正确的是
A.装置①也可用于实验室制备
氧气
B.装置②中虚线处表示的进气导管应伸至瓶底
C.实验时,应先打开活塞K1,再打开活塞K2
D.装置④中应盛装的试剂为NaOH溶液
1
2
3
4
5
6
7
8
9
√
解析 A项,①为固液不加热制气装置,MnO2催化分解H2O2制O2可用该装置;
B项,②应为防倒吸装置,两管均为短管;
C项,应先打开活塞K1,用SO2排尽装置中的空气,防止生成的Na2S2O3被氧化;
D项,尾气用碱液吸收。
1
2
3
4
5
6
7
8
9
题组三 探究反应产物与性质实验装置图的分析
6.一氧化铅(PbO)是黄或黄红色固体。实验室用草酸在浓硫酸作用下分解制备CO,其原理为H2C2O4 CO↑+CO2↑+H2O。某课题组同学设计实验探究CO还原一氧化铅并检验氧化产物(已知CO能使银氨溶液产生黑色沉淀)的装置如图所示。下列说法正确的是
1
2
3
4
5
6
7
8
9
A.装置②④⑤中的试剂依次为碱石灰、银氨溶液、澄清石灰水
B.实验时,先点燃装置①处酒精灯,当装置⑤中产生连续气泡且有明显
现象后再点燃装置③处酒精灯
C.实验完毕时,先熄灭装置①处酒精灯,再熄灭装置③处酒精灯
D.尾气处理可选用点燃、气袋收集、NaOH溶液吸收等方法
√
1
2
3
4
5
6
7
8
9
解析 装置①中发生反应生成CO、H2O和CO2,装置②中用碱石灰除去H2O和CO2,装置③中发生反应:CO+PbO Pb+CO2,装置④中用澄清石灰水检验并除去反应中产生的CO2,装置⑤中用银氨溶液检验反应前CO是否将装置中的空气排尽,尾气处理装置用于处理未反应的CO。装置②④⑤中的试剂依次为碱石灰、澄清石灰水、银氨溶液,A项错误;
1
2
3
4
5
6
7
8
9
实验时,先点燃装置①处酒精灯,当装置⑤中产生连续气泡且有明显现象后,即装置中的空气已被排尽,再点燃装置③处酒精灯,开始反应,B项正确;
实验完毕时,先熄灭装置③处酒精灯,再熄灭装置①处酒精灯,否则易发生倒吸,造成危险,C项错误;
尾气处理装置用于处理未反应的CO,可选用点燃、气袋收集,不能用NaOH溶液吸收,D项错误。
1
2
3
4
5
6
7
8
9
7.如图所示装置用于FeSO4受热分解实验及产品检验,已知亚硝酸铵受热易分解,下列相关说法正确的是
A.装置甲是N2的制备装置,实验时采用酒精灯直接加热至85 ℃
B.点燃装置乙处酒精喷灯前应先通入一段时间N2
C.装置丙依次装入品红溶液和BaCl2溶液用以检验产生的气体
D.采用装置丁,可更好地吸收尾气且避免了尾气外逸污染环境
1
2
3
4
5
6
7
8
9
√
解析 装置甲是N2的制备装置,实验时采用水浴加热才能控制温度在85 ℃,而酒精灯直接加热很难控制温度到85 ℃,A项错误;
亚铁盐易被氧气氧化,因此点燃装置乙处酒精喷灯前应先通入一段时间N2,排尽装置内的空气,B项正确;
1
2
3
4
5
6
7
8
9
FeSO4受热分解为氧化铁、二氧化硫、三氧化硫,品红溶液褪色,能够检验反应生成的二氧化硫气体,而三氧化硫与品红溶液中的水反应生成了硫酸,无法再用BaCl2溶液检验产生的三氧化硫气体,C项错误;
由于整个装置为密闭体系,多余的气体很难进入丁装置内被碱液吸收,D项错误。
1
2
3
4
5
6
7
8
9
题组四 实验方案的设计、装置的评价
8.利用如图所示实验装置进行相应实验
(部分夹持装置已略),不能达到实验目
的的是?
A.图1装置可用于实验室分离CO和CO2
B.用图2所示装置制取少量H2
C.用图3所示装置可制取并收集干燥纯
净的NH3
D.用图4所示装置可制取乙烯并验证其
易被氧化
1
2
3
4
5
6
7
8
9
√
解析 CO2能与NaOH溶液反应生成碳酸钠和水,而CO不能,因此可以先用氢氧化钠溶液吸收CO2,分离出CO,然后再向生成的碳酸钠溶液中加入过量的稀硫酸即可重新得到CO2,能达到实验目的,A项正确;
装置和原理均正确且能起到随关随停的效果,B项正确;
用图3所示装置制取的氨气中混有水蒸气,缺少干燥装置,
且收集氨气的试管口应塞一团棉花,防止氨气与空气对
流而使NH3不纯,C项错误;
乙醇与浓硫酸加热可制取乙烯,由于乙烯中混有乙醇和SO2,故可用KOH溶液除杂后再用酸性高锰酸钾溶液氧化乙烯,故可用图4所示装置制取乙烯并验证其易被氧化,D项正确。
1
2
3
4
5
6
7
8
9
9.下列装置应用于实验室制NO2并回收硝酸铜,能达到实验目的的是
A.用装置甲制取NO2
B.用装置乙除去NO2中的少量HNO3
C.用装置丙收集NO2
D.用装置丁蒸干Cu(NO3)2溶液制Cu(NO3)2·6H2O
1
2
3
4
5
6
7
8
9
√
解析 稀硝酸与铜反应生成一氧化氮,A项错误;
二氧化氮能与水反应生成硝酸且硝酸与碳酸氢钠反应生成二氧化碳,会引入新的杂质,B项错误;
用装置丙采用向上排空气法收集NO2,能达到实验目的,C项正确;
Cu(NO3)2水解产生氢氧化铜和硝酸,硝酸易挥发,用装置丁蒸干Cu(NO3)2溶液得到氢氧化铜而得不到Cu(NO3)2·6H2O,D项错误。
1
2
3
4
5
6
7
8
9
同课章节目录
