2021年中考化学工业流程专题复习教案
文档属性
| 名称 | 2021年中考化学工业流程专题复习教案 |

|
|
| 格式 | docx | ||
| 文件大小 | 178.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-01 00:00:00 | ||
图片预览

文档简介
九年级化学(人教版)中考复习
工艺流程专题复习
教学目标:
1、知识与技能:
(1)、知道工业流程题的形式、考查的关注点。
(2)、了解常见的工业流程题的突破点。
2、过程与方法:
(1)、通过精选素材,让学生能够自己发现规律。
(2)、通过交流与讨论,让学生明确工业流程题的解题方法。
3、情感态度与价值观:
(1)、明确化学对于人类社会的作用,使学生建文学好化学改善生活的信心。
(2)、帮助学生树立保护环境人人有责的思想,培养学生的社会责任感。
教学重难点:
1、教学重点:
通过几个例题的分析,找到工业流程题的一股规律、解题突破点、常用方法等有用信息。
2、教学难点:
寻找和总结规律。
教学过程:
一、什么是化学工艺流程题?
化学工艺流程题,就是将化工生产过程中的主要生产阶段用框图流程形式表示出来,并根据生产流程中有关的化学知识步步设问,形成与化工生产紧密联系的化工工艺试题。
二、化学工艺流程题的类型?
除杂提纯工艺流程题:海水制取食盐工艺流程题
制备合成工艺流程题:如海水提镁、侯氏制碱工艺流程题
三、中考流程题命题考查内容和特点
考查内容
1.化学反应原理
2.元素化合物知识
3.实验操作及名称
4.
物质除杂、分离
5.利用溶解度分离物质
6.流程中的物质转化和循环
特点
1.情境真实
2.框图信息新颖
3.问题设计广泛
4.综合性强
5.思维容量大
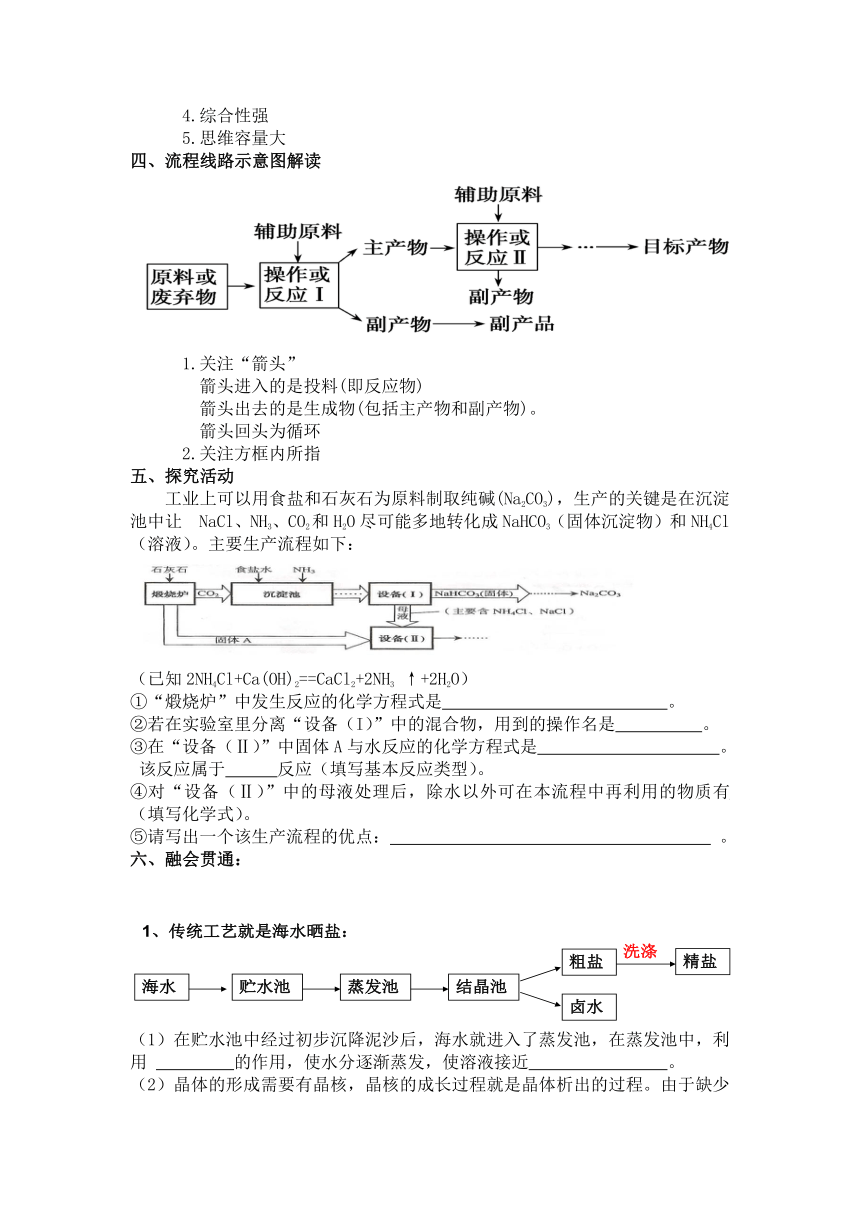
四、流程线路示意图解读
1.关注“箭头”
箭头进入的是投料(即反应物)
箭头出去的是生成物(包括主产物和副产物)。
箭头回头为循环
2.关注方框内所指
五、探究活动
工业上可以用食盐和石灰石为原料制取纯碱(Na2CO3),生产的关键是在沉淀池中让
NaCl、NH3、CO2和H2O尽可能多地转化成NaHCO3(固体沉淀物)和NH4Cl(溶液)。主要生产流程如下:
(已知2NH4Cl+Ca(OH)2==CaCl2+2NH3
↑+2H2O)
①“煅烧炉”中发生反应的化学方程式是
。
②若在实验室里分离“设备(I)”中的混合物,用到的操作名是
。
③在“设备(Ⅱ)”中固体A与水反应的化学方程式是
。
该反应属于
反应(填写基本反应类型)。
④对“设备(Ⅱ)”中的母液处理后,除水以外可在本流程中再利用的物质有
(填写化学式)。
⑤请写出一个该生产流程的优点:
。
六、融会贯通:
(1)在贮水池中经过初步沉降泥沙后,海水就进入了蒸发池,在蒸发池中,利用
的作用,使水分逐渐蒸发,使溶液接近
。
(2)晶体的形成需要有晶核,晶核的成长过程就是晶体析出的过程。由于缺少晶核,因此在结晶池中为了能使食盐更快的析出,人们会向池水中撒入
来作为晶核。
(3)粗盐在除去泥沙后,还会混有氯化镁、氯化钙等杂质,传统方法就是用高浓度的卤水进行洗涤,这样生产出来的盐我们称之为洗涤盐。利用你学过的知识,请你判断。这种高浓度的卤水应该是以
为溶质的溶液,为了减少食盐的损失,应该使用的是
卤水,这种方法利用的原理是
。
2、现代工艺:真空制盐
真空制盐的原料一般是用井矿盐或地下卤水经过净化除杂后得到的人工卤水(精盐水),即纯净的氯化钠溶液,因此卤水的净化过程就是真空制盐过程中至关重要的环节。已知某地的地下卤水中,除了氯化钠外还含有硫酸钠、氯化镁、氯化钙等可溶性杂质,他们在溶液中主要以SO42-、Ca2+、Mg2+的形式存在,为将这些杂质离子除净,应加入过量的碳酸钠、氯化钡、氢氧化钠等物质将其转化为沉淀除去;再加入适量的盐酸,得到精盐水,最后经真空蒸发即可得到精盐。
(1)步骤①中加入的A溶液是
溶液,其作用是
。
(2)步骤②中加入的B溶液是
溶液,其作用是
。
(3)步骤③中加入的C溶液是
溶液,其作用是
。
(4)操作Ⅰ是
,在实验室中进行该操作要用到的玻璃仪器有
。
(5)步骤⑤加入稀盐酸的目的是
,写出涉及的反应方程式
、
。
七、拓展:
某化学兴趣小组的同学准备进行金属铜的制备,现有原料物质:氧化铜、稀硫酸、金属锌。最终他们设计了两套方案,分别是:
请你从不同的角度分析,A、B两个方案中哪一个相对更好,为什么?
八、学习心得
解答物质制备合成类的工艺流程题,我们应该从哪些方面去思考和注意呢?
在明确生产原理后,我们应主要从以下几个方面来分析和思考
1、成本要低:原料的来源
2、操作、设备要简便
3、对环境的影响要小,绿色化生产
4、尽量做到物质的循环使用或再生
九、解题思路
1、静心读题找信息
2、寻找突破口
①从实验现象突破:颜色、沉淀、气体等
②从实验操作突破:高温煅烧、溶解、结晶、过滤等
③善于将流程分解成若干个小型实验
3、准确作答
4、顺向检查
十、基本步骤
1、从题干中获取有用信息,了解生产的
产品
2、分析流程中的每一步骤,从几个方面了解流程:
A.反应物是什么
B.发生了什么反应
C.关键点:一切反应或操作都是为获得
产品(目标物质)而服务。
十一、课堂练习:
镁合金的强度高、机械性能好。这些特性使金属镁成为制造汽车、飞机、火箭的重要材料,从而获得“国防金属”的美誉。海水提镁是国际上的主要趋势,工业流程图如下
其步骤为:
I.将海边大量存在的贝壳(主要成分为CaCO3)煅烧成生石灰,并将生石灰制成石灰乳
Ⅱ.将石灰乳加入到海水反应池中,经过沉降、过滤得到Mg(OH)2沉淀
Ⅲ.在Mg(OH)2沉淀中加入盐酸中和得到MgCl2溶液,再经蒸发结晶得到
MgCl2·6H2O
Ⅳ.将MgCl2·6H2O在一定条件下加热得到无水MgCl2
V.电解熔融的无水MgCl2可得到Mg
请根据上述步骤回答问题:
①写出步骤I、Ⅲ的有关化学方程式:
I.贝壳煅烧成生石灰
,
Ⅲ.Mg(OH)2沉淀中加入盐酸中和
。
②步骤I~V中有分解反应的是(填写步骤序号):
。
③步骤Ⅲ中的蒸发是利用风吹日晒来完成的,而在实验室中进行蒸发操作需要的主要仪器有
、
、酒精灯、带铁圈的铁架台、坩埚钳等。
④上述海水提纯镁的流程中,采取了哪些措施来降低成本、减少污染的?请写出其中一点:
。
十二、专题训练:(见学案)
工艺流程专题复习
教学目标:
1、知识与技能:
(1)、知道工业流程题的形式、考查的关注点。
(2)、了解常见的工业流程题的突破点。
2、过程与方法:
(1)、通过精选素材,让学生能够自己发现规律。
(2)、通过交流与讨论,让学生明确工业流程题的解题方法。
3、情感态度与价值观:
(1)、明确化学对于人类社会的作用,使学生建文学好化学改善生活的信心。
(2)、帮助学生树立保护环境人人有责的思想,培养学生的社会责任感。
教学重难点:
1、教学重点:
通过几个例题的分析,找到工业流程题的一股规律、解题突破点、常用方法等有用信息。
2、教学难点:
寻找和总结规律。
教学过程:
一、什么是化学工艺流程题?
化学工艺流程题,就是将化工生产过程中的主要生产阶段用框图流程形式表示出来,并根据生产流程中有关的化学知识步步设问,形成与化工生产紧密联系的化工工艺试题。
二、化学工艺流程题的类型?
除杂提纯工艺流程题:海水制取食盐工艺流程题
制备合成工艺流程题:如海水提镁、侯氏制碱工艺流程题
三、中考流程题命题考查内容和特点
考查内容
1.化学反应原理
2.元素化合物知识
3.实验操作及名称
4.
物质除杂、分离
5.利用溶解度分离物质
6.流程中的物质转化和循环
特点
1.情境真实
2.框图信息新颖
3.问题设计广泛
4.综合性强
5.思维容量大
四、流程线路示意图解读
1.关注“箭头”
箭头进入的是投料(即反应物)
箭头出去的是生成物(包括主产物和副产物)。
箭头回头为循环
2.关注方框内所指
五、探究活动
工业上可以用食盐和石灰石为原料制取纯碱(Na2CO3),生产的关键是在沉淀池中让
NaCl、NH3、CO2和H2O尽可能多地转化成NaHCO3(固体沉淀物)和NH4Cl(溶液)。主要生产流程如下:
(已知2NH4Cl+Ca(OH)2==CaCl2+2NH3
↑+2H2O)
①“煅烧炉”中发生反应的化学方程式是
。
②若在实验室里分离“设备(I)”中的混合物,用到的操作名是
。
③在“设备(Ⅱ)”中固体A与水反应的化学方程式是
。
该反应属于
反应(填写基本反应类型)。
④对“设备(Ⅱ)”中的母液处理后,除水以外可在本流程中再利用的物质有
(填写化学式)。
⑤请写出一个该生产流程的优点:
。
六、融会贯通:
(1)在贮水池中经过初步沉降泥沙后,海水就进入了蒸发池,在蒸发池中,利用
的作用,使水分逐渐蒸发,使溶液接近
。
(2)晶体的形成需要有晶核,晶核的成长过程就是晶体析出的过程。由于缺少晶核,因此在结晶池中为了能使食盐更快的析出,人们会向池水中撒入
来作为晶核。
(3)粗盐在除去泥沙后,还会混有氯化镁、氯化钙等杂质,传统方法就是用高浓度的卤水进行洗涤,这样生产出来的盐我们称之为洗涤盐。利用你学过的知识,请你判断。这种高浓度的卤水应该是以
为溶质的溶液,为了减少食盐的损失,应该使用的是
卤水,这种方法利用的原理是
。
2、现代工艺:真空制盐
真空制盐的原料一般是用井矿盐或地下卤水经过净化除杂后得到的人工卤水(精盐水),即纯净的氯化钠溶液,因此卤水的净化过程就是真空制盐过程中至关重要的环节。已知某地的地下卤水中,除了氯化钠外还含有硫酸钠、氯化镁、氯化钙等可溶性杂质,他们在溶液中主要以SO42-、Ca2+、Mg2+的形式存在,为将这些杂质离子除净,应加入过量的碳酸钠、氯化钡、氢氧化钠等物质将其转化为沉淀除去;再加入适量的盐酸,得到精盐水,最后经真空蒸发即可得到精盐。
(1)步骤①中加入的A溶液是
溶液,其作用是
。
(2)步骤②中加入的B溶液是
溶液,其作用是
。
(3)步骤③中加入的C溶液是
溶液,其作用是
。
(4)操作Ⅰ是
,在实验室中进行该操作要用到的玻璃仪器有
。
(5)步骤⑤加入稀盐酸的目的是
,写出涉及的反应方程式
、
。
七、拓展:
某化学兴趣小组的同学准备进行金属铜的制备,现有原料物质:氧化铜、稀硫酸、金属锌。最终他们设计了两套方案,分别是:
请你从不同的角度分析,A、B两个方案中哪一个相对更好,为什么?
八、学习心得
解答物质制备合成类的工艺流程题,我们应该从哪些方面去思考和注意呢?
在明确生产原理后,我们应主要从以下几个方面来分析和思考
1、成本要低:原料的来源
2、操作、设备要简便
3、对环境的影响要小,绿色化生产
4、尽量做到物质的循环使用或再生
九、解题思路
1、静心读题找信息
2、寻找突破口
①从实验现象突破:颜色、沉淀、气体等
②从实验操作突破:高温煅烧、溶解、结晶、过滤等
③善于将流程分解成若干个小型实验
3、准确作答
4、顺向检查
十、基本步骤
1、从题干中获取有用信息,了解生产的
产品
2、分析流程中的每一步骤,从几个方面了解流程:
A.反应物是什么
B.发生了什么反应
C.关键点:一切反应或操作都是为获得
产品(目标物质)而服务。
十一、课堂练习:
镁合金的强度高、机械性能好。这些特性使金属镁成为制造汽车、飞机、火箭的重要材料,从而获得“国防金属”的美誉。海水提镁是国际上的主要趋势,工业流程图如下
其步骤为:
I.将海边大量存在的贝壳(主要成分为CaCO3)煅烧成生石灰,并将生石灰制成石灰乳
Ⅱ.将石灰乳加入到海水反应池中,经过沉降、过滤得到Mg(OH)2沉淀
Ⅲ.在Mg(OH)2沉淀中加入盐酸中和得到MgCl2溶液,再经蒸发结晶得到
MgCl2·6H2O
Ⅳ.将MgCl2·6H2O在一定条件下加热得到无水MgCl2
V.电解熔融的无水MgCl2可得到Mg
请根据上述步骤回答问题:
①写出步骤I、Ⅲ的有关化学方程式:
I.贝壳煅烧成生石灰
,
Ⅲ.Mg(OH)2沉淀中加入盐酸中和
。
②步骤I~V中有分解反应的是(填写步骤序号):
。
③步骤Ⅲ中的蒸发是利用风吹日晒来完成的,而在实验室中进行蒸发操作需要的主要仪器有
、
、酒精灯、带铁圈的铁架台、坩埚钳等。
④上述海水提纯镁的流程中,采取了哪些措施来降低成本、减少污染的?请写出其中一点:
。
十二、专题训练:(见学案)
同课章节目录
