科学版九年级化学上册 名校精选精练 第二章达标检测卷(含详细解答)
文档属性
| 名称 | 科学版九年级化学上册 名校精选精练 第二章达标检测卷(含详细解答) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 其它版本 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-13 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
科学版九年级化学上册
名校精选精练
第二章达标检测卷
(100分,90分钟)
班级:
姓名:
考号:
.
题 号
一
二
三
总 分
得 分
一、选择题(每题2分,共30分)
1.空气中含量较多且化学性质比较活泼的气体是( )
A.氧气
B.氮气
C.稀有气体
D.二氧化碳
2.影响元素化学性质的最主要因素是( )
A.原子的质子数
B.原子的电子层数
C.原子的最外层电子数
D.组成某种物质的原子个数
3.杜甫的绝句《沙暖睡鸳鸯》中写到“迟日江山丽,春风花草香”。诗中描写的情景用化学原理解释正确的是( )
A.分子很小,但分子有一定的质量
B.分子很小,但分子之间有间隔
C.分子很小,但分子在不停地运动着
D.分子很小,但分子是由原子构成的
4.薯片等易碎食品宜采用充气袋包装,下列气体中最不适宜充入的是( )
A.O2
B.N2
C.CO2
D.空气
5.不会造成空气污染的物质是( )
A.一氧化碳
B.水蒸气
C.烟尘
D.二氧化硫
6.空气是我们每天都呼吸的“生命气体”。下列说法错误的是( )
A.空气中氮气的质量分数为78%
B.空气中氧气能供给呼吸和支持燃烧
C.空气中二氧化碳是造成温室效应的主要气体
D.空气中的稀有气体所占比例虽小,但用途广泛
7.下列物质属于化合物的是( )
A.水银
B.液态氧
C.蒸馏水
D.空气
8.下列有关分子、原子、离子和元素的说法正确的是( )
A.原子不能直接构成物质
B.分子是化学变化中最小的微粒
C.决定元素化学性质的是原子的电子数
D.原子得到或失去电子变成离子
9.原子序数为94的钚是一种核原料,该元素一种原子的质子数和中子数之和为239,下列关于该原子的说法不正确的是( )
A.中子数为145
B.核外电子数为94
C.质子数为94
D.核电荷数为239
10.如图是“测定空气中氧气体积分数”的实验装置,关于该实验下列说法正确的是( )
(第10题)
A.不用考虑装置气密性是否良好
B.红磷火焰熄灭后立即打开止水夹
C.依据实验现象推测,氧气约占空气总体积的1/5
D.红磷燃烧的文字表达式为磷+氧气→五氧化二磷
11.下列有关物质的分类,错误的是( )
A.冰块和水混合属于氧化物
B.过氧化氢属于化合物
C.洁净的空气属于纯净物
D.液氮属于单质
12.元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分,下列有关说法正确的是( )
(第12题)
A.铁的相对原子质量为55.85
g
B.锰元素为非金属元素
C.铬原子的原子核内有52个质子
D.等质量的铬、锰、铁中,含原子个数最多的是铬
13.对下列实验现象进行的解释错误的是( )
选项
A
B
C
D
实验现象
用扫描隧道显微镜获得的分子图像
品红加入水中后,整杯液体变红色
水分子在不同温度下的运动情况
50
mL水与50
mL酒精混合后的体积小于100
mL
解释
分子的质量和体积都很小
分子总是在不断运动着
常温时分子不运动,加热时分子才运动
分子间有间隙
14.下列关于物质组成与构成的说法,不正确的是( )
A.原子中核外电子,特别是最外层电子,是决定原子构成物质的关键因素
B.原子在分子中的配置(原子的种类、数量和排列方式)决定了分子的种类
C.化学元素只有一百多种,却组成了所有的化学物质
D.原子得失电子变成离子后,元素的种类发生了改变
15.今有四种粒子的结构示意图,下列说法正确的是( )
(第15题)
A.它们表示四种元素
B.②对应的原子在化学反应中易失去电子
C.④表示的元素是非金属元素
D.①③表示的都是阳离子
二、填空题(47分)
16.(4分)从氮气、氧气、氖气、二氧化碳中,选择符合下列题意的气体填空:
(1)太空飞行人员需要携带的供给呼吸的气体是________。
(2)白炽灯泡内含有的气体是________。
(3)电工“测电笔”内充有的气体是________。
(4)植物光合作用需要的气体是________。
17.(8分)用微粒的观点回答下列问题:
(1)保持氧气化学性质的最小微粒是________。
(2)二氧化碳是由______________构成的。
(3)水通电分解过程中,不变的微粒是____________________。
(4)用湿抹布擦过的桌面,一段时间后变干的原因是________________________。
(5)一定质量的干冰升华,其体积变大的原因是____________________________。
18.(6分)学习化学后,我们学会了从微观角度认识物质。
(1)已知碳原子和氧原子的结构示意图分别为和,两种原子中相等的是________(填字母)。
A.质子数
B.电子数
C.第一层电子数
D.第二层电子数
(2)保持一氧化碳化学性质的粒子名称是______________。
(3)如图是一氧化碳与氧气反应生成二氧化碳的微观模型图,请在下图方框中以图示的方式完成该化学反应的微观过程(提示:图中“”表示氧原子,“”表示碳原子,反应前后原子个数不变)。
(第18题)
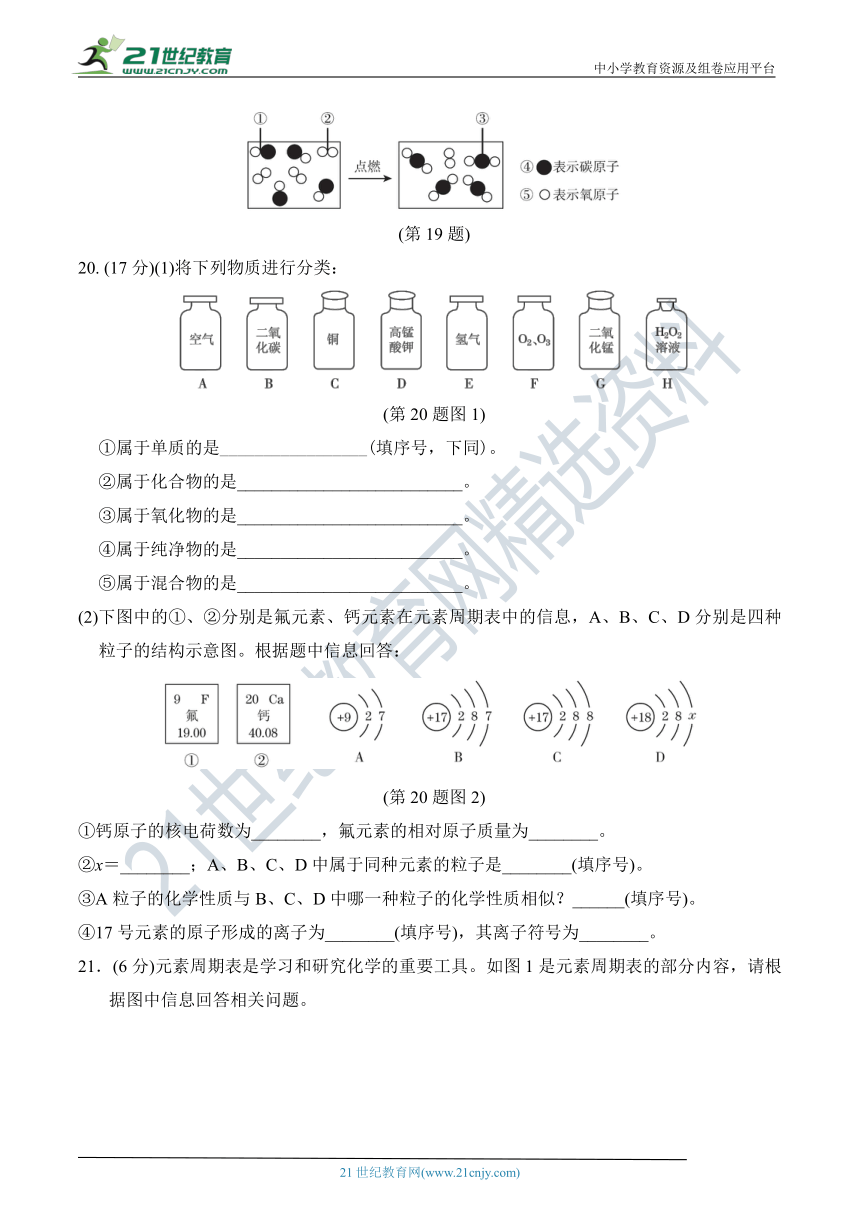
19.(6分)初中化学学习中,我们初步认识了物质的微观结构。
(1)氯化钠、金刚石、干冰三种物质中,由离子构成的物质是_________________。
(2)
是某粒子的结构示意图,该粒子在化学反应中容易________(填“得到”或“失去”)电子。
(3)如图是CO与O2反应的微观示意图,反应前后没有发生变化的粒子是________(填字母)。
A.①②
B.②③
C.③④
D.④⑤
(第19题)
20.
(17分)(1)将下列物质进行分类:
(第20题图1)
①属于单质的是_________________(填序号,下同)。
②属于化合物的是__________________________。
③属于氧化物的是__________________________。
④属于纯净物的是__________________________。
⑤属于混合物的是__________________________。
(2)下图中的①、②分别是氟元素、钙元素在元素周期表中的信息,A、B、C、D分别是四种粒子的结构示意图。根据题中信息回答:
(第20题图2)
①钙原子的核电荷数为________,氟元素的相对原子质量为________。
②x=________;A、B、C、D中属于同种元素的粒子是________(填序号)。
③A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似?______(填序号)。
④17号元素的原子形成的离子为________(填序号),其离子符号为________。
21.(6分)元素周期表是学习和研究化学的重要工具。如图1是元素周期表的部分内容,请根据图中信息回答相关问题。
(第21题)
(1)铍原子的相对原子质量是_______,它属于_______(填“金属”或“非金属”)元素。
(2)第三周期中含有的非金属元素共有________种。
(3)元素周期表的纵行叫作族,分为主族、副族、Ⅷ族和0族。主族用字母“A”来表示,共有七个主族,依次用ⅠA族、ⅡA族、ⅢA族、ⅣA族、VA族、ⅥA族、ⅦA族表示。同一主族元素化学性质相似。
①甲同学探究了同主族元素原子结构的共同点,提出将氦元素放在第ⅡA族,甲同学的依据是___________________________________________________;乙同学进行了反驳,认为氦元素属于0族元素的一种,乙同学的依据是_________________________________________________________________。
②硒元素是人体必需的微量元素之一,有防癌、抗癌的作用。硒原子结构示意图如图2所示,请你分析硒元素在元素周期表中的位置是第4周期、第________族。
三、探究实验题(23分)
22.(13分)某校化学兴趣小组就空气中氧气的含量进行实验探究:
【集体讨论】
(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其他成分反应,而且生成物为固体。他们应该选择________(填编号)。
A.蜡烛
B.红磷
为了充分消耗容器中的氧气,药品的用量应保证____________。
(2)小组同学共同设计了如图所示的两套装置,你认为合理的是_____(填编号)。为了确保实验成功,在装药品前应该_______________________________。
(第22题)
【分组实验】在讨论的基础上,他们分组进行了实验。
【数据分析】实验结束后,整理数据如下:(注:集气瓶容积为100
mL)
组别
1
2
3
4
5
6
进入集气瓶中水的体积(mL)
20
21
19
20
22
18
(3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的______。通过实验还可以推断集气瓶中剩余气体的性质是_____________________。
【实验拓展】
(4)小组的同学做完实验后又尝试用木炭重新做了以上实验,发现水几乎没有进入集气瓶。经讨论,同学们一致认为如果事先在集气瓶内注入少量的氢氧化钠溶液来吸收____________气体,实验也能取得较好的效果。
23.(10分)图Ⅰ是小红按课本进行的一个化学实验,在实验时同学们闻到了一股难闻的刺激性气味。于是小明对原实验装置进行了改进,装置如图Ⅱ所示。
(第23题)
【实验操作】a.向B、C、E三支试管中分别加入5
mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡,观察溶液颜色;
b.在A、D试管中分别加入2
mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。
【分析讨论】
(1)E试管放有酚酞溶液的目的是____________。
(2)进行操作b时观察到的现象是_____________________________________
______________________________________________________________。
(3)由此可以得到的实验结论是:①___________________________________;②___________________________________________________________。
(4)对比改进前的实验,改进后实验的优点是____________________________
______________________________________________________(写一条)。
参考答案
一、1.
A 2.
C 3.
C 4.
A 5.
B 6.
A
7.
C 点拨:水银和液态氧为单质,蒸馏水为化合物,空气为混合物。
8.
D 点拨:构成物质的微粒有分子、原子、离子等,如铁是由铁原子构成的,故A错误;原子是化学变化中的最小微粒,故B错误;元素的化学性质与原子的最外层电子数关系密切,故C错误;原子通过得失电子变成离子,故D正确。
9.
D 点拨:钚原子中,原子序数=质子数=核电荷数=核外电子数=94,中子数=239-94=145。
10.
C 点拨:实验前,应先检验装置的气密性,以防止装置漏气,造成测定结果不准确,A错误;红磷熄灭后,应冷却至室温后再打开止水夹,B错误;红磷与氧气在点燃的条件下反应生成五氧化二磷,D错误。
11.
C 点拨:冰是固态的水,水是由氢、氧两种元素组成的纯净物,为氧化物;过氧化氢是由氢、氧两种元素组成的化合物;洁净的空气中含有氮气、氧气、二氧化碳等多种物质,为混合物;液氮为液态的氮,是单质。
12.
D 点拨:铁的相对原子质量为55.
85,相对原子质量是一个比值,单位为“1”,常省略不写,A错误;锰元素为金属元素,B错误;在元素周期表中,元素名称左上角的数字表示原子序数,铬元素原子序数=质子数=24,C错误;相对原子质量反映了原子的实际质量,相对原子质量越大,原子的实际质量越大,由图可知,相对原子质量:铬<锰<铁,故等质量的铬、锰、铁中,含原子个数最多的是铬,D正确。
13.
C 点拨:分子总是在不停地运动着,加热时运动速率加快。
14.
D 点拨:原子的化学性质与最外层电子数关系密切,A正确;原子的种类、数量和排列方式决定了构成的分子种类,B正确;化学元素只有一百多种,但可组成多种化学物质,C正确;原子得失电子变成离子后,核外电子数改变,但质子数不变,元素种类不变,D不正确。
15.
B 点拨:决定元素种类的是质子数(即核电荷数),②和④核内质子数相同,属于同一种元素,图中共表示3种元素,A错误;②对应的原子最外层电子数是2,在化学反应中易失去2个电子而形成阳离子,B正确;④的核内质子数为12,为镁元素,属于金属元素,C错误;①质子数=8,核外电子数=10,质子数<核外电子数,为阴离子;③质子数=11,核外电子数=10,质子数>核外电子数,为阳离子,D错误。
二、16.
(1)氧气 (2)氮气 (3)氖气 (4)二氧化碳
17.
(1)氧分子 (2)二氧化碳分子 (3)氢原子、氧原子
(4)分子在不断地运动 (5)分子间间隔变大
18.
(1)C (2)一氧化碳分子 (3)
19.
(1)氯化钠 (2)失去 (3)D
20.
(1)①C、E ②B、D、G ③B、G ④B、C、D、E、G ⑤A、F、H
(2)①20;19.
00 ②8;B、C ③B ④C;Cl-
点拨:(1)A~H几种物质分别为混合物、化合物(氧化物)、单质、化合物、单质、混合物、化合物(氧化物)、混合物。(2)根据元素周期表中的信息,钙原子的核电荷数=原子序数=20,氟元素的相对原子质量为19.
00;原子中,核外电子数=核内质子数,则x=8;圆圈内的数字相等,质子数相同,属同种元素,即B、C属同种元素;原子最外层电子数相同的,化学性质相似,即A与B的化学性质相似;17号元素的一个原子容易得到1个电子达到相对稳定的结构,如C所示,即形成Cl-。
21.
(1)9.
012;金属 (2)5
(3)①氦元素原子最外层电子数是2;氦原子第一层也是最外层,达到了2个电子的稳定结构,化学性质不活泼 ②ⅥA
点拨:(1)铍原子的相对原子质量是9.
012,它属于金属元素。(2)第三周期中含有的非金属元素共有5种,即硅元素、磷元素、硫元素、氯元素、氩元素。(3)①甲同学研究了同主族元素原子结构的共同点,提出将氦元素放在第ⅡA族,甲同学的依据是氦元素原子最外层电子数是2;乙同学进行了反驳,认为氦元素属于0族元素的一种,乙同学的依据是氦原子第一层也是最外层,达到了2个电子的稳定结构,化学性质不活泼。②硒元素原子核外电子层数是4,最外层电子数是6,因此硒元素在元素周期表中的位置是第4周期、第ⅥA族。
三、22.
(1)B;足量(或过量)
(2)A;检查装置的气密性
(3)1/5;难溶于水、不助燃、不可燃等
(4)二氧化碳
23.
(1)进行对比
(2)B试管中的酚酞溶液慢慢变红色,C试管中的酚酞溶液很快变红色
(3)①分子客观存在,并总在不断运动着
②温度越高,分子运动速率越快
(4)能尽量防止氨气逸出污染空气,更能体现化学变化的过程(或能够说明分子运动的快慢与温度的关系等)
21世纪教育网
www.21cnjy.com
精品试卷·第
2
页
(共
2
页)
HYPERLINK
"http://21世纪教育网(www.21cnjy.com)
"
21世纪教育网(www.21cnjy.com)
科学版九年级化学上册
名校精选精练
第二章达标检测卷
(100分,90分钟)
班级:
姓名:
考号:
.
题 号
一
二
三
总 分
得 分
一、选择题(每题2分,共30分)
1.空气中含量较多且化学性质比较活泼的气体是( )
A.氧气
B.氮气
C.稀有气体
D.二氧化碳
2.影响元素化学性质的最主要因素是( )
A.原子的质子数
B.原子的电子层数
C.原子的最外层电子数
D.组成某种物质的原子个数
3.杜甫的绝句《沙暖睡鸳鸯》中写到“迟日江山丽,春风花草香”。诗中描写的情景用化学原理解释正确的是( )
A.分子很小,但分子有一定的质量
B.分子很小,但分子之间有间隔
C.分子很小,但分子在不停地运动着
D.分子很小,但分子是由原子构成的
4.薯片等易碎食品宜采用充气袋包装,下列气体中最不适宜充入的是( )
A.O2
B.N2
C.CO2
D.空气
5.不会造成空气污染的物质是( )
A.一氧化碳
B.水蒸气
C.烟尘
D.二氧化硫
6.空气是我们每天都呼吸的“生命气体”。下列说法错误的是( )
A.空气中氮气的质量分数为78%
B.空气中氧气能供给呼吸和支持燃烧
C.空气中二氧化碳是造成温室效应的主要气体
D.空气中的稀有气体所占比例虽小,但用途广泛
7.下列物质属于化合物的是( )
A.水银
B.液态氧
C.蒸馏水
D.空气
8.下列有关分子、原子、离子和元素的说法正确的是( )
A.原子不能直接构成物质
B.分子是化学变化中最小的微粒
C.决定元素化学性质的是原子的电子数
D.原子得到或失去电子变成离子
9.原子序数为94的钚是一种核原料,该元素一种原子的质子数和中子数之和为239,下列关于该原子的说法不正确的是( )
A.中子数为145
B.核外电子数为94
C.质子数为94
D.核电荷数为239
10.如图是“测定空气中氧气体积分数”的实验装置,关于该实验下列说法正确的是( )
(第10题)
A.不用考虑装置气密性是否良好
B.红磷火焰熄灭后立即打开止水夹
C.依据实验现象推测,氧气约占空气总体积的1/5
D.红磷燃烧的文字表达式为磷+氧气→五氧化二磷
11.下列有关物质的分类,错误的是( )
A.冰块和水混合属于氧化物
B.过氧化氢属于化合物
C.洁净的空气属于纯净物
D.液氮属于单质
12.元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分,下列有关说法正确的是( )
(第12题)
A.铁的相对原子质量为55.85
g
B.锰元素为非金属元素
C.铬原子的原子核内有52个质子
D.等质量的铬、锰、铁中,含原子个数最多的是铬
13.对下列实验现象进行的解释错误的是( )
选项
A
B
C
D
实验现象
用扫描隧道显微镜获得的分子图像
品红加入水中后,整杯液体变红色
水分子在不同温度下的运动情况
50
mL水与50
mL酒精混合后的体积小于100
mL
解释
分子的质量和体积都很小
分子总是在不断运动着
常温时分子不运动,加热时分子才运动
分子间有间隙
14.下列关于物质组成与构成的说法,不正确的是( )
A.原子中核外电子,特别是最外层电子,是决定原子构成物质的关键因素
B.原子在分子中的配置(原子的种类、数量和排列方式)决定了分子的种类
C.化学元素只有一百多种,却组成了所有的化学物质
D.原子得失电子变成离子后,元素的种类发生了改变
15.今有四种粒子的结构示意图,下列说法正确的是( )
(第15题)
A.它们表示四种元素
B.②对应的原子在化学反应中易失去电子
C.④表示的元素是非金属元素
D.①③表示的都是阳离子
二、填空题(47分)
16.(4分)从氮气、氧气、氖气、二氧化碳中,选择符合下列题意的气体填空:
(1)太空飞行人员需要携带的供给呼吸的气体是________。
(2)白炽灯泡内含有的气体是________。
(3)电工“测电笔”内充有的气体是________。
(4)植物光合作用需要的气体是________。
17.(8分)用微粒的观点回答下列问题:
(1)保持氧气化学性质的最小微粒是________。
(2)二氧化碳是由______________构成的。
(3)水通电分解过程中,不变的微粒是____________________。
(4)用湿抹布擦过的桌面,一段时间后变干的原因是________________________。
(5)一定质量的干冰升华,其体积变大的原因是____________________________。
18.(6分)学习化学后,我们学会了从微观角度认识物质。
(1)已知碳原子和氧原子的结构示意图分别为和,两种原子中相等的是________(填字母)。
A.质子数
B.电子数
C.第一层电子数
D.第二层电子数
(2)保持一氧化碳化学性质的粒子名称是______________。
(3)如图是一氧化碳与氧气反应生成二氧化碳的微观模型图,请在下图方框中以图示的方式完成该化学反应的微观过程(提示:图中“”表示氧原子,“”表示碳原子,反应前后原子个数不变)。
(第18题)
19.(6分)初中化学学习中,我们初步认识了物质的微观结构。
(1)氯化钠、金刚石、干冰三种物质中,由离子构成的物质是_________________。
(2)
是某粒子的结构示意图,该粒子在化学反应中容易________(填“得到”或“失去”)电子。
(3)如图是CO与O2反应的微观示意图,反应前后没有发生变化的粒子是________(填字母)。
A.①②
B.②③
C.③④
D.④⑤
(第19题)
20.
(17分)(1)将下列物质进行分类:
(第20题图1)
①属于单质的是_________________(填序号,下同)。
②属于化合物的是__________________________。
③属于氧化物的是__________________________。
④属于纯净物的是__________________________。
⑤属于混合物的是__________________________。
(2)下图中的①、②分别是氟元素、钙元素在元素周期表中的信息,A、B、C、D分别是四种粒子的结构示意图。根据题中信息回答:
(第20题图2)
①钙原子的核电荷数为________,氟元素的相对原子质量为________。
②x=________;A、B、C、D中属于同种元素的粒子是________(填序号)。
③A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似?______(填序号)。
④17号元素的原子形成的离子为________(填序号),其离子符号为________。
21.(6分)元素周期表是学习和研究化学的重要工具。如图1是元素周期表的部分内容,请根据图中信息回答相关问题。
(第21题)
(1)铍原子的相对原子质量是_______,它属于_______(填“金属”或“非金属”)元素。
(2)第三周期中含有的非金属元素共有________种。
(3)元素周期表的纵行叫作族,分为主族、副族、Ⅷ族和0族。主族用字母“A”来表示,共有七个主族,依次用ⅠA族、ⅡA族、ⅢA族、ⅣA族、VA族、ⅥA族、ⅦA族表示。同一主族元素化学性质相似。
①甲同学探究了同主族元素原子结构的共同点,提出将氦元素放在第ⅡA族,甲同学的依据是___________________________________________________;乙同学进行了反驳,认为氦元素属于0族元素的一种,乙同学的依据是_________________________________________________________________。
②硒元素是人体必需的微量元素之一,有防癌、抗癌的作用。硒原子结构示意图如图2所示,请你分析硒元素在元素周期表中的位置是第4周期、第________族。
三、探究实验题(23分)
22.(13分)某校化学兴趣小组就空气中氧气的含量进行实验探究:
【集体讨论】
(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其他成分反应,而且生成物为固体。他们应该选择________(填编号)。
A.蜡烛
B.红磷
为了充分消耗容器中的氧气,药品的用量应保证____________。
(2)小组同学共同设计了如图所示的两套装置,你认为合理的是_____(填编号)。为了确保实验成功,在装药品前应该_______________________________。
(第22题)
【分组实验】在讨论的基础上,他们分组进行了实验。
【数据分析】实验结束后,整理数据如下:(注:集气瓶容积为100
mL)
组别
1
2
3
4
5
6
进入集气瓶中水的体积(mL)
20
21
19
20
22
18
(3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的______。通过实验还可以推断集气瓶中剩余气体的性质是_____________________。
【实验拓展】
(4)小组的同学做完实验后又尝试用木炭重新做了以上实验,发现水几乎没有进入集气瓶。经讨论,同学们一致认为如果事先在集气瓶内注入少量的氢氧化钠溶液来吸收____________气体,实验也能取得较好的效果。
23.(10分)图Ⅰ是小红按课本进行的一个化学实验,在实验时同学们闻到了一股难闻的刺激性气味。于是小明对原实验装置进行了改进,装置如图Ⅱ所示。
(第23题)
【实验操作】a.向B、C、E三支试管中分别加入5
mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡,观察溶液颜色;
b.在A、D试管中分别加入2
mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。
【分析讨论】
(1)E试管放有酚酞溶液的目的是____________。
(2)进行操作b时观察到的现象是_____________________________________
______________________________________________________________。
(3)由此可以得到的实验结论是:①___________________________________;②___________________________________________________________。
(4)对比改进前的实验,改进后实验的优点是____________________________
______________________________________________________(写一条)。
参考答案
一、1.
A 2.
C 3.
C 4.
A 5.
B 6.
A
7.
C 点拨:水银和液态氧为单质,蒸馏水为化合物,空气为混合物。
8.
D 点拨:构成物质的微粒有分子、原子、离子等,如铁是由铁原子构成的,故A错误;原子是化学变化中的最小微粒,故B错误;元素的化学性质与原子的最外层电子数关系密切,故C错误;原子通过得失电子变成离子,故D正确。
9.
D 点拨:钚原子中,原子序数=质子数=核电荷数=核外电子数=94,中子数=239-94=145。
10.
C 点拨:实验前,应先检验装置的气密性,以防止装置漏气,造成测定结果不准确,A错误;红磷熄灭后,应冷却至室温后再打开止水夹,B错误;红磷与氧气在点燃的条件下反应生成五氧化二磷,D错误。
11.
C 点拨:冰是固态的水,水是由氢、氧两种元素组成的纯净物,为氧化物;过氧化氢是由氢、氧两种元素组成的化合物;洁净的空气中含有氮气、氧气、二氧化碳等多种物质,为混合物;液氮为液态的氮,是单质。
12.
D 点拨:铁的相对原子质量为55.
85,相对原子质量是一个比值,单位为“1”,常省略不写,A错误;锰元素为金属元素,B错误;在元素周期表中,元素名称左上角的数字表示原子序数,铬元素原子序数=质子数=24,C错误;相对原子质量反映了原子的实际质量,相对原子质量越大,原子的实际质量越大,由图可知,相对原子质量:铬<锰<铁,故等质量的铬、锰、铁中,含原子个数最多的是铬,D正确。
13.
C 点拨:分子总是在不停地运动着,加热时运动速率加快。
14.
D 点拨:原子的化学性质与最外层电子数关系密切,A正确;原子的种类、数量和排列方式决定了构成的分子种类,B正确;化学元素只有一百多种,但可组成多种化学物质,C正确;原子得失电子变成离子后,核外电子数改变,但质子数不变,元素种类不变,D不正确。
15.
B 点拨:决定元素种类的是质子数(即核电荷数),②和④核内质子数相同,属于同一种元素,图中共表示3种元素,A错误;②对应的原子最外层电子数是2,在化学反应中易失去2个电子而形成阳离子,B正确;④的核内质子数为12,为镁元素,属于金属元素,C错误;①质子数=8,核外电子数=10,质子数<核外电子数,为阴离子;③质子数=11,核外电子数=10,质子数>核外电子数,为阳离子,D错误。
二、16.
(1)氧气 (2)氮气 (3)氖气 (4)二氧化碳
17.
(1)氧分子 (2)二氧化碳分子 (3)氢原子、氧原子
(4)分子在不断地运动 (5)分子间间隔变大
18.
(1)C (2)一氧化碳分子 (3)
19.
(1)氯化钠 (2)失去 (3)D
20.
(1)①C、E ②B、D、G ③B、G ④B、C、D、E、G ⑤A、F、H
(2)①20;19.
00 ②8;B、C ③B ④C;Cl-
点拨:(1)A~H几种物质分别为混合物、化合物(氧化物)、单质、化合物、单质、混合物、化合物(氧化物)、混合物。(2)根据元素周期表中的信息,钙原子的核电荷数=原子序数=20,氟元素的相对原子质量为19.
00;原子中,核外电子数=核内质子数,则x=8;圆圈内的数字相等,质子数相同,属同种元素,即B、C属同种元素;原子最外层电子数相同的,化学性质相似,即A与B的化学性质相似;17号元素的一个原子容易得到1个电子达到相对稳定的结构,如C所示,即形成Cl-。
21.
(1)9.
012;金属 (2)5
(3)①氦元素原子最外层电子数是2;氦原子第一层也是最外层,达到了2个电子的稳定结构,化学性质不活泼 ②ⅥA
点拨:(1)铍原子的相对原子质量是9.
012,它属于金属元素。(2)第三周期中含有的非金属元素共有5种,即硅元素、磷元素、硫元素、氯元素、氩元素。(3)①甲同学研究了同主族元素原子结构的共同点,提出将氦元素放在第ⅡA族,甲同学的依据是氦元素原子最外层电子数是2;乙同学进行了反驳,认为氦元素属于0族元素的一种,乙同学的依据是氦原子第一层也是最外层,达到了2个电子的稳定结构,化学性质不活泼。②硒元素原子核外电子层数是4,最外层电子数是6,因此硒元素在元素周期表中的位置是第4周期、第ⅥA族。
三、22.
(1)B;足量(或过量)
(2)A;检查装置的气密性
(3)1/5;难溶于水、不助燃、不可燃等
(4)二氧化碳
23.
(1)进行对比
(2)B试管中的酚酞溶液慢慢变红色,C试管中的酚酞溶液很快变红色
(3)①分子客观存在,并总在不断运动着
②温度越高,分子运动速率越快
(4)能尽量防止氨气逸出污染空气,更能体现化学变化的过程(或能够说明分子运动的快慢与温度的关系等)
21世纪教育网
www.21cnjy.com
精品试卷·第
2
页
(共
2
页)
HYPERLINK
"http://21世纪教育网(www.21cnjy.com)
"
21世纪教育网(www.21cnjy.com)
同课章节目录
