2020-2021学年人教版九年级化学下册 8.2 金属的化学性质 同步练习卷(无答案)
文档属性
| 名称 | 2020-2021学年人教版九年级化学下册 8.2 金属的化学性质 同步练习卷(无答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 275.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-02 00:00:00 | ||
图片预览


文档简介
2020-2021学年人教版九年级化学下册
8.2
金属的化学性质同步练习卷
题号
一
二
三
四
五
总分
得分
一、单选题(本大题共16小题,共32分)
金属不具有的物理共性是?
?
A.
银白色光泽
B.
导热性
C.
延展性
D.
导电性
下列说法错误的是
A.
生铁是铁的合金
B.
铁可以在空气中燃烧
C.
铁和盐酸反应生氯化亚铁和氢气
D.
铁在潮湿的空气中会生锈
现有甲、乙、丙三种金属,将乙放入甲的硫酸盐溶液中,无明显变化;将乙、丙分别放入硝酸银溶液中,丙表面有固体析出,乙无明显变化。下列说法正确的是
A.
甲在空气中一定易被腐蚀
B.
将丙放入稀硫酸中一定会产生气泡
C.
乙在自然界中可以单质形式存在
D.
三种金属的活动性顺序为甲乙丙
在描述实验现象时,其中正确的是
A.
点燃混有空气的氢气时,安静燃烧,发出淡蓝色火焰并放出大量的热
B.
电解水时,两电极产生气泡,且负极气体是正极气体体积的2倍
C.
镁条在空气中燃烧时,发出耀眼的白光,生成白色粉末MgO
D.
红磷在空气中燃烧时,产生大量白雾,并放热
把一根洁净的没生锈的铁钉放入硫酸铜溶液中,下列实验现象叙述正确的是
A.
在铁钉表面产生气泡
B.
溶液由蓝色立即变为黄色
C.
铁钉表面有红色固体生成
D.
生成了硫酸亚铁
某同学为验证铁、铜、银三种金属的活动性顺序,他设计了以下四种实验方案,其中能达到目的的是
A.
将Fe丝、Cu丝分别放入溶液中
B.
将Fe丝、Cu丝、Ag丝分别放入稀盐酸中
C.
将Fe丝分别放入溶液、溶液中
D.
将Fe丝、Ag丝分别放入溶液中
运用推理、归纳、类比、对比的方法得出下列结论,其中合理的是
A.
二氧化碳和一氧化碳的组成元素相同,则两者的化学性质相同
B.
铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀
C.
活泼金属与酸反应放出气体,所以与酸反应放出气体的物质一定是活泼金属
D.
氯化铵与碱混合研磨放出氨气,硫酸铵与碱混合研磨也能放出氨气
向、的混合溶液中加入一定量的锌粉,充分反应后过滤,向滤液中滴加稀盐酸有白色沉淀产生.下列说法中,正确的是
A.
所得滤液中可能含有
B.
所得滤渣中可能含有铜和锌
C.
所得滤液中一定含有、、
D.
所得滤渣中一定含有银和铜
用盐酸与金属单质反应,探究锌、镁、铜的金属活动性。下列有关现象、分析或结论正确的是
A.
金属活动性由强到弱顺序为:镁锌铜
B.
锌片的试管比镁片的试管更热
C.
铜片表面可以观察到气泡
D.
三支试管中盐酸溶液的质量分数可以不同
金属钠与水反应剧烈,有气体生成,收集气体并点燃,有明显爆鸣声。该气?体可能是
A.
氢气
B.
氧气
C.
一氧化碳
D.
甲烷
小明笔记中有处错误你认为是图中的哪一处
A.
a处
B.
b?处
C.
c处
D.
d?处
有X、Y、Z三种金属片,分别放入稀硫酸中,X、Z表面有气泡产生,Y没有明显现象;X放入溶液,没有明显现象。判断这三种金属的活动性由强到弱的顺序是
A.
B.
C.
D.
能验证Zn、Cu、Ag三种金属活动性顺序的是
A.
Zn、Ag、溶液
B.
Zn、Cu、Ag、稀盐酸
C.
Cu、Ag、溶液
D.
Ag、溶液、溶液
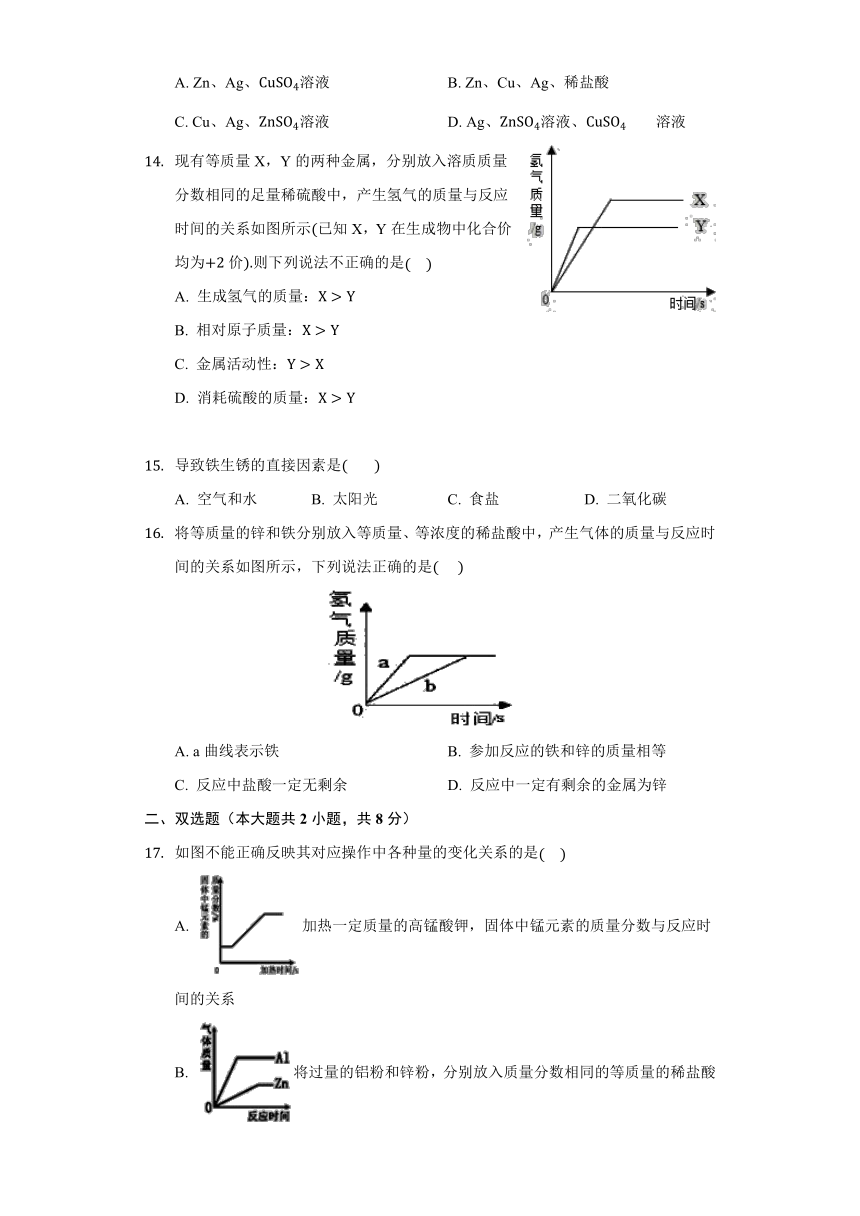
现有等质量X,Y的两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示已知X,Y在生成物中化合价均为价则下列说法不正确的是
A.
生成氢气的质量:
B.
相对原子质量:
C.
金属活动性:
D.
消耗硫酸的质量:
导致铁生锈的直接因素是?
?
?
A.
空气和水
B.
太阳光
C.
食盐
D.
二氧化碳
将等质量的锌和铁分别放入等质量、等浓度的稀盐酸中,产生气体的质量与反应时间的关系如图所示,下列说法正确的是???
A.
a曲线表示铁
B.
参加反应的铁和锌的质量相等
C.
反应中盐酸一定无剩余
D.
反应中一定有剩余的金属为锌
二、双选题(本大题共2小题,共8分)
如图不能正确反映其对应操作中各种量的变化关系的是
A.
加热一定质量的高锰酸钾,固体中锰元素的质量分数与反应时间的关系
B.
将过量的铝粉和锌粉,分别放入质量分数相同的等质量的稀盐酸中,生成气体质量与反应时间的关系
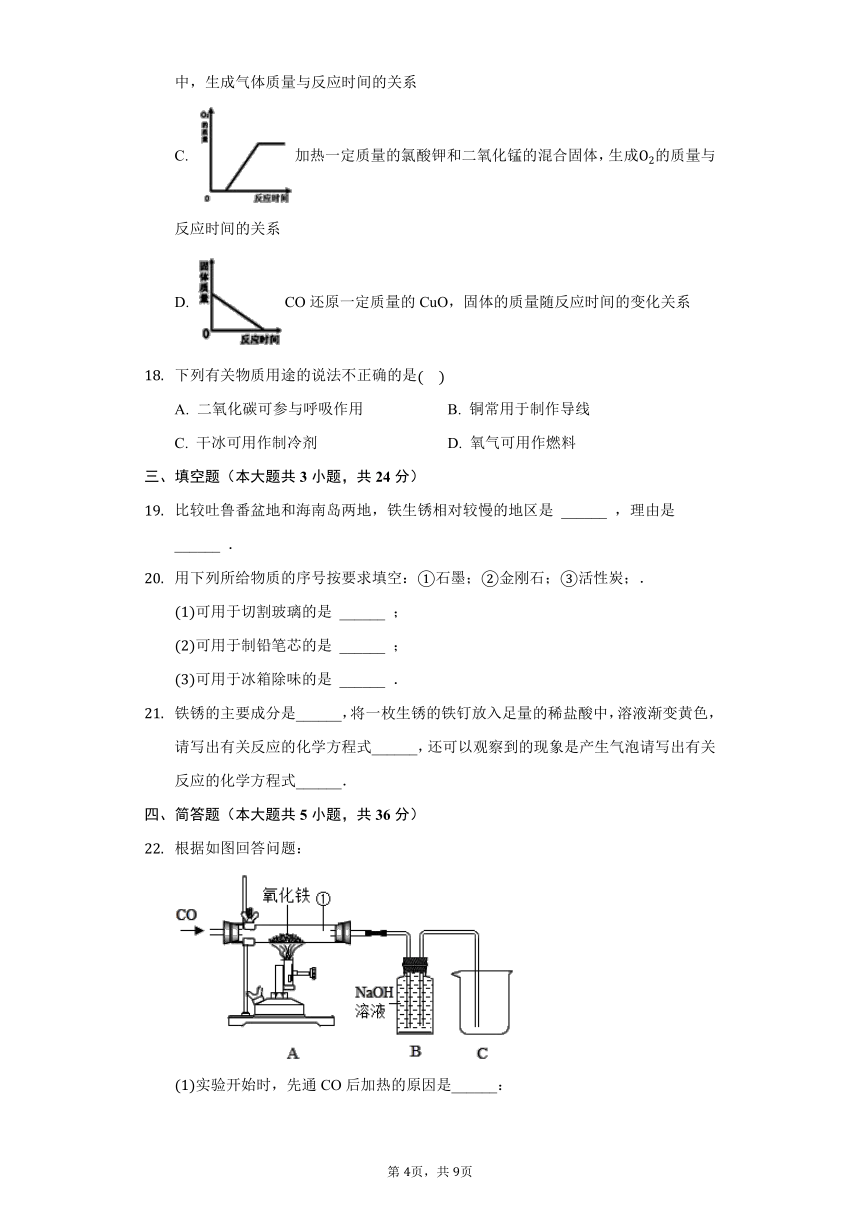
C.
加热一定质量的氯酸钾和二氧化锰的混合固体,生成的质量与反应时间的关系
D.
CO还原一定质量的CuO,固体的质量随反应时间的变化关系
下列有关物质用途的说法不正确的是
A.
二氧化碳可参与呼吸作用
B.
铜常用于制作导线
C.
干冰可用作制冷剂
D.
氧气可用作燃料
三、填空题(本大题共3小题,共24分)
比较吐鲁番盆地和海南岛两地,铁生锈相对较慢的地区是
______
,理由是
______
.
用下列所给物质的序号按要求填空:石墨;金刚石;活性炭;.
可用于切割玻璃的是
______
;
可用于制铅笔芯的是
______
;
可用于冰箱除味的是
______
.
铁锈的主要成分是______,将一枚生锈的铁钉放入足量的稀盐酸中,溶液渐变黄色,请写出有关反应的化学方程式______,还可以观察到的现象是产生气泡请写出有关反应的化学方程式______.
四、简答题(本大题共5小题,共36分)
根据如图回答问题:
实验开始时,先通CO后加热的原因是______:
加热一段时间后玻璃管内的现象是______,反应的化学方程式为______
你认为该装置是否需要添加尾气处理装置并说明理由______
2019年12月1日,阜阳高铁正式通车,实现了我市地下交通的新突破。根据下图回答下列问题:
图中所示材料中,属于金属材料的是__________填一种即可,下同;石墨电刷的使用主要利用其__________性。
轨道交通的发展与炼钢工艺的发展密不可分,钢和生铁都是铁的合金,它们的区别在于钢的含碳量_______填“高于”或“低于”生铁。合金跟纯金属相比,其组成和内部结构发生变化,从而引起________的变化填一条物理性质即可。
常温下,铝耐腐蚀的原因_________________________________________
向、、的混合溶液中加入一定量的锌粉,充分反应后过滤,向滤渣中加入稀盐酸有气泡产生,则滤渣中一定含有的物质是______,写出一个反应后溶液质量减少的化学方程式______。
如图是实验室模拟工业炼铁的装置图。
写出硬质玻璃管内产生的现象______及反应的化学方程式______。
实验开始时要先通入CO,把装置中的空气排尽后再加热,以防发生爆炸。检验装置中的空气已排尽的方法是______。
高炉炼铁中,焦炭的两个作用是______、______用化学方程式表示。
现有平板电视显示屏工厂生产过程中丢弃废玻璃粉末含、、等物质,某课题组以此粉末为原料回收铈和硫酸亚铁晶体,设计实验流程如下:
资料1:是一种金属氧化物,化学性质稳定,与稀硫酸不反应。在存在的条件下,两种物质能反应。
资料2:容易被空气中的氧化。
写出反应的化学方程式______;该反应类型为______反应;为提高中硫酸的反应效率,可采用的具体措施有______。写一种即可
将中所得溶液在氮气环境中蒸发浓缩、______、过滤,得到晶体,其中氮气的作用是______。
请补充完整反应的化学方程式:____________,滤渣B的主要成分是______。
生产过程中可循环利用的物质是______。
某兴趣小组同学用如图所示装置测定铜锌合金中铜的质量分数。
【实验准备】
将铜锌合金用砂纸打磨,其目的是______;
【实验步骤】
实验操作有:
记录量气管D的液面位置;
检查气密性,将药品和水装入各仪器中,连接好装置;
待B中不再有气体产生并恢复至室温后,记录量气管D的液面位置;
由A向B中滴加足量试剂;
将B中剩余固体过滤,洗涤,干燥,称重。
上述进行的操作的顺序是______填序号
中发生反应的化学方程式为______。
【定量计算】
若实验中,打磨后铜锌合金样品质量为5g,与稀硫酸充分反应后,测得产生的气体体积为,该条件下氢气的密度为,则生成氢气的质量为______结果保留两位小数;合金中铜的质量分数为多少?写出计算过程。
【分析讨论】
小组同学交流发现上述方法测得的铜的质量分数会偏小,则下列选项中可能的原因有______。
A.剩余固体中仍含有未反应的锌
B.生成氢气的体积包含了加入的稀硫酸体积
C.由于稀硫酸与锌粒反应放热,生成气体的温度高于常温,没有等气体恢复至室温就开始读数
D.反应后读数时,量气管液面高度高于左侧球形干燥管内液面的高度
有一无色气体,可能是由CO、、水蒸气中的一种或多种组成。为确定其组成,小明同学按下列方案进行实验,请回答下列问题:
若观察到A中黑色固体变红,B中无水硫酸铜不变色,则C中的现象为______以上现象说明原无色气体中一定不含______;写出装置A中的化学反应方程式______。
若观察到A中黑色固体变红,B中无水硫酸铜变蓝,C中澄清石灰水变浑浊,写出C装置中的化学反应方程式______。由此现象,并不能确定原无色气体中有水蒸气,理由是______。
从保护环境的角度分析,本实验的不足是______。
某校化学兴趣小组同学对甲烷燃烧的产物产生了兴趣,请你参与:
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】含碳元素的物质完全燃烧生成,不完全燃烧生成CO;无水遇水变蓝。
【猜想与假设】甲:????乙:CO??????丙:???丁:?CO??
你认为______同学的猜想是错误的,理由是______。
【实验探究】为了验证上述猜想与假设,将甲烷在一定量的中燃烧的产物依次通过下列装置:
、B装置的顺序能否颠倒?______填“能”或“否”。
实验中用纯净而不用空气的原因是______。
实验中观察到A中无水变蓝,B、D中澄清石灰水变浑浊,C中黑色粉末变成红色,由此推断______同学猜想成立。
请写出C中黑色粉末变成红色的化学方程式:______。
大气球的作用是______。
学习合金知识后,知道了不锈钢中含有金属铬。某同学想:铬与常见铁、铜相比,其金属活动性强弱如何呢?于是,和同学们一起进行了以下探究。
【查阅资料】铬是银白色有光泽的金属,在空气中,像铝一样,其表面能产生致密的氧化膜:能与稀硫酸反应,生成硫酸亚铬。
【知识回顾】金属活动性顺序:K?Ca?Na?Mg?Al?Zn______Sn?______Hg?Ag?Pt?在横线上填写对应金属的元素符号
【作出猜想】猜想;猜想;猜想______。
【设计与实验】张明同学取大小相等的铁、铜、铬三种金属片,未经打磨就分别放入等量等浓度的稀硫酸中,记录如下:
实验操作
铁片放在稀硫酸中
铜片放在稀硫酸中
铬片放在稀硫酸中
开始的现象
有少量气泡产生
无气泡
无气泡
结论
金属活动性强弱:??
李红同学也取大小相等的铁、铜、铬三种金属片,先用砂纸打磨后再分别放入等量等浓度的稀硫酸中,记录如下:
实验操作
铁片放在稀硫酸中
铜片放在稀硫酸中
铬片放在稀硫酸中
开始的现象
产生少量气泡
无气泡
产生大量气泡
结论
金属活动性强弱:
______
______
______
填元素符号
【讨论交流】为什么张明和李红两个同学记录的铬与稀硫酸反应开始的现象截然不同?原因是______。
【实验验证】为了进一步确认铁、铜、铬三种金属的活动性强弱,刘斌同学将打磨过的两块铁片分别放入硫酸亚铬溶液和硫酸铜溶液中,观察到在硫酸亚铬溶液中无明显现象,而在硫酸铜溶液中有明显的现象是______,其反应的化学方程式是______。
【拓展迁移】写出铬与稀硫酸反应,生成的化学反应方程式______。
金属材料在生产生活中有广泛的用途。
用镍钛合金制成的飞船天线在低温下折叠,进入太空后经太阳光照射可重新展开恢复原状。关于此天线制作材料的表述错误的是______
A.具有良好的导电性??
化学性质非常活泼
C.具有形状记忆功能?
具有良好的延展性
考古工作者发现铁质的出土文物往往锈蚀严重。铁生锈的条件是______。
将一包银粉和锌粉的混合物放入一定量的硫酸铜溶液中,充分反应后过滤。
写出发生反应的化学方程式______。
若向滤渣中加入稀盐酸有气泡生成,则该反应的化学方程式为______。
若滤液为蓝色,则滤液中一定含有的金属离子是______写离子符号。
如图为实验室模拟工业上炼铁的原理。当观察到______现象时,即证明该反应已经结束,可停止加热。该装置末端酒精灯的作用是______。
生铁是由含铁的矿石冶炼得到的。要炼得含铁的生铁500t,需要氧化铁的质量是多少?
第8页,共9页
8.2
金属的化学性质同步练习卷
题号
一
二
三
四
五
总分
得分
一、单选题(本大题共16小题,共32分)
金属不具有的物理共性是?
?
A.
银白色光泽
B.
导热性
C.
延展性
D.
导电性
下列说法错误的是
A.
生铁是铁的合金
B.
铁可以在空气中燃烧
C.
铁和盐酸反应生氯化亚铁和氢气
D.
铁在潮湿的空气中会生锈
现有甲、乙、丙三种金属,将乙放入甲的硫酸盐溶液中,无明显变化;将乙、丙分别放入硝酸银溶液中,丙表面有固体析出,乙无明显变化。下列说法正确的是
A.
甲在空气中一定易被腐蚀
B.
将丙放入稀硫酸中一定会产生气泡
C.
乙在自然界中可以单质形式存在
D.
三种金属的活动性顺序为甲乙丙
在描述实验现象时,其中正确的是
A.
点燃混有空气的氢气时,安静燃烧,发出淡蓝色火焰并放出大量的热
B.
电解水时,两电极产生气泡,且负极气体是正极气体体积的2倍
C.
镁条在空气中燃烧时,发出耀眼的白光,生成白色粉末MgO
D.
红磷在空气中燃烧时,产生大量白雾,并放热
把一根洁净的没生锈的铁钉放入硫酸铜溶液中,下列实验现象叙述正确的是
A.
在铁钉表面产生气泡
B.
溶液由蓝色立即变为黄色
C.
铁钉表面有红色固体生成
D.
生成了硫酸亚铁
某同学为验证铁、铜、银三种金属的活动性顺序,他设计了以下四种实验方案,其中能达到目的的是
A.
将Fe丝、Cu丝分别放入溶液中
B.
将Fe丝、Cu丝、Ag丝分别放入稀盐酸中
C.
将Fe丝分别放入溶液、溶液中
D.
将Fe丝、Ag丝分别放入溶液中
运用推理、归纳、类比、对比的方法得出下列结论,其中合理的是
A.
二氧化碳和一氧化碳的组成元素相同,则两者的化学性质相同
B.
铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀
C.
活泼金属与酸反应放出气体,所以与酸反应放出气体的物质一定是活泼金属
D.
氯化铵与碱混合研磨放出氨气,硫酸铵与碱混合研磨也能放出氨气
向、的混合溶液中加入一定量的锌粉,充分反应后过滤,向滤液中滴加稀盐酸有白色沉淀产生.下列说法中,正确的是
A.
所得滤液中可能含有
B.
所得滤渣中可能含有铜和锌
C.
所得滤液中一定含有、、
D.
所得滤渣中一定含有银和铜
用盐酸与金属单质反应,探究锌、镁、铜的金属活动性。下列有关现象、分析或结论正确的是
A.
金属活动性由强到弱顺序为:镁锌铜
B.
锌片的试管比镁片的试管更热
C.
铜片表面可以观察到气泡
D.
三支试管中盐酸溶液的质量分数可以不同
金属钠与水反应剧烈,有气体生成,收集气体并点燃,有明显爆鸣声。该气?体可能是
A.
氢气
B.
氧气
C.
一氧化碳
D.
甲烷
小明笔记中有处错误你认为是图中的哪一处
A.
a处
B.
b?处
C.
c处
D.
d?处
有X、Y、Z三种金属片,分别放入稀硫酸中,X、Z表面有气泡产生,Y没有明显现象;X放入溶液,没有明显现象。判断这三种金属的活动性由强到弱的顺序是
A.
B.
C.
D.
能验证Zn、Cu、Ag三种金属活动性顺序的是
A.
Zn、Ag、溶液
B.
Zn、Cu、Ag、稀盐酸
C.
Cu、Ag、溶液
D.
Ag、溶液、溶液
现有等质量X,Y的两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示已知X,Y在生成物中化合价均为价则下列说法不正确的是
A.
生成氢气的质量:
B.
相对原子质量:
C.
金属活动性:
D.
消耗硫酸的质量:
导致铁生锈的直接因素是?
?
?
A.
空气和水
B.
太阳光
C.
食盐
D.
二氧化碳
将等质量的锌和铁分别放入等质量、等浓度的稀盐酸中,产生气体的质量与反应时间的关系如图所示,下列说法正确的是???
A.
a曲线表示铁
B.
参加反应的铁和锌的质量相等
C.
反应中盐酸一定无剩余
D.
反应中一定有剩余的金属为锌
二、双选题(本大题共2小题,共8分)
如图不能正确反映其对应操作中各种量的变化关系的是
A.
加热一定质量的高锰酸钾,固体中锰元素的质量分数与反应时间的关系
B.
将过量的铝粉和锌粉,分别放入质量分数相同的等质量的稀盐酸中,生成气体质量与反应时间的关系
C.
加热一定质量的氯酸钾和二氧化锰的混合固体,生成的质量与反应时间的关系
D.
CO还原一定质量的CuO,固体的质量随反应时间的变化关系
下列有关物质用途的说法不正确的是
A.
二氧化碳可参与呼吸作用
B.
铜常用于制作导线
C.
干冰可用作制冷剂
D.
氧气可用作燃料
三、填空题(本大题共3小题,共24分)
比较吐鲁番盆地和海南岛两地,铁生锈相对较慢的地区是
______
,理由是
______
.
用下列所给物质的序号按要求填空:石墨;金刚石;活性炭;.
可用于切割玻璃的是
______
;
可用于制铅笔芯的是
______
;
可用于冰箱除味的是
______
.
铁锈的主要成分是______,将一枚生锈的铁钉放入足量的稀盐酸中,溶液渐变黄色,请写出有关反应的化学方程式______,还可以观察到的现象是产生气泡请写出有关反应的化学方程式______.
四、简答题(本大题共5小题,共36分)
根据如图回答问题:
实验开始时,先通CO后加热的原因是______:
加热一段时间后玻璃管内的现象是______,反应的化学方程式为______
你认为该装置是否需要添加尾气处理装置并说明理由______
2019年12月1日,阜阳高铁正式通车,实现了我市地下交通的新突破。根据下图回答下列问题:
图中所示材料中,属于金属材料的是__________填一种即可,下同;石墨电刷的使用主要利用其__________性。
轨道交通的发展与炼钢工艺的发展密不可分,钢和生铁都是铁的合金,它们的区别在于钢的含碳量_______填“高于”或“低于”生铁。合金跟纯金属相比,其组成和内部结构发生变化,从而引起________的变化填一条物理性质即可。
常温下,铝耐腐蚀的原因_________________________________________
向、、的混合溶液中加入一定量的锌粉,充分反应后过滤,向滤渣中加入稀盐酸有气泡产生,则滤渣中一定含有的物质是______,写出一个反应后溶液质量减少的化学方程式______。
如图是实验室模拟工业炼铁的装置图。
写出硬质玻璃管内产生的现象______及反应的化学方程式______。
实验开始时要先通入CO,把装置中的空气排尽后再加热,以防发生爆炸。检验装置中的空气已排尽的方法是______。
高炉炼铁中,焦炭的两个作用是______、______用化学方程式表示。
现有平板电视显示屏工厂生产过程中丢弃废玻璃粉末含、、等物质,某课题组以此粉末为原料回收铈和硫酸亚铁晶体,设计实验流程如下:
资料1:是一种金属氧化物,化学性质稳定,与稀硫酸不反应。在存在的条件下,两种物质能反应。
资料2:容易被空气中的氧化。
写出反应的化学方程式______;该反应类型为______反应;为提高中硫酸的反应效率,可采用的具体措施有______。写一种即可
将中所得溶液在氮气环境中蒸发浓缩、______、过滤,得到晶体,其中氮气的作用是______。
请补充完整反应的化学方程式:____________,滤渣B的主要成分是______。
生产过程中可循环利用的物质是______。
某兴趣小组同学用如图所示装置测定铜锌合金中铜的质量分数。
【实验准备】
将铜锌合金用砂纸打磨,其目的是______;
【实验步骤】
实验操作有:
记录量气管D的液面位置;
检查气密性,将药品和水装入各仪器中,连接好装置;
待B中不再有气体产生并恢复至室温后,记录量气管D的液面位置;
由A向B中滴加足量试剂;
将B中剩余固体过滤,洗涤,干燥,称重。
上述进行的操作的顺序是______填序号
中发生反应的化学方程式为______。
【定量计算】
若实验中,打磨后铜锌合金样品质量为5g,与稀硫酸充分反应后,测得产生的气体体积为,该条件下氢气的密度为,则生成氢气的质量为______结果保留两位小数;合金中铜的质量分数为多少?写出计算过程。
【分析讨论】
小组同学交流发现上述方法测得的铜的质量分数会偏小,则下列选项中可能的原因有______。
A.剩余固体中仍含有未反应的锌
B.生成氢气的体积包含了加入的稀硫酸体积
C.由于稀硫酸与锌粒反应放热,生成气体的温度高于常温,没有等气体恢复至室温就开始读数
D.反应后读数时,量气管液面高度高于左侧球形干燥管内液面的高度
有一无色气体,可能是由CO、、水蒸气中的一种或多种组成。为确定其组成,小明同学按下列方案进行实验,请回答下列问题:
若观察到A中黑色固体变红,B中无水硫酸铜不变色,则C中的现象为______以上现象说明原无色气体中一定不含______;写出装置A中的化学反应方程式______。
若观察到A中黑色固体变红,B中无水硫酸铜变蓝,C中澄清石灰水变浑浊,写出C装置中的化学反应方程式______。由此现象,并不能确定原无色气体中有水蒸气,理由是______。
从保护环境的角度分析,本实验的不足是______。
某校化学兴趣小组同学对甲烷燃烧的产物产生了兴趣,请你参与:
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】含碳元素的物质完全燃烧生成,不完全燃烧生成CO;无水遇水变蓝。
【猜想与假设】甲:????乙:CO??????丙:???丁:?CO??
你认为______同学的猜想是错误的,理由是______。
【实验探究】为了验证上述猜想与假设,将甲烷在一定量的中燃烧的产物依次通过下列装置:
、B装置的顺序能否颠倒?______填“能”或“否”。
实验中用纯净而不用空气的原因是______。
实验中观察到A中无水变蓝,B、D中澄清石灰水变浑浊,C中黑色粉末变成红色,由此推断______同学猜想成立。
请写出C中黑色粉末变成红色的化学方程式:______。
大气球的作用是______。
学习合金知识后,知道了不锈钢中含有金属铬。某同学想:铬与常见铁、铜相比,其金属活动性强弱如何呢?于是,和同学们一起进行了以下探究。
【查阅资料】铬是银白色有光泽的金属,在空气中,像铝一样,其表面能产生致密的氧化膜:能与稀硫酸反应,生成硫酸亚铬。
【知识回顾】金属活动性顺序:K?Ca?Na?Mg?Al?Zn______Sn?______Hg?Ag?Pt?在横线上填写对应金属的元素符号
【作出猜想】猜想;猜想;猜想______。
【设计与实验】张明同学取大小相等的铁、铜、铬三种金属片,未经打磨就分别放入等量等浓度的稀硫酸中,记录如下:
实验操作
铁片放在稀硫酸中
铜片放在稀硫酸中
铬片放在稀硫酸中
开始的现象
有少量气泡产生
无气泡
无气泡
结论
金属活动性强弱:??
李红同学也取大小相等的铁、铜、铬三种金属片,先用砂纸打磨后再分别放入等量等浓度的稀硫酸中,记录如下:
实验操作
铁片放在稀硫酸中
铜片放在稀硫酸中
铬片放在稀硫酸中
开始的现象
产生少量气泡
无气泡
产生大量气泡
结论
金属活动性强弱:
______
______
______
填元素符号
【讨论交流】为什么张明和李红两个同学记录的铬与稀硫酸反应开始的现象截然不同?原因是______。
【实验验证】为了进一步确认铁、铜、铬三种金属的活动性强弱,刘斌同学将打磨过的两块铁片分别放入硫酸亚铬溶液和硫酸铜溶液中,观察到在硫酸亚铬溶液中无明显现象,而在硫酸铜溶液中有明显的现象是______,其反应的化学方程式是______。
【拓展迁移】写出铬与稀硫酸反应,生成的化学反应方程式______。
金属材料在生产生活中有广泛的用途。
用镍钛合金制成的飞船天线在低温下折叠,进入太空后经太阳光照射可重新展开恢复原状。关于此天线制作材料的表述错误的是______
A.具有良好的导电性??
化学性质非常活泼
C.具有形状记忆功能?
具有良好的延展性
考古工作者发现铁质的出土文物往往锈蚀严重。铁生锈的条件是______。
将一包银粉和锌粉的混合物放入一定量的硫酸铜溶液中,充分反应后过滤。
写出发生反应的化学方程式______。
若向滤渣中加入稀盐酸有气泡生成,则该反应的化学方程式为______。
若滤液为蓝色,则滤液中一定含有的金属离子是______写离子符号。
如图为实验室模拟工业上炼铁的原理。当观察到______现象时,即证明该反应已经结束,可停止加热。该装置末端酒精灯的作用是______。
生铁是由含铁的矿石冶炼得到的。要炼得含铁的生铁500t,需要氧化铁的质量是多少?
第8页,共9页
同课章节目录
