山东省威海市11-12学年高二上学期期末考试 化学试题
文档属性
| 名称 | 山东省威海市11-12学年高二上学期期末考试 化学试题 |

|
|
| 格式 | zip | ||
| 文件大小 | 442.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-02-12 00:00:00 | ||
图片预览



文档简介
高二化学
本试卷分第I卷(选择题)和第II卷(非选择题)两部分,第I卷1至4页,第II卷5至8页。考试结束后,将答题卡交回。
第I卷(选择题 共46分)
注意事项:
1.答第Ⅰ卷前,将自己的姓名、考试号、考试科目涂写在答题卡上。
2.每题选出答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其他答案标号,不能答在试题上。
可能用到的相对原子质量:H 1 C 12 O 16 N 14 S 32 Cu 64 Zn 65 Br 80
I 127 Pb 207
一、选择题(本题包括18小题,1-8题每小题2分,9-18题每小题3分,共46分。每小题只有1个选项符合题意)
1.为保护环境,提高人类生存质量,各级政府大力发展绿色食品,避免“白色污染”。绿色食
品和“白色污染”是指
A.安全、无公害的营养食品和聚乙烯等白色塑料垃圾
B.绿颜色的食品和白色建筑废料
C.有叶绿素的食品和石灰窑的白色粉末
D.经济附加值高的营养食品和冶炼厂的白色烟尘
2. 建筑装潢质量的问题之一是装潢装饰材料中某些化学成分含量太高,缓慢释放出来,在空气中浓度过高,影响人体健康。这某些化学成分主要是
A.甲烷 B.乙烯
C.乙炔 D.甲醛、甲苯等有机物蒸气
3.正丁烷与2--甲基丙烷属于
A.同位素 B.同素异形体
C.同分异构体 D.同系物
4.下列各组液体混合物,用分液漏斗能分开的是
A.苯和甲苯 B.甘油和乙醇
C.乙酸乙酯和乙酸 D.正已烷和水
5.下列各组反应,实质都是取代反应的是
异戊二烯生成聚异戊二烯,酚醛树脂的生成
乙醇和氢卤酸反应,乙醇和浓硫酸加热至140℃时的反应,酯的水解
淀粉在硫酸存在下制葡萄糖,皂化反应,油脂的硬化
D.纤维素水解,浓硫酸和乙醇在170℃时的反应,蛋白质水解
6.下列说法中错误的是
A.在热化学方程式中无论反应物还是生成物必须标明聚集状态
B.热化学方程式的化学计量数不能表示分子的个数
C.反应热指的是反应过程中放出的热量
D.所有的化学反应都伴随着能量的变化
7.某小组为研究电化学原理,设计如图装置。下列叙述正确的是
A.a和b不连接时,铁片上不会有金属铜析出
B.a和b用导线连接时,铁片上发生的反应为:Cu2++2e-→Cu
C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成
浅绿色
D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+
向铜电极移动
8.下列有关钢铁腐蚀与防护的说法错误的是
A.在入海口的钢铁闸门上装一定数量的锌块可防止闸门被腐蚀
B.钢管与电源负极连接,钢管可被保护
C.钢管与铜管露天堆放在一起,加速钢管腐蚀
D.钢铁发生析氢腐蚀时,负极反应是Fe→ Fe3++3e-
9.木糖醇是一种理想的蔗糖代替品,它具有甜味足,溶解性好,防龋齿,适合糖尿病患者的优点。木糖醇是一种白色粉末状的结晶,分子式为,结构简式为,下列有关木糖醇的叙述中正确的是
A.木糖醇是一种六元醇
B.木糖醇与葡萄糖、果糖相似,均属于糖类
C.木糖醇难以被催化氧化
D.在一定条件下可以与乙酸发生反应生成酯类
10.某同学欲从苯酚的甲醇溶液中分离苯酚和甲醇,有下列操作:①蒸馏 ②过滤 ③静置分液 ④加入足量的金属钠 ⑤通入过量的二氧化碳 ⑥加入足量的NaOH溶液 ⑦加入乙酸与浓硫酸混合液加热。合理的实验操作步骤及顺序是
A.⑥①⑤③ B. ④⑤③② C.⑥①⑦② D.⑤③②①
11.有一种有机物结构简式为Cl-CH=CH2 推测它不可能具有下列哪种性质
A.能被酸性高锰酸钾溶液氧化 B.能发生缩聚反应
C.能发生水解反应 D.能与溴水发生加成反应
12.下列叙述中正确的是
A.猪油是高级脂肪酸的乙醇酯,在碱的作用下可制肥皂
B.纤维素与淀粉的通式为(C6H10O5)n 所以两者互为同分异构体
C.酶是一类蛋白质,具有特殊的催化作用,温度越高催化作用越强
D.用溴水可将酒精、苯酚溶液、四氯化碳、己烯、甲苯五种无色液体区分开来,
13.以下实验:①为检验RX是溴代烷,将RX与NaOH水溶液混合后再加入AgNO3溶液;②实验室里用无水乙醇和浓硫酸共热至170℃制乙烯;③用油脂与碳酸钠溶液混合加热制肥皂④在试管中加入2mL10%的CuSO4溶液,滴入2%的NaOH溶液4~6滴,振荡后加入乙醛溶液0.5mL,加热至沸腾;会失败的实验是:
A.①②③ B.①③④ C.②③④ D.①②③④
14.下列物质或反应的有机产物中,其中只有一种的是
A. 分子式为C3H6O2 的有机物
B.2—氯丁烷()与NaOH乙醇溶液共热
C.邻羟基苯甲酸与NaHCO3溶液反应
D.甲苯在一定条件下发生硝化生成一硝基甲苯的反应
15.运动员服用兴奋剂是违背人文道德的。某种兴奋剂的结构简式如
右图所示,有关该物质的说法错误的是
A.滴入KMnO4(H+)溶液,观察紫色褪去
B.遇FeCl3溶液不显颜色
C.1 mol该物质与浓溴水和H2反应最多消耗Br2和H2分别为4
mol、7 mol
D.该分子中的所有碳原子可能共平面
16.关于原电池的叙述正确的是
A.原电池工作时,正极和负极上不一定都发生氧化还原反应
B.xLi+Li1-xNiO2LiNiO2 放电时此电池的负极材料是Li1-xNiO2
C.在铅、银和盐酸构成的原电池工作时,铅板上有5.175 g铅溶解,正极上就有1120 mL(标准状况)气体析出
D.在理论上可将该反应:CH4(g)+2O2(g)→CO2(g)+H2O(l) ΔH<0,设计成原电池
17.已知下列数据:
2Fe(s)+O2(g) =2FeO(s) △H=-544kJ·mol-1
4Al(s)+3O2(g) =2Al2O3(s) △H=-3350kJ·mol-1
则2Al(s) +3FeO(s) =Al2O3(s) + 3Fe(s)的△H是
A.- 859 kJ·mol-1 B.+859 kJ·mol-1
C.-1403 kJ·mol-1 D.-2491 kJ·mol-1
18.某饱和一卤代烃的蒸汽对空气的相对密度为4.24,它与氢氧化钠的醇溶液共热,将产生的气体经过冷却、水洗、干燥后得到1.12升(标准状况)纯净气体,该气体通过足量溴水后,完全吸收,溴水质量增加2.1g。则此卤代烃的分子式为:
A.C3H7Br B. C3H6Br C. C3H7I D. C2H5I
高二化学
第Ⅱ卷(非选择题 共54+10分)
注意事项:
1.Ⅱ卷共4页,将答案写在答题卡上。
2.答卷前将答题卡内的项目和座号填写清楚。
二、(本题包括3小题,共24分)
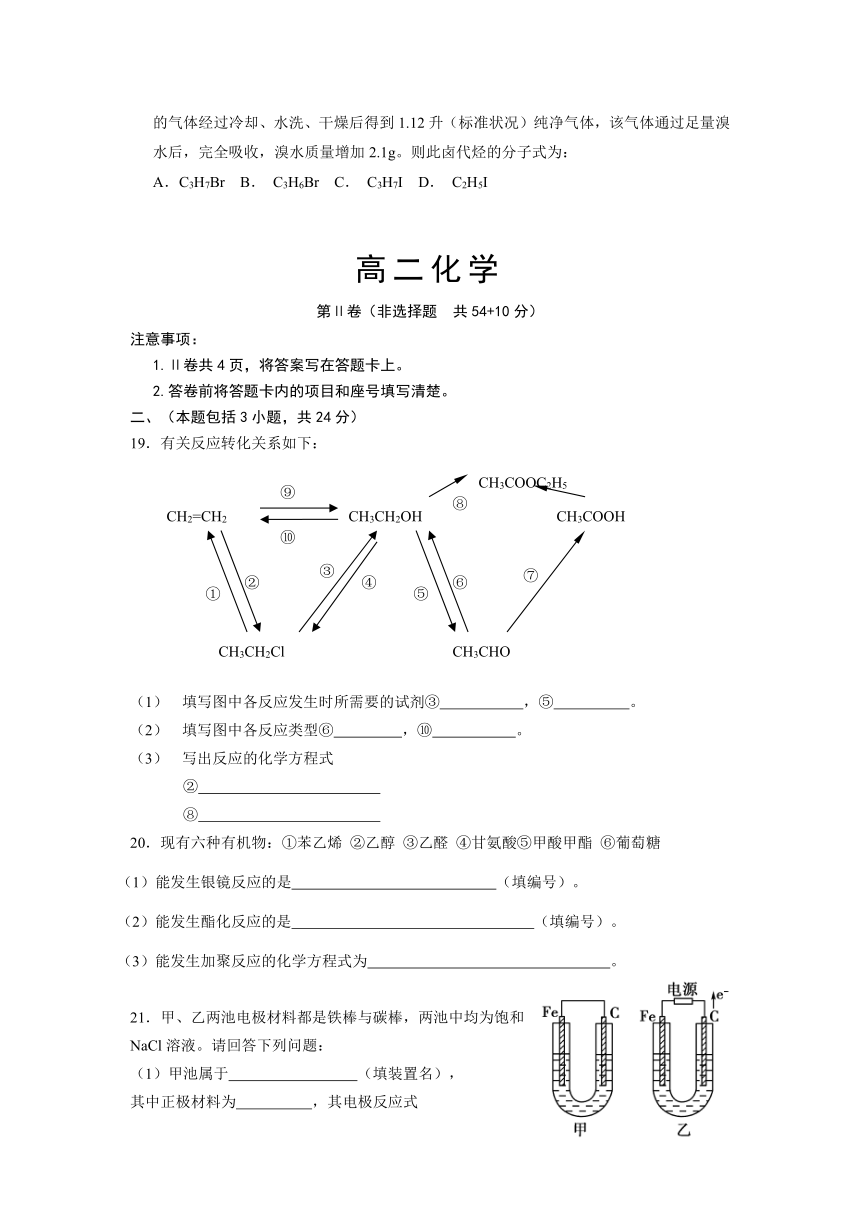
19.有关反应转化关系如下:
填写图中各反应发生时所需要的试剂③ ,⑤ 。
填写图中各反应类型⑥ ,⑩ 。
写出反应的化学方程式
②
⑧
20.现有六种有机物:①苯乙烯 ②乙醇 ③乙醛 ④甘氨酸⑤甲酸甲酯 ⑥葡萄糖
(1)能发生银镜反应的是 (填编号)。
(2)能发生酯化反应的是 (填编号)。
(3)能发生加聚反应的化学方程式为 。
21.甲、乙两池电极材料都是铁棒与碳棒,两池中均为饱和NaCl溶液。请回答下列问题:
(1)甲池属于 (填装置名),
其中正极材料为 ,其电极反应式
是_____________ 。
(2)乙池属于 (填装置名),铁极上电极反应属于____________(填“氧化反应”或“还原反应”),
写出乙池中总反应的离子方程式___________。
(3)若乙池转移0.01 mol e-后停止实验,池中溶液体积是100 mL,则溶液混匀后的[OH ]=________。(溶液体积变化忽略)
三、(本题包括2小题,共13分)
22.下列实验操作正确的是 。
A.用量热计测定中和热时,为了操作方便,可用温度计直接搅拌
B.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,重复几次,完成乙醇氧化为乙醛的实验
C.试管中先加入一定量浓硫酸,再依次加入适量冰醋酸、无水乙醇,再加热制取乙酸乙酯
D.实验室制取乙烯时,放入几片碎瓷片,以避免混合液在受热沸腾时剧烈跳动
E.配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
F.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合加热,充分振荡溶液、静置、待液体冷却后,滴加硝酸银溶液
G.向甲苯中加入酸性高锰酸钾溶液振荡,紫色不能退去
23.小强同学准备制取乙烯并探究乙烯与溴的反应(提示:在制乙烯时易生成SO2)。在I至IV的仪器中盛放的药品顺序为:无水乙醇、浓硫酸;溴水;氢氧化钠溶液;品红溶液。准备的仪器如右图。
(1)仪器各接口顺序为 。
(2)I中无水乙醇与浓硫酸的体积比
为 反应方程式为
。
(3)II中的化学方程式是
。
(4)III IV的作用为
。
若没有这两个装置,则易发生反应的离子方程式为 。
四、(本题包括2小题,共17分)
24.Ⅰ.已知:R-CH=CH-O-R′ R-CH2CHO + R′OH
(烃基烯基醚)
烃基烯基醚A的相对分子质量(M r)为162。与A相关的反应如下:
请回答下列问题:
(1)B的结构简式为_________________。
(2)写出C → D反应的化学方程式:____________________________。
Ⅱ.由E转化为对甲基苯乙炔()的一条路线如下:
(3)写出F的结构简式:____________,第③步反应的化学方程式为____________________。
第④步的反应类型为 。
25.请根据右图装置,回答相关问题:
(1)C池属于什么装置______。
(2)写出电极上发生的反应:②_____________,③___________。
(3)反应进行一段时间后,A、B、C三池中电解质溶液浓度基本不变的是________。
(4)当电路上有0.2 mol电子流过时,① 极上质量变化______g,⑥ 极上质量变化______g。
附加题(10分):
已知:①A是石油裂解气里的主要气体
②
③C物质苯环上一卤代物只有两种。
有机物A存在下列转化关系:
根据下列转化关系,回答问题:
(1)写出A物质的名称 ;D物质的结构简式 。
(2)写出反应②的类型 ;反应⑥的类型 。
(3)写出反应⑤的化学方程式: 。
(4)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出
它的结构简式:
(5)分子中具有苯环,苯环上含有两个取代基,且能与NaHCO3溶液反应的E的同分异构体有 种(不包含E)。
高二化学评分标准及参考答案
一、选择题(本题包括18小题,1-8题每小题2分,9-18题每小题3分,共46分。每小题只有1个选项符合题意)
1A 2D 3C 4D 5B 6C 7C 8D
9D 10A 11B 12D13B 14C 15B 16D 17A 18A
二、(本题包括3小题,共24分)
19.(8分)
(1)氢氧化钠水溶液(1分) 氧气、铜或CuO(1分)
(2)还原或加成(1分) 消去(1分)
(3)CH2=CH2+HCl→CH3CH2Cl (2分)
CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O (2分)
20.(6分,每小题2分)
(1)③ ⑤ ⑥ (2)② ④ ⑥
(3)
21.(10分)
(1)原电池 (1分) C(或碳)(1分) 2H2O+O2+4e-→4OH-(2分)
(2)电解池(1分) 还原反应(1分)
2Cl-+2H2O 2OH-+H2↑+Cl2↑(2分)
(3)0.1mol/L(2分)
三、(本题包括2小题,共13分)
22.BDE (3分)
23.(10分)
(1)a c d e f b (1分)
(2)1:3 (1分) C2H5OHCH2=CH2↑+H2O(2分)
(3)CH2=CH2+Br2 →CH2Br-CH2Br(2分)
(4)除去SO2 ,并检验是否除净 ;(2分)Br2+SO2+2H2O==2Br +4H++SO42 (2分)
四、(本题包括2小题,共17分)
24. (8分)
(1)CH3CH2OH(1分)
(2) CH3CHO+2Cu(OH)2CH3COOH+Cu2O↓+2H2O(2分)
(3) (2分);
(2分)
消去反应(1分)
25.(9分)
(1)电解精炼铜(电解池) (1分)
(2)2H++2e- → H2↑(1分) 4OH →2H2O+O2↑+4e- (2分)
(3)C池(1分)
(4)6.5 6.4 (4分)
附加题(10分,前2小题每空1分,后3小题每空2分。)
(1)乙烯,
(2)取代反应,加聚反应
(3)
(4)
(5)5
CH2=CH2
CH3COOH
⑨
⑩
CH3CH2OH
CH3COOC2H5
CH3CH2Cl
CH3CHO
①
②
③
④
⑤
⑥
⑦
⑧
催化剂
反应②
Br2/CCl4
反应①
反应⑤
D
C9H12O
[O]
反应④
C
C9H11Br
B
A
反应③
E
C9H10O2
CH3
F
G
(C9H10)n
一定条件
反应⑥
nCH2=CH
引发剂
[CH2-CH ]n
H3C--CH=CH2 +HBr
NaOH醇溶液
加热
-CH2-CH2Br
H3C-
本试卷分第I卷(选择题)和第II卷(非选择题)两部分,第I卷1至4页,第II卷5至8页。考试结束后,将答题卡交回。
第I卷(选择题 共46分)
注意事项:
1.答第Ⅰ卷前,将自己的姓名、考试号、考试科目涂写在答题卡上。
2.每题选出答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其他答案标号,不能答在试题上。
可能用到的相对原子质量:H 1 C 12 O 16 N 14 S 32 Cu 64 Zn 65 Br 80
I 127 Pb 207
一、选择题(本题包括18小题,1-8题每小题2分,9-18题每小题3分,共46分。每小题只有1个选项符合题意)
1.为保护环境,提高人类生存质量,各级政府大力发展绿色食品,避免“白色污染”。绿色食
品和“白色污染”是指
A.安全、无公害的营养食品和聚乙烯等白色塑料垃圾
B.绿颜色的食品和白色建筑废料
C.有叶绿素的食品和石灰窑的白色粉末
D.经济附加值高的营养食品和冶炼厂的白色烟尘
2. 建筑装潢质量的问题之一是装潢装饰材料中某些化学成分含量太高,缓慢释放出来,在空气中浓度过高,影响人体健康。这某些化学成分主要是
A.甲烷 B.乙烯
C.乙炔 D.甲醛、甲苯等有机物蒸气
3.正丁烷与2--甲基丙烷属于
A.同位素 B.同素异形体
C.同分异构体 D.同系物
4.下列各组液体混合物,用分液漏斗能分开的是
A.苯和甲苯 B.甘油和乙醇
C.乙酸乙酯和乙酸 D.正已烷和水
5.下列各组反应,实质都是取代反应的是
异戊二烯生成聚异戊二烯,酚醛树脂的生成
乙醇和氢卤酸反应,乙醇和浓硫酸加热至140℃时的反应,酯的水解
淀粉在硫酸存在下制葡萄糖,皂化反应,油脂的硬化
D.纤维素水解,浓硫酸和乙醇在170℃时的反应,蛋白质水解
6.下列说法中错误的是
A.在热化学方程式中无论反应物还是生成物必须标明聚集状态
B.热化学方程式的化学计量数不能表示分子的个数
C.反应热指的是反应过程中放出的热量
D.所有的化学反应都伴随着能量的变化
7.某小组为研究电化学原理,设计如图装置。下列叙述正确的是
A.a和b不连接时,铁片上不会有金属铜析出
B.a和b用导线连接时,铁片上发生的反应为:Cu2++2e-→Cu
C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成
浅绿色
D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+
向铜电极移动
8.下列有关钢铁腐蚀与防护的说法错误的是
A.在入海口的钢铁闸门上装一定数量的锌块可防止闸门被腐蚀
B.钢管与电源负极连接,钢管可被保护
C.钢管与铜管露天堆放在一起,加速钢管腐蚀
D.钢铁发生析氢腐蚀时,负极反应是Fe→ Fe3++3e-
9.木糖醇是一种理想的蔗糖代替品,它具有甜味足,溶解性好,防龋齿,适合糖尿病患者的优点。木糖醇是一种白色粉末状的结晶,分子式为,结构简式为,下列有关木糖醇的叙述中正确的是
A.木糖醇是一种六元醇
B.木糖醇与葡萄糖、果糖相似,均属于糖类
C.木糖醇难以被催化氧化
D.在一定条件下可以与乙酸发生反应生成酯类
10.某同学欲从苯酚的甲醇溶液中分离苯酚和甲醇,有下列操作:①蒸馏 ②过滤 ③静置分液 ④加入足量的金属钠 ⑤通入过量的二氧化碳 ⑥加入足量的NaOH溶液 ⑦加入乙酸与浓硫酸混合液加热。合理的实验操作步骤及顺序是
A.⑥①⑤③ B. ④⑤③② C.⑥①⑦② D.⑤③②①
11.有一种有机物结构简式为Cl-CH=CH2 推测它不可能具有下列哪种性质
A.能被酸性高锰酸钾溶液氧化 B.能发生缩聚反应
C.能发生水解反应 D.能与溴水发生加成反应
12.下列叙述中正确的是
A.猪油是高级脂肪酸的乙醇酯,在碱的作用下可制肥皂
B.纤维素与淀粉的通式为(C6H10O5)n 所以两者互为同分异构体
C.酶是一类蛋白质,具有特殊的催化作用,温度越高催化作用越强
D.用溴水可将酒精、苯酚溶液、四氯化碳、己烯、甲苯五种无色液体区分开来,
13.以下实验:①为检验RX是溴代烷,将RX与NaOH水溶液混合后再加入AgNO3溶液;②实验室里用无水乙醇和浓硫酸共热至170℃制乙烯;③用油脂与碳酸钠溶液混合加热制肥皂④在试管中加入2mL10%的CuSO4溶液,滴入2%的NaOH溶液4~6滴,振荡后加入乙醛溶液0.5mL,加热至沸腾;会失败的实验是:
A.①②③ B.①③④ C.②③④ D.①②③④
14.下列物质或反应的有机产物中,其中只有一种的是
A. 分子式为C3H6O2 的有机物
B.2—氯丁烷()与NaOH乙醇溶液共热
C.邻羟基苯甲酸与NaHCO3溶液反应
D.甲苯在一定条件下发生硝化生成一硝基甲苯的反应
15.运动员服用兴奋剂是违背人文道德的。某种兴奋剂的结构简式如
右图所示,有关该物质的说法错误的是
A.滴入KMnO4(H+)溶液,观察紫色褪去
B.遇FeCl3溶液不显颜色
C.1 mol该物质与浓溴水和H2反应最多消耗Br2和H2分别为4
mol、7 mol
D.该分子中的所有碳原子可能共平面
16.关于原电池的叙述正确的是
A.原电池工作时,正极和负极上不一定都发生氧化还原反应
B.xLi+Li1-xNiO2LiNiO2 放电时此电池的负极材料是Li1-xNiO2
C.在铅、银和盐酸构成的原电池工作时,铅板上有5.175 g铅溶解,正极上就有1120 mL(标准状况)气体析出
D.在理论上可将该反应:CH4(g)+2O2(g)→CO2(g)+H2O(l) ΔH<0,设计成原电池
17.已知下列数据:
2Fe(s)+O2(g) =2FeO(s) △H=-544kJ·mol-1
4Al(s)+3O2(g) =2Al2O3(s) △H=-3350kJ·mol-1
则2Al(s) +3FeO(s) =Al2O3(s) + 3Fe(s)的△H是
A.- 859 kJ·mol-1 B.+859 kJ·mol-1
C.-1403 kJ·mol-1 D.-2491 kJ·mol-1
18.某饱和一卤代烃的蒸汽对空气的相对密度为4.24,它与氢氧化钠的醇溶液共热,将产生的气体经过冷却、水洗、干燥后得到1.12升(标准状况)纯净气体,该气体通过足量溴水后,完全吸收,溴水质量增加2.1g。则此卤代烃的分子式为:
A.C3H7Br B. C3H6Br C. C3H7I D. C2H5I
高二化学
第Ⅱ卷(非选择题 共54+10分)
注意事项:
1.Ⅱ卷共4页,将答案写在答题卡上。
2.答卷前将答题卡内的项目和座号填写清楚。
二、(本题包括3小题,共24分)
19.有关反应转化关系如下:
填写图中各反应发生时所需要的试剂③ ,⑤ 。
填写图中各反应类型⑥ ,⑩ 。
写出反应的化学方程式
②
⑧
20.现有六种有机物:①苯乙烯 ②乙醇 ③乙醛 ④甘氨酸⑤甲酸甲酯 ⑥葡萄糖
(1)能发生银镜反应的是 (填编号)。
(2)能发生酯化反应的是 (填编号)。
(3)能发生加聚反应的化学方程式为 。
21.甲、乙两池电极材料都是铁棒与碳棒,两池中均为饱和NaCl溶液。请回答下列问题:
(1)甲池属于 (填装置名),
其中正极材料为 ,其电极反应式
是_____________ 。
(2)乙池属于 (填装置名),铁极上电极反应属于____________(填“氧化反应”或“还原反应”),
写出乙池中总反应的离子方程式___________。
(3)若乙池转移0.01 mol e-后停止实验,池中溶液体积是100 mL,则溶液混匀后的[OH ]=________。(溶液体积变化忽略)
三、(本题包括2小题,共13分)
22.下列实验操作正确的是 。
A.用量热计测定中和热时,为了操作方便,可用温度计直接搅拌
B.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,重复几次,完成乙醇氧化为乙醛的实验
C.试管中先加入一定量浓硫酸,再依次加入适量冰醋酸、无水乙醇,再加热制取乙酸乙酯
D.实验室制取乙烯时,放入几片碎瓷片,以避免混合液在受热沸腾时剧烈跳动
E.配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
F.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合加热,充分振荡溶液、静置、待液体冷却后,滴加硝酸银溶液
G.向甲苯中加入酸性高锰酸钾溶液振荡,紫色不能退去
23.小强同学准备制取乙烯并探究乙烯与溴的反应(提示:在制乙烯时易生成SO2)。在I至IV的仪器中盛放的药品顺序为:无水乙醇、浓硫酸;溴水;氢氧化钠溶液;品红溶液。准备的仪器如右图。
(1)仪器各接口顺序为 。
(2)I中无水乙醇与浓硫酸的体积比
为 反应方程式为
。
(3)II中的化学方程式是
。
(4)III IV的作用为
。
若没有这两个装置,则易发生反应的离子方程式为 。
四、(本题包括2小题,共17分)
24.Ⅰ.已知:R-CH=CH-O-R′ R-CH2CHO + R′OH
(烃基烯基醚)
烃基烯基醚A的相对分子质量(M r)为162。与A相关的反应如下:
请回答下列问题:
(1)B的结构简式为_________________。
(2)写出C → D反应的化学方程式:____________________________。
Ⅱ.由E转化为对甲基苯乙炔()的一条路线如下:
(3)写出F的结构简式:____________,第③步反应的化学方程式为____________________。
第④步的反应类型为 。
25.请根据右图装置,回答相关问题:
(1)C池属于什么装置______。
(2)写出电极上发生的反应:②_____________,③___________。
(3)反应进行一段时间后,A、B、C三池中电解质溶液浓度基本不变的是________。
(4)当电路上有0.2 mol电子流过时,① 极上质量变化______g,⑥ 极上质量变化______g。
附加题(10分):
已知:①A是石油裂解气里的主要气体
②
③C物质苯环上一卤代物只有两种。
有机物A存在下列转化关系:
根据下列转化关系,回答问题:
(1)写出A物质的名称 ;D物质的结构简式 。
(2)写出反应②的类型 ;反应⑥的类型 。
(3)写出反应⑤的化学方程式: 。
(4)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出
它的结构简式:
(5)分子中具有苯环,苯环上含有两个取代基,且能与NaHCO3溶液反应的E的同分异构体有 种(不包含E)。
高二化学评分标准及参考答案
一、选择题(本题包括18小题,1-8题每小题2分,9-18题每小题3分,共46分。每小题只有1个选项符合题意)
1A 2D 3C 4D 5B 6C 7C 8D
9D 10A 11B 12D13B 14C 15B 16D 17A 18A
二、(本题包括3小题,共24分)
19.(8分)
(1)氢氧化钠水溶液(1分) 氧气、铜或CuO(1分)
(2)还原或加成(1分) 消去(1分)
(3)CH2=CH2+HCl→CH3CH2Cl (2分)
CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O (2分)
20.(6分,每小题2分)
(1)③ ⑤ ⑥ (2)② ④ ⑥
(3)
21.(10分)
(1)原电池 (1分) C(或碳)(1分) 2H2O+O2+4e-→4OH-(2分)
(2)电解池(1分) 还原反应(1分)
2Cl-+2H2O 2OH-+H2↑+Cl2↑(2分)
(3)0.1mol/L(2分)
三、(本题包括2小题,共13分)
22.BDE (3分)
23.(10分)
(1)a c d e f b (1分)
(2)1:3 (1分) C2H5OHCH2=CH2↑+H2O(2分)
(3)CH2=CH2+Br2 →CH2Br-CH2Br(2分)
(4)除去SO2 ,并检验是否除净 ;(2分)Br2+SO2+2H2O==2Br +4H++SO42 (2分)
四、(本题包括2小题,共17分)
24. (8分)
(1)CH3CH2OH(1分)
(2) CH3CHO+2Cu(OH)2CH3COOH+Cu2O↓+2H2O(2分)
(3) (2分);
(2分)
消去反应(1分)
25.(9分)
(1)电解精炼铜(电解池) (1分)
(2)2H++2e- → H2↑(1分) 4OH →2H2O+O2↑+4e- (2分)
(3)C池(1分)
(4)6.5 6.4 (4分)
附加题(10分,前2小题每空1分,后3小题每空2分。)
(1)乙烯,
(2)取代反应,加聚反应
(3)
(4)
(5)5
CH2=CH2
CH3COOH
⑨
⑩
CH3CH2OH
CH3COOC2H5
CH3CH2Cl
CH3CHO
①
②
③
④
⑤
⑥
⑦
⑧
催化剂
反应②
Br2/CCl4
反应①
反应⑤
D
C9H12O
[O]
反应④
C
C9H11Br
B
A
反应③
E
C9H10O2
CH3
F
G
(C9H10)n
一定条件
反应⑥
nCH2=CH
引发剂
[CH2-CH ]n
H3C--CH=CH2 +HBr
NaOH醇溶液
加热
-CH2-CH2Br
H3C-
同课章节目录
