2020-2021学年人教版九年级下册化学 第九单元 溶液 复习题(含答案)
文档属性
| 名称 | 2020-2021学年人教版九年级下册化学 第九单元 溶液 复习题(含答案) |  | |
| 格式 | zip | ||
| 文件大小 | 172.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-03 10:02:40 | ||
图片预览


文档简介
第九单元
溶液
复习题
一.选择题(共20小题)
1.将厨房中的下列物质放入适量水中,充分搅拌,能形成溶液的是( )
A.植物油
B.面粉
C.食盐
D.牛奶
2.逻辑推理是一种重要的化学思维方法。下列推理正确的是( )
A.溶液是均一、稳定的混合物,但均一、稳定的物质不一定是溶液
B.化合物由不同种元素组成,所以由不同种元素组成的物质一定是化合物
C.同种元素的粒子质子数都相同,所以含有相同质子数的粒子一定属于同种元素
D.洗涤剂除油污是乳化作用,所以汽油除油污也是乳化作用
3.下列清洗污渍的方法中,利用了乳化原理的是( )
A.用自来水洗手
B.用生理盐水清洗伤口
C.用洗洁精洗碗
D.用酒精清洗医疗器械
4.下列关于溶液的叙述中正确的是( )
A.溶液不一定是混合物
B.溶液都是无色的
C.凡是均一的、稳定的液体就一定是溶液
D.溶液都是均一、稳定的混合物
5.10℃时,将3g甲、乙两种可溶性固体分别放入盛有10mL水的试管中。两种物质的溶解情况见图Ⅰ,两种物质的溶解度随温度的变化见图Ⅱ。下面对甲、乙两种物质的判断,正确的是( )
A.10℃时,甲、乙两物质的溶液都是饱和溶液
B.甲物质对应的溶解度曲线为b
C.当温度升高至25℃时,甲、乙两物质的溶质质量分数均不变
D.10℃时,甲溶液中溶质与溶剂的质量比为1:5
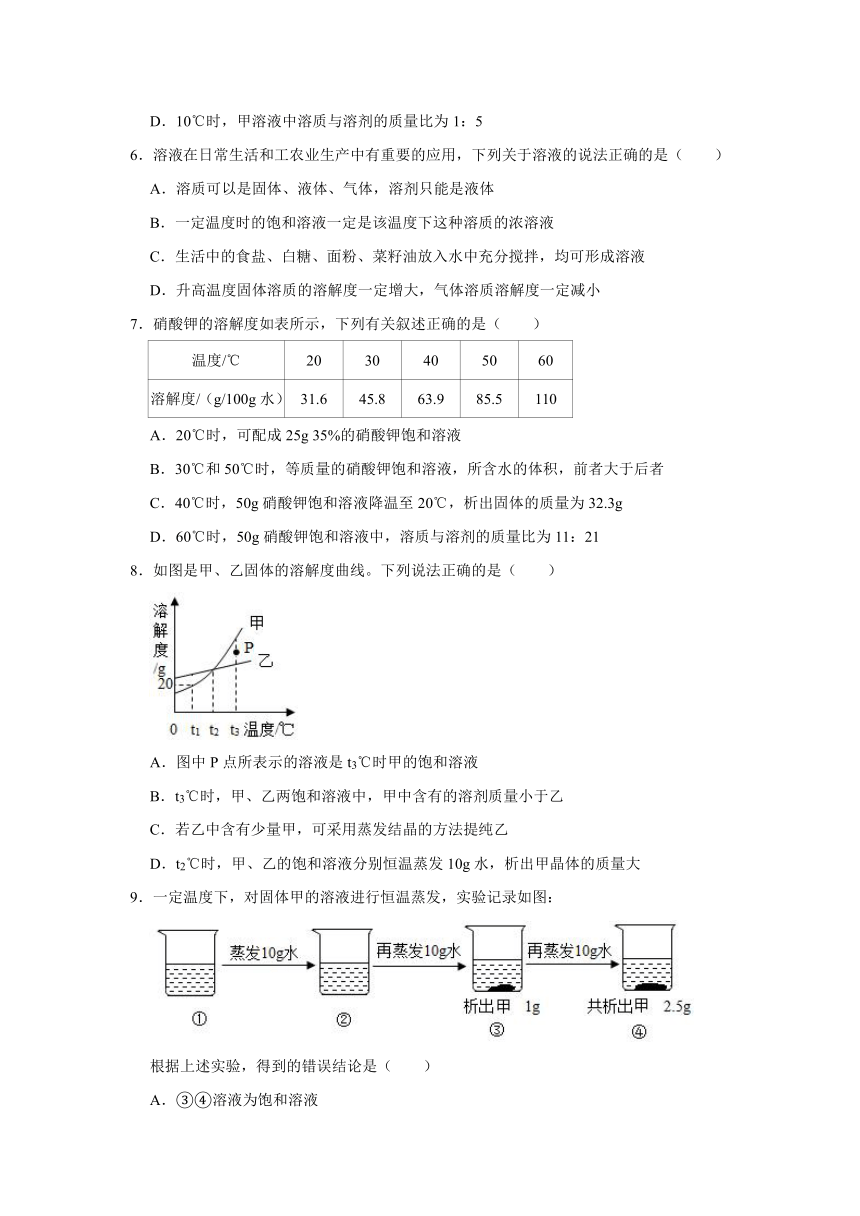
6.溶液在日常生活和工农业生产中有重要的应用,下列关于溶液的说法正确的是( )
A.溶质可以是固体、液体、气体,溶剂只能是液体
B.一定温度时的饱和溶液一定是该温度下这种溶质的浓溶液
C.生活中的食盐、白糖、面粉、菜籽油放入水中充分搅拌,均可形成溶液
D.升高温度固体溶质的溶解度一定增大,气体溶质溶解度一定减小
7.硝酸钾的溶解度如表所示,下列有关叙述正确的是( )
温度/℃
20
30
40
50
60
溶解度/(g/100g水)
31.6
45.8
63.9
85.5
110
A.20℃时,可配成25g
35%的硝酸钾饱和溶液
B.30℃和50℃时,等质量的硝酸钾饱和溶液,所含水的体积,前者大于后者
C.40℃时,50g硝酸钾饱和溶液降温至20℃,析出固体的质量为32.3g
D.60℃时,50g硝酸钾饱和溶液中,溶质与溶剂的质量比为11:21
8.如图是甲、乙固体的溶解度曲线。下列说法正确的是( )
A.图中P点所表示的溶液是t3℃时甲的饱和溶液
B.t3℃时,甲、乙两饱和溶液中,甲中含有的溶剂质量小于乙
C.若乙中含有少量甲,可采用蒸发结晶的方法提纯乙
D.t2℃时,甲、乙的饱和溶液分别恒温蒸发10g水,析出甲晶体的质量大
9.一定温度下,对固体甲的溶液进行恒温蒸发,实验记录如图:
根据上述实验,得到的错误结论是( )
A.③④溶液为饱和溶液
B.④中再加15g水又可以将析出固体完全溶解
C.不能确定固体甲的溶解度随温度的变化情况
D.①~④溶液的溶质质量分数:①<②<③=④
10.甲和乙两种物质的溶解度曲线如图所示。下列叙述正确的是( )
A.甲的溶解度随温度的升高而增大
B.40℃时,使甲的饱和溶液析出晶体可用加热升温、冷却降温和蒸发溶剂三种方法
C.20℃时,向50g溶剂中加入20g的乙固体并充分溶解,溶液的溶质质量分数约为28.6%
D.将甲和乙的饱和溶液分别从40℃降温至10℃,甲析出晶体的质量大
11.在实验室中,用氯化钠固体配制50g溶质质量分数为6%的氯化钠溶液。下列操作或说法错误的是( )
A.配制步骤:计算、称量、量取、溶解、装瓶
B.用量筒量取水时仰视读数,所得溶液的溶质质量分数小于6%
C.把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中,并贴上标签
D.若用12%的氯化钠溶液稀释配制该溶液,需要12%的氯化钠溶液25g
12.现有下列仪器①漏斗②玻璃棒③托盘天平④试管⑤烧杯⑥量筒⑦胶头滴管⑧药匙,用98%的浓硫酸配制成20%的稀硫酸,需要用到的玻璃仪器是( )
A.①②④⑤⑥⑦
B.②③④⑤⑥⑦
C.②③⑤⑥⑦⑧
D.②⑤⑥⑦
13.配制70克14%的NaCl溶液,下列操作会使所配溶液溶质质量分数大于14%的是( )
A.称量NaCl
B.溶解固体
C.量取水
D.把配制好的溶液装在试剂瓶中
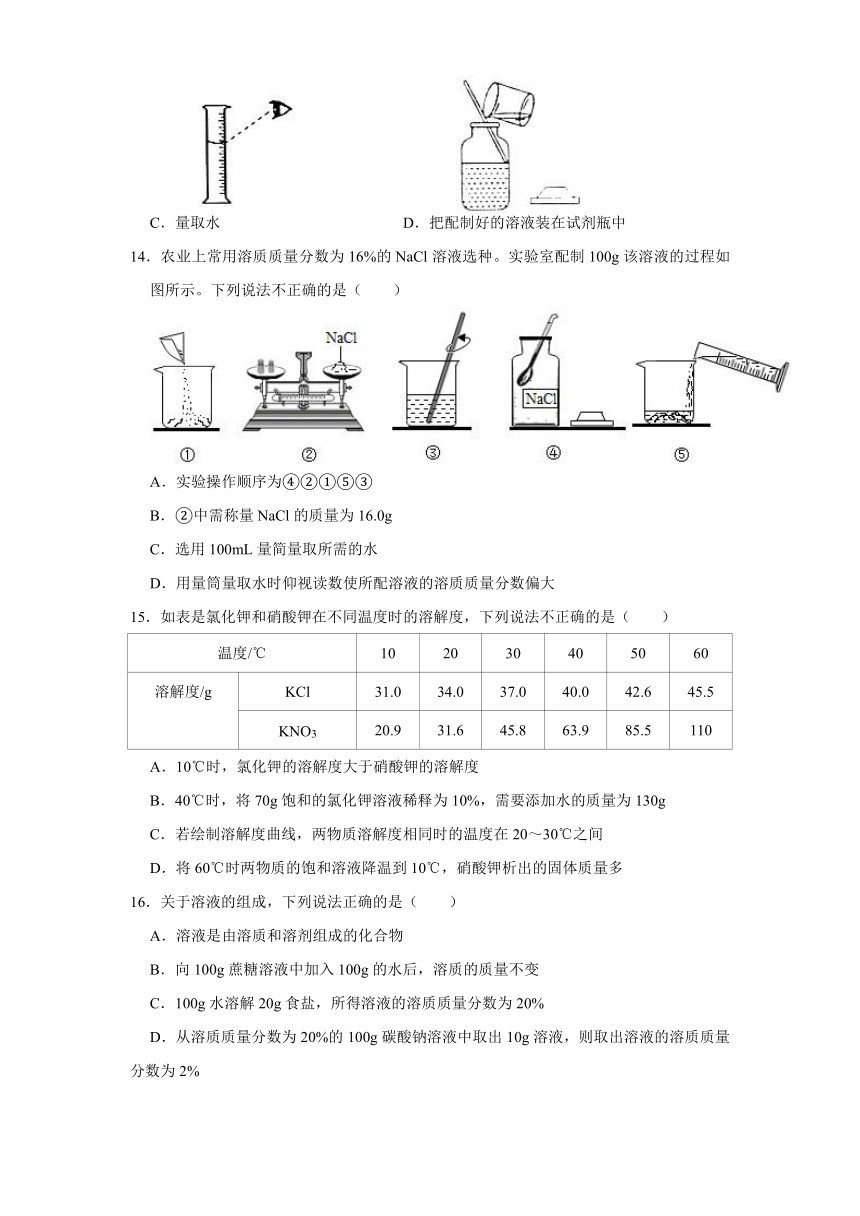
14.农业上常用溶质质量分数为16%的NaCl溶液选种。实验室配制100g该溶液的过程如图所示。下列说法不正确的是( )
A.实验操作顺序为④②①⑤③
B.②中需称量NaCl的质量为16.0g
C.选用100mL量简量取所需的水
D.用量筒量取水时仰视读数使所配溶液的溶质质量分数偏大
15.如表是氯化钾和硝酸钾在不同温度时的溶解度,下列说法不正确的是( )
温度/℃
10
20
30
40
50
60
溶解度/g
KCl
31.0
34.0
37.0
40.0
42.6
45.5
KNO3
20.9
31.6
45.8
63.9
85.5
110
A.10℃时,氯化钾的溶解度大于硝酸钾的溶解度
B.40℃时,将70g饱和的氯化钾溶液稀释为10%,需要添加水的质量为130g
C.若绘制溶解度曲线,两物质溶解度相同时的温度在20~30℃之间
D.将60℃时两物质的饱和溶液降温到10℃,硝酸钾析出的固体质量多
16.关于溶液的组成,下列说法正确的是( )
A.溶液是由溶质和溶剂组成的化合物
B.向100g蔗糖溶液中加入100g的水后,溶质的质量不变
C.100g水溶解20g食盐,所得溶液的溶质质量分数为20%
D.从溶质质量分数为20%的100g碳酸钠溶液中取出10g溶液,则取出溶液的溶质质量分数为2%
17.实验室用氯化钠固体配制50g溶质质量分数为5%的氯化钠溶液。下列说法正确的是( )
A.称量时托盘天平指针偏左,移动游码至天平平衡
B.量取水时,用规格为50mL的量筒
C.若在量取水时仰视读数,则配制的溶液的溶质质量分数大于5%
D.把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中,并贴上标签
18.如图是甲、乙、丙三种物质的溶解度曲线。下列有关说法正确的是( )
A.甲、乙、丙三种物质中甲的溶解度最大
B.t1℃时甲、丙二者的溶液,其溶质质量分数相等
C.若乙中含有少量甲,可采用冷却热饱和溶液的方法提纯乙
D.将等质量的甲、乙、丙三种物质的饱和溶液从t3℃降至t1℃时,甲析出的晶体最多
19.如图为甲、乙两固体(不含结晶水)的溶解度曲线,下列说法正确的是( )
A.甲的溶液度一定大于乙
B.T1℃时的甲乙饱和溶液的溶质质量分数相等
C.T2℃时,将60g甲放入100g水中,可以得到160g甲溶液
D.降低温度可以使不饱和的乙溶液变成饱和
20.某同学在探究物质溶解的热现象及温度对物质溶解度影响时,设计了如下实验,现象如图一所示,溶解度曲线如图二所示,下列说法正确的是( )
A.M的溶解度曲线为a曲线
B.升温可以使N的饱和溶液变浑浊
C.M的饱和溶液从t2℃降温到t1℃时,溶质质量分数变大
D.如果t2℃时,M、N的饱和溶液质量相等,则溶剂质量M>N
二.解答题(共4小题)
21.如图是X、Y、Z三种物质的溶解度曲线图,认真阅读完成下列各小题。
(1)在
℃时,Y、Z两物质溶解度相等。
(2)t2℃时,将20g
Z放入装有50g水的烧杯中,充分搅拌可能到
g
Z的饱和溶液。
(3)在t1℃时把质量均为mg的X、Y、Z三种固体溶于水中形成饱和溶液,需水质量最多的是
。
(4)下列说法正确的有
(只需填正确的选项序号)。
①Z物质有可能是气体
②若X中含有少量的Y,可用蒸发结晶提纯X
③将t3℃时等质量的X、Y饱和溶液同时降温到t1℃,析出晶体的质量是X>Y
④要将t1℃时接近饱和的X溶液变成饱和溶液,如不改变该溶液的组成,可选择降低温度的方法
⑤将t3℃时Z的饱和溶液降温至t2℃后,溶液的溶质质量分数会变大
22.甲、乙两种固体的溶解度曲线如图一所示,t2℃时,100克水中加入60克硝酸钾,充分搅拌,直到固体完全消失,然后按图二进行实验,分别采用不同方法(每种方法只改变一个量),得到三个恰好饱和的溶液,且溶液质量依次减小。
(1)t1℃时,溶解度大小关系为:甲
乙(填“>”或“<”或“=”);
(2)由图二推测硝酸钾是图一中的
物质(填“甲”或“乙”);
(3)图二中“某一步操作”得到D溶液前后的溶液状态变化过程可以在图一中表示为
;
A.b点→a点
B.c点→a点
C.b点→c点
D.c点→d点
(4)图二中得到的C、D、E溶液中质量分数大小关系是
(用“>或<或=”表示)。
23.氯化铵、硫酸钠两种物质的溶解度曲线如图一所示,根据图示回答下列问题:
(1)40℃时,硫酸钠的饱和溶液中溶质质量与溶剂质量比为
。
(2)70℃时,将65g硫酸钠加入到100g水中充分搅拌,形成硫酸钠溶液的质量为
g。
(3)将60℃时氯化铵的不饱和溶液转变成饱和,可以采用一种方法是
。
(4)要使40℃时的硫酸钠饱和溶液析出晶体,可以采取的措施是
(填选项序号)。
A.蒸发溶剂
B.增加溶剂
C.降低温度
D.升高温度
(5)如图二所示,20℃时,把试管放入盛有氯化铵饱和溶液的烧杯中(无剩余晶体),在试管中加入几小段镁条,再加入5mL稀硫酸,立即产生大量的气泡,反应中试管外壁会发烫,发生反应的化学方程式为
,关于烧杯中氯化铵溶液一定不变的量是
(填数字序号)。
①溶液温度
②溶质质量
③溶剂质量
④溶解度
⑤溶质质量分数
(6)小强同学要在实验室配制15%的氯化铵溶液50g。需要氯化铵的质量为
克,若将该溶液稀释成5%的氯化铵溶液,需要加水
克。
24.如图1是A、B、C三种物质的溶解度曲线,请回答。
(1)t2℃时,将30克A物质放入50克水中,充分溶解后所得溶液中溶质与溶剂的质量比为
。
(2)A物质中混有少量B物质,若提纯A物质,可采取的结晶方法是
。
(3)t1℃时,取等质量的A、C饱和溶液分别置于甲、乙两支试管中,如图2所示。在大烧杯中加入一定质量的硝酸铵固体溶解后,A、C溶液的溶质质量分数的大小关系是
。
参考答案
一.选择题(共20小题)
1.C;
2.A;
3.C;
4.D;
5.D;
6.B;
7.B;
8.C;
9.B;
10.B;
11.C;
12.D;
13.C;
14.D;
15.D;
16.B;
17.B;
18.D;
19.B;
20.D;
二.解答题(共4小题)
21.t2;65;X;①③④;
22.>;甲;B;C=E>D;
23.1:2;145;增加溶质;ACD;Mg+H2SO4=MgSO4+H2↑;②③⑤;7.5;100;
24.2:5;降温结晶;A<C;
溶液
复习题
一.选择题(共20小题)
1.将厨房中的下列物质放入适量水中,充分搅拌,能形成溶液的是( )
A.植物油
B.面粉
C.食盐
D.牛奶
2.逻辑推理是一种重要的化学思维方法。下列推理正确的是( )
A.溶液是均一、稳定的混合物,但均一、稳定的物质不一定是溶液
B.化合物由不同种元素组成,所以由不同种元素组成的物质一定是化合物
C.同种元素的粒子质子数都相同,所以含有相同质子数的粒子一定属于同种元素
D.洗涤剂除油污是乳化作用,所以汽油除油污也是乳化作用
3.下列清洗污渍的方法中,利用了乳化原理的是( )
A.用自来水洗手
B.用生理盐水清洗伤口
C.用洗洁精洗碗
D.用酒精清洗医疗器械
4.下列关于溶液的叙述中正确的是( )
A.溶液不一定是混合物
B.溶液都是无色的
C.凡是均一的、稳定的液体就一定是溶液
D.溶液都是均一、稳定的混合物
5.10℃时,将3g甲、乙两种可溶性固体分别放入盛有10mL水的试管中。两种物质的溶解情况见图Ⅰ,两种物质的溶解度随温度的变化见图Ⅱ。下面对甲、乙两种物质的判断,正确的是( )
A.10℃时,甲、乙两物质的溶液都是饱和溶液
B.甲物质对应的溶解度曲线为b
C.当温度升高至25℃时,甲、乙两物质的溶质质量分数均不变
D.10℃时,甲溶液中溶质与溶剂的质量比为1:5
6.溶液在日常生活和工农业生产中有重要的应用,下列关于溶液的说法正确的是( )
A.溶质可以是固体、液体、气体,溶剂只能是液体
B.一定温度时的饱和溶液一定是该温度下这种溶质的浓溶液
C.生活中的食盐、白糖、面粉、菜籽油放入水中充分搅拌,均可形成溶液
D.升高温度固体溶质的溶解度一定增大,气体溶质溶解度一定减小
7.硝酸钾的溶解度如表所示,下列有关叙述正确的是( )
温度/℃
20
30
40
50
60
溶解度/(g/100g水)
31.6
45.8
63.9
85.5
110
A.20℃时,可配成25g
35%的硝酸钾饱和溶液
B.30℃和50℃时,等质量的硝酸钾饱和溶液,所含水的体积,前者大于后者
C.40℃时,50g硝酸钾饱和溶液降温至20℃,析出固体的质量为32.3g
D.60℃时,50g硝酸钾饱和溶液中,溶质与溶剂的质量比为11:21
8.如图是甲、乙固体的溶解度曲线。下列说法正确的是( )
A.图中P点所表示的溶液是t3℃时甲的饱和溶液
B.t3℃时,甲、乙两饱和溶液中,甲中含有的溶剂质量小于乙
C.若乙中含有少量甲,可采用蒸发结晶的方法提纯乙
D.t2℃时,甲、乙的饱和溶液分别恒温蒸发10g水,析出甲晶体的质量大
9.一定温度下,对固体甲的溶液进行恒温蒸发,实验记录如图:
根据上述实验,得到的错误结论是( )
A.③④溶液为饱和溶液
B.④中再加15g水又可以将析出固体完全溶解
C.不能确定固体甲的溶解度随温度的变化情况
D.①~④溶液的溶质质量分数:①<②<③=④
10.甲和乙两种物质的溶解度曲线如图所示。下列叙述正确的是( )
A.甲的溶解度随温度的升高而增大
B.40℃时,使甲的饱和溶液析出晶体可用加热升温、冷却降温和蒸发溶剂三种方法
C.20℃时,向50g溶剂中加入20g的乙固体并充分溶解,溶液的溶质质量分数约为28.6%
D.将甲和乙的饱和溶液分别从40℃降温至10℃,甲析出晶体的质量大
11.在实验室中,用氯化钠固体配制50g溶质质量分数为6%的氯化钠溶液。下列操作或说法错误的是( )
A.配制步骤:计算、称量、量取、溶解、装瓶
B.用量筒量取水时仰视读数,所得溶液的溶质质量分数小于6%
C.把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中,并贴上标签
D.若用12%的氯化钠溶液稀释配制该溶液,需要12%的氯化钠溶液25g
12.现有下列仪器①漏斗②玻璃棒③托盘天平④试管⑤烧杯⑥量筒⑦胶头滴管⑧药匙,用98%的浓硫酸配制成20%的稀硫酸,需要用到的玻璃仪器是( )
A.①②④⑤⑥⑦
B.②③④⑤⑥⑦
C.②③⑤⑥⑦⑧
D.②⑤⑥⑦
13.配制70克14%的NaCl溶液,下列操作会使所配溶液溶质质量分数大于14%的是( )
A.称量NaCl
B.溶解固体
C.量取水
D.把配制好的溶液装在试剂瓶中
14.农业上常用溶质质量分数为16%的NaCl溶液选种。实验室配制100g该溶液的过程如图所示。下列说法不正确的是( )
A.实验操作顺序为④②①⑤③
B.②中需称量NaCl的质量为16.0g
C.选用100mL量简量取所需的水
D.用量筒量取水时仰视读数使所配溶液的溶质质量分数偏大
15.如表是氯化钾和硝酸钾在不同温度时的溶解度,下列说法不正确的是( )
温度/℃
10
20
30
40
50
60
溶解度/g
KCl
31.0
34.0
37.0
40.0
42.6
45.5
KNO3
20.9
31.6
45.8
63.9
85.5
110
A.10℃时,氯化钾的溶解度大于硝酸钾的溶解度
B.40℃时,将70g饱和的氯化钾溶液稀释为10%,需要添加水的质量为130g
C.若绘制溶解度曲线,两物质溶解度相同时的温度在20~30℃之间
D.将60℃时两物质的饱和溶液降温到10℃,硝酸钾析出的固体质量多
16.关于溶液的组成,下列说法正确的是( )
A.溶液是由溶质和溶剂组成的化合物
B.向100g蔗糖溶液中加入100g的水后,溶质的质量不变
C.100g水溶解20g食盐,所得溶液的溶质质量分数为20%
D.从溶质质量分数为20%的100g碳酸钠溶液中取出10g溶液,则取出溶液的溶质质量分数为2%
17.实验室用氯化钠固体配制50g溶质质量分数为5%的氯化钠溶液。下列说法正确的是( )
A.称量时托盘天平指针偏左,移动游码至天平平衡
B.量取水时,用规格为50mL的量筒
C.若在量取水时仰视读数,则配制的溶液的溶质质量分数大于5%
D.把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中,并贴上标签
18.如图是甲、乙、丙三种物质的溶解度曲线。下列有关说法正确的是( )
A.甲、乙、丙三种物质中甲的溶解度最大
B.t1℃时甲、丙二者的溶液,其溶质质量分数相等
C.若乙中含有少量甲,可采用冷却热饱和溶液的方法提纯乙
D.将等质量的甲、乙、丙三种物质的饱和溶液从t3℃降至t1℃时,甲析出的晶体最多
19.如图为甲、乙两固体(不含结晶水)的溶解度曲线,下列说法正确的是( )
A.甲的溶液度一定大于乙
B.T1℃时的甲乙饱和溶液的溶质质量分数相等
C.T2℃时,将60g甲放入100g水中,可以得到160g甲溶液
D.降低温度可以使不饱和的乙溶液变成饱和
20.某同学在探究物质溶解的热现象及温度对物质溶解度影响时,设计了如下实验,现象如图一所示,溶解度曲线如图二所示,下列说法正确的是( )
A.M的溶解度曲线为a曲线
B.升温可以使N的饱和溶液变浑浊
C.M的饱和溶液从t2℃降温到t1℃时,溶质质量分数变大
D.如果t2℃时,M、N的饱和溶液质量相等,则溶剂质量M>N
二.解答题(共4小题)
21.如图是X、Y、Z三种物质的溶解度曲线图,认真阅读完成下列各小题。
(1)在
℃时,Y、Z两物质溶解度相等。
(2)t2℃时,将20g
Z放入装有50g水的烧杯中,充分搅拌可能到
g
Z的饱和溶液。
(3)在t1℃时把质量均为mg的X、Y、Z三种固体溶于水中形成饱和溶液,需水质量最多的是
。
(4)下列说法正确的有
(只需填正确的选项序号)。
①Z物质有可能是气体
②若X中含有少量的Y,可用蒸发结晶提纯X
③将t3℃时等质量的X、Y饱和溶液同时降温到t1℃,析出晶体的质量是X>Y
④要将t1℃时接近饱和的X溶液变成饱和溶液,如不改变该溶液的组成,可选择降低温度的方法
⑤将t3℃时Z的饱和溶液降温至t2℃后,溶液的溶质质量分数会变大
22.甲、乙两种固体的溶解度曲线如图一所示,t2℃时,100克水中加入60克硝酸钾,充分搅拌,直到固体完全消失,然后按图二进行实验,分别采用不同方法(每种方法只改变一个量),得到三个恰好饱和的溶液,且溶液质量依次减小。
(1)t1℃时,溶解度大小关系为:甲
乙(填“>”或“<”或“=”);
(2)由图二推测硝酸钾是图一中的
物质(填“甲”或“乙”);
(3)图二中“某一步操作”得到D溶液前后的溶液状态变化过程可以在图一中表示为
;
A.b点→a点
B.c点→a点
C.b点→c点
D.c点→d点
(4)图二中得到的C、D、E溶液中质量分数大小关系是
(用“>或<或=”表示)。
23.氯化铵、硫酸钠两种物质的溶解度曲线如图一所示,根据图示回答下列问题:
(1)40℃时,硫酸钠的饱和溶液中溶质质量与溶剂质量比为
。
(2)70℃时,将65g硫酸钠加入到100g水中充分搅拌,形成硫酸钠溶液的质量为
g。
(3)将60℃时氯化铵的不饱和溶液转变成饱和,可以采用一种方法是
。
(4)要使40℃时的硫酸钠饱和溶液析出晶体,可以采取的措施是
(填选项序号)。
A.蒸发溶剂
B.增加溶剂
C.降低温度
D.升高温度
(5)如图二所示,20℃时,把试管放入盛有氯化铵饱和溶液的烧杯中(无剩余晶体),在试管中加入几小段镁条,再加入5mL稀硫酸,立即产生大量的气泡,反应中试管外壁会发烫,发生反应的化学方程式为
,关于烧杯中氯化铵溶液一定不变的量是
(填数字序号)。
①溶液温度
②溶质质量
③溶剂质量
④溶解度
⑤溶质质量分数
(6)小强同学要在实验室配制15%的氯化铵溶液50g。需要氯化铵的质量为
克,若将该溶液稀释成5%的氯化铵溶液,需要加水
克。
24.如图1是A、B、C三种物质的溶解度曲线,请回答。
(1)t2℃时,将30克A物质放入50克水中,充分溶解后所得溶液中溶质与溶剂的质量比为
。
(2)A物质中混有少量B物质,若提纯A物质,可采取的结晶方法是
。
(3)t1℃时,取等质量的A、C饱和溶液分别置于甲、乙两支试管中,如图2所示。在大烧杯中加入一定质量的硝酸铵固体溶解后,A、C溶液的溶质质量分数的大小关系是
。
参考答案
一.选择题(共20小题)
1.C;
2.A;
3.C;
4.D;
5.D;
6.B;
7.B;
8.C;
9.B;
10.B;
11.C;
12.D;
13.C;
14.D;
15.D;
16.B;
17.B;
18.D;
19.B;
20.D;
二.解答题(共4小题)
21.t2;65;X;①③④;
22.>;甲;B;C=E>D;
23.1:2;145;增加溶质;ACD;Mg+H2SO4=MgSO4+H2↑;②③⑤;7.5;100;
24.2:5;降温结晶;A<C;
同课章节目录
