2021届高中化学考前三个月专项复习课件(101张ppt) 题型三 逐空突破
文档属性
| 名称 | 2021届高中化学考前三个月专项复习课件(101张ppt) 题型三 逐空突破 |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-03 00:00:00 | ||
图片预览










文档简介
逐空突破
题型三 化学反应原理综合题的研究
1.书写热化学方程式的“五环节”
常考题空1 热化学方程式及反应热的计算
2.利用盖斯定律书写热化学方程式
题组一 热化学方程式的书写
1.依据反应事实书写有关热化学方程式:
(1)[2020·浙江7月选,29(1)①]C2H6(g)+2CO2(g) 4CO(g)+3H2(g) ΔH=______kJ·mol-1。
已知:298 K时,相关物质的相对能量(如图)。
可根据相关物质的相对能量计算反应或变化的ΔH(ΔH随温度变化可忽略)。例如:
对点集训
1
2
3
4
5
H2O(g)===H2O(l) ΔH=-286 kJ·mol-1-(-242 kJ·mol-1)=-44 kJ·mol-1。
430
(2)[2017·天津,7(3)]0.1 mol Cl2与焦炭、TiO2完全反应,生成一种还原性气体和一种易水解成TiO2·xH2O的液态化合物,放热4.28 kJ,该反应的热化学方程式为__________________________________________________
______________。
1
2
3
4
5
2Cl2(g)+TiO2(s)+2C(s)===TiCl4(l)+2CO(g) ΔH=
-85.6 kJ·mol-1
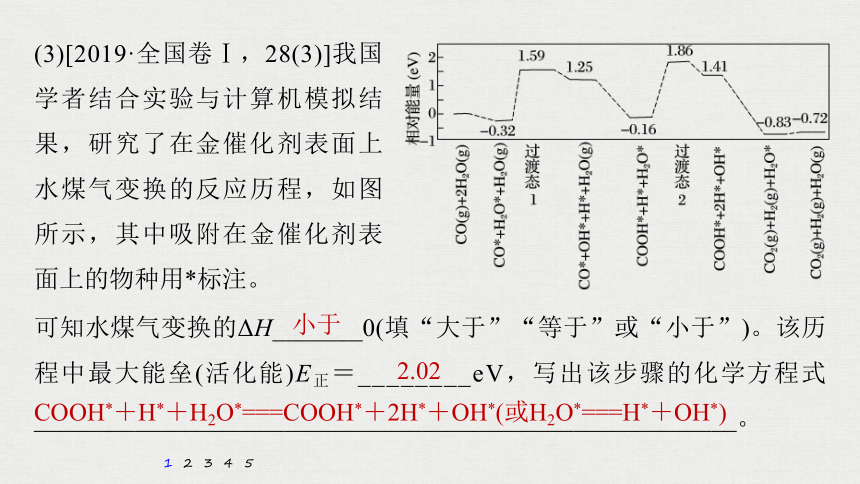
(3)[2019·全国卷Ⅰ,28(3)]我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。
1
2
3
4
5
可知水煤气变换的ΔH_______0(填“大于”“等于”或“小于”)。该历程中最大能垒(活化能)E正=________eV,写出该步骤的化学方程式________________________________________________________。
小于
2.02
COOH*+H*+H2O*===COOH*+2H*+OH*(或H2O*===H*+OH*)
解析 观察始态物质的相对能量与终态物质的相对能量知,终态物质相对能量低于始态物质相对能量,说明该反应是放热反应,ΔH小于0。过渡态物质相对能量与始态物质相对能量相差越大,活化能越大,由题图
1
2
3
4
5
知,最大活化能E正=1.86 eV-(-0.16 eV)=2.02 eV,该步起始物质为COOH*+H*+H2O*,产物为COOH*+2H*+OH*。
2.运用盖斯定律书写下列热化学方程式:
已知:25 ℃、101 kPa时,Mn(s)+O2(g)===MnO2(s) ΔH=-520 kJ·mol-1
S(s)+O2(g)===SO2(g) ΔH=-297 kJ·mol-1
Mn(s)+S(s)+2O2(g)===MnSO4(s) ΔH=-1 065 kJ·mol-1
则SO2与MnO2反应生成无水MnSO4的热化学方程式是_________________
_________________________________。
1
2
3
4
5
MnO2(s)+SO2(g)
===MnSO4(s) ΔH=-248 kJ·mol-1
解析 将题给三个热化学方程式依次编号为①②③,根据盖斯定律,由③-①-②可得SO2(g)+MnO2(s)===MnSO4(s) ΔH=(-1 065 kJ·mol-1)-(-520 kJ·mol-1)-(-297 kJ·mol-1)=-248 kJ·mol-1。
解析 将已知热化学方程式依次编号为①②③,根据盖斯定律,由(①+②+③)×2得4HCl(g)+O2(g)===2Cl2(g)+2H2O(g) ΔH=-116 kJ·mol-1。
题组二 计算化学反应的焓变(ΔH)
3.[2019·全国卷Ⅲ,28(1)]Deacon发明的直接氧化法为:4HCl(g)+O2(g)===2Cl2(g)+2H2O(g)。可按下列催化过程进行:
CuCl2(s)===CuCl(s)+ Cl2(g) ΔH1=83 kJ·mol-1
CuCl(s)+ O2(g)===CuO(s)+ Cl2(g) ΔH2=-20 kJ·mol-1
CuO(s)+2HCl(g)===CuCl2(s)+H2O(g) ΔH3=-121 kJ·mol-1
则4HCl(g)+O2(g)===2Cl2(g)+2H2O(g)的ΔH=________kJ·mol-1。
1
2
3
4
5
-116
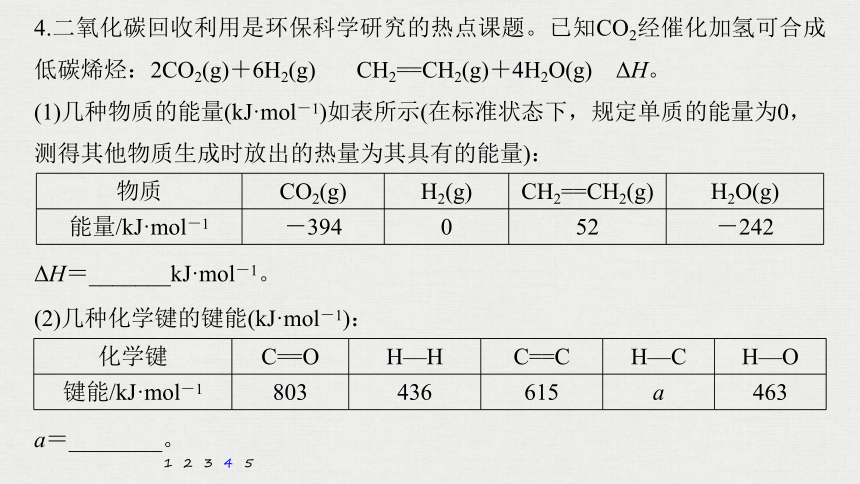
a=________。
4.二氧化碳回收利用是环保科学研究的热点课题。已知CO2经催化加氢可合成低碳烯烃:2CO2(g)+6H2(g) CH2==CH2(g)+4H2O(g) ΔH。
(1)几种物质的能量(kJ·mol-1)如表所示(在标准状态下,规定单质的能量为0,测得其他物质生成时放出的热量为其具有的能量):
1
2
3
4
5
物质
CO2(g)
H2(g)
CH2==CH2(g)
H2O(g)
能量/kJ·mol-1
-394
0
52
-242
(2)几种化学键的键能(kJ·mol-1):
化学键
C==O
H—H
C==C
H—C
H—O
键能/kJ·mol-1
803
436
615
a
463
ΔH=_______kJ·mol-1。
1
2
3
4
5
[思路点拨] 从宏观的角度讲,反应热是生成物自身的总能量与反应物自身的总能量的差值,根据第(1)问中所给出的各物质所具有的能量,可以计算反应的热效应。从微观的角度讲,反应热是旧化学键断裂吸收的能量与新化学键形成放出的能量的差值,已知反应的热效应和部分化学键的键能,可求某一化学键的键能。
4.二氧化碳回收利用是环保科学研究的热点课题。已知CO2经催化加氢可合成低碳烯烃:2CO2(g)+6H2(g) CH2==CH2(g)+4H2O(g) ΔH。
(1)几种物质的能量(kJ·mol-1)如表所示(在标准状态下,规定单质的能量为0,测得其他物质生成时放出的热量为其具有的能量):
1
2
3
4
5
物质
CO2(g)
H2(g)
CH2==CH2(g)
H2O(g)
能量/kJ·mol-1
-394
0
52
-242
ΔH=_______kJ·mol-1。
-128
解析 ΔH=生成物的总能量-反应物的总能量=(52-242×4-0+394×2)kJ·mol-1=-128 kJ·mol-1。
1
2
3
4
5
(2)几种化学键的键能(kJ·mol-1):
化学键
C==O
H—H
C==C
H—C
H—O
键能/kJ·mol-1
803
436
615
a
463
a=________。
409.25
解析 ΔH=断裂化学键的总键能-形成化学键的总键能=(803×4+436
×6-615-4a-463×8)kJ·mol-1=-128 kJ·mol-1,解得a=409.25。
5.(1)[2018·全国卷Ⅲ,28(1)(2)]三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。回答下列问题:
①SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式_____________________________
______。
1
2
3
4
5
2SiHCl3+3H2O===(HSiO)2O+
6HCl
解析 SiHCl3遇潮气时发烟生成(HSiO)2O等,结合原子守恒推知SiHCl3与水蒸气反应除生成(HSiO)2O外,还生成HCl,化学方程式为2SiHCl3+3H2O===(HSiO)2O+6HCl。
②SiHCl3在催化剂作用下发生反应:
2SiHCl3(g)===SiH2Cl2(g)+SiCl4(g) ΔH1=48 kJ·mol-1
3SiH2Cl2(g)===SiH4(g)+2SiHCl3(g) ΔH2=-30 kJ·mol-1
则反应4SiHCl3(g)===SiH4(g)+3SiCl4(g)的ΔH为____kJ·mol-1。
1
2
3
4
5
114
解析 将题给两个热化学方程式依次编号为①②,根据盖斯定律,由①×3+②可得:
4SiHCl3(g)===SiH4(g)+3SiCl4(g),则有ΔH=3ΔH1+ΔH2=3×48 kJ·mol-1+(-30 kJ·mol-1)=114 kJ·mol-1。
(2)[2020·浙江7月选考,29(1)③]有研究表明,在催化剂存在下,反应C2H6(g)+CO2(g) C2H4(g)+H2O(g)+CO(g) ΔH=177 kJ·mol-1分两步进行,过程如下:[C2H6(g)+CO2(g)]―→[C2H4(g)+H2(g)+CO2(g)]―→[C2H4(g)+CO(g)+H2O(g)],且第二步速率较慢(反应活化能为210 kJ·mol-1)。根据相关物质的相对能量,画出反应分两步进行的“能量—反应过程图”,起点从[C2H6(g)+CO2(g)]的能量-477 kJ·mol-1开始(如图)。
1
2
3
4
5
已知:C2H6(g) C2H4(g)+H2(g) ΔH=136 kJ·mol-1
CO2(g)+H2(g) CO(g)+H2O(g) ΔH=41 kJ·mol-1
答案
1
2
3
4
5
1.有关化学反应速率计算公式的理解
对于反应mA(g)+nB(g)===cC(g)+dD(g)
(1)计算公式: 。
(2)同一反应用不同的物质表示反应速率时,数值可能不同,但意义相同。不同物质表示的反应速率,存在如下关系:v(A)∶v(B)∶v(C)∶v(D)=m∶n∶c∶d。
常考题空2 有关反应速率、平衡常数、转化率的计算
(3)注意事项
①浓度变化只适用于气体和溶液中的溶质,不适用于固体和纯液体。
②化学反应速率是某段时间内的平均反应速率,而不是瞬时速率,且计算时取正值。
2.化学平衡计算中常用公式
(1)对于可逆反应:aA(g)+bB(g) cC(g)+dD(g)在一定温度下达到化学平衡时,其化学平衡常数计算的表达式为
K= (式中的浓度是指平衡状态的浓度)
Kp=
其中p(A)、p(B)、p(C)、p(D)分别为A、B、C、D各气体的分压,
气体的分压=气体总压×体积分数=气体总压×气体的物质的量分数。
(2)同一化学反应,化学反应方程式写法不同,其平衡常数表达式亦不同。例如:
N2O4(g) NO2(g) K′= =
因此书写平衡常数表达式时,要与化学反应方程式相对应。
(3)转化率计算公式
比较a、b处反应速率大小:va______vb(填“大于”“小于”或“等于”)。反应速率v=v正-v逆= ,k正、k逆分别为正、逆向反应速率
常数,x为物质的量分数,计算a处的 =_____(保留1位小数)。
题组一 有关化学反应速率的计算
1.[2018·全国卷Ⅲ,28(3)]对于反应2SiHCl3(g)=== SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
对点集训
1
2
3
4
5
6
7
8
大于
1.3
1
2
3
4
5
6
7
8
解析 温度越高,反应速率越快,a点温度为343 K,b点温度为323 K,故反应速率:va>vb。反应速率v=v正-v逆=k正 -k逆 ,则有v正=
k正 ,v逆=k逆 ,343 K下反应达到平衡状态时v正=v逆,即k正 =k逆 ,此时SiHCl3的平衡转化率α=22%,
经计算可得SiHCl3、SiH2Cl2、SiCl4的物质的量分数分别为0.78、0.11、0.11,
a处SiHCl3的平衡转化率α=20%,此时SiHCl3、SiH2Cl2、SiCl4的物质的量分数分别为0.8、0.1、0.1,
1
2
3
4
5
6
7
8
则有 = = = ≈1.3。
2.CO与Ni发生羰化反应形成的络合物可作为催化烯烃反应的催化剂。Ni的羰化反应为Ni(s)+4CO(g) Ni(CO)4(g) ΔH<0,T0温度下,将足量的Ni粉和3.7 mol CO加入到刚性密闭容器中,10 min时反应达到平衡,测
得体系的压强为原来的 。则:
(1)0~10 min内平均反应速率v(Ni)=_____g·min-1。
1
2
3
4
5
6
7
8
5.31
1
2
3
4
5
6
7
8
解析 在恒容密闭容器中,气体的压强之比等于气体的物质的量之比,在反应开始时加入了3.7 mol CO,反应达到平衡时测得体系的压强为原来的 ,则气体的物质的量为n(气体)= ×3.7 mol=1 mol,假设平衡时反应产生Ni(CO)4(g)为x mol,则反应消耗CO物质的量为4x mol,平衡时CO物质的量为(3.7-4x) mol,则(3.7-4x) mol+x mol=1 mol,解得x=0.9,由方程式可知消耗的Ni与反应产生的Ni(CO)4(g)的物质的量相同,因此10 min内反应消耗Ni的物质的量为0.9 mol,其质量是m(Ni)=0.9 mol ×59 g·mol-1=53.1 g,所以0~10 min内平均反应速率v(Ni)=53.1 g÷10 min=5.31 g·min-1;
(2)研究表明,正反应速率v正=k正·x4(CO),逆反应速率v逆=k逆·x[Ni(CO)4]
(k正和k逆分别表示正反应和逆反应的速率常数,x为物质的量分数),计算
T0温度下的 =_______。
1
2
3
4
5
6
7
8
9×103
解析 当反应达到平衡时v正=v逆,由于正反应速率v正=k正·x4(CO),逆反应速率v逆=k逆·x[Ni(CO)4],
1
2
3
4
5
6
7
8
根据①可知平衡时n[Ni(CO)4]=0.9 mol,n(CO)=1.0 mol-0.9 mol=0.1 mol,
题组二 有关平衡常数及转化率的计算
3.(1)[2019·全国卷Ⅱ,27(2)]已知: (g)+I2(g)=== (g)+2HI(g) ΔH>0。
某温度,等物质的量的碘和环戊烯( )在刚性容器内发生反应,起始总压为105 Pa,平衡时总压增加了20%,环戊烯的转化率为______,该反应的平衡常数Kp=__________Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有_____(填标号)。
A.通入惰性气体 B.提高温度
C.增加环戊烯浓度 D.增加碘浓度
1
2
3
4
5
6
7
8
40%
3.56×104
BD
解析 设容器中起始加入I2(g)和环戊烯的物质的量均为a,平衡时转化的环戊烯的物质的量为x,列出三段式:
1
2
3
4
5
6
7
8
(g) + I2(g) === (g)+2HI(g)
起始: a a 0 0
转化: x x x 2x
平衡: a-x a-x x 2x
根据平衡时总压强增加了20%,且恒温恒容时,压强之比等于气体物质的量之比,
通入惰性气体,对反应的平衡无影响,A项不符合题意;
1
2
3
4
5
6
7
8
反应为吸热反应,提高温度,平衡正向移动,可提高环戊烯的平衡转化率,B项符合题意;
增加环戊烯浓度,能提高I2(g)的平衡转化率,但环戊烯的平衡转化率降低,C项不符合题意;
增加I2(g)的浓度,能提高环戊烯的平衡转化率,D项符合题意。
1
2
3
4
5
6
7
8
(2)(2020·福建适应性测试)将H2O与COS以体积比1∶2置于恒温恒容密闭容器中反应:H2O(g)+COS(g)===H2S(g)+CO2(g),若测得该反应平衡时 H2O与COS的体积比1∶6,则该温度下,脱除反应的平衡常数K=______
(保留两位小数)。
1
2
3
4
5
6
7
8
2.67
解析 根据题意列三段式:
H2O(g)+COS(g) H2S(g)+CO2(g)(单位:mol)
起始量:1 2 0 0
转化量:x x x x
平衡量:1-x 2-x x x
1
2
3
4
5
6
7
8
4.(2020·皖南八校第三次联考)(1)在某密闭容器中发生反应:2CO2(g) 2CO(g)+O2(g),0.995 mol CO2在不同温度下的平衡分解情况如图所示。
1
2
3
4
5
6
7
8
①图中a、b、c三点的平衡常数K(a)、K(b)、K(c)的大小关系为__________。
Ka=Kb②若1 660 ℃时反应达到平衡状态,且容器体积为1 L,则该温度下,该反应的逆反应2CO(g)+O2(g) 2CO2 (g)的平衡常数K=________。
1.9×106
解析 设生成O2为x mol
1
2
3
4
5
6
7
8
2CO2(g) 2CO(g)+O2(g)
起:0.995 0 0
转:2x 2x x
平:0.995-2x 2x x
平衡时氧气的体积分数为0.5%
(2)573.2 K时,向一刚性密闭容器中充入5.00 MPa CH3OH使其分解,CH3OH(g) CO(g)+2H2(g),t h后达平衡时H2的物质的量分数为60%,
则t h内v(CH3OH)=_____MPa·h-1,其分压平衡常数Kp=_______(MPa)2。
1
2
3
4
5
6
7
8
168.75
1
2
3
4
5
6
7
8
解析 CH3OH(g) CO(g)+2H2(g)
始 5 MPa 0 0
转 a a 2a
平 5 MPa-a a 2a
得a=3.75 MPa,
5.亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO和Cl2反应得到,化学方程式为2NO(g)+Cl2(g) 2NOCl(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
①2NO2(g)+NaCl(s) NaNO3(s)+NOCl(g)
②4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)
③2NO(g)+Cl2(g) 2NOCl(g)
设反应①②③对应的平衡常数依次为K1、K2、K3,则K1、K2、K3之间的关系为__________。
1
2
3
4
5
6
7
8
解析 根据①×2-②=③,从而可推知平衡常数之间的关系。
(2)在1 L恒容密闭容器中充入2 mol NO(g)和1 mol Cl2(g),在不同温度下测得c(NOCl)与时间t的关系如图A所示:
1
2
3
4
5
6
7
8
①反应开始到10 min时NO的平均反应速率v(NO)=____ mol·L-1·min-1。
0.1
解析 10 min时,c(NOCl)=1 mol·L-1,则转化的NO的物质的量为1 mol,
则v(NO)= =0.1 mol·L-1·min-1。
②T2时该反应的平衡常数K为____。
1
2
3
4
5
6
7
8
2
③T2时Cl2的平衡转化率为______。
50%
(3)若按投料比[n(NO)∶n(Cl2)]=2∶1把NO和Cl2加入到一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强p(总压)的关系如图B所示:
1
2
3
4
5
6
7
8
①该反应的ΔH____(填“>”“<”或“=”)0。
<
解析 根据图像,升高温度,平衡时NO的转化率减小,说明平衡逆向移动,说明该反应正反应属于放热反应,ΔH<0。
②在p压强条件下,M点时容器内NO的体积分数为______。
1
2
3
4
5
6
7
8
40%
解析 根据图像,在p压强条件下,M点时容器内NO的转化率为50%,根据2NO(g)+Cl2(g) 2NOCl(g)可知,气体减小的体积为反应的NO的
体积的一半,因此NO的体积分数为 ×100%=40%。
③若反应一直保持在p压强条件下进行,则
M点的分压平衡常数Kp=____(用含p的表达式表示,用平衡分压代替平衡浓度计算,分压=总压×体积分数)。
1
2
3
4
5
6
7
8
解析 设NO的物质的量为2 mol,则Cl2的物质的量为1 mol。
2NO(g) + Cl2(g) 2NOCl(g)
起始/mol 2 1 0
反应/mol 1 0.5 1
平衡/mol 1 0.5 1
1
2
3
4
5
6
7
8
题组三 平衡常数与速率常数的关系
6.顺-1,2-二甲基环丙烷和反-1,2-二甲基环丙烷可发生如右转化:
1
2
3
4
5
6
7
8
该反应的速率方程可表示为v(正)=
k(正)c(顺)和v(逆)=k(逆)c(反),k(正)和k(逆)在一定温度时为常数,分别称作正、逆反应速率常数。回答下列问题:
(1)已知:t1温度下,k(正)=0.006 s-1,k(逆)=0.002 s-1,该温度下反应的平衡常数值K1=____;该反应的活化能Ea(正)小于Ea(逆),则ΔH______
(填“小于”“等于”或“大于”)0。
3
小于
1
2
3
4
5
6
7
8
解析 根据v(正)=k(正)c(顺),k(正)=0.006 s-1,则v(正)=0.006 c(顺),v(逆)=k(逆)c(反),k(逆)=0.002 s-1,则v(逆)=0.002c(反),化学平衡状态时正、逆反应速率相等,则0.006c(顺)=0.002c(反),该温度下反应的
平衡常数 ;该反应的活化能Ea(正)小于Ea(逆),说明
断键吸收的能量小于成键释放的能量,即该反应为放热反应,则ΔH小于0。
(2)t2温度下,图中能表示顺式异构体的质量分数随时间变化的曲线是_____(填曲线编号),平
衡常数值K2=_____;温度t1______(填“小于”
1
2
3
4
5
6
7
8
B
小于
“等于”或“大于”)t2,判断理由是_______________________________
_________________。
该反应是放热反应,升高温度平衡
向逆反应方向移动
1
2
3
4
5
6
7
8
解析 随着时间的推移,顺式异构体的质量分数不断减少,且减少速率随时间减小,则符合条件的曲线是B。设顺式异构体的起始浓度为x,可逆反应左右物质的化学计量数相等,均为1,则平衡时,顺式异构体为
0.3x,反式异构体为0.7x,所以平衡常数为 。因为K1>K2,
对于放热反应升高温度时平衡逆向移动,所以温度t2>t1。
1
2
3
4
5
6
7
8
7.纳米铁是重要的储氢材料,可用反应Fe(s)+5CO(g)
Fe(CO)5(g)制得。在1 L恒容密闭容器中加入足量铁粉和0.48 mol CO,在T1、T2不同温度下进行反应,测得c(CO)与温度、时间的关系如图所示。
(1)T1_____T2,ΔH_____0(填“>”或“<”)。
>
<
解析 温度越高反应速率越快,达到平衡所需要的时间越短,所以T1>T2,据图可知温度越高平衡时CO的浓度越大,说明温度升高平衡左移,所以该反应正反应为放热反应,ΔH<0;
(2)T2温度下,平衡时体系的压强为p,反应的标准
平衡常数Kθ=________(已知:标准平衡常数Kθ
=,其中pθ为标准压强(1×105Pa),
p[Fe(CO)5]、p(CO)为各组分的平衡分压)。
1
2
3
4
5
6
7
8
解析 反应初始投料为足量铁粉和0.48 mol CO,平衡时n(CO)=0.08 mol,则消耗的n(CO)=0.4 mol,根据方程式可知生成的n[Fe(CO)5]=0.08 mol,平衡时压强为p,压强比等于物质的量之比,
1
2
3
4
5
6
7
8
8.某化学小组查阅资料后得知:2NO(g)+O2(g) 2NO2(g) 的反应历程分两步:
①2NO(g)===N2O2(g) (快)
v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2)
②N2O2(g)+O2(g)===2NO2(g)(慢)
v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2)
请回答下列问题:
(1)已知决定2NO(g)+O2(g) 2NO2(g)反应速率的是反应②,则反应①的活化能E1与反应②的活化能E2的大小关系为E1____E2(填“>”“<”或“=”)。
1
2
3
4
5
6
7
8
<
1
2
3
4
5
6
7
8
解析 决定2NO(g)+O2(g) 2NO2(g)速率的是反应②,活化能越高,反应速率越慢,因此反应①的活化能E1与反应②的活化能E2的大小关系为E1(2)一定温度下,反应2NO(g)+O2(g) 2NO2(g)达到平衡状态,写出用
k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=________。
1
2
3
4
5
6
7
8
常考题空3 电解质溶液中有关平衡常数的计算
1.依据电离常数表达式计算(以弱酸HA为例)
2.溶度积(Ksp)的常见计算类型
(1)已知溶度积求溶液中的某种离子的浓度,如Ksp=a的饱和AgCl溶液中c(Ag+)= mol·L-1。
(2)已知溶度积、溶液中某离子的浓度,求溶液中的另一种离子的浓度,如某温度下AgCl的Ksp=a,在0.1 mol·L-1的NaCl溶液中加入过量的AgCl固体,达到平衡后c(Ag+)=10a mol·L-1。
题组一 有关电离常数的计算
1.(1)[2020·天津,16(5)节选]已知25 ℃碳酸电离常数为Ka1、Ka2,当溶液pH=12时, =1∶________∶__________。
1
2
3
4
5
6
对点集训
1024·Ka1·Ka2
1012·Ka1
当溶液pH=12时,c(H+)=10-12 mol·L-1,代入Ka1、Ka1·Ka2可得:c(H2CO3)∶ =1∶(1012·Ka1),c(H2CO3)∶ =1∶(1024·Ka1·Ka2),
1
2
3
4
5
6
综合可得:c(H2CO3)∶ ∶ =1∶(1012·Ka1)∶(1024·Ka1·Ka2)。
(2)[2020·全国卷Ⅱ,26(2)]次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各
成分的组成分数δ[δ(X)= ,
X为HClO或ClO-]与pH的关系如图所示。HClO的电离常数Ka值为______。
1
2
3
4
5
6
10-7.5
1
2
3
4
5
6
2.25 ℃时,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合所得溶液中 =c(Cl-),则溶液显_____(填“酸”“碱”或“中”)性;用含a
的代数式表示NH3·H2O的电离平衡常数Kb=________。
1
2
3
4
5
6
中
3.大气污染物SO2可用NaOH溶液吸收。已知pKa=-lgKa,25 ℃时,用0.1 mol·L-1 NaOH溶液滴定20 mL 0.1 mol·L-1 H2SO3溶液的滴定曲线如图。
1
2
3
4
5
6
(1)c点所得溶液中:c(Na+)____ (填“>”“<”或“=”)。
>
(2)依据图像计算H2SO3在25 ℃的pKa1=_____,pKa2=_____。
1
2
3
4
5
6
1.85
7.19
4.常温下,用0.100 0 mol·L-1的NaOH溶液滴定某浓度的二元弱酸(H2X)溶液,所得溶液中各种含X的微粒的物质的量分数(δ)与pH的变化曲线如图所示。
1
2
3
4
5
6
(1)计算H2X的一级电离常数Ka1=_______(幂指数的形式且可以是小数,下同)。
10-1.2
(2)X2-的一级水解常数Kh=_______。
1
2
3
4
5
6
10-9.8
题组二 有关Ksp的计算
5.(1)[2017·海南,14(3)]向含有BaSO4固体的溶液中滴加Na2CO3溶液,当
有BaCO3沉淀生成时溶液中 =______。[已知Ksp(BaCO3)=2.6×
10-9,Ksp(BaSO4)=1.1×10-10]。
1
2
3
4
5
6
23.6
解析 根据Ksp(AgCl)=c(Ag+)·c(Cl-)=2.0×10-10,可计算出当溶液中Cl-恰好完全沉淀(即浓度等于1.0×10-5 mol·L-1)时,溶液中c(Ag+)=2.0×10-5 mol·L-1,然后再根据Ksp(Ag2CrO4)=c2(Ag+)·c( )=2.0×
10-12,又可计算出此时溶液中c( )=5.0×10-3 mol·L-1。
(2)[2016·全国卷Ⅰ,27(3)]在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中的Cl-,利用Ag+与 生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好完全沉淀(浓度等于1.0×10-5 mol·L-1)时,溶液中c(Ag+)为_____________mol·L-1,此时溶液中c( )等于___________mol·L-1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)
1
2
3
4
5
6
2.0×10-5
5.0×10-3
(3)[2015·全国卷Ⅱ,26(4)]用废电池的锌皮制备ZnSO4·7H2O的过程中,需除去锌皮中的少量杂质铁,其方法是:加稀H2SO4和H2O2溶解,铁变为______,加碱调节至pH为_____时,铁刚好沉淀完全(离子浓度小于1×10-5 mol·L-1时,即可认为该离子沉淀完全);继续加碱至pH为_____时,锌开始沉淀(假定Zn2+浓度为0.1 mol·L-1)。若上述过程不加H2O2后果是____________________,原因是___________________________。
(已知Ksp[Zn(OH)2]=10-17,Ksp[Fe(OH)2]=10-17,Ksp[Fe(OH)3]=10-39)
1
2
3
4
5
6
Fe3+
2.7
6
Zn2+和Fe2+不能分离
Fe(OH)2和Zn(OH)2的Ksp相近
Zn(OH)2和Fe(OH)2的Ksp相近,若不加双氧水,沉淀Fe2+的同时Zn2+也会被沉淀,从而使Zn2+和Fe2+不能分离。
解析 铁溶于稀硫酸生成Fe2+,Fe2+被双氧水氧化为Fe3+。
Ksp[Fe(OH)3]=c(Fe3+)·c3(OH-)=10-39,
1
2
3
4
5
6
Ksp[Zn(OH)2]=c(Zn2+)·c2(OH-)=10-17,
6.常温下,在一定量的氯化铜溶液中逐滴加入氨水至过量,可观察到先产生蓝色沉淀,后蓝色沉淀溶解转化成蓝色溶液。[已知Ksp[Cu(OH)2]=2.2×10-20]
(1)当pH=8时,表明已完全沉淀,计算此时c(Cu2+)=_________ mol·L-1。
1
2
3
4
5
6
2.2×10-8
(2)常温下,Cu2+(aq)+4NH3(aq) [Cu(NH3)4]2+(aq) K1=2.0×1013,蓝色沉淀溶解过程中存在平衡:Cu(OH)2(s)+4NH3(aq) [Cu(NH3)4]2+(aq)+2OH-(aq),其平衡常数K2=_________。
1
2
3
4
5
6
4.4×10-7
一、图像题的审题要领
1.看题干,明方向:看清题目要求,在题干中圈出关键词,明确是速率问题还是平衡移动问题,分清楚是“恒温恒压”还是“恒温恒容”,或其他限制条件。
常考题空4 读懂图像——精准判断速率、平衡对实际生产的调控作用
2.识图表,“面、点、线”
识图是解题的基础,①面即坐标系,明晰横、纵坐标所表示的化学含义,这是理解题意和进行正确思维的前提。明晰坐标含义,也就是用变量的观点分析坐标,找出横、纵坐标的关系,再结合教材,联系相应的知识点。②找点:找出曲线中的特殊点(起点、顶点、拐点、终点、交叉点、平衡点等),分析这些点所表示的化学意义以及影响这些点的主要因素及限制因素等,大多考题就落在这些点的含义分析上,因为这些点往往隐含着某些限制条件或某些特殊的化学含义。③析线:正确分析曲线的走向、变化趋势(上升、下降、平缓、转折等),同时对走势有转折变化的曲线,要分区段进行分析,研究找出各段曲线的变化趋势及其含义。
二、应用举列
1.涉及温度、压强对平衡影响类简答题
答题要领:叙特点(反应特点或容器特点)→变条件→定方向→得结论(或结果)
例1 在密闭容器中充入一定量H2S,发生反应2H2S(g) 2H2(g)+S2(g) ΔH=+169.8 kJ·mol-1。如图为H2S气体的平衡转化率与温度、压强的关系。
(1)图中压强(p1、p2、p3)的大小顺序为________,理由是______________________________________。
(2)该反应平衡常数大小:K(T1)________(填“>”“<”或“=”)K(T2),理由是_________________________________________________________。
(3)如果要进一步提高H2S的平衡转化率,除改变温度、压强外,还可以采取的措施有___________________________________________________。
[解题思路]
例1 在密闭容器中充入一定量H2S,发生反应2H2S(g) 2H2(g)+S2(g) ΔH=+169.8 kJ·mol-1。如图为H2S气体的平衡转化率与温度、压强的关系。
(1)图中压强(p1、p2、p3)的大小顺序为________,
理由是_________________________________________________________
____________________________________________________________________________________________________________________________。
p1 该反应的正反应是气体分子数增大的反应,其他条件不变时,减小压强使平衡正向移动,H2S的平衡转化率增大,由图像上看,相同温度,p1条件下H2S的平衡转化率最大,p3条件下H2S的平衡转化率最小
(2)该反应平衡常数大小:K(T1)______(填“>” “<”或“=”)K(T2),理由是________________
___________________________________________。
(3)如果要进一步提高H2S的平衡转化率,除改变温度、压强外,还可以采取的措施有___________
_____。
<
该反应正向是吸热
反应,升高温度,平衡正向移动,平衡常数增大
及时分离出
产物
2.图像中转化率变化分析
答题要领:转化率问题首先看是否是平衡转化率,若为非平衡状态的转化率,则侧重分析温度、压强、浓度对反应快慢、催化剂对反应快慢及选择性(主副反应)的影响;若为平衡转化率,则侧重分析温度、压强、浓度对化学平衡的影响,有时也涉及温度对催化活性的影响。
例2 (2017·全国卷Ⅱ,27改编)丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。C4H10(g)===C4H8(g)+H2(g) ΔH=+123 kJ·mol-1
回答下列问题:
(1)图(a)是该反应平衡转化率与反应温度及压强的
关系图,x________0.1(填“大于”或“小于”);
欲使丁烯的平衡产率提高,应采取的措施是_____
(填标号)。
A.升高温度 B.降低温度
C.增大压强 D.降低压强
[审题要领] 抓关键词,“平衡产率”。
小于
AD
解析 由图(a)可以看出,温度相同时,由0.1 MPa变化到x MPa,丁烷的转化率增大,即平衡正向移动,所以x<0.1。由于反应为吸热反应,所以温度升高时,平衡正向移动,丁烯的平衡产率增大,因此A正确,B错误;
反应正向进行时体积增大,加压时平衡逆向移动,丁烯的平衡产率减小,因此C错误,D正确。
(2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。图(b)为丁烯产率与进料气中n(氢气)/n(丁烷)的关系。图中曲线呈现先升高后降低的变化趋势,
[审题要领] “产率”“氢气的作用”。
其降低的原因是_________________________________________________
_________________。
氢气是产物之一,随着n(氢气)/n(丁烷)的增大,该反应
向逆反应方向进行
解析 反应初期,H2可以活化催化剂,进料气中n(氢气)/n(丁烷)较小,丁烷浓度大,反应向正反应方向进行的程度大,丁烯产率升高;随着进料气中n(氢气)/n(丁烷)增大,原料中过量的H2会使反应平衡逆向移动,所以丁烯产率下降。
(3)图(c)为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。丁烯产率在590 ℃之前随温度升高而增大的原因可能是________________________________、____________________________;590 ℃之后,
[审题要领] “副产物”产生的原因。
升高温度有利于反应向吸热方向进行
升高温度时,反应速率加快
丁烯产率快速降低的主要原因可能是___________________________。
丁烯高温裂解生成短碳链烃类
解析 590 ℃之前,温度升高时反应速率加快,生成的丁烯会更多,同时由于反应是吸热反应,升高温度平衡正向移动,平衡体系中会含有更多的丁烯。而温度超过590 ℃时,丁烯高温会裂解生成短碳链烃类,使产率降低。
3.依据图像,优选生产条件
[解题模型] 要从以下几个层面依次分析其中的“物理量”:
例3 [2017·天津理综,10(2)]已知:生物脱H2S的原理:
H2S+Fe2(SO4)3===S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4 2Fe2(SO4)3+2H2O
由图1和图2判断使用硫杆菌的最佳条件为_______________。若反应温度过高,反应速率下降,其原因是_____________________________。
30 ℃、pH=2.0
蛋白质变性(或硫杆菌失去活性)
解析 由图1可知,温度在30 ℃左右时,Fe2+氧化速率最快;由图2可知,反应混合液的pH=2.0左右时,Fe2+氧化速率最快。由此可推断使用硫杆菌的最佳条件为温度为30 ℃、混合液的pH=2.0。硫杆菌属于蛋白质,若反应温度过高,受热变性失活,导致反应速率下降。
解析 据图可知,温度控制在 650 ℃ ,丙烯选择性高,且此时温度较高,反应速率快,而且该温度条件下平衡常数较大。
1.丙烷催化直接脱氢反应:C3H8(g) C3H6(g)+H2(g) ΔH1=+124.3 kJ·mol -1 (ⅰ) 副反应:C3H8 (g) C2H4 (g)+CH4(g) ΔH2(ⅱ)
对点集训
1
2
3
(1)反应ⅰ的平衡常数、产物丙烯选择性、
副产物乙烯选择性与温度关系如图所示,
分析工业生产中采用的温度为 650 ℃ 左右的原因是_______________________
_________________________________。
温度控制在 650 ℃,丙烯
选择性高,反应速率快,平衡常数大
(2)温度为 670 ℃ 时,若在1 L的容器中投入 8 mol C3H8,充分反应后,平衡混合气体中有 2 mol CH4和一定量C3H8、C3H6、H2、C2H4,计算该条件下C3H6 的选择性为____%。(C3H6的选择性=
×100%)
1
2
3
50
解析 平衡混合气体中有 2 mol CH4,则根据反应ⅱ可知平衡时该反应消耗的n1(C3H8)=2 mol;设平衡时C3H6的物质的量为x,根据反应ⅰ可知平衡时n(H2)=x mol,反应ⅰ消耗的n2(C3H8)=x,则平衡时容器n(C3H8)=(8-2-x)mol,
1
2
3
(3)欲使丙烯的产率提高,下列措施可行
的是____(填字母)。
a.恒压条件下向原料气中掺杂水蒸气
b.增大氢气与丙烷的投料比
c.选择对脱氢反应更好选择性的催化剂
d.增大压强
1
2
3
ac
氢气为产物,增大氢气的量会使平衡逆向移动,丙烯的产率降低,故b错误;
选择对脱氢反应更好选择性的催化剂,增大丙烯的选择性,提高产率,故c正确;
该反应正反应为压强增大的反应,增大压强会使平衡逆向移动,降低产率,故d错误。
解析 恒压条件下向原料气中掺杂水蒸气,则反应物和生成物的分压减小,该反应正反应为压强增大的反应,减小压强平衡正向移动,可以提高丙烯的产率,故a正确;
1
2
3
(4)科学家探索出利用无机膜催化丙烷脱氢制丙烯的新工艺,该工艺利用特定功能膜将生成的氢气从反应区一侧有选择性的及时移走,从平衡角度分析该工艺的优点_____________________________
1
2
3
_______________________________________________。
将氢气及时移走,化学平衡
解析 氢气是反应ⅰ的产物,将氢气及时移走,C3H8(g) C3H6(g)+H2(g) 的化学平衡正向移动,提高丙烯产率。
2.乙苯催化脱氢制苯乙烯反应:
1
2
3
+H2(g) ΔH=+124 kJ·mol-1
工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1∶9),控制反应温度600 ℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)变化如图:
(1)掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实:___________________
______________________________________________________。
1
2
3
正反应方向气体分
子数增加,压强不变,加入水蒸气稀释,相当于起减压的效果
(2)控制反应温度为600 ℃的理由是___________________________________
________________________________________________________________________________________________。
600 ℃,乙苯的转化率和苯乙烯的选择
性均较高。温度过低,反应速率慢,转化率低;温度过高,选择性下降,高温还可能使催化剂失活,且能耗大
3.已知CO2催化加氢合成乙醇的反应原理为:2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) ΔH<0。
1
2
3
(1)图1、图2分别是CO2的平衡转化率随压强及温度的变化关系,已知m为起始时的
投料比,即m= 。①图1中投料比相
同,温度从高到低的顺序为__________,判断依据是___________________________
_____________________________________。
T3>T2>T1
正反应放热,升高温度平衡逆
向移动,温度越高,CO2的平衡转化率越小
②图2中m1、m2、m3从大到小的顺序为__________,判断依据是_____________
__________________________________________________。
1
2
3
m1>m2>m3
保持n(CO2)不
变,增大n(H2),平衡正向移动,CO2的平衡转化率增大
(2)图3表示在总压为5 MPa的恒压条件下,且m=3时,平衡状态时各物质的物质的量分数与温度的关系。则曲线d代表的物质为________(填化学式),T4温度时,该反应的平衡常数Kp=_____(提示:用平衡分压代替平衡浓度来计算,某组分平衡分压=总压×该组分的物质的量分数,结果保留小数点后三位)。
1
2
3
C2H5OH
0.243
1
2
3
题型三 化学反应原理综合题的研究
1.书写热化学方程式的“五环节”
常考题空1 热化学方程式及反应热的计算
2.利用盖斯定律书写热化学方程式
题组一 热化学方程式的书写
1.依据反应事实书写有关热化学方程式:
(1)[2020·浙江7月选,29(1)①]C2H6(g)+2CO2(g) 4CO(g)+3H2(g) ΔH=______kJ·mol-1。
已知:298 K时,相关物质的相对能量(如图)。
可根据相关物质的相对能量计算反应或变化的ΔH(ΔH随温度变化可忽略)。例如:
对点集训
1
2
3
4
5
H2O(g)===H2O(l) ΔH=-286 kJ·mol-1-(-242 kJ·mol-1)=-44 kJ·mol-1。
430
(2)[2017·天津,7(3)]0.1 mol Cl2与焦炭、TiO2完全反应,生成一种还原性气体和一种易水解成TiO2·xH2O的液态化合物,放热4.28 kJ,该反应的热化学方程式为__________________________________________________
______________。
1
2
3
4
5
2Cl2(g)+TiO2(s)+2C(s)===TiCl4(l)+2CO(g) ΔH=
-85.6 kJ·mol-1
(3)[2019·全国卷Ⅰ,28(3)]我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。
1
2
3
4
5
可知水煤气变换的ΔH_______0(填“大于”“等于”或“小于”)。该历程中最大能垒(活化能)E正=________eV,写出该步骤的化学方程式________________________________________________________。
小于
2.02
COOH*+H*+H2O*===COOH*+2H*+OH*(或H2O*===H*+OH*)
解析 观察始态物质的相对能量与终态物质的相对能量知,终态物质相对能量低于始态物质相对能量,说明该反应是放热反应,ΔH小于0。过渡态物质相对能量与始态物质相对能量相差越大,活化能越大,由题图
1
2
3
4
5
知,最大活化能E正=1.86 eV-(-0.16 eV)=2.02 eV,该步起始物质为COOH*+H*+H2O*,产物为COOH*+2H*+OH*。
2.运用盖斯定律书写下列热化学方程式:
已知:25 ℃、101 kPa时,Mn(s)+O2(g)===MnO2(s) ΔH=-520 kJ·mol-1
S(s)+O2(g)===SO2(g) ΔH=-297 kJ·mol-1
Mn(s)+S(s)+2O2(g)===MnSO4(s) ΔH=-1 065 kJ·mol-1
则SO2与MnO2反应生成无水MnSO4的热化学方程式是_________________
_________________________________。
1
2
3
4
5
MnO2(s)+SO2(g)
===MnSO4(s) ΔH=-248 kJ·mol-1
解析 将题给三个热化学方程式依次编号为①②③,根据盖斯定律,由③-①-②可得SO2(g)+MnO2(s)===MnSO4(s) ΔH=(-1 065 kJ·mol-1)-(-520 kJ·mol-1)-(-297 kJ·mol-1)=-248 kJ·mol-1。
解析 将已知热化学方程式依次编号为①②③,根据盖斯定律,由(①+②+③)×2得4HCl(g)+O2(g)===2Cl2(g)+2H2O(g) ΔH=-116 kJ·mol-1。
题组二 计算化学反应的焓变(ΔH)
3.[2019·全国卷Ⅲ,28(1)]Deacon发明的直接氧化法为:4HCl(g)+O2(g)===2Cl2(g)+2H2O(g)。可按下列催化过程进行:
CuCl2(s)===CuCl(s)+ Cl2(g) ΔH1=83 kJ·mol-1
CuCl(s)+ O2(g)===CuO(s)+ Cl2(g) ΔH2=-20 kJ·mol-1
CuO(s)+2HCl(g)===CuCl2(s)+H2O(g) ΔH3=-121 kJ·mol-1
则4HCl(g)+O2(g)===2Cl2(g)+2H2O(g)的ΔH=________kJ·mol-1。
1
2
3
4
5
-116
a=________。
4.二氧化碳回收利用是环保科学研究的热点课题。已知CO2经催化加氢可合成低碳烯烃:2CO2(g)+6H2(g) CH2==CH2(g)+4H2O(g) ΔH。
(1)几种物质的能量(kJ·mol-1)如表所示(在标准状态下,规定单质的能量为0,测得其他物质生成时放出的热量为其具有的能量):
1
2
3
4
5
物质
CO2(g)
H2(g)
CH2==CH2(g)
H2O(g)
能量/kJ·mol-1
-394
0
52
-242
(2)几种化学键的键能(kJ·mol-1):
化学键
C==O
H—H
C==C
H—C
H—O
键能/kJ·mol-1
803
436
615
a
463
ΔH=_______kJ·mol-1。
1
2
3
4
5
[思路点拨] 从宏观的角度讲,反应热是生成物自身的总能量与反应物自身的总能量的差值,根据第(1)问中所给出的各物质所具有的能量,可以计算反应的热效应。从微观的角度讲,反应热是旧化学键断裂吸收的能量与新化学键形成放出的能量的差值,已知反应的热效应和部分化学键的键能,可求某一化学键的键能。
4.二氧化碳回收利用是环保科学研究的热点课题。已知CO2经催化加氢可合成低碳烯烃:2CO2(g)+6H2(g) CH2==CH2(g)+4H2O(g) ΔH。
(1)几种物质的能量(kJ·mol-1)如表所示(在标准状态下,规定单质的能量为0,测得其他物质生成时放出的热量为其具有的能量):
1
2
3
4
5
物质
CO2(g)
H2(g)
CH2==CH2(g)
H2O(g)
能量/kJ·mol-1
-394
0
52
-242
ΔH=_______kJ·mol-1。
-128
解析 ΔH=生成物的总能量-反应物的总能量=(52-242×4-0+394×2)kJ·mol-1=-128 kJ·mol-1。
1
2
3
4
5
(2)几种化学键的键能(kJ·mol-1):
化学键
C==O
H—H
C==C
H—C
H—O
键能/kJ·mol-1
803
436
615
a
463
a=________。
409.25
解析 ΔH=断裂化学键的总键能-形成化学键的总键能=(803×4+436
×6-615-4a-463×8)kJ·mol-1=-128 kJ·mol-1,解得a=409.25。
5.(1)[2018·全国卷Ⅲ,28(1)(2)]三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。回答下列问题:
①SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式_____________________________
______。
1
2
3
4
5
2SiHCl3+3H2O===(HSiO)2O+
6HCl
解析 SiHCl3遇潮气时发烟生成(HSiO)2O等,结合原子守恒推知SiHCl3与水蒸气反应除生成(HSiO)2O外,还生成HCl,化学方程式为2SiHCl3+3H2O===(HSiO)2O+6HCl。
②SiHCl3在催化剂作用下发生反应:
2SiHCl3(g)===SiH2Cl2(g)+SiCl4(g) ΔH1=48 kJ·mol-1
3SiH2Cl2(g)===SiH4(g)+2SiHCl3(g) ΔH2=-30 kJ·mol-1
则反应4SiHCl3(g)===SiH4(g)+3SiCl4(g)的ΔH为____kJ·mol-1。
1
2
3
4
5
114
解析 将题给两个热化学方程式依次编号为①②,根据盖斯定律,由①×3+②可得:
4SiHCl3(g)===SiH4(g)+3SiCl4(g),则有ΔH=3ΔH1+ΔH2=3×48 kJ·mol-1+(-30 kJ·mol-1)=114 kJ·mol-1。
(2)[2020·浙江7月选考,29(1)③]有研究表明,在催化剂存在下,反应C2H6(g)+CO2(g) C2H4(g)+H2O(g)+CO(g) ΔH=177 kJ·mol-1分两步进行,过程如下:[C2H6(g)+CO2(g)]―→[C2H4(g)+H2(g)+CO2(g)]―→[C2H4(g)+CO(g)+H2O(g)],且第二步速率较慢(反应活化能为210 kJ·mol-1)。根据相关物质的相对能量,画出反应分两步进行的“能量—反应过程图”,起点从[C2H6(g)+CO2(g)]的能量-477 kJ·mol-1开始(如图)。
1
2
3
4
5
已知:C2H6(g) C2H4(g)+H2(g) ΔH=136 kJ·mol-1
CO2(g)+H2(g) CO(g)+H2O(g) ΔH=41 kJ·mol-1
答案
1
2
3
4
5
1.有关化学反应速率计算公式的理解
对于反应mA(g)+nB(g)===cC(g)+dD(g)
(1)计算公式: 。
(2)同一反应用不同的物质表示反应速率时,数值可能不同,但意义相同。不同物质表示的反应速率,存在如下关系:v(A)∶v(B)∶v(C)∶v(D)=m∶n∶c∶d。
常考题空2 有关反应速率、平衡常数、转化率的计算
(3)注意事项
①浓度变化只适用于气体和溶液中的溶质,不适用于固体和纯液体。
②化学反应速率是某段时间内的平均反应速率,而不是瞬时速率,且计算时取正值。
2.化学平衡计算中常用公式
(1)对于可逆反应:aA(g)+bB(g) cC(g)+dD(g)在一定温度下达到化学平衡时,其化学平衡常数计算的表达式为
K= (式中的浓度是指平衡状态的浓度)
Kp=
其中p(A)、p(B)、p(C)、p(D)分别为A、B、C、D各气体的分压,
气体的分压=气体总压×体积分数=气体总压×气体的物质的量分数。
(2)同一化学反应,化学反应方程式写法不同,其平衡常数表达式亦不同。例如:
N2O4(g) NO2(g) K′= =
因此书写平衡常数表达式时,要与化学反应方程式相对应。
(3)转化率计算公式
比较a、b处反应速率大小:va______vb(填“大于”“小于”或“等于”)。反应速率v=v正-v逆= ,k正、k逆分别为正、逆向反应速率
常数,x为物质的量分数,计算a处的 =_____(保留1位小数)。
题组一 有关化学反应速率的计算
1.[2018·全国卷Ⅲ,28(3)]对于反应2SiHCl3(g)=== SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl3的转化率随时间变化的结果如图所示。
对点集训
1
2
3
4
5
6
7
8
大于
1.3
1
2
3
4
5
6
7
8
解析 温度越高,反应速率越快,a点温度为343 K,b点温度为323 K,故反应速率:va>vb。反应速率v=v正-v逆=k正 -k逆 ,则有v正=
k正 ,v逆=k逆 ,343 K下反应达到平衡状态时v正=v逆,即k正 =k逆 ,此时SiHCl3的平衡转化率α=22%,
经计算可得SiHCl3、SiH2Cl2、SiCl4的物质的量分数分别为0.78、0.11、0.11,
a处SiHCl3的平衡转化率α=20%,此时SiHCl3、SiH2Cl2、SiCl4的物质的量分数分别为0.8、0.1、0.1,
1
2
3
4
5
6
7
8
则有 = = = ≈1.3。
2.CO与Ni发生羰化反应形成的络合物可作为催化烯烃反应的催化剂。Ni的羰化反应为Ni(s)+4CO(g) Ni(CO)4(g) ΔH<0,T0温度下,将足量的Ni粉和3.7 mol CO加入到刚性密闭容器中,10 min时反应达到平衡,测
得体系的压强为原来的 。则:
(1)0~10 min内平均反应速率v(Ni)=_____g·min-1。
1
2
3
4
5
6
7
8
5.31
1
2
3
4
5
6
7
8
解析 在恒容密闭容器中,气体的压强之比等于气体的物质的量之比,在反应开始时加入了3.7 mol CO,反应达到平衡时测得体系的压强为原来的 ,则气体的物质的量为n(气体)= ×3.7 mol=1 mol,假设平衡时反应产生Ni(CO)4(g)为x mol,则反应消耗CO物质的量为4x mol,平衡时CO物质的量为(3.7-4x) mol,则(3.7-4x) mol+x mol=1 mol,解得x=0.9,由方程式可知消耗的Ni与反应产生的Ni(CO)4(g)的物质的量相同,因此10 min内反应消耗Ni的物质的量为0.9 mol,其质量是m(Ni)=0.9 mol ×59 g·mol-1=53.1 g,所以0~10 min内平均反应速率v(Ni)=53.1 g÷10 min=5.31 g·min-1;
(2)研究表明,正反应速率v正=k正·x4(CO),逆反应速率v逆=k逆·x[Ni(CO)4]
(k正和k逆分别表示正反应和逆反应的速率常数,x为物质的量分数),计算
T0温度下的 =_______。
1
2
3
4
5
6
7
8
9×103
解析 当反应达到平衡时v正=v逆,由于正反应速率v正=k正·x4(CO),逆反应速率v逆=k逆·x[Ni(CO)4],
1
2
3
4
5
6
7
8
根据①可知平衡时n[Ni(CO)4]=0.9 mol,n(CO)=1.0 mol-0.9 mol=0.1 mol,
题组二 有关平衡常数及转化率的计算
3.(1)[2019·全国卷Ⅱ,27(2)]已知: (g)+I2(g)=== (g)+2HI(g) ΔH>0。
某温度,等物质的量的碘和环戊烯( )在刚性容器内发生反应,起始总压为105 Pa,平衡时总压增加了20%,环戊烯的转化率为______,该反应的平衡常数Kp=__________Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有_____(填标号)。
A.通入惰性气体 B.提高温度
C.增加环戊烯浓度 D.增加碘浓度
1
2
3
4
5
6
7
8
40%
3.56×104
BD
解析 设容器中起始加入I2(g)和环戊烯的物质的量均为a,平衡时转化的环戊烯的物质的量为x,列出三段式:
1
2
3
4
5
6
7
8
(g) + I2(g) === (g)+2HI(g)
起始: a a 0 0
转化: x x x 2x
平衡: a-x a-x x 2x
根据平衡时总压强增加了20%,且恒温恒容时,压强之比等于气体物质的量之比,
通入惰性气体,对反应的平衡无影响,A项不符合题意;
1
2
3
4
5
6
7
8
反应为吸热反应,提高温度,平衡正向移动,可提高环戊烯的平衡转化率,B项符合题意;
增加环戊烯浓度,能提高I2(g)的平衡转化率,但环戊烯的平衡转化率降低,C项不符合题意;
增加I2(g)的浓度,能提高环戊烯的平衡转化率,D项符合题意。
1
2
3
4
5
6
7
8
(2)(2020·福建适应性测试)将H2O与COS以体积比1∶2置于恒温恒容密闭容器中反应:H2O(g)+COS(g)===H2S(g)+CO2(g),若测得该反应平衡时 H2O与COS的体积比1∶6,则该温度下,脱除反应的平衡常数K=______
(保留两位小数)。
1
2
3
4
5
6
7
8
2.67
解析 根据题意列三段式:
H2O(g)+COS(g) H2S(g)+CO2(g)(单位:mol)
起始量:1 2 0 0
转化量:x x x x
平衡量:1-x 2-x x x
1
2
3
4
5
6
7
8
4.(2020·皖南八校第三次联考)(1)在某密闭容器中发生反应:2CO2(g) 2CO(g)+O2(g),0.995 mol CO2在不同温度下的平衡分解情况如图所示。
1
2
3
4
5
6
7
8
①图中a、b、c三点的平衡常数K(a)、K(b)、K(c)的大小关系为__________。
Ka=Kb
1.9×106
解析 设生成O2为x mol
1
2
3
4
5
6
7
8
2CO2(g) 2CO(g)+O2(g)
起:0.995 0 0
转:2x 2x x
平:0.995-2x 2x x
平衡时氧气的体积分数为0.5%
(2)573.2 K时,向一刚性密闭容器中充入5.00 MPa CH3OH使其分解,CH3OH(g) CO(g)+2H2(g),t h后达平衡时H2的物质的量分数为60%,
则t h内v(CH3OH)=_____MPa·h-1,其分压平衡常数Kp=_______(MPa)2。
1
2
3
4
5
6
7
8
168.75
1
2
3
4
5
6
7
8
解析 CH3OH(g) CO(g)+2H2(g)
始 5 MPa 0 0
转 a a 2a
平 5 MPa-a a 2a
得a=3.75 MPa,
5.亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO和Cl2反应得到,化学方程式为2NO(g)+Cl2(g) 2NOCl(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
①2NO2(g)+NaCl(s) NaNO3(s)+NOCl(g)
②4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)
③2NO(g)+Cl2(g) 2NOCl(g)
设反应①②③对应的平衡常数依次为K1、K2、K3,则K1、K2、K3之间的关系为__________。
1
2
3
4
5
6
7
8
解析 根据①×2-②=③,从而可推知平衡常数之间的关系。
(2)在1 L恒容密闭容器中充入2 mol NO(g)和1 mol Cl2(g),在不同温度下测得c(NOCl)与时间t的关系如图A所示:
1
2
3
4
5
6
7
8
①反应开始到10 min时NO的平均反应速率v(NO)=____ mol·L-1·min-1。
0.1
解析 10 min时,c(NOCl)=1 mol·L-1,则转化的NO的物质的量为1 mol,
则v(NO)= =0.1 mol·L-1·min-1。
②T2时该反应的平衡常数K为____。
1
2
3
4
5
6
7
8
2
③T2时Cl2的平衡转化率为______。
50%
(3)若按投料比[n(NO)∶n(Cl2)]=2∶1把NO和Cl2加入到一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强p(总压)的关系如图B所示:
1
2
3
4
5
6
7
8
①该反应的ΔH____(填“>”“<”或“=”)0。
<
解析 根据图像,升高温度,平衡时NO的转化率减小,说明平衡逆向移动,说明该反应正反应属于放热反应,ΔH<0。
②在p压强条件下,M点时容器内NO的体积分数为______。
1
2
3
4
5
6
7
8
40%
解析 根据图像,在p压强条件下,M点时容器内NO的转化率为50%,根据2NO(g)+Cl2(g) 2NOCl(g)可知,气体减小的体积为反应的NO的
体积的一半,因此NO的体积分数为 ×100%=40%。
③若反应一直保持在p压强条件下进行,则
M点的分压平衡常数Kp=____(用含p的表达式表示,用平衡分压代替平衡浓度计算,分压=总压×体积分数)。
1
2
3
4
5
6
7
8
解析 设NO的物质的量为2 mol,则Cl2的物质的量为1 mol。
2NO(g) + Cl2(g) 2NOCl(g)
起始/mol 2 1 0
反应/mol 1 0.5 1
平衡/mol 1 0.5 1
1
2
3
4
5
6
7
8
题组三 平衡常数与速率常数的关系
6.顺-1,2-二甲基环丙烷和反-1,2-二甲基环丙烷可发生如右转化:
1
2
3
4
5
6
7
8
该反应的速率方程可表示为v(正)=
k(正)c(顺)和v(逆)=k(逆)c(反),k(正)和k(逆)在一定温度时为常数,分别称作正、逆反应速率常数。回答下列问题:
(1)已知:t1温度下,k(正)=0.006 s-1,k(逆)=0.002 s-1,该温度下反应的平衡常数值K1=____;该反应的活化能Ea(正)小于Ea(逆),则ΔH______
(填“小于”“等于”或“大于”)0。
3
小于
1
2
3
4
5
6
7
8
解析 根据v(正)=k(正)c(顺),k(正)=0.006 s-1,则v(正)=0.006 c(顺),v(逆)=k(逆)c(反),k(逆)=0.002 s-1,则v(逆)=0.002c(反),化学平衡状态时正、逆反应速率相等,则0.006c(顺)=0.002c(反),该温度下反应的
平衡常数 ;该反应的活化能Ea(正)小于Ea(逆),说明
断键吸收的能量小于成键释放的能量,即该反应为放热反应,则ΔH小于0。
(2)t2温度下,图中能表示顺式异构体的质量分数随时间变化的曲线是_____(填曲线编号),平
衡常数值K2=_____;温度t1______(填“小于”
1
2
3
4
5
6
7
8
B
小于
“等于”或“大于”)t2,判断理由是_______________________________
_________________。
该反应是放热反应,升高温度平衡
向逆反应方向移动
1
2
3
4
5
6
7
8
解析 随着时间的推移,顺式异构体的质量分数不断减少,且减少速率随时间减小,则符合条件的曲线是B。设顺式异构体的起始浓度为x,可逆反应左右物质的化学计量数相等,均为1,则平衡时,顺式异构体为
0.3x,反式异构体为0.7x,所以平衡常数为 。因为K1>K2,
对于放热反应升高温度时平衡逆向移动,所以温度t2>t1。
1
2
3
4
5
6
7
8
7.纳米铁是重要的储氢材料,可用反应Fe(s)+5CO(g)
Fe(CO)5(g)制得。在1 L恒容密闭容器中加入足量铁粉和0.48 mol CO,在T1、T2不同温度下进行反应,测得c(CO)与温度、时间的关系如图所示。
(1)T1_____T2,ΔH_____0(填“>”或“<”)。
>
<
解析 温度越高反应速率越快,达到平衡所需要的时间越短,所以T1>T2,据图可知温度越高平衡时CO的浓度越大,说明温度升高平衡左移,所以该反应正反应为放热反应,ΔH<0;
(2)T2温度下,平衡时体系的压强为p,反应的标准
平衡常数Kθ=________(已知:标准平衡常数Kθ
=,其中pθ为标准压强(1×105Pa),
p[Fe(CO)5]、p(CO)为各组分的平衡分压)。
1
2
3
4
5
6
7
8
解析 反应初始投料为足量铁粉和0.48 mol CO,平衡时n(CO)=0.08 mol,则消耗的n(CO)=0.4 mol,根据方程式可知生成的n[Fe(CO)5]=0.08 mol,平衡时压强为p,压强比等于物质的量之比,
1
2
3
4
5
6
7
8
8.某化学小组查阅资料后得知:2NO(g)+O2(g) 2NO2(g) 的反应历程分两步:
①2NO(g)===N2O2(g) (快)
v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2)
②N2O2(g)+O2(g)===2NO2(g)(慢)
v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2)
请回答下列问题:
(1)已知决定2NO(g)+O2(g) 2NO2(g)反应速率的是反应②,则反应①的活化能E1与反应②的活化能E2的大小关系为E1____E2(填“>”“<”或“=”)。
1
2
3
4
5
6
7
8
<
1
2
3
4
5
6
7
8
解析 决定2NO(g)+O2(g) 2NO2(g)速率的是反应②,活化能越高,反应速率越慢,因此反应①的活化能E1与反应②的活化能E2的大小关系为E1
k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=________。
1
2
3
4
5
6
7
8
常考题空3 电解质溶液中有关平衡常数的计算
1.依据电离常数表达式计算(以弱酸HA为例)
2.溶度积(Ksp)的常见计算类型
(1)已知溶度积求溶液中的某种离子的浓度,如Ksp=a的饱和AgCl溶液中c(Ag+)= mol·L-1。
(2)已知溶度积、溶液中某离子的浓度,求溶液中的另一种离子的浓度,如某温度下AgCl的Ksp=a,在0.1 mol·L-1的NaCl溶液中加入过量的AgCl固体,达到平衡后c(Ag+)=10a mol·L-1。
题组一 有关电离常数的计算
1.(1)[2020·天津,16(5)节选]已知25 ℃碳酸电离常数为Ka1、Ka2,当溶液pH=12时, =1∶________∶__________。
1
2
3
4
5
6
对点集训
1024·Ka1·Ka2
1012·Ka1
当溶液pH=12时,c(H+)=10-12 mol·L-1,代入Ka1、Ka1·Ka2可得:c(H2CO3)∶ =1∶(1012·Ka1),c(H2CO3)∶ =1∶(1024·Ka1·Ka2),
1
2
3
4
5
6
综合可得:c(H2CO3)∶ ∶ =1∶(1012·Ka1)∶(1024·Ka1·Ka2)。
(2)[2020·全国卷Ⅱ,26(2)]次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各
成分的组成分数δ[δ(X)= ,
X为HClO或ClO-]与pH的关系如图所示。HClO的电离常数Ka值为______。
1
2
3
4
5
6
10-7.5
1
2
3
4
5
6
2.25 ℃时,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合所得溶液中 =c(Cl-),则溶液显_____(填“酸”“碱”或“中”)性;用含a
的代数式表示NH3·H2O的电离平衡常数Kb=________。
1
2
3
4
5
6
中
3.大气污染物SO2可用NaOH溶液吸收。已知pKa=-lgKa,25 ℃时,用0.1 mol·L-1 NaOH溶液滴定20 mL 0.1 mol·L-1 H2SO3溶液的滴定曲线如图。
1
2
3
4
5
6
(1)c点所得溶液中:c(Na+)____ (填“>”“<”或“=”)。
>
(2)依据图像计算H2SO3在25 ℃的pKa1=_____,pKa2=_____。
1
2
3
4
5
6
1.85
7.19
4.常温下,用0.100 0 mol·L-1的NaOH溶液滴定某浓度的二元弱酸(H2X)溶液,所得溶液中各种含X的微粒的物质的量分数(δ)与pH的变化曲线如图所示。
1
2
3
4
5
6
(1)计算H2X的一级电离常数Ka1=_______(幂指数的形式且可以是小数,下同)。
10-1.2
(2)X2-的一级水解常数Kh=_______。
1
2
3
4
5
6
10-9.8
题组二 有关Ksp的计算
5.(1)[2017·海南,14(3)]向含有BaSO4固体的溶液中滴加Na2CO3溶液,当
有BaCO3沉淀生成时溶液中 =______。[已知Ksp(BaCO3)=2.6×
10-9,Ksp(BaSO4)=1.1×10-10]。
1
2
3
4
5
6
23.6
解析 根据Ksp(AgCl)=c(Ag+)·c(Cl-)=2.0×10-10,可计算出当溶液中Cl-恰好完全沉淀(即浓度等于1.0×10-5 mol·L-1)时,溶液中c(Ag+)=2.0×10-5 mol·L-1,然后再根据Ksp(Ag2CrO4)=c2(Ag+)·c( )=2.0×
10-12,又可计算出此时溶液中c( )=5.0×10-3 mol·L-1。
(2)[2016·全国卷Ⅰ,27(3)]在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中的Cl-,利用Ag+与 生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好完全沉淀(浓度等于1.0×10-5 mol·L-1)时,溶液中c(Ag+)为_____________mol·L-1,此时溶液中c( )等于___________mol·L-1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)
1
2
3
4
5
6
2.0×10-5
5.0×10-3
(3)[2015·全国卷Ⅱ,26(4)]用废电池的锌皮制备ZnSO4·7H2O的过程中,需除去锌皮中的少量杂质铁,其方法是:加稀H2SO4和H2O2溶解,铁变为______,加碱调节至pH为_____时,铁刚好沉淀完全(离子浓度小于1×10-5 mol·L-1时,即可认为该离子沉淀完全);继续加碱至pH为_____时,锌开始沉淀(假定Zn2+浓度为0.1 mol·L-1)。若上述过程不加H2O2后果是____________________,原因是___________________________。
(已知Ksp[Zn(OH)2]=10-17,Ksp[Fe(OH)2]=10-17,Ksp[Fe(OH)3]=10-39)
1
2
3
4
5
6
Fe3+
2.7
6
Zn2+和Fe2+不能分离
Fe(OH)2和Zn(OH)2的Ksp相近
Zn(OH)2和Fe(OH)2的Ksp相近,若不加双氧水,沉淀Fe2+的同时Zn2+也会被沉淀,从而使Zn2+和Fe2+不能分离。
解析 铁溶于稀硫酸生成Fe2+,Fe2+被双氧水氧化为Fe3+。
Ksp[Fe(OH)3]=c(Fe3+)·c3(OH-)=10-39,
1
2
3
4
5
6
Ksp[Zn(OH)2]=c(Zn2+)·c2(OH-)=10-17,
6.常温下,在一定量的氯化铜溶液中逐滴加入氨水至过量,可观察到先产生蓝色沉淀,后蓝色沉淀溶解转化成蓝色溶液。[已知Ksp[Cu(OH)2]=2.2×10-20]
(1)当pH=8时,表明已完全沉淀,计算此时c(Cu2+)=_________ mol·L-1。
1
2
3
4
5
6
2.2×10-8
(2)常温下,Cu2+(aq)+4NH3(aq) [Cu(NH3)4]2+(aq) K1=2.0×1013,蓝色沉淀溶解过程中存在平衡:Cu(OH)2(s)+4NH3(aq) [Cu(NH3)4]2+(aq)+2OH-(aq),其平衡常数K2=_________。
1
2
3
4
5
6
4.4×10-7
一、图像题的审题要领
1.看题干,明方向:看清题目要求,在题干中圈出关键词,明确是速率问题还是平衡移动问题,分清楚是“恒温恒压”还是“恒温恒容”,或其他限制条件。
常考题空4 读懂图像——精准判断速率、平衡对实际生产的调控作用
2.识图表,“面、点、线”
识图是解题的基础,①面即坐标系,明晰横、纵坐标所表示的化学含义,这是理解题意和进行正确思维的前提。明晰坐标含义,也就是用变量的观点分析坐标,找出横、纵坐标的关系,再结合教材,联系相应的知识点。②找点:找出曲线中的特殊点(起点、顶点、拐点、终点、交叉点、平衡点等),分析这些点所表示的化学意义以及影响这些点的主要因素及限制因素等,大多考题就落在这些点的含义分析上,因为这些点往往隐含着某些限制条件或某些特殊的化学含义。③析线:正确分析曲线的走向、变化趋势(上升、下降、平缓、转折等),同时对走势有转折变化的曲线,要分区段进行分析,研究找出各段曲线的变化趋势及其含义。
二、应用举列
1.涉及温度、压强对平衡影响类简答题
答题要领:叙特点(反应特点或容器特点)→变条件→定方向→得结论(或结果)
例1 在密闭容器中充入一定量H2S,发生反应2H2S(g) 2H2(g)+S2(g) ΔH=+169.8 kJ·mol-1。如图为H2S气体的平衡转化率与温度、压强的关系。
(1)图中压强(p1、p2、p3)的大小顺序为________,理由是______________________________________。
(2)该反应平衡常数大小:K(T1)________(填“>”“<”或“=”)K(T2),理由是_________________________________________________________。
(3)如果要进一步提高H2S的平衡转化率,除改变温度、压强外,还可以采取的措施有___________________________________________________。
[解题思路]
例1 在密闭容器中充入一定量H2S,发生反应2H2S(g) 2H2(g)+S2(g) ΔH=+169.8 kJ·mol-1。如图为H2S气体的平衡转化率与温度、压强的关系。
(1)图中压强(p1、p2、p3)的大小顺序为________,
理由是_________________________________________________________
____________________________________________________________________________________________________________________________。
p1
(2)该反应平衡常数大小:K(T1)______(填“>” “<”或“=”)K(T2),理由是________________
___________________________________________。
(3)如果要进一步提高H2S的平衡转化率,除改变温度、压强外,还可以采取的措施有___________
_____。
<
该反应正向是吸热
反应,升高温度,平衡正向移动,平衡常数增大
及时分离出
产物
2.图像中转化率变化分析
答题要领:转化率问题首先看是否是平衡转化率,若为非平衡状态的转化率,则侧重分析温度、压强、浓度对反应快慢、催化剂对反应快慢及选择性(主副反应)的影响;若为平衡转化率,则侧重分析温度、压强、浓度对化学平衡的影响,有时也涉及温度对催化活性的影响。
例2 (2017·全国卷Ⅱ,27改编)丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。C4H10(g)===C4H8(g)+H2(g) ΔH=+123 kJ·mol-1
回答下列问题:
(1)图(a)是该反应平衡转化率与反应温度及压强的
关系图,x________0.1(填“大于”或“小于”);
欲使丁烯的平衡产率提高,应采取的措施是_____
(填标号)。
A.升高温度 B.降低温度
C.增大压强 D.降低压强
[审题要领] 抓关键词,“平衡产率”。
小于
AD
解析 由图(a)可以看出,温度相同时,由0.1 MPa变化到x MPa,丁烷的转化率增大,即平衡正向移动,所以x<0.1。由于反应为吸热反应,所以温度升高时,平衡正向移动,丁烯的平衡产率增大,因此A正确,B错误;
反应正向进行时体积增大,加压时平衡逆向移动,丁烯的平衡产率减小,因此C错误,D正确。
(2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。图(b)为丁烯产率与进料气中n(氢气)/n(丁烷)的关系。图中曲线呈现先升高后降低的变化趋势,
[审题要领] “产率”“氢气的作用”。
其降低的原因是_________________________________________________
_________________。
氢气是产物之一,随着n(氢气)/n(丁烷)的增大,该反应
向逆反应方向进行
解析 反应初期,H2可以活化催化剂,进料气中n(氢气)/n(丁烷)较小,丁烷浓度大,反应向正反应方向进行的程度大,丁烯产率升高;随着进料气中n(氢气)/n(丁烷)增大,原料中过量的H2会使反应平衡逆向移动,所以丁烯产率下降。
(3)图(c)为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。丁烯产率在590 ℃之前随温度升高而增大的原因可能是________________________________、____________________________;590 ℃之后,
[审题要领] “副产物”产生的原因。
升高温度有利于反应向吸热方向进行
升高温度时,反应速率加快
丁烯产率快速降低的主要原因可能是___________________________。
丁烯高温裂解生成短碳链烃类
解析 590 ℃之前,温度升高时反应速率加快,生成的丁烯会更多,同时由于反应是吸热反应,升高温度平衡正向移动,平衡体系中会含有更多的丁烯。而温度超过590 ℃时,丁烯高温会裂解生成短碳链烃类,使产率降低。
3.依据图像,优选生产条件
[解题模型] 要从以下几个层面依次分析其中的“物理量”:
例3 [2017·天津理综,10(2)]已知:生物脱H2S的原理:
H2S+Fe2(SO4)3===S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4 2Fe2(SO4)3+2H2O
由图1和图2判断使用硫杆菌的最佳条件为_______________。若反应温度过高,反应速率下降,其原因是_____________________________。
30 ℃、pH=2.0
蛋白质变性(或硫杆菌失去活性)
解析 由图1可知,温度在30 ℃左右时,Fe2+氧化速率最快;由图2可知,反应混合液的pH=2.0左右时,Fe2+氧化速率最快。由此可推断使用硫杆菌的最佳条件为温度为30 ℃、混合液的pH=2.0。硫杆菌属于蛋白质,若反应温度过高,受热变性失活,导致反应速率下降。
解析 据图可知,温度控制在 650 ℃ ,丙烯选择性高,且此时温度较高,反应速率快,而且该温度条件下平衡常数较大。
1.丙烷催化直接脱氢反应:C3H8(g) C3H6(g)+H2(g) ΔH1=+124.3 kJ·mol -1 (ⅰ) 副反应:C3H8 (g) C2H4 (g)+CH4(g) ΔH2(ⅱ)
对点集训
1
2
3
(1)反应ⅰ的平衡常数、产物丙烯选择性、
副产物乙烯选择性与温度关系如图所示,
分析工业生产中采用的温度为 650 ℃ 左右的原因是_______________________
_________________________________。
温度控制在 650 ℃,丙烯
选择性高,反应速率快,平衡常数大
(2)温度为 670 ℃ 时,若在1 L的容器中投入 8 mol C3H8,充分反应后,平衡混合气体中有 2 mol CH4和一定量C3H8、C3H6、H2、C2H4,计算该条件下C3H6 的选择性为____%。(C3H6的选择性=
×100%)
1
2
3
50
解析 平衡混合气体中有 2 mol CH4,则根据反应ⅱ可知平衡时该反应消耗的n1(C3H8)=2 mol;设平衡时C3H6的物质的量为x,根据反应ⅰ可知平衡时n(H2)=x mol,反应ⅰ消耗的n2(C3H8)=x,则平衡时容器n(C3H8)=(8-2-x)mol,
1
2
3
(3)欲使丙烯的产率提高,下列措施可行
的是____(填字母)。
a.恒压条件下向原料气中掺杂水蒸气
b.增大氢气与丙烷的投料比
c.选择对脱氢反应更好选择性的催化剂
d.增大压强
1
2
3
ac
氢气为产物,增大氢气的量会使平衡逆向移动,丙烯的产率降低,故b错误;
选择对脱氢反应更好选择性的催化剂,增大丙烯的选择性,提高产率,故c正确;
该反应正反应为压强增大的反应,增大压强会使平衡逆向移动,降低产率,故d错误。
解析 恒压条件下向原料气中掺杂水蒸气,则反应物和生成物的分压减小,该反应正反应为压强增大的反应,减小压强平衡正向移动,可以提高丙烯的产率,故a正确;
1
2
3
(4)科学家探索出利用无机膜催化丙烷脱氢制丙烯的新工艺,该工艺利用特定功能膜将生成的氢气从反应区一侧有选择性的及时移走,从平衡角度分析该工艺的优点_____________________________
1
2
3
_______________________________________________。
将氢气及时移走,化学平衡
解析 氢气是反应ⅰ的产物,将氢气及时移走,C3H8(g) C3H6(g)+H2(g) 的化学平衡正向移动,提高丙烯产率。
2.乙苯催化脱氢制苯乙烯反应:
1
2
3
+H2(g) ΔH=+124 kJ·mol-1
工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1∶9),控制反应温度600 ℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)变化如图:
(1)掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实:___________________
______________________________________________________。
1
2
3
正反应方向气体分
子数增加,压强不变,加入水蒸气稀释,相当于起减压的效果
(2)控制反应温度为600 ℃的理由是___________________________________
________________________________________________________________________________________________。
600 ℃,乙苯的转化率和苯乙烯的选择
性均较高。温度过低,反应速率慢,转化率低;温度过高,选择性下降,高温还可能使催化剂失活,且能耗大
3.已知CO2催化加氢合成乙醇的反应原理为:2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) ΔH<0。
1
2
3
(1)图1、图2分别是CO2的平衡转化率随压强及温度的变化关系,已知m为起始时的
投料比,即m= 。①图1中投料比相
同,温度从高到低的顺序为__________,判断依据是___________________________
_____________________________________。
T3>T2>T1
正反应放热,升高温度平衡逆
向移动,温度越高,CO2的平衡转化率越小
②图2中m1、m2、m3从大到小的顺序为__________,判断依据是_____________
__________________________________________________。
1
2
3
m1>m2>m3
保持n(CO2)不
变,增大n(H2),平衡正向移动,CO2的平衡转化率增大
(2)图3表示在总压为5 MPa的恒压条件下,且m=3时,平衡状态时各物质的物质的量分数与温度的关系。则曲线d代表的物质为________(填化学式),T4温度时,该反应的平衡常数Kp=_____(提示:用平衡分压代替平衡浓度来计算,某组分平衡分压=总压×该组分的物质的量分数,结果保留小数点后三位)。
1
2
3
C2H5OH
0.243
1
2
3
同课章节目录
