2020-2021学年九年级化学人教版(五四学制)全一册 第三单元 探寻生活中的酸--酸的化学性质 课件(共20张PPT)
文档属性
| 名称 | 2020-2021学年九年级化学人教版(五四学制)全一册 第三单元 探寻生活中的酸--酸的化学性质 课件(共20张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 12.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-03 00:00:00 | ||
图片预览






文档简介
探寻生活中的酸
—酸的化学性质
生活中“酸”的用途调查报告
活动一
蒸馒头
调味 碳酸饮料
除铁锈 除水垢
土壤 胃酸
酸性电池
酸
生活中“酸”的用途调查报告
活动一
小组展示,几种“酸的用途” 深度调查。
王文希组
路思齐组
贾兆鹏组
韩天远组
王博扬组
丁怡园组
胡芳蕊组
陈永辉组
李欣哲组
这些有关“酸”的用途,是由“酸” 的哪些性质决定的?
思考
结构
性质
用途
“酸”的作用原理实验验证
活动二
演示实验,观察记录现象,推理结论。
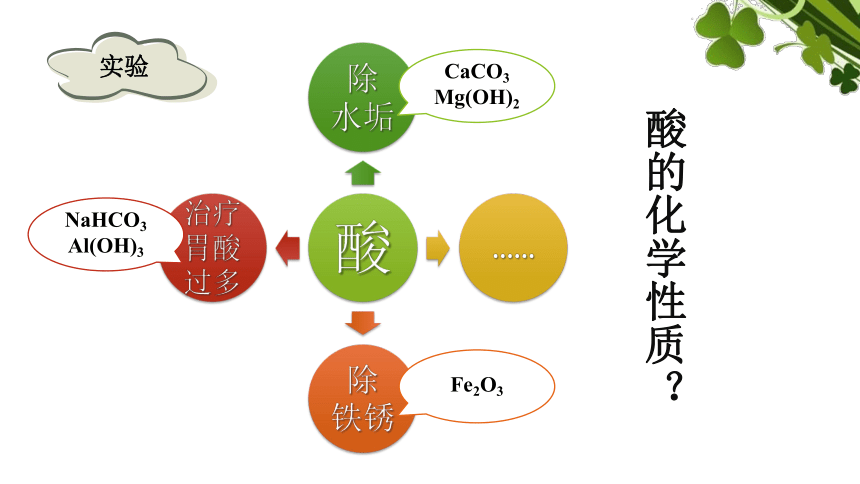
酸的化学性质?
实验
CaCO3
Mg(OH)2
Fe2O3
NaHCO3
Al(OH)3
用“酸”的化学性质解释现象
活动三
与碳酸盐反应 与碱反应
与H前金属反应 与金属氧化物反应
酸的
化学性质
生活现象解释
1、洁厕灵是广泛使用的清洁剂,其使用说明如右图。
洁厕灵为什么不能
用于清洁大理石和
金属?
HCl
生活现象解释
2、初一的科学实践课上,我们曾用生活中的原料自制碳酸饮料。主要原料:小苏打、柠檬、糖、水等。解释自制碳酸饮料过程中所蕴含的化学原理。
小苏打
柠檬汁
如何除水垢
一.方法:用稀盐酸或醋浸泡水垢
二.原理:
(1)水垢的主要成分:碳酸钙、氢氧化镁等。
(2)反应原理:
碳酸钙+盐酸→氯化钙+水+二氧化碳
氢氧化镁+盐酸→氯化镁+水
(3)盐酸与不溶的碳酸钙和氢氧化镁发生反应,生成可溶的氯化钙和氯化镁。
用食醋除铁锈
一、除铁锈的方法:
把金属浸在白醋里数小时,然后用把锈层擦掉。
二、除铁锈的原理:
铁锈的主要成分是 Fe2O3
食醋的主要成分是乙酸(醋酸)
乙酸与铁锈反应:
Fe2O3+6CH3COOH=2 (CH3COO)3Fe + 3H2O
胃酸
胃酸的主要成分:盐酸
胃酸的主要功能:活化胃蛋白酶元为胃蛋白酶及副胃蛋白酶,以消化分解蛋白质
胃酸过多的药物治疗:
碳酸氢钠:与胃酸反应的生成物中含有CO2气体,因此,有胃溃疡者慎用会导致胃溃疡的病情加重
氢氧化铝:难溶于水,且具有两性(弱酸性和弱碱性),既能中和过多的胃酸,又不刺激胃粘膜,生成氯化铝和水
氢氧化镁:与胃酸反应生成氯化镁和水
铝碳酸镁(达喜)
除水垢
就是将白醋或食醋(白醋效果要比食醋好)倒入水壶,用量是水壶刻度的10%,之后加入清水烧开,静置一个小时之后洗刷,就可以非常容易的清洗掉电水壶中的水垢了。一般多试几次,就可以完全清楚水壶上的水垢了。
开水中放入一勺小苏打,之后再多煮沸几分钟,水垢就可以去除啦。或者是倒入浓度1%的小苏打水500克,摇动轻耍电水壶,水垢也能立即出掉。
白醋的主要成份是醋酸(化学式CH3COOH)
水垢的主要成分是碳酸钙(化学式CaCO3)和氢氧化镁(化学式Mg(OH)2)
碳酸钙和氢氧化镁都是难溶于水的盐,醋酸可以和碳酸钙或氢氧化镁发生复分解反应,生成新的可溶于水的盐,即除去水垢。方程式如下:CH3COOH+CaCO3=(CH3COO)2Ca+CO2↑+H2O
CH3COOH+Mg(OH)2=(CH3COO)2Mg+2H2O
水垢的主要成分:CaCO? Mg(OH)2
清除方法:醋里面的醋酸会与水垢发生反应
利用稀盐酸清除
原理:CaCo3+2HCl=CaCl2+H2O+CO2↑
Mg(OH)2+2HCl=MgCl2+2H2O
除水垢
除水垢
水垢的主要成分是碳酸钙、氢氧化镁,它们可以和酸起化学变化.
①醋除水垢 如烧水壶有了水垢,可将几勺醋放入水中,烧一二个小时,水垢即除。如水垢中的主要成分是硫酸钙,则可将纯碱溶液倒在水壶里烧煮,可去垢。
②小苏打除水垢 用结了水垢的铝制水壶烧水时,放1小匙小苏打,烧沸几分钟,水垢即除。
③热胀冷缩除水垢 将空水壶放在炉上烧干水垢中的水分,烧至壶底有裂纹或烧至壶底有“嘭”响之时,将壶取下,迅速注入凉水,或用抹布包上提手和壶嘴,两手握住,将烧干的水壶迅速坐在冷水中(不要让水注入壶内)。重复2次至3次,壶底水垢会因热胀冷缩而脱落。
化学原理
*原理:盐酸与不溶的
CaCO3和Mg(OH)2
发生反应,生成可溶盐。
*水垢成因:
Ca(HCO3)2和
Mg(HCO3)2在沸水里
分解放出CO2,生成的。
2HCl+CaCO3=CaCl2+H2O+CO2↑
(与实验室制取CO2的化学方程式相同)
2HCl+Mg(OH)2=MgCl2+2H2O
胃酸的作用:
1.杀菌
2.促进胰液,胆汁分泌
3.促进铁和钙的吸收
胃酸的危害:
胃酸倒流
胃酸过多:会伤及胃、十二指肠黏膜,造成胃溃疡或十二指肠溃疡等疾病。
胃酸过少:细菌容易在胃内繁殖,可造成慢性胃炎。
胃液
主要成分:盐酸( HCl )
作用:杀死细菌、促进胰液、胆汁、肠液的分泌,还有助于小肠对铁和钙的吸收。
过多如何治:多吃碱性食物如苏打饼干,焦面包;严重的用“小苏打片”“胃舒平”等药物进行治疗。小苏打的成分是碳酸氢钠,胃舒平中则舍有氢氧化铝。它们都能跟胃液中的酸发生离子反应,从而中和过多的胃酸。
杀死进入胃的大部分细菌,有一段时期医界认为胃部不可能有细菌,直到幽门杆菌的发现。
提供一个酸性的pH环境使蛋白酶能将蛋白质分解为肽。
使蛋白质变性,即破坏其三级结构的构象,更好被分解。
作为胃蛋白酶、凝乳酶等酶的激活物。
将食物中的钙、铁转化为更易吸收的形式。
治疗胃酸过多,通常使用中和胃酸的药物
无机弱碱性物质,能中和过多的胃酸,降低胃蛋白酶分解胃壁蛋白的能力,减弱或解除胃酸对胃及十二指肠溃疡面的腐蚀和刺激作用,有利于溃疡面的愈合。抗酸治疗的目的在于使溃疡完全愈合,愈合的时间一般需要8周。
成分:由盐酸(HCl)(0.2%~0.5%的盐酸)和大量的氯化钾(KCl)、氯化钠(NaCl)所组成。
胃酸
谢谢!
—酸的化学性质
生活中“酸”的用途调查报告
活动一
蒸馒头
调味 碳酸饮料
除铁锈 除水垢
土壤 胃酸
酸性电池
酸
生活中“酸”的用途调查报告
活动一
小组展示,几种“酸的用途” 深度调查。
王文希组
路思齐组
贾兆鹏组
韩天远组
王博扬组
丁怡园组
胡芳蕊组
陈永辉组
李欣哲组
这些有关“酸”的用途,是由“酸” 的哪些性质决定的?
思考
结构
性质
用途
“酸”的作用原理实验验证
活动二
演示实验,观察记录现象,推理结论。
酸的化学性质?
实验
CaCO3
Mg(OH)2
Fe2O3
NaHCO3
Al(OH)3
用“酸”的化学性质解释现象
活动三
与碳酸盐反应 与碱反应
与H前金属反应 与金属氧化物反应
酸的
化学性质
生活现象解释
1、洁厕灵是广泛使用的清洁剂,其使用说明如右图。
洁厕灵为什么不能
用于清洁大理石和
金属?
HCl
生活现象解释
2、初一的科学实践课上,我们曾用生活中的原料自制碳酸饮料。主要原料:小苏打、柠檬、糖、水等。解释自制碳酸饮料过程中所蕴含的化学原理。
小苏打
柠檬汁
如何除水垢
一.方法:用稀盐酸或醋浸泡水垢
二.原理:
(1)水垢的主要成分:碳酸钙、氢氧化镁等。
(2)反应原理:
碳酸钙+盐酸→氯化钙+水+二氧化碳
氢氧化镁+盐酸→氯化镁+水
(3)盐酸与不溶的碳酸钙和氢氧化镁发生反应,生成可溶的氯化钙和氯化镁。
用食醋除铁锈
一、除铁锈的方法:
把金属浸在白醋里数小时,然后用把锈层擦掉。
二、除铁锈的原理:
铁锈的主要成分是 Fe2O3
食醋的主要成分是乙酸(醋酸)
乙酸与铁锈反应:
Fe2O3+6CH3COOH=2 (CH3COO)3Fe + 3H2O
胃酸
胃酸的主要成分:盐酸
胃酸的主要功能:活化胃蛋白酶元为胃蛋白酶及副胃蛋白酶,以消化分解蛋白质
胃酸过多的药物治疗:
碳酸氢钠:与胃酸反应的生成物中含有CO2气体,因此,有胃溃疡者慎用会导致胃溃疡的病情加重
氢氧化铝:难溶于水,且具有两性(弱酸性和弱碱性),既能中和过多的胃酸,又不刺激胃粘膜,生成氯化铝和水
氢氧化镁:与胃酸反应生成氯化镁和水
铝碳酸镁(达喜)
除水垢
就是将白醋或食醋(白醋效果要比食醋好)倒入水壶,用量是水壶刻度的10%,之后加入清水烧开,静置一个小时之后洗刷,就可以非常容易的清洗掉电水壶中的水垢了。一般多试几次,就可以完全清楚水壶上的水垢了。
开水中放入一勺小苏打,之后再多煮沸几分钟,水垢就可以去除啦。或者是倒入浓度1%的小苏打水500克,摇动轻耍电水壶,水垢也能立即出掉。
白醋的主要成份是醋酸(化学式CH3COOH)
水垢的主要成分是碳酸钙(化学式CaCO3)和氢氧化镁(化学式Mg(OH)2)
碳酸钙和氢氧化镁都是难溶于水的盐,醋酸可以和碳酸钙或氢氧化镁发生复分解反应,生成新的可溶于水的盐,即除去水垢。方程式如下:CH3COOH+CaCO3=(CH3COO)2Ca+CO2↑+H2O
CH3COOH+Mg(OH)2=(CH3COO)2Mg+2H2O
水垢的主要成分:CaCO? Mg(OH)2
清除方法:醋里面的醋酸会与水垢发生反应
利用稀盐酸清除
原理:CaCo3+2HCl=CaCl2+H2O+CO2↑
Mg(OH)2+2HCl=MgCl2+2H2O
除水垢
除水垢
水垢的主要成分是碳酸钙、氢氧化镁,它们可以和酸起化学变化.
①醋除水垢 如烧水壶有了水垢,可将几勺醋放入水中,烧一二个小时,水垢即除。如水垢中的主要成分是硫酸钙,则可将纯碱溶液倒在水壶里烧煮,可去垢。
②小苏打除水垢 用结了水垢的铝制水壶烧水时,放1小匙小苏打,烧沸几分钟,水垢即除。
③热胀冷缩除水垢 将空水壶放在炉上烧干水垢中的水分,烧至壶底有裂纹或烧至壶底有“嘭”响之时,将壶取下,迅速注入凉水,或用抹布包上提手和壶嘴,两手握住,将烧干的水壶迅速坐在冷水中(不要让水注入壶内)。重复2次至3次,壶底水垢会因热胀冷缩而脱落。
化学原理
*原理:盐酸与不溶的
CaCO3和Mg(OH)2
发生反应,生成可溶盐。
*水垢成因:
Ca(HCO3)2和
Mg(HCO3)2在沸水里
分解放出CO2,生成的。
2HCl+CaCO3=CaCl2+H2O+CO2↑
(与实验室制取CO2的化学方程式相同)
2HCl+Mg(OH)2=MgCl2+2H2O
胃酸的作用:
1.杀菌
2.促进胰液,胆汁分泌
3.促进铁和钙的吸收
胃酸的危害:
胃酸倒流
胃酸过多:会伤及胃、十二指肠黏膜,造成胃溃疡或十二指肠溃疡等疾病。
胃酸过少:细菌容易在胃内繁殖,可造成慢性胃炎。
胃液
主要成分:盐酸( HCl )
作用:杀死细菌、促进胰液、胆汁、肠液的分泌,还有助于小肠对铁和钙的吸收。
过多如何治:多吃碱性食物如苏打饼干,焦面包;严重的用“小苏打片”“胃舒平”等药物进行治疗。小苏打的成分是碳酸氢钠,胃舒平中则舍有氢氧化铝。它们都能跟胃液中的酸发生离子反应,从而中和过多的胃酸。
杀死进入胃的大部分细菌,有一段时期医界认为胃部不可能有细菌,直到幽门杆菌的发现。
提供一个酸性的pH环境使蛋白酶能将蛋白质分解为肽。
使蛋白质变性,即破坏其三级结构的构象,更好被分解。
作为胃蛋白酶、凝乳酶等酶的激活物。
将食物中的钙、铁转化为更易吸收的形式。
治疗胃酸过多,通常使用中和胃酸的药物
无机弱碱性物质,能中和过多的胃酸,降低胃蛋白酶分解胃壁蛋白的能力,减弱或解除胃酸对胃及十二指肠溃疡面的腐蚀和刺激作用,有利于溃疡面的愈合。抗酸治疗的目的在于使溃疡完全愈合,愈合的时间一般需要8周。
成分:由盐酸(HCl)(0.2%~0.5%的盐酸)和大量的氯化钾(KCl)、氯化钠(NaCl)所组成。
胃酸
谢谢!
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
