2021届高中化学考前三个月专项复习课件 命题区间一 角度三 物质的组成与分类、性质与变化
文档属性
| 名称 | 2021届高中化学考前三个月专项复习课件 命题区间一 角度三 物质的组成与分类、性质与变化 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-05 00:00:00 | ||
图片预览







文档简介
物质的组成与分类、性质与变化
角度三
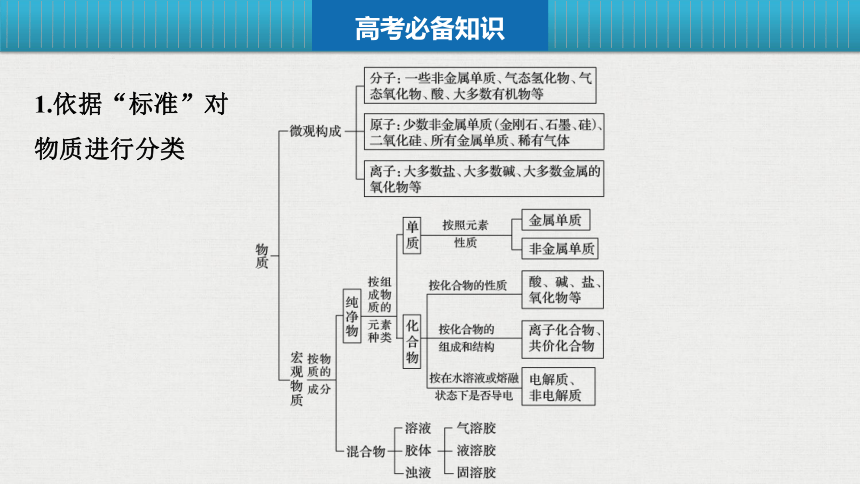
1.依据“标准”对
物质进行分类
高考必备知识
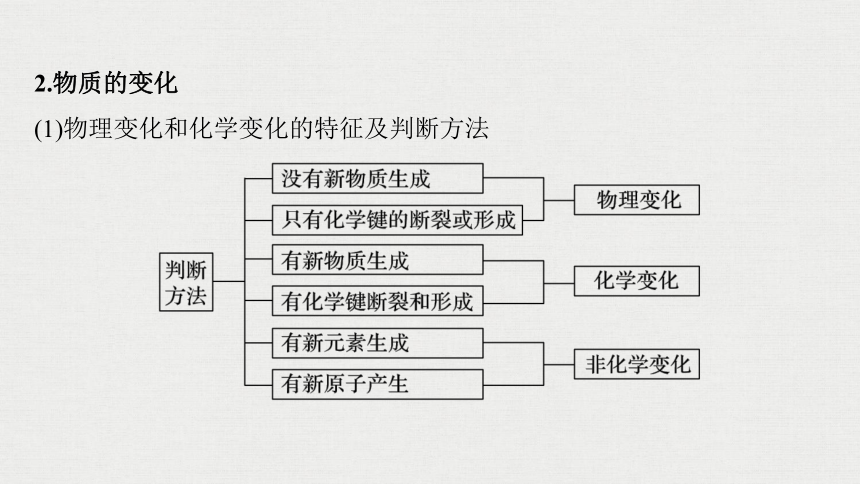
2.物质的变化
(1)物理变化和化学变化的特征及判断方法
(2)熟记物质变化过程中的“三馏”“四色”“五解”“十八化”。
?
物理变化
化学变化
三馏
分馏、蒸馏
干馏
四色
焰色反应
显色反应、颜色反应、指示剂变色反应
五解
潮解
分解、电解、水解、裂解
十八化
熔化、汽化、液化(煤的液化除外)、升华
氢化、氧化、水化、风化、碳化、钝化、煤的气化、煤的液化、皂化、歧化、卤化、硝化、酯化、裂化
1.(2020·浙江7月选考,3)下列物质在熔融状态下不导电的是
A.NaOH B.CaCl2
C.HCl D.K2SO4
1
2
3
4
5
√
重练高考真题
2.(2020·浙江7月选考,4)下列物质对应的组成不正确的是
A.干冰:CO2 B.熟石灰:CaSO4·2H2O
C.胆矾:CuSO4·5H2O D.小苏打:NaHCO3
1
2
3
4
5
√
3.(2019·浙江4月选考,2)下列属于强电解质的是
A.硫酸钡 B.食盐水
C.二氧化硅 D.醋酸
1
2
3
4
5
解析 强电解质包含强酸、强碱及大部分盐等。硫酸钡是强电解质,A项正确;
食盐水为混合物,不是强电解质,B项错误;
二氧化硅是非电解质,C项错误;
醋酸在水中不能完全电离,属于弱电解质,D项错误。
√
4.(2019·海南,10)下列说法正确的是
A.MgO和Al2O3都属于两性氧化物
B.悬浊液和乳浊液的分散质均为液态
C.Fe3O4和Pb3O4中的金属都呈现两种价态
D.葡萄糖溶液和淀粉溶液都具有丁达尔效应
√
1
2
3
4
5
解析 MgO不属于两性氧化物,A项错误;
悬浊液的分散质是固体小颗粒,B项错误;
Fe3O4可表示为FeO·Fe2O3,Fe元素化合价为+2、+3价,Pb3O4可表示为2PbO·PbO2,Pb元素化合价为+2、+4价,因此二者中的金属都呈现两种价态,C项正确;
葡萄糖分子是小分子,葡萄糖溶液中溶质粒子直径小于1 nm,所以葡萄糖溶液不能产生丁达尔效应,D项错误。
1
2
3
4
5
1
2
3
4
5
5.(2019·天津,1)化学在人类社会发展中发挥着重要作用,下列事实不涉及化学反应的是
A.利用废弃的秸秆生产生物质燃料乙醇
B.利用石油生产塑料、化纤等高分子材料
C.利用基本的化学原料生产化学合成药物
D.利用反渗透膜从海水中分离出淡水
√
1
2
3
4
5
解析 利用废弃的秸秆生产乙醇的过程中,秸秆中的纤维素水解生成葡萄糖,葡萄糖再转化成乙醇,A项不符合题意;
利用石油生产塑料、化纤等高分子材料的过程中,发生加聚反应或缩聚反应,B项不符合题意;
利用基本的化学原料生产化学合成药物的过程中,发生了化学反应,C项不符合题意;
利用反渗透膜从海水中分离出淡水,属于物理变化,D项符合题意。
题组一 物质的组成与分类
1.(2019·泰安模拟)分类方法在化学学科的发展中起到重要的作用。下列分类标准合理的是
A.根据溶液导电能力强弱,将电解质分为强电解质和弱电解质
B.根据分散系是否具有丁达尔效应,将分散系分为溶液、胶体和浊液
C.根据纯净物中的元素组成,将纯净物分为单质和化合物
D.根据反应中的能量变化,将化学反应分为氧化还原反应和非氧化还原
反应
1
2
3
4
5
6
√
精练预测押题
1
2
3
4
5
6
解析 弱电解质是在水溶液里部分电离的电解质,强电解质是在水溶液中能完全电离的电解质,强电解质和弱电解质的分类标准并不是电解质在水溶液中导电性的强弱,而是在水溶液中能否完全电离,A项不合理;
根据分散质粒子直径的大小,可将分散系分为溶液、胶体和浊液,不是根据是否具有丁达尔效应,B项不合理;
根据纯净物中的元素组成,将纯净物分成单质和化合物,只由一种元素组成的纯净物称为单质,含有两种或两种以上元素组成的纯净物称为化合物,C项合理;
1
2
3
4
5
6
根据反应中的能量变化,可将化学反应分为放热反应和吸热反应;氧化还原反应和非氧化还原反应的分类标准为反应中是否有电子的转移,D项不合理。
选项
X
Y
Z
A
二氧化氮
酸性氧化物
氧化物
B
硫酸
化合物
电解质
C
胶体
分散系
混合物
D
置换反应
氧化还原反应
离子反应
2.(2019·太原模拟)如图表示的一些物质或概念间的从属关系中正确的是
1
2
3
4
5
6
√
解析 酸性氧化物是与水反应生成相应的酸,或与碱反应生成相应的盐和水,NO2与水反应:3NO2+H2O===2HNO3+NO,
但二氧化氮并不属于酸性氧化物,A项错误;
硫酸属于化合物,但化合物不一定属于电解质,如CO2、NO等,它们属于化合物,但不属于电解质,B项错误;
分散系包括胶体、溶液、浊液等,分散系都属于混合物,C项正确;
置换反应属于氧化还原反应,氧化还原反应不一定是离子反应,如H2+Cl2 2HCl,D项错误。
1
2
3
4
5
6
题组二 胶体的性质和应用
3.(2019·衡阳联考)下列有关Fe(OH)3胶体的制备、提纯和性质的实验图示中,正确的是
1
2
3
4
5
6
√
1
2
3
4
5
6
解析 制备氢氧化铁胶体,是将几滴饱和FeCl3溶液滴加到沸水中,加热至出现红褐色液体,即为氢氧化铁胶体,FeCl3滴入氢氧化钠溶液中出现红褐色沉淀,不是胶体,A项错误;
胶体粒子不能透过半透膜,溶液中溶质分子或离子可以透过半透膜,能做到胶体的分离提纯,B项正确;
空气中不会形成光亮的通路,C项错误;
氢氧化铁胶粒带正电荷,应是阴极颜色加深,D项错误。
4.(2019·海淀期中)食盐在不同分散剂中形成不同分散系。
分散系1:食盐分散在水中形成无色透明溶液
分散系2:食盐分散在乙醇中形成无色透明胶体
下列说法正确的是
A.分散系1中只有两种离子
B.分散系2为电解质
C.可用丁达尔效应区分两个分散系
D.两个分散系中分散质粒子直径相同
1
2
3
4
5
6
√
解析 分散系1为食盐水,其中除了Na+、Cl-这两种离子外,还存在微量的H+和OH-,A项错误;
分散系2为混合物,既不是电解质,也不是非电解质,B项错误;
由于分散系2为胶体,会产生丁达尔效应;分散系1为溶液,没有丁达尔效应,可用丁达尔效应来区分两个分散系,C项正确;
分散系2中胶粒的直径介于1~100 nm之间,而分散系1中分散质微粒直径小于1 nm,两者的微粒直径大小不同,D项错误。
1
2
3
4
5
6
题组三 物质的性质与变化
5.(2020·北京模拟)下列物质制造或使用过程中没有发生化学变化的是
A
B
C
D
?
?
?
?
明矾做净水剂
丙烯制造聚丙烯熔喷布
氨气制造液氨冷却剂
含碳酸氢钠的抗酸药治疗胃酸过多
1
2
3
4
5
6
√
解析 明矾溶于水,铝离子水解为氢氧化铝胶体,发生化学变化,故不选A;
丙烯发生加聚反应生成聚丙烯,有新物质生成,属于化学反应,故不选B;
氨气制造液氨冷却剂,氨气的状态发生改变,没有生成新物质,不属于化学变化,故选C;
碳酸氢钠治疗胃酸过多,碳酸氢钠和盐酸反应生成氯化钠、二氧化碳、水,有新物质生成,属于化学反应,故不选D。
1
2
3
4
5
6
6.(2020·淮北一模)许多无机颜料在缤纷的世界扮演了重要角色。如历史悠久的铅白[2PbCO3·Pb(OH)2],安全环保的钛白(TiO2),鲜艳的朱砂(HgS),稳定的铁红(Fe2O3)等。下列解释错误的是
A.《周易参同契》中提到“胡粉(含铅白)投火中,色坏还原为铅”,其
中含铅元素的物质转化为2PbCO3·Pb(OH)2→PbO2→Pb
B.纳米级的钛白可由TiCl4水解制得:TiCl4+2H2O TiO2+4HCl
C.《本草经疏》中记载朱砂“若经伏火及一切烹、炼,则毒等砒、硇服
之必毙”,体现了HgS受热易分解的性质
D.铁红可由无水FeSO4高温煅烧制得:2FeSO4 Fe2O3+SO2↑+SO3↑
√
1
2
3
4
5
6
解析 铅元素的物质转化为2PbCO3·Pb(OH)2→PbO→Pb,故A错误;
纳米级的钛白可由TiCl4水解生成氧化钛和盐酸,化学方程式:TiCl4+2H2O TiO2+4HCl,故B正确;
硫化汞受热分解生成汞单质和硫,体现了HgS受热易分解的性质,故C正确;
铁红可由无水FeSO4高温煅烧制得,其化学方程式为:2FeSO4 Fe2O3+SO2↑+SO3↑,故D正确。
1
2
3
4
5
6
角度三
1.依据“标准”对
物质进行分类
高考必备知识
2.物质的变化
(1)物理变化和化学变化的特征及判断方法
(2)熟记物质变化过程中的“三馏”“四色”“五解”“十八化”。
?
物理变化
化学变化
三馏
分馏、蒸馏
干馏
四色
焰色反应
显色反应、颜色反应、指示剂变色反应
五解
潮解
分解、电解、水解、裂解
十八化
熔化、汽化、液化(煤的液化除外)、升华
氢化、氧化、水化、风化、碳化、钝化、煤的气化、煤的液化、皂化、歧化、卤化、硝化、酯化、裂化
1.(2020·浙江7月选考,3)下列物质在熔融状态下不导电的是
A.NaOH B.CaCl2
C.HCl D.K2SO4
1
2
3
4
5
√
重练高考真题
2.(2020·浙江7月选考,4)下列物质对应的组成不正确的是
A.干冰:CO2 B.熟石灰:CaSO4·2H2O
C.胆矾:CuSO4·5H2O D.小苏打:NaHCO3
1
2
3
4
5
√
3.(2019·浙江4月选考,2)下列属于强电解质的是
A.硫酸钡 B.食盐水
C.二氧化硅 D.醋酸
1
2
3
4
5
解析 强电解质包含强酸、强碱及大部分盐等。硫酸钡是强电解质,A项正确;
食盐水为混合物,不是强电解质,B项错误;
二氧化硅是非电解质,C项错误;
醋酸在水中不能完全电离,属于弱电解质,D项错误。
√
4.(2019·海南,10)下列说法正确的是
A.MgO和Al2O3都属于两性氧化物
B.悬浊液和乳浊液的分散质均为液态
C.Fe3O4和Pb3O4中的金属都呈现两种价态
D.葡萄糖溶液和淀粉溶液都具有丁达尔效应
√
1
2
3
4
5
解析 MgO不属于两性氧化物,A项错误;
悬浊液的分散质是固体小颗粒,B项错误;
Fe3O4可表示为FeO·Fe2O3,Fe元素化合价为+2、+3价,Pb3O4可表示为2PbO·PbO2,Pb元素化合价为+2、+4价,因此二者中的金属都呈现两种价态,C项正确;
葡萄糖分子是小分子,葡萄糖溶液中溶质粒子直径小于1 nm,所以葡萄糖溶液不能产生丁达尔效应,D项错误。
1
2
3
4
5
1
2
3
4
5
5.(2019·天津,1)化学在人类社会发展中发挥着重要作用,下列事实不涉及化学反应的是
A.利用废弃的秸秆生产生物质燃料乙醇
B.利用石油生产塑料、化纤等高分子材料
C.利用基本的化学原料生产化学合成药物
D.利用反渗透膜从海水中分离出淡水
√
1
2
3
4
5
解析 利用废弃的秸秆生产乙醇的过程中,秸秆中的纤维素水解生成葡萄糖,葡萄糖再转化成乙醇,A项不符合题意;
利用石油生产塑料、化纤等高分子材料的过程中,发生加聚反应或缩聚反应,B项不符合题意;
利用基本的化学原料生产化学合成药物的过程中,发生了化学反应,C项不符合题意;
利用反渗透膜从海水中分离出淡水,属于物理变化,D项符合题意。
题组一 物质的组成与分类
1.(2019·泰安模拟)分类方法在化学学科的发展中起到重要的作用。下列分类标准合理的是
A.根据溶液导电能力强弱,将电解质分为强电解质和弱电解质
B.根据分散系是否具有丁达尔效应,将分散系分为溶液、胶体和浊液
C.根据纯净物中的元素组成,将纯净物分为单质和化合物
D.根据反应中的能量变化,将化学反应分为氧化还原反应和非氧化还原
反应
1
2
3
4
5
6
√
精练预测押题
1
2
3
4
5
6
解析 弱电解质是在水溶液里部分电离的电解质,强电解质是在水溶液中能完全电离的电解质,强电解质和弱电解质的分类标准并不是电解质在水溶液中导电性的强弱,而是在水溶液中能否完全电离,A项不合理;
根据分散质粒子直径的大小,可将分散系分为溶液、胶体和浊液,不是根据是否具有丁达尔效应,B项不合理;
根据纯净物中的元素组成,将纯净物分成单质和化合物,只由一种元素组成的纯净物称为单质,含有两种或两种以上元素组成的纯净物称为化合物,C项合理;
1
2
3
4
5
6
根据反应中的能量变化,可将化学反应分为放热反应和吸热反应;氧化还原反应和非氧化还原反应的分类标准为反应中是否有电子的转移,D项不合理。
选项
X
Y
Z
A
二氧化氮
酸性氧化物
氧化物
B
硫酸
化合物
电解质
C
胶体
分散系
混合物
D
置换反应
氧化还原反应
离子反应
2.(2019·太原模拟)如图表示的一些物质或概念间的从属关系中正确的是
1
2
3
4
5
6
√
解析 酸性氧化物是与水反应生成相应的酸,或与碱反应生成相应的盐和水,NO2与水反应:3NO2+H2O===2HNO3+NO,
但二氧化氮并不属于酸性氧化物,A项错误;
硫酸属于化合物,但化合物不一定属于电解质,如CO2、NO等,它们属于化合物,但不属于电解质,B项错误;
分散系包括胶体、溶液、浊液等,分散系都属于混合物,C项正确;
置换反应属于氧化还原反应,氧化还原反应不一定是离子反应,如H2+Cl2 2HCl,D项错误。
1
2
3
4
5
6
题组二 胶体的性质和应用
3.(2019·衡阳联考)下列有关Fe(OH)3胶体的制备、提纯和性质的实验图示中,正确的是
1
2
3
4
5
6
√
1
2
3
4
5
6
解析 制备氢氧化铁胶体,是将几滴饱和FeCl3溶液滴加到沸水中,加热至出现红褐色液体,即为氢氧化铁胶体,FeCl3滴入氢氧化钠溶液中出现红褐色沉淀,不是胶体,A项错误;
胶体粒子不能透过半透膜,溶液中溶质分子或离子可以透过半透膜,能做到胶体的分离提纯,B项正确;
空气中不会形成光亮的通路,C项错误;
氢氧化铁胶粒带正电荷,应是阴极颜色加深,D项错误。
4.(2019·海淀期中)食盐在不同分散剂中形成不同分散系。
分散系1:食盐分散在水中形成无色透明溶液
分散系2:食盐分散在乙醇中形成无色透明胶体
下列说法正确的是
A.分散系1中只有两种离子
B.分散系2为电解质
C.可用丁达尔效应区分两个分散系
D.两个分散系中分散质粒子直径相同
1
2
3
4
5
6
√
解析 分散系1为食盐水,其中除了Na+、Cl-这两种离子外,还存在微量的H+和OH-,A项错误;
分散系2为混合物,既不是电解质,也不是非电解质,B项错误;
由于分散系2为胶体,会产生丁达尔效应;分散系1为溶液,没有丁达尔效应,可用丁达尔效应来区分两个分散系,C项正确;
分散系2中胶粒的直径介于1~100 nm之间,而分散系1中分散质微粒直径小于1 nm,两者的微粒直径大小不同,D项错误。
1
2
3
4
5
6
题组三 物质的性质与变化
5.(2020·北京模拟)下列物质制造或使用过程中没有发生化学变化的是
A
B
C
D
?
?
?
?
明矾做净水剂
丙烯制造聚丙烯熔喷布
氨气制造液氨冷却剂
含碳酸氢钠的抗酸药治疗胃酸过多
1
2
3
4
5
6
√
解析 明矾溶于水,铝离子水解为氢氧化铝胶体,发生化学变化,故不选A;
丙烯发生加聚反应生成聚丙烯,有新物质生成,属于化学反应,故不选B;
氨气制造液氨冷却剂,氨气的状态发生改变,没有生成新物质,不属于化学变化,故选C;
碳酸氢钠治疗胃酸过多,碳酸氢钠和盐酸反应生成氯化钠、二氧化碳、水,有新物质生成,属于化学反应,故不选D。
1
2
3
4
5
6
6.(2020·淮北一模)许多无机颜料在缤纷的世界扮演了重要角色。如历史悠久的铅白[2PbCO3·Pb(OH)2],安全环保的钛白(TiO2),鲜艳的朱砂(HgS),稳定的铁红(Fe2O3)等。下列解释错误的是
A.《周易参同契》中提到“胡粉(含铅白)投火中,色坏还原为铅”,其
中含铅元素的物质转化为2PbCO3·Pb(OH)2→PbO2→Pb
B.纳米级的钛白可由TiCl4水解制得:TiCl4+2H2O TiO2+4HCl
C.《本草经疏》中记载朱砂“若经伏火及一切烹、炼,则毒等砒、硇服
之必毙”,体现了HgS受热易分解的性质
D.铁红可由无水FeSO4高温煅烧制得:2FeSO4 Fe2O3+SO2↑+SO3↑
√
1
2
3
4
5
6
解析 铅元素的物质转化为2PbCO3·Pb(OH)2→PbO→Pb,故A错误;
纳米级的钛白可由TiCl4水解生成氧化钛和盐酸,化学方程式:TiCl4+2H2O TiO2+4HCl,故B正确;
硫化汞受热分解生成汞单质和硫,体现了HgS受热易分解的性质,故C正确;
铁红可由无水FeSO4高温煅烧制得,其化学方程式为:2FeSO4 Fe2O3+SO2↑+SO3↑,故D正确。
1
2
3
4
5
6
同课章节目录
