2021届高中化学考前三个月专项复习课件命题区间八 角度一 常见有机物的结构、性质和用途判断
文档属性
| 名称 | 2021届高中化学考前三个月专项复习课件命题区间八 角度一 常见有机物的结构、性质和用途判断 |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-05 00:00:00 | ||
图片预览








文档简介
常见有机物的结构、性质和用途判断
角度一
1.常见有机物的重要物理性质
(1)常温常压下,分子中碳原子个数不多于4的烃是气体,烃的密度都比水小。
(2)烃、烃的卤代物、酯类物质均不溶于水,低级醇、酸能溶于水。
(3)随着分子中碳原子数目的增多,各类有机物的同系物熔、沸点逐渐升高。同分异构体的支链越多,熔、沸点越低。
高考必备知识
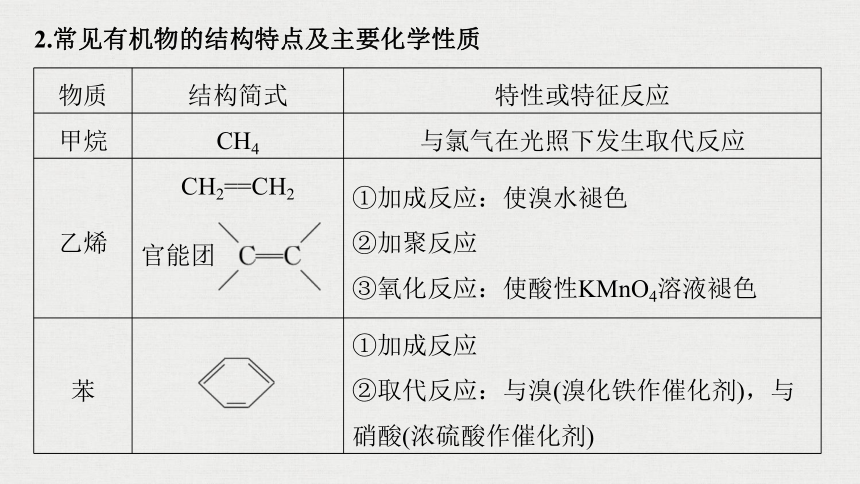
物质
结构简式
特性或特征反应
甲烷
CH4
与氯气在光照下发生取代反应
乙烯
CH2==CH2
官能团
①加成反应:使溴水褪色
②加聚反应
③氧化反应:使酸性KMnO4溶液褪色
苯
?
①加成反应
②取代反应:与溴(溴化铁作催化剂),与硝酸(浓硫酸作催化剂)
2.常见有机物的结构特点及主要化学性质
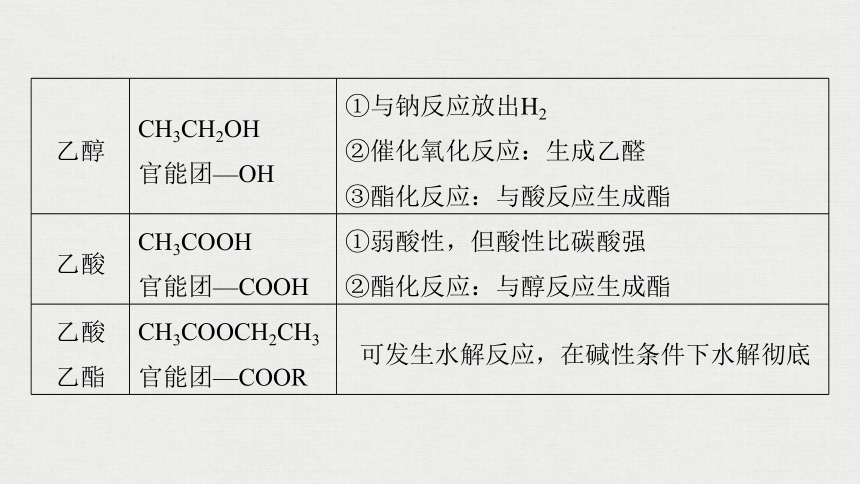
乙醇
CH3CH2OH
官能团—OH
①与钠反应放出H2
②催化氧化反应:生成乙醛
③酯化反应:与酸反应生成酯
乙酸
CH3COOH
官能团—COOH
①弱酸性,但酸性比碳酸强
②酯化反应:与醇反应生成酯
乙酸
乙酯
CH3COOCH2CH3
官能团—COOR
可发生水解反应,在碱性条件下水解彻底
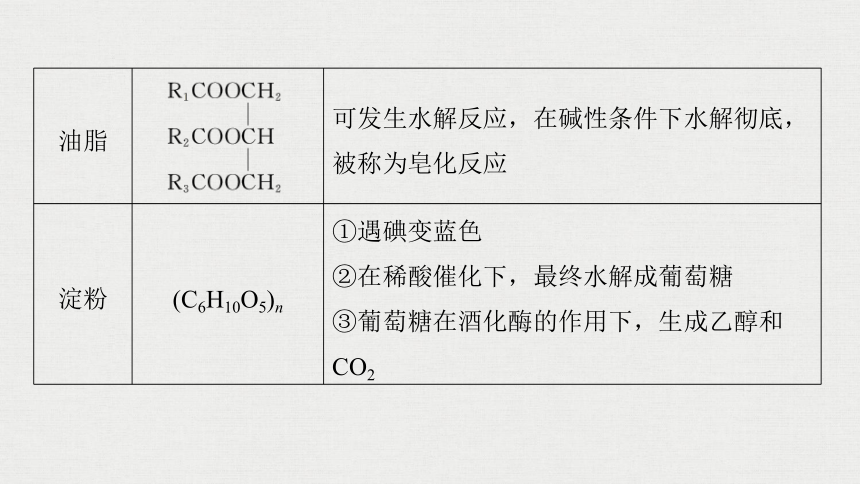
油脂
?
可发生水解反应,在碱性条件下水解彻底,被称为皂化反应
淀粉
(C6H10O5)n
①遇碘变蓝色
②在稀酸催化下,最终水解成葡萄糖
③葡萄糖在酒化酶的作用下,生成乙醇和CO2
蛋白质
含有肽键
①水解反应生成氨基酸
②两性
③变性
④盐析
⑤颜色反应
⑥灼烧产生特殊气味
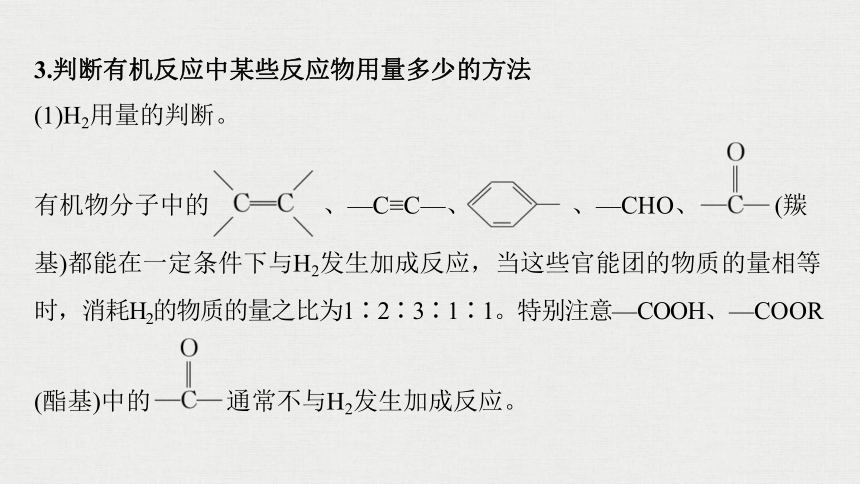
3.判断有机反应中某些反应物用量多少的方法
(1)H2用量的判断。
有机物分子中的 、—C≡C—、 、—CHO、 (羰
基)都能在一定条件下与H2发生加成反应,当这些官能团的物质的量相等
时,消耗H2的物质的量之比为1∶2∶3∶1∶1。特别注意—COOH、—COOR
(酯基)中的 通常不与H2发生加成反应。
(2)能与NaOH反应的有机物及其用量比例(设有机物分子官能团个数为1):①卤代烃:1∶1,②苯环上连接的卤原子:1∶2;③酚羟基:1∶1;④羧
基:1∶1,⑤普通酯:1∶1;⑥酚酯:1∶2。
(3)Br2用量的判断。
烷烃(光照下1 mol Br2可取代1 mol氢原子)、苯(FeBr3催化下1 mol Br2可取代1 mol氢原子)、酚类(1 mol Br2可取代与—OH所连碳原子处于邻、对位
碳原子上的1 mol H原子)、 (1 mol双键可与1 mol Br2发生加成反
应)、—C≡C—(1 mol三键可与2 mol Br2发生加成反应)。
4.有机物与日常生活
(1)医用酒精中乙醇的体积分数为75%,使蛋白质变性,用于消毒。
(2)福尔马林是35%~40%的甲醛水溶液,使蛋白质变性,良好的杀菌剂,常作为浸制标本的溶液(不可用于食品保鲜)。
(3)蛋白质受热变性,加热能杀死流感病毒。
(4)蚕丝灼烧有烧焦羽毛的气味,灼烧法可以区别蚕丝和人造纤维。
(5)聚乙烯性质稳定,无毒,可作食品包装袋。
(6)聚氯乙烯有毒,不能用作食品包装袋。
(7)食用油反复加热会产生稠环芳香烃等有害物质,不能反复加热。
(8)聚四氟乙烯具有抗酸、抗碱、抗各种有机溶剂的特点,用于厨具表面涂层。
(9)甘油具有吸水性,作护肤保湿剂。
(10)淀粉遇碘显蓝色,鉴别淀粉与其他物质(如蛋白质、木纤维等)。
(11)食醋与碳酸钙反应生成可溶于水的醋酸钙,可除水垢(主要成分为碳酸钙)。
(12)阿司匹林水解生成水杨酸,显酸性,服用阿司匹林出现水杨酸反应时,用NaHCO3溶液解毒。
(13)加工后具有吸水性的植物纤维,可用作食品干燥剂。
(14)谷氨酸钠具有鲜味,可作味精。
(15)油脂在碱性条件下水解为高级脂肪酸盐和甘油,制肥皂。
1.(2020·浙江7月选考,14)下列说法不正确的是
A.相同条件下等质量的甲烷、汽油、氢气完全燃烧,放出的热量依次增加
B.油脂在碱性条件下水解生成的高级脂肪酸盐是肥皂的主要成分
C.根据纤维在火焰上燃烧产生的气味,可以鉴别蚕丝与棉花
D.淀粉、纤维素、蛋白质都属于高分子化合物
1
2
3
4
5
6
√
重练高考真题
解析 相同条件下等质量的甲烷、汽油、氢气完全燃烧放出的热量由小到大依次是汽油、甲烷、氢气,A错误。
2.(2020·天津,3)下列说法错误的是
A.淀粉和纤维素均可水解产生葡萄糖
B.油脂的水解反应可用于生产甘油
C.氨基酸是组成蛋白质的基本结构单元
D.淀粉、纤维素和油脂均是天然高分子
1
2
3
4
5
6
√
解析 油脂是指高级脂肪酸甘油酯,不属于高分子化合物。高分子化合物是指相对分子质量很大(104~106,甚至更大)的化合物。
3.(2017·全国卷Ⅰ,7)下列生活用品中主要由合成纤维制造的是
A.尼龙绳 B.宣纸 C.羊绒衫 D.棉衬衣
1
2
3
4
5
6
解析 A项,尼龙的主要成分是聚酰胺纤维(锦纶),属于合成纤维,正确;
B项,宣纸的主要成分是纤维素,错误;
C项,羊绒衫的主要成分是蛋白质,错误;
棉衬衣的主要成分是纤维素,错误。
√
4.(2018·全国卷Ⅲ,9)苯乙烯是重要的化工原料。下列有关苯乙烯的说法错误的是
A.与液溴混合后加入铁粉可发生取代反应
B.能使酸性高锰酸钾溶液褪色
C.与氯化氢反应可以生成氯代苯乙烯
D.在催化剂存在下可以制得聚苯乙烯
√
1
2
3
4
5
6
1
2
3
4
5
6
解析 与氯化氢的反应是发生在碳碳双键上的加成反应,产物是氯代苯乙烷,C项错误;
“铁粉”“液溴”是苯乙烯( )在苯环上发生溴代反应的条件,A项正确;
含有碳碳双键,能使酸性高锰酸钾溶液褪色,B项正确;
含有碳碳双键,能发生加聚反应生成聚苯乙烯,D项正确。
选项
实验
结论
A
将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明
生成的1,2-二溴乙烷无色、可溶于四氯化碳
B
乙醇和水都可与金属钠反应产生可燃性气体
乙醇分子中的氢与水分子中的氢具有相同的活性
C
用乙酸浸泡水壶中的水垢,可将其清除
乙酸的酸性小于碳酸的酸性
D
甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红
生成的氯甲烷具有酸性
1
2
3
4
5
6
5.(2017·全国卷Ⅱ,10)下列由实验得出的结论正确的是
√
1
2
3
4
5
6
解析 B项,钠与水反应比钠与乙醇反应剧烈,说明水中的氢比乙醇中的氢活泼,错误;
C项,根据强酸制弱酸,可知乙酸酸性大于碳酸,错误;
D项,甲烷与氯气在光照下发生取代反应生成了HCl,HCl气体能使湿润的石蕊试纸变红,错误。
6.(2019·浙江4月选考,16)下列表述正确的是
A.苯和氯气生成C6H6Cl6的反应是取代反应
B.乙烯与溴水发生加成反应的产物是CH2CH2Br2
C.等物质的量的甲烷与氯气反应的产物是CH3Cl
D.硫酸作催化剂,CH3CO18OCH2CH3水解所得乙醇分子中有18O
1
2
3
4
5
6
√
解析 苯和氯气生成C6H6Cl6的反应是加成反应,A错误;
乙烯与溴水发生加成反应的产物应为CH2BrCH2Br,B错误;
甲烷与氯气反应生成的是CH3Cl、CH2Cl2、CHCl3、CCl4、HCl的混合物,C错误;
CH3CO18OCH2CH3水解生成CH3COOH和CH3CH218OH,D正确。
1
2
3
4
5
6
1
2
3
4
5
6
7
8
9
10
题组一 生活中常见有机物的应用判断
1.化学与生活联系密切。下列材料的主要成分是无机物的是
A.不粘锅涂层材料——聚四氟乙烯
B.生产服装面料的材料——涤纶
C.常用于制作饰物的材料——玛瑙
D.制造公共自行车实心轮胎的材料——橡胶
√
精练预测押题
1
2
3
4
5
6
7
8
9
10
解析 A项,聚四氟乙烯属于有机物;
B项,涤纶是聚酯纤维的商品名,属于有机物;
C项,玛瑙的主要成分是二氧化硅,属于无机物;
D项,橡胶属于有机物。
2.化学与生活密切相关。下列说法正确的是
A.福尔马林可作食品保鲜剂
B.乙烯可作水果的催熟剂
C.做衣服的棉和麻均与淀粉互为同分异构体
D.磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸
1
2
3
4
5
6
7
8
9
10
√
解析 福尔马林是甲醛的水溶液,有毒,不能作食品保鲜剂,A项错误;
乙烯可作水果的催熟剂,B项正确;
棉和麻的主要成分为纤维素,纤维素与淀粉的分子式都用(C6H10O5)n表示,但n值不同,所以不互为同分异构体,C项错误;
豆浆煮沸后蛋白质发生变性,但不会发生水解,D项错误。
1
2
3
4
5
6
7
8
9
10
题组二 常见有机物的性质及反应类型判断
3.下列关于有机化合物的叙述中正确的是
A.乙烯和聚乙烯都能使溴的四氯化碳溶液褪色
B.向溴的CCl4溶液和酸性KMnO4溶液中分别通入乙烯,溶液均褪色,且
褪色原理相同
C.乙醇、乙酸的官能团不同,但均能发生取代反应
D.可通过加入金属钠观察是否产生气体的方法检验乙醇中是否混有水
1
2
3
4
5
6
7
8
9
10
√
1
2
3
4
5
6
7
8
9
10
解析 A项,聚乙烯中没有碳碳双键,不能使溴的四氯化碳溶液褪色,错误;
B项,乙烯与溴的CCl4溶液发生加成反应而使溶液褪色,而乙烯被酸性KMnO4溶液氧化而使溶液褪色,错误;
C项,乙醇与乙酸的酯化反应为取代反应,正确;
D项,乙醇和水均能与Na反应产生H2,错误。
4.下列说法正确的是
A.乙烯使溴水或酸性高锰酸钾溶液褪色均属于加成反应
B.乙醇与浓硫酸混合,加热至170 ℃制乙烯的反应属于取代反应
C.用酸性重铬酸钾溶液检验酒驾,发生的反应属于乙醇的氧化反应
D.等质量的乙烯和乙醇完全燃烧,消耗O2的物质的量相同
1
2
3
4
5
6
7
8
9
10
√
解析 乙烯与溴水发生加成反应,与酸性KMnO4溶液发生氧化还原反应,二者褪色的原理不同,A项错误;
乙醇与浓硫酸混合在170 ℃时发生消去反应生成乙烯,B项错误;
乙醇具有还原性,能被酸性K2Cr2O7溶液氧化成乙酸,C项正确;
等物质的量的乙烯和乙醇完全燃烧,消耗O2的物质的量相同,但等质量的乙烯和乙醇完全燃烧时,前者消耗的O2多,D项错误。
1
2
3
4
5
6
7
8
9
10
题组三 结构给予型有机物性质的判断
5.(2020·日照一模)研究发现,药物磷酸氯喹在细胞水平上能有效抑制新型冠状病毒的感染,其结构如下图所示,下列有关磷酸氯喹的说法错误的是
A.分子式为C18H26ClN3O8P2
B.分子中含有1个手性碳原子
C.能溶于水且水溶液呈酸性
D.能发生取代反应和加成反应
1
2
3
4
5
6
7
8
9
10
√
解析 该有机物的分子式为C18H32ClN3O8P2,A选项错误;
该分子中含有1个手性碳原子,B选项正确;
该物质是氯喹和磷酸反应得到的酸式盐,在水中易溶,且其水溶液呈酸性,C选项正确;
该分子中苯环能够发生取代、加成反应,D选项正确。
1
2
3
4
5
6
7
8
9
10
6.(2020·山东5月等级模拟考,4)中医药是中华民族的瑰宝,厚朴酚是一种常见中药的主要成分之一,有抗菌、消炎等功效,其结构简式如图a所示。下列说法错误的是
A.厚朴酚与溴水既可发生加成反应又可
发生取代反应
B.图b所示为厚朴酚的一种同分异构体
C.厚朴酚分子中所有碳原子可能共平面
D.厚朴酚分子中不含手性碳原子
√
1
2
3
4
5
6
7
8
9
10
解析 厚朴酚含有酚羟基、碳碳双键,既可与溴水发生加成反应又可发生取代反应,故A正确;
图b结构与厚朴酚相同,和厚朴酚为同一
物质,故B错误;
厚朴酚分子中苯环中所有原子共面,碳
碳双键中所有原子共面,则所有碳原子可能共面,故C正确;
手性碳原子是指与四个各不相同原子或原子团相连的碳原子,由结构图可知厚朴酚分子中不含手性碳原子,故D正确。
1
2
3
4
5
6
7
8
9
10
7.(2020·青岛一模)磷酸奥司他韦是临床常用的抗病毒药物,常用于甲型和乙型流感治疗。其中间体结构简式如图所示,关于该有机物下列说法错误的是
A.分子式为C16H28N2O4
B.该有机物既能与酸反应又能与碱反应
C.该有机物分子中含有3个手性碳原子
D.1 mol 该有机物最多能与3 mol H2发生加成反应
1
2
3
4
5
6
7
8
9
10
√
解析 分子式为C16H28N2O4,A正确;
在中间体结构简式中,—NH2可以与酸反应,同时又存
在酯基与酰胺键,既能与酸反应又能与碱反应,B正确;
该有机物分子中含有3个手性碳原子,C正确;
1 mol 该有机物含1 mol碳碳双键,最多能与1 mol H2发生加成反应,而酯基和酰胺键都不能与H2发生加成,D错误。
1
2
3
4
5
6
7
8
9
10
题组四 常见有机物的制备、性质与检验
8.下列鉴别方法不可行的是
A.用水鉴别乙醇和苯
B.用溴水鉴别己烯和苯乙烯
C.用碳酸钠溶液鉴别乙酸和乙酸乙酯
D.用酸性高锰酸钾溶液鉴别甲苯和环己烷
1
2
3
4
5
6
7
8
9
10
√
1
2
3
4
5
6
7
8
9
10
解析 乙醇能溶于水,而苯不溶于水且在水的上层,A项可鉴别;
溴水与己烯、苯乙烯均能发生加成反应而褪色,B项无法鉴别;
碳酸钠与乙酸反应生成CO2气体(现象为有气泡产生),乙酸乙酯不溶于碳酸钠溶液且在上层,C项可鉴别;
高锰酸钾溶液与甲苯反应而褪色,环己烷不与高锰酸钾溶液反应但出现分层,D项可鉴别。
9.将漫射日光照射到装有氯气和甲烷混合气体(体积比为4∶1)的装置上(如图)。现列出如下现象,其中正确的是
①试管内黄绿色逐渐消失
②试管内黄绿色加深
③无任何现象
④试管内液面上升
⑤试管内壁上有油状物生成
A.① B.①④⑤ C.①⑤ D.②⑤
1
2
3
4
5
6
7
8
9
10
√
解析 因为反应物和生成物中只有氯气为有色物质,在光照条件下氯气与甲烷发生了取代反应,所以试管内气体颜色
逐渐消失,①正确,②、③错误;
氯气与甲烷反应生成各种氯代产物和氯化氢,
氯化氢极易溶于水,试管中气体体积减小,所
以试管内液面上升,④正确;
反应生成的二氯甲烷、三氯甲烷和四氯化碳均为不溶于水的油状液体,所以试管内壁上有油状物生成,⑤正确。
1
2
3
4
5
6
7
8
9
10
10.(2020·德州一模)乙酸丁酯是重要的化工原料。实验室用乙酸、丁醇在浓硫酸作催化剂、加热条件下制备乙酸丁酯的装置示意图(加热和夹持装置已省略)和有关信息如下:
1
2
3
4
5
6
7
8
9
10
?
乙酸
正丁醇
乙酸丁酯
熔点/℃
16.6
-89.5
-73.5
沸点/℃
117.9
117
126.0
密度/g·cm-3
1.1
0.80
0.88
下列说法正确的是
A.加热一段时间后,发现烧瓶C中忘记加沸石,可打开瓶
塞直接加入即可
B.装置B的作用是不断分离出乙酸丁酯,提高产率
C.装置A可以装配蒸馏装置的冷凝器,且冷凝水由a口进,
b口出
D.乙酸丁酯中残留的乙酸和正丁醇可用饱和碳酸钠溶液除去
1
2
3
4
5
6
7
8
9
10
√
1
2
3
4
5
6
7
8
9
10
解析 液体加热时要加沸石或碎瓷片,防止溶液暴沸,如果加热一段时间后发现忘记加碎瓷片,应该采取停止加热,待溶液冷却
后重新添加碎瓷片,故A错误;
装置B是水分离器,作用是不断分离出水,提高乙酸丁酯的
产率,故B错误;
装置A不能用于装配蒸馏装置的冷凝器,故C错误;
饱和碳酸钠溶液可以降低乙酸丁酯的溶解度,吸收正丁醇,除去乙酸,则乙酸丁酯中残留的乙酸和正丁醇可用饱和碳酸钠溶液除去,故D正确。
角度一
1.常见有机物的重要物理性质
(1)常温常压下,分子中碳原子个数不多于4的烃是气体,烃的密度都比水小。
(2)烃、烃的卤代物、酯类物质均不溶于水,低级醇、酸能溶于水。
(3)随着分子中碳原子数目的增多,各类有机物的同系物熔、沸点逐渐升高。同分异构体的支链越多,熔、沸点越低。
高考必备知识
物质
结构简式
特性或特征反应
甲烷
CH4
与氯气在光照下发生取代反应
乙烯
CH2==CH2
官能团
①加成反应:使溴水褪色
②加聚反应
③氧化反应:使酸性KMnO4溶液褪色
苯
?
①加成反应
②取代反应:与溴(溴化铁作催化剂),与硝酸(浓硫酸作催化剂)
2.常见有机物的结构特点及主要化学性质
乙醇
CH3CH2OH
官能团—OH
①与钠反应放出H2
②催化氧化反应:生成乙醛
③酯化反应:与酸反应生成酯
乙酸
CH3COOH
官能团—COOH
①弱酸性,但酸性比碳酸强
②酯化反应:与醇反应生成酯
乙酸
乙酯
CH3COOCH2CH3
官能团—COOR
可发生水解反应,在碱性条件下水解彻底
油脂
?
可发生水解反应,在碱性条件下水解彻底,被称为皂化反应
淀粉
(C6H10O5)n
①遇碘变蓝色
②在稀酸催化下,最终水解成葡萄糖
③葡萄糖在酒化酶的作用下,生成乙醇和CO2
蛋白质
含有肽键
①水解反应生成氨基酸
②两性
③变性
④盐析
⑤颜色反应
⑥灼烧产生特殊气味
3.判断有机反应中某些反应物用量多少的方法
(1)H2用量的判断。
有机物分子中的 、—C≡C—、 、—CHO、 (羰
基)都能在一定条件下与H2发生加成反应,当这些官能团的物质的量相等
时,消耗H2的物质的量之比为1∶2∶3∶1∶1。特别注意—COOH、—COOR
(酯基)中的 通常不与H2发生加成反应。
(2)能与NaOH反应的有机物及其用量比例(设有机物分子官能团个数为1):①卤代烃:1∶1,②苯环上连接的卤原子:1∶2;③酚羟基:1∶1;④羧
基:1∶1,⑤普通酯:1∶1;⑥酚酯:1∶2。
(3)Br2用量的判断。
烷烃(光照下1 mol Br2可取代1 mol氢原子)、苯(FeBr3催化下1 mol Br2可取代1 mol氢原子)、酚类(1 mol Br2可取代与—OH所连碳原子处于邻、对位
碳原子上的1 mol H原子)、 (1 mol双键可与1 mol Br2发生加成反
应)、—C≡C—(1 mol三键可与2 mol Br2发生加成反应)。
4.有机物与日常生活
(1)医用酒精中乙醇的体积分数为75%,使蛋白质变性,用于消毒。
(2)福尔马林是35%~40%的甲醛水溶液,使蛋白质变性,良好的杀菌剂,常作为浸制标本的溶液(不可用于食品保鲜)。
(3)蛋白质受热变性,加热能杀死流感病毒。
(4)蚕丝灼烧有烧焦羽毛的气味,灼烧法可以区别蚕丝和人造纤维。
(5)聚乙烯性质稳定,无毒,可作食品包装袋。
(6)聚氯乙烯有毒,不能用作食品包装袋。
(7)食用油反复加热会产生稠环芳香烃等有害物质,不能反复加热。
(8)聚四氟乙烯具有抗酸、抗碱、抗各种有机溶剂的特点,用于厨具表面涂层。
(9)甘油具有吸水性,作护肤保湿剂。
(10)淀粉遇碘显蓝色,鉴别淀粉与其他物质(如蛋白质、木纤维等)。
(11)食醋与碳酸钙反应生成可溶于水的醋酸钙,可除水垢(主要成分为碳酸钙)。
(12)阿司匹林水解生成水杨酸,显酸性,服用阿司匹林出现水杨酸反应时,用NaHCO3溶液解毒。
(13)加工后具有吸水性的植物纤维,可用作食品干燥剂。
(14)谷氨酸钠具有鲜味,可作味精。
(15)油脂在碱性条件下水解为高级脂肪酸盐和甘油,制肥皂。
1.(2020·浙江7月选考,14)下列说法不正确的是
A.相同条件下等质量的甲烷、汽油、氢气完全燃烧,放出的热量依次增加
B.油脂在碱性条件下水解生成的高级脂肪酸盐是肥皂的主要成分
C.根据纤维在火焰上燃烧产生的气味,可以鉴别蚕丝与棉花
D.淀粉、纤维素、蛋白质都属于高分子化合物
1
2
3
4
5
6
√
重练高考真题
解析 相同条件下等质量的甲烷、汽油、氢气完全燃烧放出的热量由小到大依次是汽油、甲烷、氢气,A错误。
2.(2020·天津,3)下列说法错误的是
A.淀粉和纤维素均可水解产生葡萄糖
B.油脂的水解反应可用于生产甘油
C.氨基酸是组成蛋白质的基本结构单元
D.淀粉、纤维素和油脂均是天然高分子
1
2
3
4
5
6
√
解析 油脂是指高级脂肪酸甘油酯,不属于高分子化合物。高分子化合物是指相对分子质量很大(104~106,甚至更大)的化合物。
3.(2017·全国卷Ⅰ,7)下列生活用品中主要由合成纤维制造的是
A.尼龙绳 B.宣纸 C.羊绒衫 D.棉衬衣
1
2
3
4
5
6
解析 A项,尼龙的主要成分是聚酰胺纤维(锦纶),属于合成纤维,正确;
B项,宣纸的主要成分是纤维素,错误;
C项,羊绒衫的主要成分是蛋白质,错误;
棉衬衣的主要成分是纤维素,错误。
√
4.(2018·全国卷Ⅲ,9)苯乙烯是重要的化工原料。下列有关苯乙烯的说法错误的是
A.与液溴混合后加入铁粉可发生取代反应
B.能使酸性高锰酸钾溶液褪色
C.与氯化氢反应可以生成氯代苯乙烯
D.在催化剂存在下可以制得聚苯乙烯
√
1
2
3
4
5
6
1
2
3
4
5
6
解析 与氯化氢的反应是发生在碳碳双键上的加成反应,产物是氯代苯乙烷,C项错误;
“铁粉”“液溴”是苯乙烯( )在苯环上发生溴代反应的条件,A项正确;
含有碳碳双键,能使酸性高锰酸钾溶液褪色,B项正确;
含有碳碳双键,能发生加聚反应生成聚苯乙烯,D项正确。
选项
实验
结论
A
将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明
生成的1,2-二溴乙烷无色、可溶于四氯化碳
B
乙醇和水都可与金属钠反应产生可燃性气体
乙醇分子中的氢与水分子中的氢具有相同的活性
C
用乙酸浸泡水壶中的水垢,可将其清除
乙酸的酸性小于碳酸的酸性
D
甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红
生成的氯甲烷具有酸性
1
2
3
4
5
6
5.(2017·全国卷Ⅱ,10)下列由实验得出的结论正确的是
√
1
2
3
4
5
6
解析 B项,钠与水反应比钠与乙醇反应剧烈,说明水中的氢比乙醇中的氢活泼,错误;
C项,根据强酸制弱酸,可知乙酸酸性大于碳酸,错误;
D项,甲烷与氯气在光照下发生取代反应生成了HCl,HCl气体能使湿润的石蕊试纸变红,错误。
6.(2019·浙江4月选考,16)下列表述正确的是
A.苯和氯气生成C6H6Cl6的反应是取代反应
B.乙烯与溴水发生加成反应的产物是CH2CH2Br2
C.等物质的量的甲烷与氯气反应的产物是CH3Cl
D.硫酸作催化剂,CH3CO18OCH2CH3水解所得乙醇分子中有18O
1
2
3
4
5
6
√
解析 苯和氯气生成C6H6Cl6的反应是加成反应,A错误;
乙烯与溴水发生加成反应的产物应为CH2BrCH2Br,B错误;
甲烷与氯气反应生成的是CH3Cl、CH2Cl2、CHCl3、CCl4、HCl的混合物,C错误;
CH3CO18OCH2CH3水解生成CH3COOH和CH3CH218OH,D正确。
1
2
3
4
5
6
1
2
3
4
5
6
7
8
9
10
题组一 生活中常见有机物的应用判断
1.化学与生活联系密切。下列材料的主要成分是无机物的是
A.不粘锅涂层材料——聚四氟乙烯
B.生产服装面料的材料——涤纶
C.常用于制作饰物的材料——玛瑙
D.制造公共自行车实心轮胎的材料——橡胶
√
精练预测押题
1
2
3
4
5
6
7
8
9
10
解析 A项,聚四氟乙烯属于有机物;
B项,涤纶是聚酯纤维的商品名,属于有机物;
C项,玛瑙的主要成分是二氧化硅,属于无机物;
D项,橡胶属于有机物。
2.化学与生活密切相关。下列说法正确的是
A.福尔马林可作食品保鲜剂
B.乙烯可作水果的催熟剂
C.做衣服的棉和麻均与淀粉互为同分异构体
D.磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸
1
2
3
4
5
6
7
8
9
10
√
解析 福尔马林是甲醛的水溶液,有毒,不能作食品保鲜剂,A项错误;
乙烯可作水果的催熟剂,B项正确;
棉和麻的主要成分为纤维素,纤维素与淀粉的分子式都用(C6H10O5)n表示,但n值不同,所以不互为同分异构体,C项错误;
豆浆煮沸后蛋白质发生变性,但不会发生水解,D项错误。
1
2
3
4
5
6
7
8
9
10
题组二 常见有机物的性质及反应类型判断
3.下列关于有机化合物的叙述中正确的是
A.乙烯和聚乙烯都能使溴的四氯化碳溶液褪色
B.向溴的CCl4溶液和酸性KMnO4溶液中分别通入乙烯,溶液均褪色,且
褪色原理相同
C.乙醇、乙酸的官能团不同,但均能发生取代反应
D.可通过加入金属钠观察是否产生气体的方法检验乙醇中是否混有水
1
2
3
4
5
6
7
8
9
10
√
1
2
3
4
5
6
7
8
9
10
解析 A项,聚乙烯中没有碳碳双键,不能使溴的四氯化碳溶液褪色,错误;
B项,乙烯与溴的CCl4溶液发生加成反应而使溶液褪色,而乙烯被酸性KMnO4溶液氧化而使溶液褪色,错误;
C项,乙醇与乙酸的酯化反应为取代反应,正确;
D项,乙醇和水均能与Na反应产生H2,错误。
4.下列说法正确的是
A.乙烯使溴水或酸性高锰酸钾溶液褪色均属于加成反应
B.乙醇与浓硫酸混合,加热至170 ℃制乙烯的反应属于取代反应
C.用酸性重铬酸钾溶液检验酒驾,发生的反应属于乙醇的氧化反应
D.等质量的乙烯和乙醇完全燃烧,消耗O2的物质的量相同
1
2
3
4
5
6
7
8
9
10
√
解析 乙烯与溴水发生加成反应,与酸性KMnO4溶液发生氧化还原反应,二者褪色的原理不同,A项错误;
乙醇与浓硫酸混合在170 ℃时发生消去反应生成乙烯,B项错误;
乙醇具有还原性,能被酸性K2Cr2O7溶液氧化成乙酸,C项正确;
等物质的量的乙烯和乙醇完全燃烧,消耗O2的物质的量相同,但等质量的乙烯和乙醇完全燃烧时,前者消耗的O2多,D项错误。
1
2
3
4
5
6
7
8
9
10
题组三 结构给予型有机物性质的判断
5.(2020·日照一模)研究发现,药物磷酸氯喹在细胞水平上能有效抑制新型冠状病毒的感染,其结构如下图所示,下列有关磷酸氯喹的说法错误的是
A.分子式为C18H26ClN3O8P2
B.分子中含有1个手性碳原子
C.能溶于水且水溶液呈酸性
D.能发生取代反应和加成反应
1
2
3
4
5
6
7
8
9
10
√
解析 该有机物的分子式为C18H32ClN3O8P2,A选项错误;
该分子中含有1个手性碳原子,B选项正确;
该物质是氯喹和磷酸反应得到的酸式盐,在水中易溶,且其水溶液呈酸性,C选项正确;
该分子中苯环能够发生取代、加成反应,D选项正确。
1
2
3
4
5
6
7
8
9
10
6.(2020·山东5月等级模拟考,4)中医药是中华民族的瑰宝,厚朴酚是一种常见中药的主要成分之一,有抗菌、消炎等功效,其结构简式如图a所示。下列说法错误的是
A.厚朴酚与溴水既可发生加成反应又可
发生取代反应
B.图b所示为厚朴酚的一种同分异构体
C.厚朴酚分子中所有碳原子可能共平面
D.厚朴酚分子中不含手性碳原子
√
1
2
3
4
5
6
7
8
9
10
解析 厚朴酚含有酚羟基、碳碳双键,既可与溴水发生加成反应又可发生取代反应,故A正确;
图b结构与厚朴酚相同,和厚朴酚为同一
物质,故B错误;
厚朴酚分子中苯环中所有原子共面,碳
碳双键中所有原子共面,则所有碳原子可能共面,故C正确;
手性碳原子是指与四个各不相同原子或原子团相连的碳原子,由结构图可知厚朴酚分子中不含手性碳原子,故D正确。
1
2
3
4
5
6
7
8
9
10
7.(2020·青岛一模)磷酸奥司他韦是临床常用的抗病毒药物,常用于甲型和乙型流感治疗。其中间体结构简式如图所示,关于该有机物下列说法错误的是
A.分子式为C16H28N2O4
B.该有机物既能与酸反应又能与碱反应
C.该有机物分子中含有3个手性碳原子
D.1 mol 该有机物最多能与3 mol H2发生加成反应
1
2
3
4
5
6
7
8
9
10
√
解析 分子式为C16H28N2O4,A正确;
在中间体结构简式中,—NH2可以与酸反应,同时又存
在酯基与酰胺键,既能与酸反应又能与碱反应,B正确;
该有机物分子中含有3个手性碳原子,C正确;
1 mol 该有机物含1 mol碳碳双键,最多能与1 mol H2发生加成反应,而酯基和酰胺键都不能与H2发生加成,D错误。
1
2
3
4
5
6
7
8
9
10
题组四 常见有机物的制备、性质与检验
8.下列鉴别方法不可行的是
A.用水鉴别乙醇和苯
B.用溴水鉴别己烯和苯乙烯
C.用碳酸钠溶液鉴别乙酸和乙酸乙酯
D.用酸性高锰酸钾溶液鉴别甲苯和环己烷
1
2
3
4
5
6
7
8
9
10
√
1
2
3
4
5
6
7
8
9
10
解析 乙醇能溶于水,而苯不溶于水且在水的上层,A项可鉴别;
溴水与己烯、苯乙烯均能发生加成反应而褪色,B项无法鉴别;
碳酸钠与乙酸反应生成CO2气体(现象为有气泡产生),乙酸乙酯不溶于碳酸钠溶液且在上层,C项可鉴别;
高锰酸钾溶液与甲苯反应而褪色,环己烷不与高锰酸钾溶液反应但出现分层,D项可鉴别。
9.将漫射日光照射到装有氯气和甲烷混合气体(体积比为4∶1)的装置上(如图)。现列出如下现象,其中正确的是
①试管内黄绿色逐渐消失
②试管内黄绿色加深
③无任何现象
④试管内液面上升
⑤试管内壁上有油状物生成
A.① B.①④⑤ C.①⑤ D.②⑤
1
2
3
4
5
6
7
8
9
10
√
解析 因为反应物和生成物中只有氯气为有色物质,在光照条件下氯气与甲烷发生了取代反应,所以试管内气体颜色
逐渐消失,①正确,②、③错误;
氯气与甲烷反应生成各种氯代产物和氯化氢,
氯化氢极易溶于水,试管中气体体积减小,所
以试管内液面上升,④正确;
反应生成的二氯甲烷、三氯甲烷和四氯化碳均为不溶于水的油状液体,所以试管内壁上有油状物生成,⑤正确。
1
2
3
4
5
6
7
8
9
10
10.(2020·德州一模)乙酸丁酯是重要的化工原料。实验室用乙酸、丁醇在浓硫酸作催化剂、加热条件下制备乙酸丁酯的装置示意图(加热和夹持装置已省略)和有关信息如下:
1
2
3
4
5
6
7
8
9
10
?
乙酸
正丁醇
乙酸丁酯
熔点/℃
16.6
-89.5
-73.5
沸点/℃
117.9
117
126.0
密度/g·cm-3
1.1
0.80
0.88
下列说法正确的是
A.加热一段时间后,发现烧瓶C中忘记加沸石,可打开瓶
塞直接加入即可
B.装置B的作用是不断分离出乙酸丁酯,提高产率
C.装置A可以装配蒸馏装置的冷凝器,且冷凝水由a口进,
b口出
D.乙酸丁酯中残留的乙酸和正丁醇可用饱和碳酸钠溶液除去
1
2
3
4
5
6
7
8
9
10
√
1
2
3
4
5
6
7
8
9
10
解析 液体加热时要加沸石或碎瓷片,防止溶液暴沸,如果加热一段时间后发现忘记加碎瓷片,应该采取停止加热,待溶液冷却
后重新添加碎瓷片,故A错误;
装置B是水分离器,作用是不断分离出水,提高乙酸丁酯的
产率,故B错误;
装置A不能用于装配蒸馏装置的冷凝器,故C错误;
饱和碳酸钠溶液可以降低乙酸丁酯的溶解度,吸收正丁醇,除去乙酸,则乙酸丁酯中残留的乙酸和正丁醇可用饱和碳酸钠溶液除去,故D正确。
同课章节目录
