2021年人教版化学中考总复习专题训练 常见的酸和碱 导学案
文档属性
| 名称 | 2021年人教版化学中考总复习专题训练 常见的酸和碱 导学案 |  | |
| 格式 | docx | ||
| 文件大小 | 352.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-05 08:49:33 | ||
图片预览



文档简介
常见的酸和碱
【化学用语检查站9】
1.写出下列常见碱的化学式,并按要求填空:
①氢氧化钠
②氢氧化钡
③氨水
④氢氧化钙
⑤氢氧化铜
⑥氢氧化铁
⑦氢氧化镁
其中属于可溶性碱的有
;微溶性碱
;难溶性碱
.(填序号)
2.写出下列反应的化学方程式,其中属于中和反应的是
.(填序号)
(1)生石灰溶于水:
.
(2)氢氧化钠在空气中变质:
.
(3)氢氧化钠溶液和硫酸:
.
(4)盐酸溶解氢氧化铜:
[基础巩固]
1.下列物质的分类,不正确的一组是(
)
A.H2O、MgO、H2CO3
都属于氧化物
B.HCl、H2SO3、H2SO4
都属于酸
C.NaOH、Ca(OH)2、Fe(OH)2
都属于碱
D.NaCl、Na2CO3、NaHCO3
都属于盐
2.如图是盐酸滴入NaOH溶液中,有关粒子之间反应的示意图.下列说法错误的是(
)
A.盐酸溶液中含有氢离子和氯离子
B.氢氧化钠溶液中含有钠离子和氢氧根离子
C.两种溶液混合时,氢离子与氢氧根离子结合生成了水分子
D.两种溶液混合时,钠离子与氯离子结合生成了氯化钠分子
3.醋酸(CH3COOH)是食醋的成分之一,其水溶液中存在H+和CH3COO-.下列说法正确的是(
)
A.醋酸属于氧化物
B.醋酸不能用于除铁锈
C.醋酸能与镁反应产生氢气
D.醋酸中碳元素的质量分数最大
4.(2020·重庆)某同学将一定量的Na2CO3与Ba(OH)2溶液混合,要想检验反应后Ba(OH)2是否过量,应选用的试剂是(
)
A.酚酞
B.CuCl2溶液
C.Na2CO3溶液
D.NaCl溶液
5.下列关于H2SO4性质描述中,不属于酸的通性的是(
)
A.使紫色石蕊溶液变红
B.与NaOH发生中和反应
C.浓硫酸滴到白纸上使纸变黑
D.与Mg反应放出氢气
6.下列除杂(括号内的是杂质)所选试剂合理的是(
)
A.Cu(Zn):稀盐酸
B.CO2气体(HCl):氢氧化钠溶液
C.CuO(Cu):浓硫酸
D.Ca(OH)2(CaCO3):稀盐酸
7.“见著知微”是化学学科的重要特点,它是通过对宏观现象的观察、思考、推理,建立起对微观粒子的认识.下列说法不正确的是(
)
A.品红在水中扩散,说明分子在不断地运动
B.电解水生成氢气和氧气,说明水是由氢分子和氧分子构成的
C.盐酸、稀硫酸具有相似的化学性质,说明它们的溶液中都含有氢离子
D.无色酚酞溶液滴入某稀溶液中显红色,说明该溶液中含有氢氧根离子
8.X是两种金属氧化物组成的混合物,为了研究混合物的成分,进行了如图所示的实验.
(1)X中含有的金属元素是
(填元素符号).
(2)写出X中一种成分与盐酸反应的化学方程式:
.
(3)若Y为固体,写出Y与X中一种成分反应的化学方程式
;若Y为气体,Y还可以是
(填化学式).
9.(广东经典)下图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种.
(1)写出乙和丙的化学式:乙
,丙
.
(2)写出下列化学方程式:
①甲和乙:
.
②丙和丁:
.
(3)图中反应①属于基本反应类型中的
反应,又称为
反应.
[能力提升]
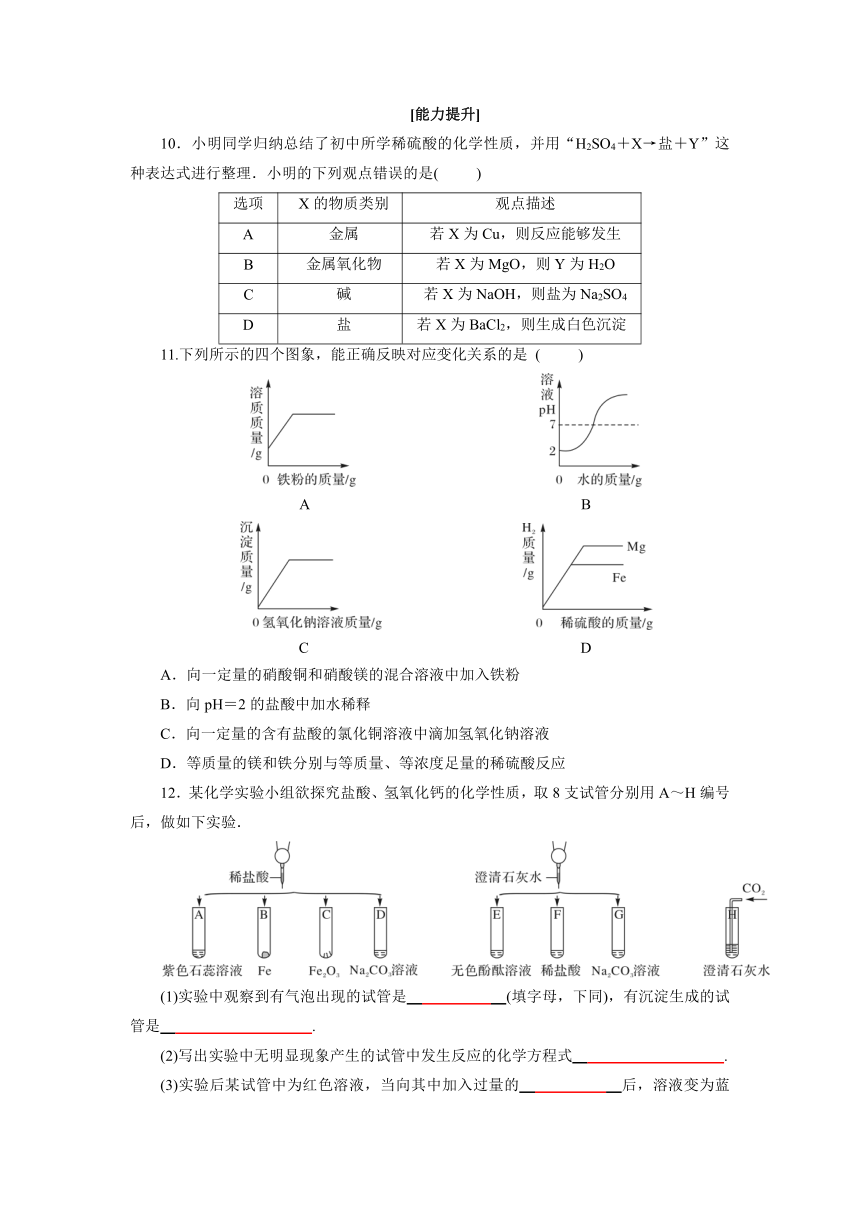
10.小明同学归纳总结了初中所学稀硫酸的化学性质,并用“H2SO4+X→盐+Y”这种表达式进行整理.小明的下列观点错误的是(
)
选项
X的物质类别
观点描述
A
金属
若X为Cu,则反应能够发生
B
金属氧化物
若X为MgO,则Y为H2O
C
碱
若X为NaOH,则盐为Na2SO4
D
盐
若X为BaCl2,则生成白色沉淀
11.下列所示的四个图象,能正确反映对应变化关系的是
(
)
A
B
C
D
A.向一定量的硝酸铜和硝酸镁的混合溶液中加入铁粉
B.向pH=2的盐酸中加水稀释
C.向一定量的含有盐酸的氯化铜溶液中滴加氢氧化钠溶液
D.等质量的镁和铁分别与等质量、等浓度足量的稀硫酸反应
12.某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用A~H编号后,做如下实验.
(1)实验中观察到有气泡出现的试管是
(填字母,下同),有沉淀生成的试管是
.
(2)写出实验中无明显现象产生的试管中发生反应的化学方程式
.
(3)实验后某试管中为红色溶液,当向其中加入过量的
后,溶液变为蓝色.由此推断,该试管中最初盛有的物质是
.
(4)实验后某试管的底部有白色固体,过滤后向滤液中滴加盐酸,一段时间后有气泡冒出,则该滤液中的溶质是
.
13.(2020·广东模拟)碲(Te)广泛用于彩色玻璃和陶瓷工艺,难溶于水.用某工业废渣(主要含有TeO2、少量Ag、Au)为原料制备碲的一种工艺流程如下:
回答下列问题:
(1)类比CO2与NaOH的反应,写出“碱浸”时发生反应的化学方程式:
,产物盐中Te元素的化合价是
.
(2)滤液1中的两种溶质是H2SO4和
(填化学式).
(3)上述工艺流程中设计“废渣→……→TeO2”的目的是
.
(4)“酸溶”后,在TeCl4溶液中通入SO2,反应生成碲和初中化学中两种常见的酸,则该反应的化学方程式是
.
常见的酸和碱
【化学用语检查站9】
1.写出下列常见碱的化学式,并按要求填空:
①氢氧化钠 NaOH ②氢氧化钡 Ba(OH)2 ③氨水 NH3·H2O ④氢氧化钙 Ca(OH)2
⑤氢氧化铜 Cu(OH)2 ⑥氢氧化铁 Fe(OH)3 ⑦氢氧化镁 Mg(OH)2
其中属于可溶性碱的有 ①②③ ;微溶性碱 ④ ;难溶性碱 ⑤⑥⑦ .(填序号)
2.写出下列反应的化学方程式,其中属于中和反应的是 (3)(4) .(填序号)
(1)生石灰溶于水: CaO+H2O===Ca(OH)2 .
(2)氢氧化钠在空气中变质: 2NaOH+CO2===Na2CO3+H2O .
(3)氢氧化钠溶液和硫酸: 2NaOH+H2SO4===Na2SO4+2H2O .
(4)盐酸溶解氢氧化铜: 2HCl+Cu(OH)2===CuCl2+2H2O .
[基础巩固]
1.下列物质的分类,不正确的一组是( A )
A.H2O、MgO、H2CO3
都属于氧化物
B.HCl、H2SO3、H2SO4
都属于酸
C.NaOH、Ca(OH)2、Fe(OH)2
都属于碱
D.NaCl、Na2CO3、NaHCO3
都属于盐
2.如图是盐酸滴入NaOH溶液中,有关粒子之间反应的示意图.下列说法错误的是( D )
A.盐酸溶液中含有氢离子和氯离子
B.氢氧化钠溶液中含有钠离子和氢氧根离子
C.两种溶液混合时,氢离子与氢氧根离子结合生成了水分子
D.两种溶液混合时,钠离子与氯离子结合生成了氯化钠分子
3.醋酸(CH3COOH)是食醋的成分之一,其水溶液中存在H+和CH3COO-.下列说法正确的是( C )
A.醋酸属于氧化物
B.醋酸不能用于除铁锈
C.醋酸能与镁反应产生氢气
D.醋酸中碳元素的质量分数最大
4.(2020·重庆)某同学将一定量的Na2CO3与Ba(OH)2溶液混合,要想检验反应后Ba(OH)2是否过量,应选用的试剂是( C )
A.酚酞
B.CuCl2溶液
C.Na2CO3溶液
D.NaCl溶液
5.下列关于H2SO4性质描述中,不属于酸的通性的是( C )
A.使紫色石蕊溶液变红
B.与NaOH发生中和反应
C.浓硫酸滴到白纸上使纸变黑
D.与Mg反应放出氢气
6.下列除杂(括号内的是杂质)所选试剂合理的是( A )
A.Cu(Zn):稀盐酸
B.CO2气体(HCl):氢氧化钠溶液
C.CuO(Cu):浓硫酸
D.Ca(OH)2(CaCO3):稀盐酸
7.“见著知微”是化学学科的重要特点,它是通过对宏观现象的观察、思考、推理,建立起对微观粒子的认识.下列说法不正确的是( B )
A.品红在水中扩散,说明分子在不断地运动
B.电解水生成氢气和氧气,说明水是由氢分子和氧分子构成的
C.盐酸、稀硫酸具有相似的化学性质,说明它们的溶液中都含有氢离子
D.无色酚酞溶液滴入某稀溶液中显红色,说明该溶液中含有氢氧根离子
8.X是两种金属氧化物组成的混合物,为了研究混合物的成分,进行了如图所示的实验.
(1)X中含有的金属元素是 Fe,Cu (填元素符号).
(2)写出X中一种成分与盐酸反应的化学方程式: CuO+2HCl===CuCl2+H2O .
(3)若Y为固体,写出Y与X中一种成分反应的化学方程式 C+2CuO2Cu+CO2↑ ;若Y为气体,Y还可以是 CO (填化学式).
9.(广东经典)下图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种.
(1)写出乙和丙的化学式:乙 Na2CO3 ,丙 HCl .
(2)写出下列化学方程式:
①甲和乙: BaCl2+Na2CO3===BaCO3↓+2NaCl .
②丙和丁: 2HCl+Mg===MgCl2+H2↑ .
(3)图中反应①属于基本反应类型中的 复分解 反应,又称为 中和 反应.
[能力提升]
10.小明同学归纳总结了初中所学稀硫酸的化学性质,并用“H2SO4+X→盐+Y”这种表达式进行整理.小明的下列观点错误的是( A )
选项
X的物质类别
观点描述
A
金属
若X为Cu,则反应能够发生
B
金属氧化物
若X为MgO,则Y为H2O
C
碱
若X为NaOH,则盐为Na2SO4
D
盐
若X为BaCl2,则生成白色沉淀
11.下列所示的四个图象,能正确反映对应变化关系的是
( D )
A
B
C
D
A.向一定量的硝酸铜和硝酸镁的混合溶液中加入铁粉
B.向pH=2的盐酸中加水稀释
C.向一定量的含有盐酸的氯化铜溶液中滴加氢氧化钠溶液
D.等质量的镁和铁分别与等质量、等浓度足量的稀硫酸反应
12.某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用A~H编号后,做如下实验.
(1)实验中观察到有气泡出现的试管是 B、D (填字母,下同),有沉淀生成的试管是 G、H .
(2)写出实验中无明显现象产生的试管中发生反应的化学方程式 Ca(OH)2+2HCl===CaCl2+2H2O .
(3)实验后某试管中为红色溶液,当向其中加入过量的 NaOH溶液 后,溶液变为蓝色.由此推断,该试管中最初盛有的物质是 紫色石蕊溶液 .
(4)实验后某试管的底部有白色固体,过滤后向滤液中滴加盐酸,一段时间后有气泡冒出,则该滤液中的溶质是 NaOH和Na2CO3 .
13.(2020·广东模拟)碲(Te)广泛用于彩色玻璃和陶瓷工艺,难溶于水.用某工业废渣(主要含有TeO2、少量Ag、Au)为原料制备碲的一种工艺流程如下:
回答下列问题:
(1)类比CO2与NaOH的反应,写出“碱浸”时发生反应的化学方程式: NaOH+TeO2===Na2TeO3+H2O ,产物盐中Te元素的化合价是 +4 .
(2)滤液1中的两种溶质是H2SO4和 Na2SO4 (填化学式).
(3)上述工艺流程中设计“废渣→……→TeO2”的目的是 除去杂质,提纯二氧化碲 .
(4)“酸溶”后,在TeCl4溶液中通入SO2,反应生成碲和初中化学中两种常见的酸,则该反应的化学方程式是 TeCl4+2SO2+4H2O===Te↓+4HCl+2H2SO4 .
【化学用语检查站9】
1.写出下列常见碱的化学式,并按要求填空:
①氢氧化钠
②氢氧化钡
③氨水
④氢氧化钙
⑤氢氧化铜
⑥氢氧化铁
⑦氢氧化镁
其中属于可溶性碱的有
;微溶性碱
;难溶性碱
.(填序号)
2.写出下列反应的化学方程式,其中属于中和反应的是
.(填序号)
(1)生石灰溶于水:
.
(2)氢氧化钠在空气中变质:
.
(3)氢氧化钠溶液和硫酸:
.
(4)盐酸溶解氢氧化铜:
[基础巩固]
1.下列物质的分类,不正确的一组是(
)
A.H2O、MgO、H2CO3
都属于氧化物
B.HCl、H2SO3、H2SO4
都属于酸
C.NaOH、Ca(OH)2、Fe(OH)2
都属于碱
D.NaCl、Na2CO3、NaHCO3
都属于盐
2.如图是盐酸滴入NaOH溶液中,有关粒子之间反应的示意图.下列说法错误的是(
)
A.盐酸溶液中含有氢离子和氯离子
B.氢氧化钠溶液中含有钠离子和氢氧根离子
C.两种溶液混合时,氢离子与氢氧根离子结合生成了水分子
D.两种溶液混合时,钠离子与氯离子结合生成了氯化钠分子
3.醋酸(CH3COOH)是食醋的成分之一,其水溶液中存在H+和CH3COO-.下列说法正确的是(
)
A.醋酸属于氧化物
B.醋酸不能用于除铁锈
C.醋酸能与镁反应产生氢气
D.醋酸中碳元素的质量分数最大
4.(2020·重庆)某同学将一定量的Na2CO3与Ba(OH)2溶液混合,要想检验反应后Ba(OH)2是否过量,应选用的试剂是(
)
A.酚酞
B.CuCl2溶液
C.Na2CO3溶液
D.NaCl溶液
5.下列关于H2SO4性质描述中,不属于酸的通性的是(
)
A.使紫色石蕊溶液变红
B.与NaOH发生中和反应
C.浓硫酸滴到白纸上使纸变黑
D.与Mg反应放出氢气
6.下列除杂(括号内的是杂质)所选试剂合理的是(
)
A.Cu(Zn):稀盐酸
B.CO2气体(HCl):氢氧化钠溶液
C.CuO(Cu):浓硫酸
D.Ca(OH)2(CaCO3):稀盐酸
7.“见著知微”是化学学科的重要特点,它是通过对宏观现象的观察、思考、推理,建立起对微观粒子的认识.下列说法不正确的是(
)
A.品红在水中扩散,说明分子在不断地运动
B.电解水生成氢气和氧气,说明水是由氢分子和氧分子构成的
C.盐酸、稀硫酸具有相似的化学性质,说明它们的溶液中都含有氢离子
D.无色酚酞溶液滴入某稀溶液中显红色,说明该溶液中含有氢氧根离子
8.X是两种金属氧化物组成的混合物,为了研究混合物的成分,进行了如图所示的实验.
(1)X中含有的金属元素是
(填元素符号).
(2)写出X中一种成分与盐酸反应的化学方程式:
.
(3)若Y为固体,写出Y与X中一种成分反应的化学方程式
;若Y为气体,Y还可以是
(填化学式).
9.(广东经典)下图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种.
(1)写出乙和丙的化学式:乙
,丙
.
(2)写出下列化学方程式:
①甲和乙:
.
②丙和丁:
.
(3)图中反应①属于基本反应类型中的
反应,又称为
反应.
[能力提升]
10.小明同学归纳总结了初中所学稀硫酸的化学性质,并用“H2SO4+X→盐+Y”这种表达式进行整理.小明的下列观点错误的是(
)
选项
X的物质类别
观点描述
A
金属
若X为Cu,则反应能够发生
B
金属氧化物
若X为MgO,则Y为H2O
C
碱
若X为NaOH,则盐为Na2SO4
D
盐
若X为BaCl2,则生成白色沉淀
11.下列所示的四个图象,能正确反映对应变化关系的是
(
)
A
B
C
D
A.向一定量的硝酸铜和硝酸镁的混合溶液中加入铁粉
B.向pH=2的盐酸中加水稀释
C.向一定量的含有盐酸的氯化铜溶液中滴加氢氧化钠溶液
D.等质量的镁和铁分别与等质量、等浓度足量的稀硫酸反应
12.某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用A~H编号后,做如下实验.
(1)实验中观察到有气泡出现的试管是
(填字母,下同),有沉淀生成的试管是
.
(2)写出实验中无明显现象产生的试管中发生反应的化学方程式
.
(3)实验后某试管中为红色溶液,当向其中加入过量的
后,溶液变为蓝色.由此推断,该试管中最初盛有的物质是
.
(4)实验后某试管的底部有白色固体,过滤后向滤液中滴加盐酸,一段时间后有气泡冒出,则该滤液中的溶质是
.
13.(2020·广东模拟)碲(Te)广泛用于彩色玻璃和陶瓷工艺,难溶于水.用某工业废渣(主要含有TeO2、少量Ag、Au)为原料制备碲的一种工艺流程如下:
回答下列问题:
(1)类比CO2与NaOH的反应,写出“碱浸”时发生反应的化学方程式:
,产物盐中Te元素的化合价是
.
(2)滤液1中的两种溶质是H2SO4和
(填化学式).
(3)上述工艺流程中设计“废渣→……→TeO2”的目的是
.
(4)“酸溶”后,在TeCl4溶液中通入SO2,反应生成碲和初中化学中两种常见的酸,则该反应的化学方程式是
.
常见的酸和碱
【化学用语检查站9】
1.写出下列常见碱的化学式,并按要求填空:
①氢氧化钠 NaOH ②氢氧化钡 Ba(OH)2 ③氨水 NH3·H2O ④氢氧化钙 Ca(OH)2
⑤氢氧化铜 Cu(OH)2 ⑥氢氧化铁 Fe(OH)3 ⑦氢氧化镁 Mg(OH)2
其中属于可溶性碱的有 ①②③ ;微溶性碱 ④ ;难溶性碱 ⑤⑥⑦ .(填序号)
2.写出下列反应的化学方程式,其中属于中和反应的是 (3)(4) .(填序号)
(1)生石灰溶于水: CaO+H2O===Ca(OH)2 .
(2)氢氧化钠在空气中变质: 2NaOH+CO2===Na2CO3+H2O .
(3)氢氧化钠溶液和硫酸: 2NaOH+H2SO4===Na2SO4+2H2O .
(4)盐酸溶解氢氧化铜: 2HCl+Cu(OH)2===CuCl2+2H2O .
[基础巩固]
1.下列物质的分类,不正确的一组是( A )
A.H2O、MgO、H2CO3
都属于氧化物
B.HCl、H2SO3、H2SO4
都属于酸
C.NaOH、Ca(OH)2、Fe(OH)2
都属于碱
D.NaCl、Na2CO3、NaHCO3
都属于盐
2.如图是盐酸滴入NaOH溶液中,有关粒子之间反应的示意图.下列说法错误的是( D )
A.盐酸溶液中含有氢离子和氯离子
B.氢氧化钠溶液中含有钠离子和氢氧根离子
C.两种溶液混合时,氢离子与氢氧根离子结合生成了水分子
D.两种溶液混合时,钠离子与氯离子结合生成了氯化钠分子
3.醋酸(CH3COOH)是食醋的成分之一,其水溶液中存在H+和CH3COO-.下列说法正确的是( C )
A.醋酸属于氧化物
B.醋酸不能用于除铁锈
C.醋酸能与镁反应产生氢气
D.醋酸中碳元素的质量分数最大
4.(2020·重庆)某同学将一定量的Na2CO3与Ba(OH)2溶液混合,要想检验反应后Ba(OH)2是否过量,应选用的试剂是( C )
A.酚酞
B.CuCl2溶液
C.Na2CO3溶液
D.NaCl溶液
5.下列关于H2SO4性质描述中,不属于酸的通性的是( C )
A.使紫色石蕊溶液变红
B.与NaOH发生中和反应
C.浓硫酸滴到白纸上使纸变黑
D.与Mg反应放出氢气
6.下列除杂(括号内的是杂质)所选试剂合理的是( A )
A.Cu(Zn):稀盐酸
B.CO2气体(HCl):氢氧化钠溶液
C.CuO(Cu):浓硫酸
D.Ca(OH)2(CaCO3):稀盐酸
7.“见著知微”是化学学科的重要特点,它是通过对宏观现象的观察、思考、推理,建立起对微观粒子的认识.下列说法不正确的是( B )
A.品红在水中扩散,说明分子在不断地运动
B.电解水生成氢气和氧气,说明水是由氢分子和氧分子构成的
C.盐酸、稀硫酸具有相似的化学性质,说明它们的溶液中都含有氢离子
D.无色酚酞溶液滴入某稀溶液中显红色,说明该溶液中含有氢氧根离子
8.X是两种金属氧化物组成的混合物,为了研究混合物的成分,进行了如图所示的实验.
(1)X中含有的金属元素是 Fe,Cu (填元素符号).
(2)写出X中一种成分与盐酸反应的化学方程式: CuO+2HCl===CuCl2+H2O .
(3)若Y为固体,写出Y与X中一种成分反应的化学方程式 C+2CuO2Cu+CO2↑ ;若Y为气体,Y还可以是 CO (填化学式).
9.(广东经典)下图中每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种.
(1)写出乙和丙的化学式:乙 Na2CO3 ,丙 HCl .
(2)写出下列化学方程式:
①甲和乙: BaCl2+Na2CO3===BaCO3↓+2NaCl .
②丙和丁: 2HCl+Mg===MgCl2+H2↑ .
(3)图中反应①属于基本反应类型中的 复分解 反应,又称为 中和 反应.
[能力提升]
10.小明同学归纳总结了初中所学稀硫酸的化学性质,并用“H2SO4+X→盐+Y”这种表达式进行整理.小明的下列观点错误的是( A )
选项
X的物质类别
观点描述
A
金属
若X为Cu,则反应能够发生
B
金属氧化物
若X为MgO,则Y为H2O
C
碱
若X为NaOH,则盐为Na2SO4
D
盐
若X为BaCl2,则生成白色沉淀
11.下列所示的四个图象,能正确反映对应变化关系的是
( D )
A
B
C
D
A.向一定量的硝酸铜和硝酸镁的混合溶液中加入铁粉
B.向pH=2的盐酸中加水稀释
C.向一定量的含有盐酸的氯化铜溶液中滴加氢氧化钠溶液
D.等质量的镁和铁分别与等质量、等浓度足量的稀硫酸反应
12.某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用A~H编号后,做如下实验.
(1)实验中观察到有气泡出现的试管是 B、D (填字母,下同),有沉淀生成的试管是 G、H .
(2)写出实验中无明显现象产生的试管中发生反应的化学方程式 Ca(OH)2+2HCl===CaCl2+2H2O .
(3)实验后某试管中为红色溶液,当向其中加入过量的 NaOH溶液 后,溶液变为蓝色.由此推断,该试管中最初盛有的物质是 紫色石蕊溶液 .
(4)实验后某试管的底部有白色固体,过滤后向滤液中滴加盐酸,一段时间后有气泡冒出,则该滤液中的溶质是 NaOH和Na2CO3 .
13.(2020·广东模拟)碲(Te)广泛用于彩色玻璃和陶瓷工艺,难溶于水.用某工业废渣(主要含有TeO2、少量Ag、Au)为原料制备碲的一种工艺流程如下:
回答下列问题:
(1)类比CO2与NaOH的反应,写出“碱浸”时发生反应的化学方程式: NaOH+TeO2===Na2TeO3+H2O ,产物盐中Te元素的化合价是 +4 .
(2)滤液1中的两种溶质是H2SO4和 Na2SO4 (填化学式).
(3)上述工艺流程中设计“废渣→……→TeO2”的目的是 除去杂质,提纯二氧化碲 .
(4)“酸溶”后,在TeCl4溶液中通入SO2,反应生成碲和初中化学中两种常见的酸,则该反应的化学方程式是 TeCl4+2SO2+4H2O===Te↓+4HCl+2H2SO4 .
同课章节目录
