2021年人教版化学中考总复习专题训练 空气 导学案
文档属性
| 名称 | 2021年人教版化学中考总复习专题训练 空气 导学案 |

|
|
| 格式 | docx | ||
| 文件大小 | 245.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-05 00:00:00 | ||
图片预览


文档简介
空气、氧气
【化学用语检查站1】
写出下列反应的化学方程式:
(1)碳在氧气中燃烧:
.
(2)硫在氧气中燃烧:
.
(3)铁丝在氧气中燃烧:
.
(4)镁条在氧气中燃烧:
[基础巩固]
1.(2020·黑龙江)下列关于空气成分的说法错误的是(
)
A.氧气约占空气总体积4/5
B.稀有气体可制成多种用途的电光源,如霓虹灯
C.氮气充入食品包装中以防腐
D.二氧化碳在大气中含量不断上升,从而导致温室效应增强
2.在中央电视台发布的重点城市空气质量日报中可看到,造成空气污染的首要污染物是可吸入颗粒物和二氧化硫.下列对其形成主要原因的分析不合理的是(
)
A.环境绿化不好,粉尘随风飘扬
B.生活和生产中燃烧煤炭
C.工业生产排放废水
D.机动车排放尾气
3.(2020·广州)测定空气里氧气含量的实验装置和步骤如下:(已完成装置气密性检查)
①在集气瓶内加入少量水,并将水面上方空间分为5等份;
②用弹簧夹夹紧胶皮管;
③点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧,观察现象;
④红磷熄灭后,立即打开弹簧夹,观察现象.
其中有错误的实验步骤是(
)
A.①
B.②
C.③
D.④
4.下列有关空气及其成分的说法正确的是(
)
A.空气中体积分数最大的气体是氧气
B.鱼能在水中生存,说明氧气易溶于水
C.空气中可吸入颗粒物的多少不会影响人体健康
D.氮气的化学性质比较稳定,可以作保护气
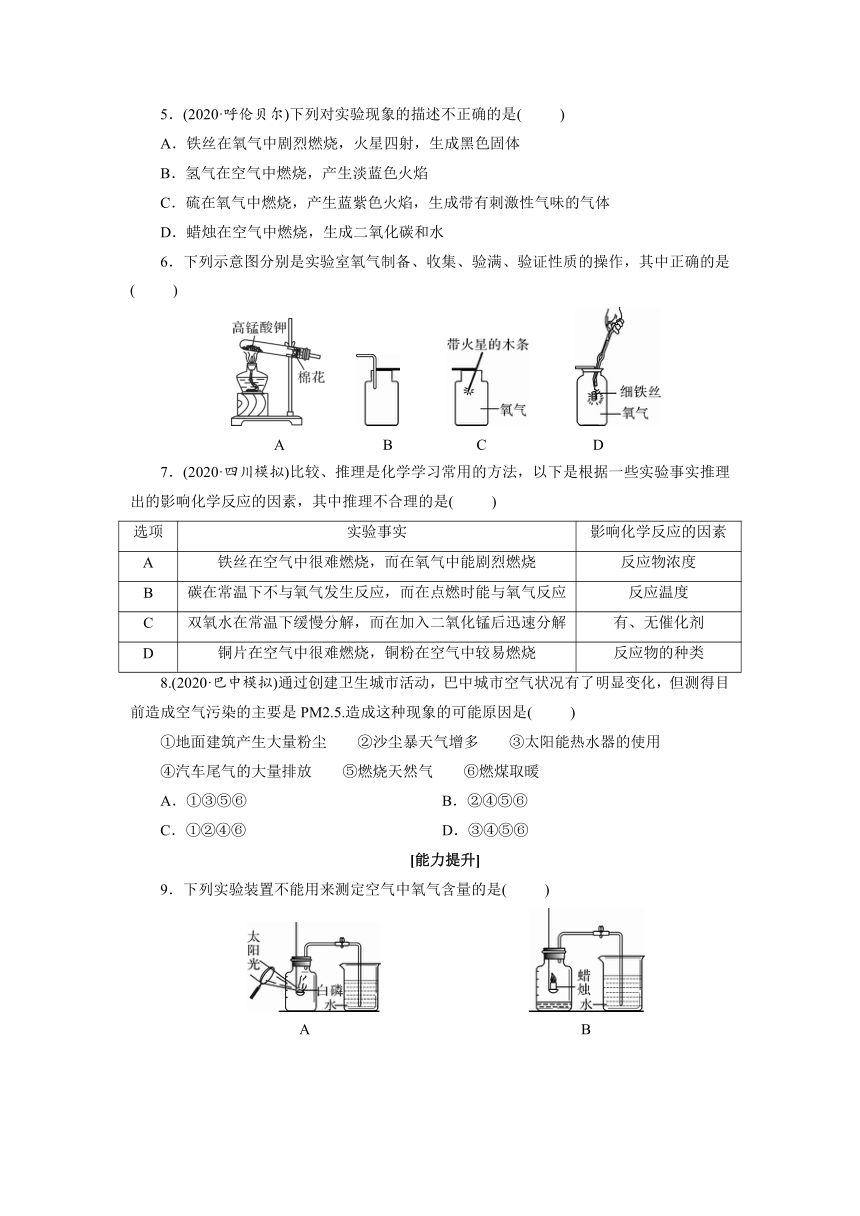
5.(2020·呼伦贝尔)下列对实验现象的描述不正确的是(
)
A.铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
B.氢气在空气中燃烧,产生淡蓝色火焰
C.硫在氧气中燃烧,产生蓝紫色火焰,生成带有刺激性气味的气体
D.蜡烛在空气中燃烧,生成二氧化碳和水
6.下列示意图分别是实验室氧气制备、收集、验满、验证性质的操作,其中正确的是(
)
A
B
C
D
7.(2020·四川模拟)比较、推理是化学学习常用的方法,以下是根据一些实验事实推理出的影响化学反应的因素,其中推理不合理的是(
)
选项
实验事实
影响化学反应的因素
A
铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧
反应物浓度
B
碳在常温下不与氧气发生反应,而在点燃时能与氧气反应
反应温度
C
双氧水在常温下缓慢分解,而在加入二氧化锰后迅速分解
有、无催化剂
D
铜片在空气中很难燃烧,铜粉在空气中较易燃烧
反应物的种类
8.(2020·巴中模拟)通过创建卫生城市活动,巴中城市空气状况有了明显变化,但测得目前造成空气污染的主要是PM2.5.造成这种现象的可能原因是(
)
①地面建筑产生大量粉尘 ②沙尘暴天气增多 ③太阳能热水器的使用
④汽车尾气的大量排放 ⑤燃烧天然气 ⑥燃煤取暖
A.①③⑤⑥
B.②④⑤⑥
C.①②④⑥
D.③④⑤⑥
[能力提升]
9.下列实验装置不能用来测定空气中氧气含量的是(
)
A
B
C
D
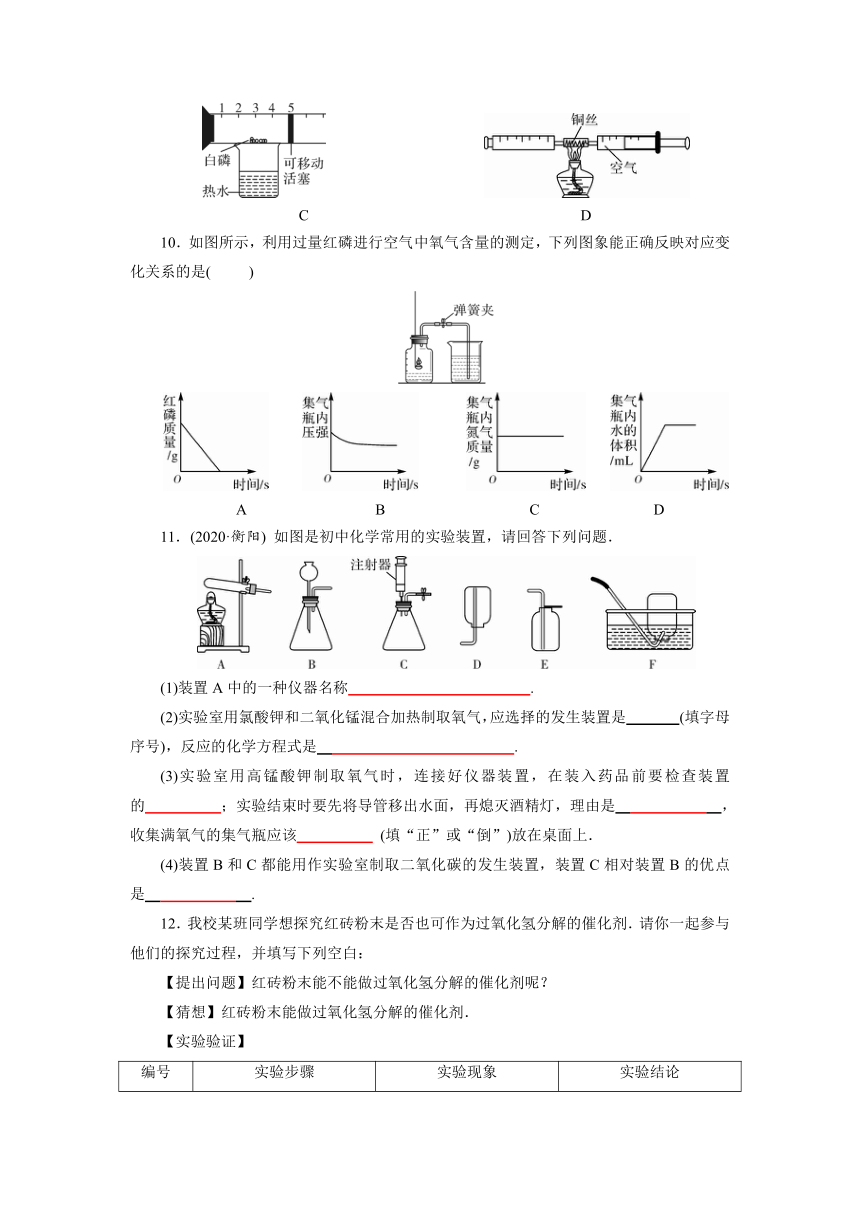
10.如图所示,利用过量红磷进行空气中氧气含量的测定,下列图象能正确反映对应变化关系的是(
)
A
B
C
D
11.(2020·衡阳)
如图是初中化学常用的实验装置,请回答下列问题.
(1)装置A中的一种仪器名称
.
(2)实验室用氯酸钾和二氧化锰混合加热制取氧气,应选择的发生装置是
(填字母序号),反应的化学方程式是
.
(3)实验室用高锰酸钾制取氧气时,连接好仪器装置,在装入药品前要检查装置的
;实验结束时要先将导管移出水面,再熄灭酒精灯,理由是
,收集满氧气的集气瓶应该
(填“正”或“倒”)放在桌面上.
(4)装置B和C都能用作实验室制取二氧化碳的发生装置,装置C相对装置B的优点是
.
12.我校某班同学想探究红砖粉末是否也可作为过氧化氢分解的催化剂.请你一起参与他们的探究过程,并填写下列空白:
【提出问题】红砖粉末能不能做过氧化氢分解的催化剂呢?
【猜想】红砖粉末能做过氧化氢分解的催化剂.
【实验验证】
编号
实验步骤
实验现象
实验结论
实验一
木条不复燃
常温下过氧化氢分解放出氧气速率很慢
实验二
在装有过氧化氢的试管中加入红砖粉末,然后将带火星的木条伸入试管中
大量气泡产生,木条复燃
【结论】红砖粉末能做过氧化氢的催化剂.写出反应的化学方程式
;实验一和实验二所起的作用是
.
【讨论与反思】有同学认为:仅凭上述两个实验还不能证明红砖粉末能做过氧化氢的催化剂,还需要增加一个探究实验.
实验三:
【实验目的】探究
.
【实验步骤】
①准确称量红砖粉末的质量.
②完成实验二.
③待反应结束,将实验二试管中的物质进行过滤、洗涤、干燥、
.
④对比反应前后红砖粉末的质量.
【分析】如果红砖粉末反应前后的质量不变,则说明红砖粉末可以作为过氧化氢的催化剂.
【反思】但也有同学认为:要证明猜想,上述三个实验还是不够,还需要再补充一个探究实验.你认为还需要探究
.
13.(2020·中山模拟)根据下列实验装置图回答问题:
(1)利用高锰酸钾制取较为纯净的氧气应选用的装置是
(填编号),反应的符号表达式为
.
(2)双氧水制氧气选用的发生装置是
,反应的符号表达式为
.
(3)用C装置收集氧气时,
最宜收集氧气,当观察到
时,证明氧气已经集满.
(4)氢气是目前已知的气体中最轻的气体且不溶于水,利用金属锌和稀盐酸溶液在常温下反应即可制得,判断制取氢气的发生装置应选
.如果用右图装置进行排空气法收集氢气,氢气应从
(填“a”或“b”,下同)导管端通入.如果用右图装置进行排水法收集氢气,则氢气应从
导管端通入.
(5)空气中氧气含量测定的装置如图F所示.下列有关说法正确的是
(填字母).
A.燃烧匙中的红磷越多,水位上升越高
B.燃烧匙中的红磷不可以换成硫或铁
C.选用红磷是因为反应可以耗尽氧气,生成固态的P2O5
D.本实验可以证明空气含有N2、O2、CO2和稀有气体
空气、氧气
【化学用语检查站1】
写出下列反应的化学方程式:
(1)碳在氧气中燃烧: C+O2CO2 .
(2)硫在氧气中燃烧: S+O2SO2 .
(3)铁丝在氧气中燃烧: 3Fe+2O2Fe3O4 .
(4)镁条在氧气中燃烧: 2Mg+O22MgO .
[基础巩固]
1.(2020·黑龙江)下列关于空气成分的说法错误的是( A )
A.氧气约占空气总体积4/5
B.稀有气体可制成多种用途的电光源,如霓虹灯
C.氮气充入食品包装中以防腐
D.二氧化碳在大气中含量不断上升,从而导致温室效应增强
2.在中央电视台发布的重点城市空气质量日报中可看到,造成空气污染的首要污染物是可吸入颗粒物和二氧化硫.下列对其形成主要原因的分析不合理的是( C )
A.环境绿化不好,粉尘随风飘扬
B.生活和生产中燃烧煤炭
C.工业生产排放废水
D.机动车排放尾气
3.(2020·广州)测定空气里氧气含量的实验装置和步骤如下:(已完成装置气密性检查)
①在集气瓶内加入少量水,并将水面上方空间分为5等份;
②用弹簧夹夹紧胶皮管;
③点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧,观察现象;
④红磷熄灭后,立即打开弹簧夹,观察现象.
其中有错误的实验步骤是( D )
A.①
B.②
C.③
D.④
4.下列有关空气及其成分的说法正确的是( D )
A.空气中体积分数最大的气体是氧气
B.鱼能在水中生存,说明氧气易溶于水
C.空气中可吸入颗粒物的多少不会影响人体健康
D.氮气的化学性质比较稳定,可以作保护气
5.(2020·呼伦贝尔)下列对实验现象的描述不正确的是( D )
A.铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
B.氢气在空气中燃烧,产生淡蓝色火焰
C.硫在氧气中燃烧,产生蓝紫色火焰,生成带有刺激性气味的气体
D.蜡烛在空气中燃烧,生成二氧化碳和水
6.下列示意图分别是实验室氧气制备、收集、验满、验证性质的操作,其中正确的是( A )
A
B
C
D
7.(2020·四川模拟)比较、推理是化学学习常用的方法,以下是根据一些实验事实推理出的影响化学反应的因素,其中推理不合理的是( D )
选项
实验事实
影响化学反应的因素
A
铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧
反应物浓度
B
碳在常温下不与氧气发生反应,而在点燃时能与氧气反应
反应温度
C
双氧水在常温下缓慢分解,而在加入二氧化锰后迅速分解
有、无催化剂
D
铜片在空气中很难燃烧,铜粉在空气中较易燃烧
反应物的种类
8.(2020·巴中模拟)通过创建卫生城市活动,巴中城市空气状况有了明显变化,但测得目前造成空气污染的主要是PM2.5.造成这种现象的可能原因是( C )
①地面建筑产生大量粉尘 ②沙尘暴天气增多 ③太阳能热水器的使用
④汽车尾气的大量排放 ⑤燃烧天然气 ⑥燃煤取暖
A.①③⑤⑥
B.②④⑤⑥
C.①②④⑥
D.③④⑤⑥
[能力提升]
9.下列实验装置不能用来测定空气中氧气含量的是( B )
A
B
C
D
10.如图所示,利用过量红磷进行空气中氧气含量的测定,下列图象能正确反映对应变化关系的是( C )
A
B
C
D
11.(2020·衡阳)
如图是初中化学常用的实验装置,请回答下列问题.
(1)装置A中的一种仪器名称 酒精灯(或试管、铁架台) .
(2)实验室用氯酸钾和二氧化锰混合加热制取氧气,应选择的发生装置是 A (填字母序号),反应的化学方程式是 2KClO32KCl+3O2↑ .
(3)实验室用高锰酸钾制取氧气时,连接好仪器装置,在装入药品前要检查装置的 气密性 ;实验结束时要先将导管移出水面,再熄灭酒精灯,理由是 防止水倒流,炸裂试管 ,收集满氧气的集气瓶应该 正 (填“正”或“倒”)放在桌面上.
(4)装置B和C都能用作实验室制取二氧化碳的发生装置,装置C相对装置B的优点是 可以控制反应速率 .
12.我校某班同学想探究红砖粉末是否也可作为过氧化氢分解的催化剂.请你一起参与他们的探究过程,并填写下列空白:
【提出问题】红砖粉末能不能做过氧化氢分解的催化剂呢?
【猜想】红砖粉末能做过氧化氢分解的催化剂.
【实验验证】
编号
实验步骤
实验现象
实验结论
实验一
将带火星的木条伸入装有过氧化氢的试管中
木条不复燃
常温下过氧化氢分解放出氧气速率很慢
实验二
在装有过氧化氢的试管中加入红砖粉末,然后将带火星的木条伸入试管中
大量气泡产生,木条复燃
红砖粉末加速了过氧化氢分解的速率
【结论】红砖粉末能做过氧化氢的催化剂.写出反应的化学方程式 2H2O22H2O+O2↑ ;实验一和实验二所起的作用是 对比 .
【讨论与反思】有同学认为:仅凭上述两个实验还不能证明红砖粉末能做过氧化氢的催化剂,还需要增加一个探究实验.
实验三:
【实验目的】探究 红砖粉末反应前后的质量是否不变 .
【实验步骤】
①准确称量红砖粉末的质量.
②完成实验二.
③待反应结束,将实验二试管中的物质进行过滤、洗涤、干燥、 称量 .
④对比反应前后红砖粉末的质量.
【分析】如果红砖粉末反应前后的质量不变,则说明红砖粉末可以作为过氧化氢的催化剂.
【反思】但也有同学认为:要证明猜想,上述三个实验还是不够,还需要再补充一个探究实验.你认为还需要探究 红砖粉末能否继续加速过氧化氢的分解速率 .
13.(2020·中山模拟)根据下列实验装置图回答问题:
(1)利用高锰酸钾制取较为纯净的氧气应选用的装置是 AC (填编号),反应的符号表达式为 2KMnO4K2MnO4+MnO2+O2↑ .
(2)双氧水制氧气选用的发生装置是 B ,反应的符号表达式为 2H2O22H2O+O2↑ .
(3)用C装置收集氧气时, 当气泡连续均匀冒出时 最宜收集氧气,当观察到 瓶口有大量气泡冒出 时,证明氧气已经集满.
(4)氢气是目前已知的气体中最轻的气体且不溶于水,利用金属锌和稀盐酸溶液在常温下反应即可制得,判断制取氢气的发生装置应选
B .如果用右图装置进行排空气法收集氢气,氢气应从 a (填“a”或“b”,下同)导管端通入.如果用右图装置进行排水法收集氢气,则氢气应从 a 导管端通入.
(5)空气中氧气含量测定的装置如图F所示.下列有关说法正确的是 BC (填字母).
A.燃烧匙中的红磷越多,水位上升越高
B.燃烧匙中的红磷不可以换成硫或铁
C.选用红磷是因为反应可以耗尽氧气,生成固态的P2O5
D.本实验可以证明空气含有N2、O2、CO2和稀有气体
【化学用语检查站1】
写出下列反应的化学方程式:
(1)碳在氧气中燃烧:
.
(2)硫在氧气中燃烧:
.
(3)铁丝在氧气中燃烧:
.
(4)镁条在氧气中燃烧:
[基础巩固]
1.(2020·黑龙江)下列关于空气成分的说法错误的是(
)
A.氧气约占空气总体积4/5
B.稀有气体可制成多种用途的电光源,如霓虹灯
C.氮气充入食品包装中以防腐
D.二氧化碳在大气中含量不断上升,从而导致温室效应增强
2.在中央电视台发布的重点城市空气质量日报中可看到,造成空气污染的首要污染物是可吸入颗粒物和二氧化硫.下列对其形成主要原因的分析不合理的是(
)
A.环境绿化不好,粉尘随风飘扬
B.生活和生产中燃烧煤炭
C.工业生产排放废水
D.机动车排放尾气
3.(2020·广州)测定空气里氧气含量的实验装置和步骤如下:(已完成装置气密性检查)
①在集气瓶内加入少量水,并将水面上方空间分为5等份;
②用弹簧夹夹紧胶皮管;
③点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧,观察现象;
④红磷熄灭后,立即打开弹簧夹,观察现象.
其中有错误的实验步骤是(
)
A.①
B.②
C.③
D.④
4.下列有关空气及其成分的说法正确的是(
)
A.空气中体积分数最大的气体是氧气
B.鱼能在水中生存,说明氧气易溶于水
C.空气中可吸入颗粒物的多少不会影响人体健康
D.氮气的化学性质比较稳定,可以作保护气
5.(2020·呼伦贝尔)下列对实验现象的描述不正确的是(
)
A.铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
B.氢气在空气中燃烧,产生淡蓝色火焰
C.硫在氧气中燃烧,产生蓝紫色火焰,生成带有刺激性气味的气体
D.蜡烛在空气中燃烧,生成二氧化碳和水
6.下列示意图分别是实验室氧气制备、收集、验满、验证性质的操作,其中正确的是(
)
A
B
C
D
7.(2020·四川模拟)比较、推理是化学学习常用的方法,以下是根据一些实验事实推理出的影响化学反应的因素,其中推理不合理的是(
)
选项
实验事实
影响化学反应的因素
A
铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧
反应物浓度
B
碳在常温下不与氧气发生反应,而在点燃时能与氧气反应
反应温度
C
双氧水在常温下缓慢分解,而在加入二氧化锰后迅速分解
有、无催化剂
D
铜片在空气中很难燃烧,铜粉在空气中较易燃烧
反应物的种类
8.(2020·巴中模拟)通过创建卫生城市活动,巴中城市空气状况有了明显变化,但测得目前造成空气污染的主要是PM2.5.造成这种现象的可能原因是(
)
①地面建筑产生大量粉尘 ②沙尘暴天气增多 ③太阳能热水器的使用
④汽车尾气的大量排放 ⑤燃烧天然气 ⑥燃煤取暖
A.①③⑤⑥
B.②④⑤⑥
C.①②④⑥
D.③④⑤⑥
[能力提升]
9.下列实验装置不能用来测定空气中氧气含量的是(
)
A
B
C
D
10.如图所示,利用过量红磷进行空气中氧气含量的测定,下列图象能正确反映对应变化关系的是(
)
A
B
C
D
11.(2020·衡阳)
如图是初中化学常用的实验装置,请回答下列问题.
(1)装置A中的一种仪器名称
.
(2)实验室用氯酸钾和二氧化锰混合加热制取氧气,应选择的发生装置是
(填字母序号),反应的化学方程式是
.
(3)实验室用高锰酸钾制取氧气时,连接好仪器装置,在装入药品前要检查装置的
;实验结束时要先将导管移出水面,再熄灭酒精灯,理由是
,收集满氧气的集气瓶应该
(填“正”或“倒”)放在桌面上.
(4)装置B和C都能用作实验室制取二氧化碳的发生装置,装置C相对装置B的优点是
.
12.我校某班同学想探究红砖粉末是否也可作为过氧化氢分解的催化剂.请你一起参与他们的探究过程,并填写下列空白:
【提出问题】红砖粉末能不能做过氧化氢分解的催化剂呢?
【猜想】红砖粉末能做过氧化氢分解的催化剂.
【实验验证】
编号
实验步骤
实验现象
实验结论
实验一
木条不复燃
常温下过氧化氢分解放出氧气速率很慢
实验二
在装有过氧化氢的试管中加入红砖粉末,然后将带火星的木条伸入试管中
大量气泡产生,木条复燃
【结论】红砖粉末能做过氧化氢的催化剂.写出反应的化学方程式
;实验一和实验二所起的作用是
.
【讨论与反思】有同学认为:仅凭上述两个实验还不能证明红砖粉末能做过氧化氢的催化剂,还需要增加一个探究实验.
实验三:
【实验目的】探究
.
【实验步骤】
①准确称量红砖粉末的质量.
②完成实验二.
③待反应结束,将实验二试管中的物质进行过滤、洗涤、干燥、
.
④对比反应前后红砖粉末的质量.
【分析】如果红砖粉末反应前后的质量不变,则说明红砖粉末可以作为过氧化氢的催化剂.
【反思】但也有同学认为:要证明猜想,上述三个实验还是不够,还需要再补充一个探究实验.你认为还需要探究
.
13.(2020·中山模拟)根据下列实验装置图回答问题:
(1)利用高锰酸钾制取较为纯净的氧气应选用的装置是
(填编号),反应的符号表达式为
.
(2)双氧水制氧气选用的发生装置是
,反应的符号表达式为
.
(3)用C装置收集氧气时,
最宜收集氧气,当观察到
时,证明氧气已经集满.
(4)氢气是目前已知的气体中最轻的气体且不溶于水,利用金属锌和稀盐酸溶液在常温下反应即可制得,判断制取氢气的发生装置应选
.如果用右图装置进行排空气法收集氢气,氢气应从
(填“a”或“b”,下同)导管端通入.如果用右图装置进行排水法收集氢气,则氢气应从
导管端通入.
(5)空气中氧气含量测定的装置如图F所示.下列有关说法正确的是
(填字母).
A.燃烧匙中的红磷越多,水位上升越高
B.燃烧匙中的红磷不可以换成硫或铁
C.选用红磷是因为反应可以耗尽氧气,生成固态的P2O5
D.本实验可以证明空气含有N2、O2、CO2和稀有气体
空气、氧气
【化学用语检查站1】
写出下列反应的化学方程式:
(1)碳在氧气中燃烧: C+O2CO2 .
(2)硫在氧气中燃烧: S+O2SO2 .
(3)铁丝在氧气中燃烧: 3Fe+2O2Fe3O4 .
(4)镁条在氧气中燃烧: 2Mg+O22MgO .
[基础巩固]
1.(2020·黑龙江)下列关于空气成分的说法错误的是( A )
A.氧气约占空气总体积4/5
B.稀有气体可制成多种用途的电光源,如霓虹灯
C.氮气充入食品包装中以防腐
D.二氧化碳在大气中含量不断上升,从而导致温室效应增强
2.在中央电视台发布的重点城市空气质量日报中可看到,造成空气污染的首要污染物是可吸入颗粒物和二氧化硫.下列对其形成主要原因的分析不合理的是( C )
A.环境绿化不好,粉尘随风飘扬
B.生活和生产中燃烧煤炭
C.工业生产排放废水
D.机动车排放尾气
3.(2020·广州)测定空气里氧气含量的实验装置和步骤如下:(已完成装置气密性检查)
①在集气瓶内加入少量水,并将水面上方空间分为5等份;
②用弹簧夹夹紧胶皮管;
③点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧,观察现象;
④红磷熄灭后,立即打开弹簧夹,观察现象.
其中有错误的实验步骤是( D )
A.①
B.②
C.③
D.④
4.下列有关空气及其成分的说法正确的是( D )
A.空气中体积分数最大的气体是氧气
B.鱼能在水中生存,说明氧气易溶于水
C.空气中可吸入颗粒物的多少不会影响人体健康
D.氮气的化学性质比较稳定,可以作保护气
5.(2020·呼伦贝尔)下列对实验现象的描述不正确的是( D )
A.铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
B.氢气在空气中燃烧,产生淡蓝色火焰
C.硫在氧气中燃烧,产生蓝紫色火焰,生成带有刺激性气味的气体
D.蜡烛在空气中燃烧,生成二氧化碳和水
6.下列示意图分别是实验室氧气制备、收集、验满、验证性质的操作,其中正确的是( A )
A
B
C
D
7.(2020·四川模拟)比较、推理是化学学习常用的方法,以下是根据一些实验事实推理出的影响化学反应的因素,其中推理不合理的是( D )
选项
实验事实
影响化学反应的因素
A
铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧
反应物浓度
B
碳在常温下不与氧气发生反应,而在点燃时能与氧气反应
反应温度
C
双氧水在常温下缓慢分解,而在加入二氧化锰后迅速分解
有、无催化剂
D
铜片在空气中很难燃烧,铜粉在空气中较易燃烧
反应物的种类
8.(2020·巴中模拟)通过创建卫生城市活动,巴中城市空气状况有了明显变化,但测得目前造成空气污染的主要是PM2.5.造成这种现象的可能原因是( C )
①地面建筑产生大量粉尘 ②沙尘暴天气增多 ③太阳能热水器的使用
④汽车尾气的大量排放 ⑤燃烧天然气 ⑥燃煤取暖
A.①③⑤⑥
B.②④⑤⑥
C.①②④⑥
D.③④⑤⑥
[能力提升]
9.下列实验装置不能用来测定空气中氧气含量的是( B )
A
B
C
D
10.如图所示,利用过量红磷进行空气中氧气含量的测定,下列图象能正确反映对应变化关系的是( C )
A
B
C
D
11.(2020·衡阳)
如图是初中化学常用的实验装置,请回答下列问题.
(1)装置A中的一种仪器名称 酒精灯(或试管、铁架台) .
(2)实验室用氯酸钾和二氧化锰混合加热制取氧气,应选择的发生装置是 A (填字母序号),反应的化学方程式是 2KClO32KCl+3O2↑ .
(3)实验室用高锰酸钾制取氧气时,连接好仪器装置,在装入药品前要检查装置的 气密性 ;实验结束时要先将导管移出水面,再熄灭酒精灯,理由是 防止水倒流,炸裂试管 ,收集满氧气的集气瓶应该 正 (填“正”或“倒”)放在桌面上.
(4)装置B和C都能用作实验室制取二氧化碳的发生装置,装置C相对装置B的优点是 可以控制反应速率 .
12.我校某班同学想探究红砖粉末是否也可作为过氧化氢分解的催化剂.请你一起参与他们的探究过程,并填写下列空白:
【提出问题】红砖粉末能不能做过氧化氢分解的催化剂呢?
【猜想】红砖粉末能做过氧化氢分解的催化剂.
【实验验证】
编号
实验步骤
实验现象
实验结论
实验一
将带火星的木条伸入装有过氧化氢的试管中
木条不复燃
常温下过氧化氢分解放出氧气速率很慢
实验二
在装有过氧化氢的试管中加入红砖粉末,然后将带火星的木条伸入试管中
大量气泡产生,木条复燃
红砖粉末加速了过氧化氢分解的速率
【结论】红砖粉末能做过氧化氢的催化剂.写出反应的化学方程式 2H2O22H2O+O2↑ ;实验一和实验二所起的作用是 对比 .
【讨论与反思】有同学认为:仅凭上述两个实验还不能证明红砖粉末能做过氧化氢的催化剂,还需要增加一个探究实验.
实验三:
【实验目的】探究 红砖粉末反应前后的质量是否不变 .
【实验步骤】
①准确称量红砖粉末的质量.
②完成实验二.
③待反应结束,将实验二试管中的物质进行过滤、洗涤、干燥、 称量 .
④对比反应前后红砖粉末的质量.
【分析】如果红砖粉末反应前后的质量不变,则说明红砖粉末可以作为过氧化氢的催化剂.
【反思】但也有同学认为:要证明猜想,上述三个实验还是不够,还需要再补充一个探究实验.你认为还需要探究 红砖粉末能否继续加速过氧化氢的分解速率 .
13.(2020·中山模拟)根据下列实验装置图回答问题:
(1)利用高锰酸钾制取较为纯净的氧气应选用的装置是 AC (填编号),反应的符号表达式为 2KMnO4K2MnO4+MnO2+O2↑ .
(2)双氧水制氧气选用的发生装置是 B ,反应的符号表达式为 2H2O22H2O+O2↑ .
(3)用C装置收集氧气时, 当气泡连续均匀冒出时 最宜收集氧气,当观察到 瓶口有大量气泡冒出 时,证明氧气已经集满.
(4)氢气是目前已知的气体中最轻的气体且不溶于水,利用金属锌和稀盐酸溶液在常温下反应即可制得,判断制取氢气的发生装置应选
B .如果用右图装置进行排空气法收集氢气,氢气应从 a (填“a”或“b”,下同)导管端通入.如果用右图装置进行排水法收集氢气,则氢气应从 a 导管端通入.
(5)空气中氧气含量测定的装置如图F所示.下列有关说法正确的是 BC (填字母).
A.燃烧匙中的红磷越多,水位上升越高
B.燃烧匙中的红磷不可以换成硫或铁
C.选用红磷是因为反应可以耗尽氧气,生成固态的P2O5
D.本实验可以证明空气含有N2、O2、CO2和稀有气体
同课章节目录
