2020-2021学年高二化学人教版选修五第三章《烃的含氧衍生物》测试题(含答案)
文档属性
| 名称 | 2020-2021学年高二化学人教版选修五第三章《烃的含氧衍生物》测试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 309.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-07 00:00:00 | ||
图片预览



文档简介
第三章《烃的含氧衍生物》测试题
一、单选题
1.下列实验过程中需要水浴加热的是( )
A.由乙醇制乙烯 B.乙酸乙酯的制取
C.甲醛的银镜反应 D.苯酚与浓溴水的反应
2.提纯下列物质(括号中为杂质),所选除杂试剂和分离方法都正确的是
选项
被提纯的物质(杂质)
除杂试剂
分离方法
A
乙烯(二氧化硫)
酸性KMnO4溶液
洗气
B
乙酸乙酯(乙醇)
饱和Na2CO3溶液
蒸馏
C
苯(苯酚)
浓溴水
过滤
D
苯甲酸(NaCl)
-----
重结晶
A.A B.B C.C D.D
3.84消毒液()、甲醛()、过氧乙酸()、均可用于杀菌消毒下列说法错误的是( )
A.84消毒液和洁厕灵混合使用效果更好
B.甲醛水溶液可用于浸泡生物标本
C.过氧乙酸()配制过程中应佩戴橡胶手套
D.与空气中的和作用形成
4.下列说法正确的是
A.煤的液化、气化是物理变化,煤的干馏是化学变化
B.蛋白质、淀粉、纤维素、油脂均属于高分子化合物
C.乙酸乙酯在碱性条件下的水解反应属于皂化反应
D.石油裂化的目的是为了提高汽油等轻质液态油的产量和质量
5.学习化学应有辩证的观点和方法.下列说法正确的是( )
A.催化剂不参加化学反应
B.醇和酸反应的产物未必是酯
C.卤代烃的水解产物一定是醇
D.醇脱水的反应都属于消去反应
6.下列叙述中不正确的是
A.乙烯可作水果的催熟剂
B.福尔马林可用来保存海参等海鲜产品
C.苯酚可用来消毒杀菌
D.通过石油的催化裂化及裂解可以得到轻质油和气态烯烃
7.茶多酚是一类目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂的总称。其中没食子儿茶素(EGC)的结构如图所示。关于EGC的下列叙述中正确的是
A.EGC是一种芳香烃
B.1molEGC与4molNaOH恰好完全反应
C.遇FeCl3溶液能不发生显色反应
D.易发生氧化反应和取代反应,相对较难发生加成反应
8.达菲是治疗流感的重要药物,M是合成达菲的重要中间体,下列说法错误的是
A.化合物M分子式为C16H27O5N B.化合物M能发生消去反应、加聚反应
C.化合物M能使酸性高锰酸钾溶液褪色 D.化合物M有4种不同的官能团
9.属于醇的同分异构体有
A.3种 B.4种 C.5种 D.6种
10.核黄素又称维生素B,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳。核黄素分子的结构为:
有关核黄素的下列说法中,正确的是
A.该物质属于有机高分子
B.不能发生酯化反应
C.不能与氢气发生加成反应
D.酸性条件下加热水解,有CO2生成
11.下列实验操作正确且能达到预期目的的是( )
实验目的
操作
A
欲证明CH2=CHCHO中含有碳碳双键
滴入酸性KMnO4溶液
B
欲除去苯中混有的少量苯酚
向混合液中加入浓溴水,充分反应后,过滤
C
证明SO2具有漂白性
将SO2通入酸性KMnO4溶液中
D
确定碳和硅两元素非金属性强弱
测同温同浓度Na2CO3和Na2SiO3水溶液的pH
A.A B.B C.C D.D
12.双羟香豆素医学上用作抗凝剂,其结构如右图。下列有关双羟香豆素的说法正确的是
A.分子式为C19H10O6
B.遇FeCl3溶液能发生显色反应
C.1 mol双羟香豆素最多能与含 4 mol氢氧化钠的水溶液完全反应
D.1 mol双羟香豆素最多能与 10 mol氢气发生加成反应
13.下列有关用水杨酸和乙酸酐制备阿司匹林(乙酰水杨酸)的说法中不正确的是( )
A.制备阿司匹林的反应属于取代反应
B.待反应结束后向锥形瓶中加水,冰水浴中冷却结晶,减压过滤,用少量冷水淋洗锥形瓶收集所有晶体
C.粗产品中常混有聚合物杂质,可利用溶液溶解、过滤、洗涤、盐酸酸化、结晶等操作进行精制
D.可用溶液检验阿司匹林中是否含有未反应完的水杨酸
14.下列4个化学反应中,与其他3个反应类型不同的是( )
A.CH3CHO+2Cu(OH)2CH3COOH+Cu2O↓+2H2O
B.CH3CH2OH+CuOCH3CHO+Cu+H2O
C.2CH2===CH2+O22CH3CHO
D.CH3CH2OH+HBr―→CH3CH2Br+H2O
15.环己醇,丙酮和乙醛混合物1.75g,完全燃烧后,所得气体通过P2O5吸收瓶,瓶增重1.8g,则混合物的平均相对分子质量为( )
A.68 B.75 C.80 D.87.5
二、填空题
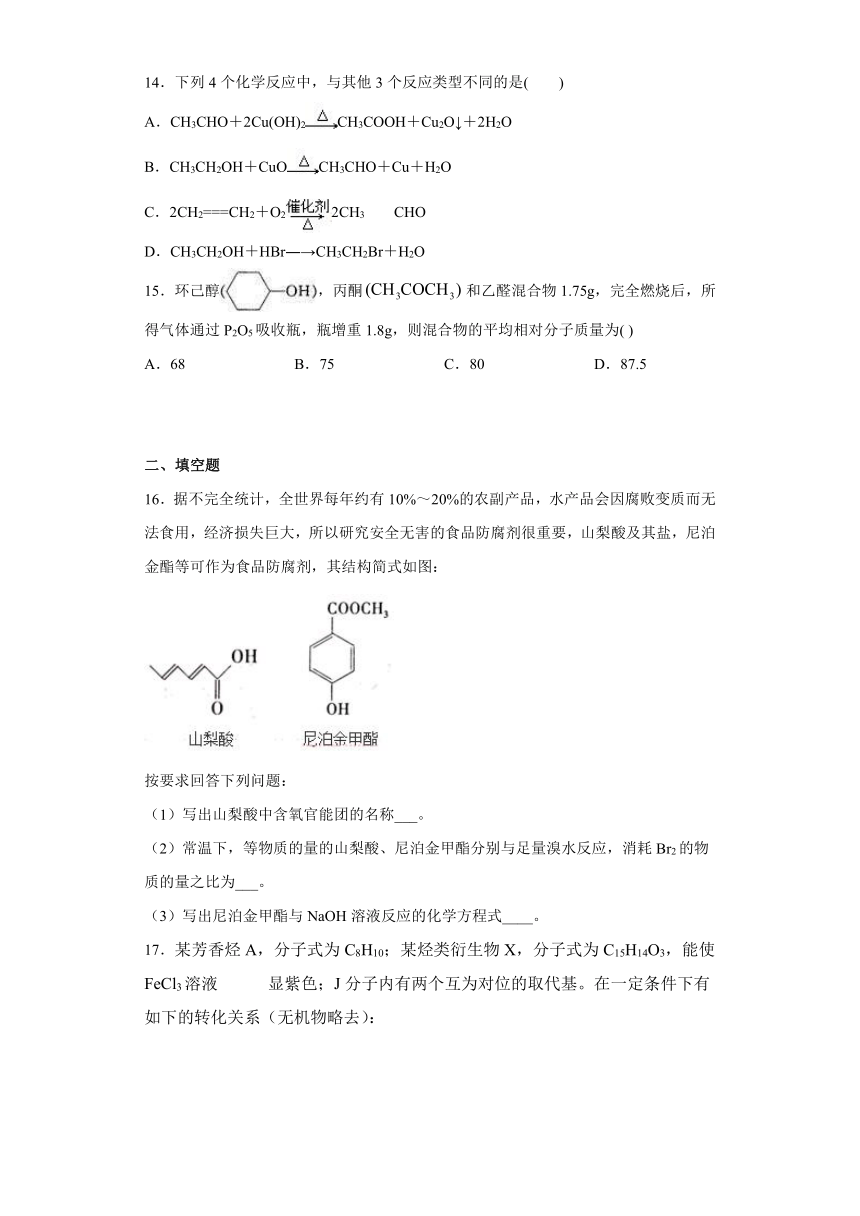
16.据不完全统计,全世界每年约有10%~20%的农副产品,水产品会因腐败变质而无法食用,经济损失巨大,所以研究安全无害的食品防腐剂很重要,山梨酸及其盐,尼泊金酯等可作为食品防腐剂,其结构简式如图:
按要求回答下列问题:
(1)写出山梨酸中含氧官能团的名称___。
(2)常温下,等物质的量的山梨酸、尼泊金甲酯分别与足量溴水反应,消耗Br2的物质的量之比为___。
(3)写出尼泊金甲酯与NaOH溶液反应的化学方程式____。
17.某芳香烃A,分子式为C8H10;某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液 显紫色;J分子内有两个互为对位的取代基。在一定条件下有如下的转化关系(无机物略去):
(1)属于芳香烃类的A的同分异构体(不包括A)中,在同一平面的原子最多有__________个;
(2)J中所含的含氧官能团的名称为__________。
(3)E与H反应的化学方程式是____________________________________;
(4)B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物M,以M为单体合成的高分子化合物的名称是_________________________。
(5)已知J有多种同分异构体,写出一种符合下列性质的J的同分异构体的结构简式。①与FeCl3溶液作用显紫色;②与新制Cu(OH)2悬浊液作用产生红色沉淀;③苯环上的一卤代物有2种。
______________________________________________
18.乙基香兰素是最重要的合成香料之一,常作为婴幼儿奶粉的添加剂。制备乙基香兰素的一种合成路线(部分反应条件略去)如下图所示:
已知:①R-ONa+R′-Br-→R-O-R′+NaBr
②Ⅲ中生成的Cu2O经氧化后可以循环利用
回答下列问题:
(1)A的核磁共振氢谱有3组峰.A的结构简式为______________________;
(2)Ⅰ中可能生成的一种烃是_________(填名称);催化剂PEG可看作乙二醇脱水缩聚的产物,PEG的结构简式为___________;若PEG的平均相对分子质量为17618,则其平均聚合度约为________;
(3)Ⅱ中,发生的反应属于____________(填反应类型);
(4)Ⅳ中,有机物脱去的官能团是______________________(填名称);
(5)D是乙基香兰素的同分异构体,其分子结构中不含乙基.由A制备D的一种合成路线(中间产物 及部分反应条件略去)如图所示:
C和D的结构简式分别为___________、__________。
三、推断题
19.化学式为C8H10O的化合物A具有如下性质:①A+Na→慢慢产生气泡 ②A+RCOOH有香味的产物 ③A苯甲酸 ④催化脱氢产物不能发生银镜反应 ⑤脱水反应的产物,经聚合反应可制得一种塑料制品(它是目前造成“白色污染”主要的污染源之一)。
试回答:
(1)根据上述信息,对该化合物的结构?可作出的判断是___________。
a.苯环上直接连有羟基 b.肯定有醇羟基
c.苯环侧链末端有甲基 d.肯定是芳香烃
(2)化合物A的结构简式____________________。
(3)A和金属钠反应的化学方程式________________________________。
四、实验题
20.甲苯()是一种重要的化工原料,能用于生产苯甲醛()、苯甲酸()等产品。下表列出有关物质的部分物理性质。
注:甲苯、苯甲醛、苯甲酸三者互溶,且均易溶于有机溶剂中。
实验室可用如图装置模拟制备苯甲醛:
实验时先在三颈瓶中加入0.5 g固态难溶性催化剂,再加入15 mL冰醋酸和2 mL甲苯,搅拌升温至70 ℃,同时缓慢加入12 mL过氧化氢,在此温度下搅拌反应3小时。试回答下列问题:
(1)装置a的名称是____________。三颈瓶中发生反应的化学方程式为______________________________________________,加入的冰醋酸并未参与反应,其作用可能为____________。
(2)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是________________________________________(答一条即可)。
(3)反应完毕后,反应混合液经过自然冷却至室温时,还应经过________(填操作名称)等操作,才能得到苯甲醛粗产品。
(4)实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯甲酸。
①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是__________(按步骤顺序填字母代号)。
a.对混合液进行分液
b.过滤、洗涤、干燥
c.水层中加入盐酸调节pH=2
d.与适量碳酸氢钠溶液混合震荡
②若对实验①中获得的苯甲酸产品进行纯度测定,可称取2.500 g产品,溶于200 mL乙醇配成溶液,量取所得的乙醇溶液20.00 mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.100 0 mol/L的KOH标准液滴定,到达滴定终点时消耗KOH溶液18.00 mL。产品中苯甲酸的质量分数为________(注:苯甲酸的相对分子质量为122)。
五、计算题
21.已知4.6克无水乙醇在氧气中完全燃烧,只生成8.8克CO2 和5.4克H2O,则无水乙醇中含有哪几种元素___?写出其化学式___?完成乙醇燃烧的化学方程式____。
22.含有C、H、O的化合物,其C、H、O的质量比为12∶1∶16,其摩尔质量为116g/mol,它的水溶液能使甲基橙变红,0.58g这种物质能与50mL0.2mol/L的氢氧化钠溶液完全反应,它能使溴水褪色。推断这种物质的结构简式_________(要求写出推断过程)。
参考答案
1.C 2.D 3.A 4.D 5.B 6.B 7.D 8.D 9.B 10.D 11.D 12.C 13.B 14.D 15.C
16.羧基 1:1 +2NaOH+CH3OH+H2O
17.(1)14(2分) (2)(酚)羟基、羧基(2+2=4分)
(3分)
酯化反应(或取代反应)(2分) (4)聚苯乙烯(2分)
(2分)
18. 乙烯 400 加成反应 羧基 CH3Br
19.b c +2Na→2+H2↑
20.(1)球形冷凝管(2分)冷凝回流,防止甲苯的挥发而降低产品产率(2分)
(2)(2分) 66.25%(2分)
(3)H2O2在较高温度时分解速度加快,使实际参加反应的H2O2减少,影响产量(2分)
(4)过滤(2分) 蒸馏(2分)(5)①dacb(2分) ②87.84﹪(2分)
21.C、H、O三元素 C2H6O C2H5OH+3O2 2CO2+3H2O
22.HOOC-CH=CH-COOH或CH2=CH(COOH)2
一、单选题
1.下列实验过程中需要水浴加热的是( )
A.由乙醇制乙烯 B.乙酸乙酯的制取
C.甲醛的银镜反应 D.苯酚与浓溴水的反应
2.提纯下列物质(括号中为杂质),所选除杂试剂和分离方法都正确的是
选项
被提纯的物质(杂质)
除杂试剂
分离方法
A
乙烯(二氧化硫)
酸性KMnO4溶液
洗气
B
乙酸乙酯(乙醇)
饱和Na2CO3溶液
蒸馏
C
苯(苯酚)
浓溴水
过滤
D
苯甲酸(NaCl)
-----
重结晶
A.A B.B C.C D.D
3.84消毒液()、甲醛()、过氧乙酸()、均可用于杀菌消毒下列说法错误的是( )
A.84消毒液和洁厕灵混合使用效果更好
B.甲醛水溶液可用于浸泡生物标本
C.过氧乙酸()配制过程中应佩戴橡胶手套
D.与空气中的和作用形成
4.下列说法正确的是
A.煤的液化、气化是物理变化,煤的干馏是化学变化
B.蛋白质、淀粉、纤维素、油脂均属于高分子化合物
C.乙酸乙酯在碱性条件下的水解反应属于皂化反应
D.石油裂化的目的是为了提高汽油等轻质液态油的产量和质量
5.学习化学应有辩证的观点和方法.下列说法正确的是( )
A.催化剂不参加化学反应
B.醇和酸反应的产物未必是酯
C.卤代烃的水解产物一定是醇
D.醇脱水的反应都属于消去反应
6.下列叙述中不正确的是
A.乙烯可作水果的催熟剂
B.福尔马林可用来保存海参等海鲜产品
C.苯酚可用来消毒杀菌
D.通过石油的催化裂化及裂解可以得到轻质油和气态烯烃
7.茶多酚是一类目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂的总称。其中没食子儿茶素(EGC)的结构如图所示。关于EGC的下列叙述中正确的是
A.EGC是一种芳香烃
B.1molEGC与4molNaOH恰好完全反应
C.遇FeCl3溶液能不发生显色反应
D.易发生氧化反应和取代反应,相对较难发生加成反应
8.达菲是治疗流感的重要药物,M是合成达菲的重要中间体,下列说法错误的是
A.化合物M分子式为C16H27O5N B.化合物M能发生消去反应、加聚反应
C.化合物M能使酸性高锰酸钾溶液褪色 D.化合物M有4种不同的官能团
9.属于醇的同分异构体有
A.3种 B.4种 C.5种 D.6种
10.核黄素又称维生素B,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳。核黄素分子的结构为:
有关核黄素的下列说法中,正确的是
A.该物质属于有机高分子
B.不能发生酯化反应
C.不能与氢气发生加成反应
D.酸性条件下加热水解,有CO2生成
11.下列实验操作正确且能达到预期目的的是( )
实验目的
操作
A
欲证明CH2=CHCHO中含有碳碳双键
滴入酸性KMnO4溶液
B
欲除去苯中混有的少量苯酚
向混合液中加入浓溴水,充分反应后,过滤
C
证明SO2具有漂白性
将SO2通入酸性KMnO4溶液中
D
确定碳和硅两元素非金属性强弱
测同温同浓度Na2CO3和Na2SiO3水溶液的pH
A.A B.B C.C D.D
12.双羟香豆素医学上用作抗凝剂,其结构如右图。下列有关双羟香豆素的说法正确的是
A.分子式为C19H10O6
B.遇FeCl3溶液能发生显色反应
C.1 mol双羟香豆素最多能与含 4 mol氢氧化钠的水溶液完全反应
D.1 mol双羟香豆素最多能与 10 mol氢气发生加成反应
13.下列有关用水杨酸和乙酸酐制备阿司匹林(乙酰水杨酸)的说法中不正确的是( )
A.制备阿司匹林的反应属于取代反应
B.待反应结束后向锥形瓶中加水,冰水浴中冷却结晶,减压过滤,用少量冷水淋洗锥形瓶收集所有晶体
C.粗产品中常混有聚合物杂质,可利用溶液溶解、过滤、洗涤、盐酸酸化、结晶等操作进行精制
D.可用溶液检验阿司匹林中是否含有未反应完的水杨酸
14.下列4个化学反应中,与其他3个反应类型不同的是( )
A.CH3CHO+2Cu(OH)2CH3COOH+Cu2O↓+2H2O
B.CH3CH2OH+CuOCH3CHO+Cu+H2O
C.2CH2===CH2+O22CH3CHO
D.CH3CH2OH+HBr―→CH3CH2Br+H2O
15.环己醇,丙酮和乙醛混合物1.75g,完全燃烧后,所得气体通过P2O5吸收瓶,瓶增重1.8g,则混合物的平均相对分子质量为( )
A.68 B.75 C.80 D.87.5
二、填空题
16.据不完全统计,全世界每年约有10%~20%的农副产品,水产品会因腐败变质而无法食用,经济损失巨大,所以研究安全无害的食品防腐剂很重要,山梨酸及其盐,尼泊金酯等可作为食品防腐剂,其结构简式如图:
按要求回答下列问题:
(1)写出山梨酸中含氧官能团的名称___。
(2)常温下,等物质的量的山梨酸、尼泊金甲酯分别与足量溴水反应,消耗Br2的物质的量之比为___。
(3)写出尼泊金甲酯与NaOH溶液反应的化学方程式____。
17.某芳香烃A,分子式为C8H10;某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液 显紫色;J分子内有两个互为对位的取代基。在一定条件下有如下的转化关系(无机物略去):
(1)属于芳香烃类的A的同分异构体(不包括A)中,在同一平面的原子最多有__________个;
(2)J中所含的含氧官能团的名称为__________。
(3)E与H反应的化学方程式是____________________________________;
(4)B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物M,以M为单体合成的高分子化合物的名称是_________________________。
(5)已知J有多种同分异构体,写出一种符合下列性质的J的同分异构体的结构简式。①与FeCl3溶液作用显紫色;②与新制Cu(OH)2悬浊液作用产生红色沉淀;③苯环上的一卤代物有2种。
______________________________________________
18.乙基香兰素是最重要的合成香料之一,常作为婴幼儿奶粉的添加剂。制备乙基香兰素的一种合成路线(部分反应条件略去)如下图所示:
已知:①R-ONa+R′-Br-→R-O-R′+NaBr
②Ⅲ中生成的Cu2O经氧化后可以循环利用
回答下列问题:
(1)A的核磁共振氢谱有3组峰.A的结构简式为______________________;
(2)Ⅰ中可能生成的一种烃是_________(填名称);催化剂PEG可看作乙二醇脱水缩聚的产物,PEG的结构简式为___________;若PEG的平均相对分子质量为17618,则其平均聚合度约为________;
(3)Ⅱ中,发生的反应属于____________(填反应类型);
(4)Ⅳ中,有机物脱去的官能团是______________________(填名称);
(5)D是乙基香兰素的同分异构体,其分子结构中不含乙基.由A制备D的一种合成路线(中间产物 及部分反应条件略去)如图所示:
C和D的结构简式分别为___________、__________。
三、推断题
19.化学式为C8H10O的化合物A具有如下性质:①A+Na→慢慢产生气泡 ②A+RCOOH有香味的产物 ③A苯甲酸 ④催化脱氢产物不能发生银镜反应 ⑤脱水反应的产物,经聚合反应可制得一种塑料制品(它是目前造成“白色污染”主要的污染源之一)。
试回答:
(1)根据上述信息,对该化合物的结构?可作出的判断是___________。
a.苯环上直接连有羟基 b.肯定有醇羟基
c.苯环侧链末端有甲基 d.肯定是芳香烃
(2)化合物A的结构简式____________________。
(3)A和金属钠反应的化学方程式________________________________。
四、实验题
20.甲苯()是一种重要的化工原料,能用于生产苯甲醛()、苯甲酸()等产品。下表列出有关物质的部分物理性质。
注:甲苯、苯甲醛、苯甲酸三者互溶,且均易溶于有机溶剂中。
实验室可用如图装置模拟制备苯甲醛:
实验时先在三颈瓶中加入0.5 g固态难溶性催化剂,再加入15 mL冰醋酸和2 mL甲苯,搅拌升温至70 ℃,同时缓慢加入12 mL过氧化氢,在此温度下搅拌反应3小时。试回答下列问题:
(1)装置a的名称是____________。三颈瓶中发生反应的化学方程式为______________________________________________,加入的冰醋酸并未参与反应,其作用可能为____________。
(2)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是________________________________________(答一条即可)。
(3)反应完毕后,反应混合液经过自然冷却至室温时,还应经过________(填操作名称)等操作,才能得到苯甲醛粗产品。
(4)实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯甲酸。
①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是__________(按步骤顺序填字母代号)。
a.对混合液进行分液
b.过滤、洗涤、干燥
c.水层中加入盐酸调节pH=2
d.与适量碳酸氢钠溶液混合震荡
②若对实验①中获得的苯甲酸产品进行纯度测定,可称取2.500 g产品,溶于200 mL乙醇配成溶液,量取所得的乙醇溶液20.00 mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.100 0 mol/L的KOH标准液滴定,到达滴定终点时消耗KOH溶液18.00 mL。产品中苯甲酸的质量分数为________(注:苯甲酸的相对分子质量为122)。
五、计算题
21.已知4.6克无水乙醇在氧气中完全燃烧,只生成8.8克CO2 和5.4克H2O,则无水乙醇中含有哪几种元素___?写出其化学式___?完成乙醇燃烧的化学方程式____。
22.含有C、H、O的化合物,其C、H、O的质量比为12∶1∶16,其摩尔质量为116g/mol,它的水溶液能使甲基橙变红,0.58g这种物质能与50mL0.2mol/L的氢氧化钠溶液完全反应,它能使溴水褪色。推断这种物质的结构简式_________(要求写出推断过程)。
参考答案
1.C 2.D 3.A 4.D 5.B 6.B 7.D 8.D 9.B 10.D 11.D 12.C 13.B 14.D 15.C
16.羧基 1:1 +2NaOH+CH3OH+H2O
17.(1)14(2分) (2)(酚)羟基、羧基(2+2=4分)
(3分)
酯化反应(或取代反应)(2分) (4)聚苯乙烯(2分)
(2分)
18. 乙烯 400 加成反应 羧基 CH3Br
19.b c +2Na→2+H2↑
20.(1)球形冷凝管(2分)冷凝回流,防止甲苯的挥发而降低产品产率(2分)
(2)(2分) 66.25%(2分)
(3)H2O2在较高温度时分解速度加快,使实际参加反应的H2O2减少,影响产量(2分)
(4)过滤(2分) 蒸馏(2分)(5)①dacb(2分) ②87.84﹪(2分)
21.C、H、O三元素 C2H6O C2H5OH+3O2 2CO2+3H2O
22.HOOC-CH=CH-COOH或CH2=CH(COOH)2
