2020-2021年鲁教五四版化学八年级全学期第5单元 《定量研究化学反应》高频易错题集1带答案
文档属性
| 名称 | 2020-2021年鲁教五四版化学八年级全学期第5单元 《定量研究化学反应》高频易错题集1带答案 |
|
|
| 格式 | zip | ||
| 文件大小 | 118.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-09 00:00:00 | ||
图片预览


文档简介
2020-2021年鲁教五四版化学八年级全学期第5单元
《定量研究化学反应》高频易错题集1带答案
一.选择题(共10小题)
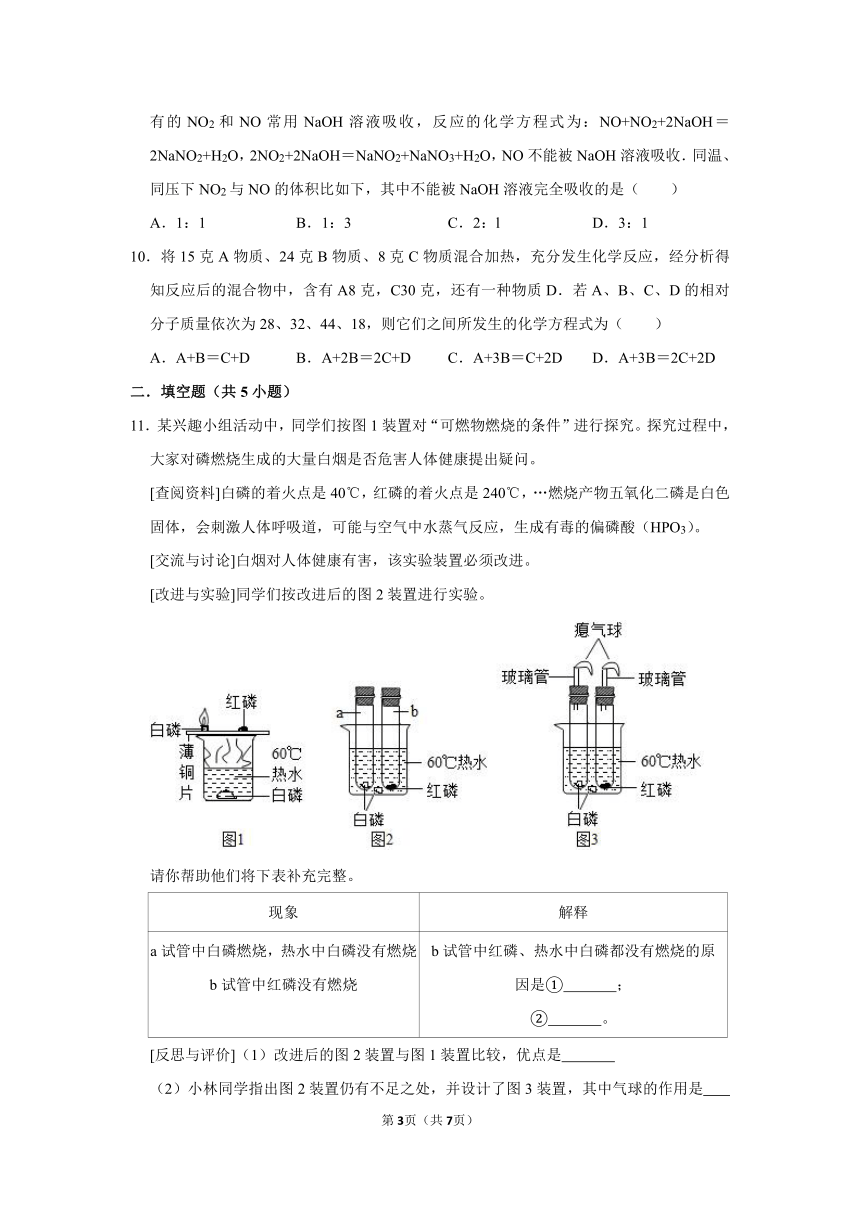
1.用如图装置完成以下试验:
(1)探究燃烧条件:若B处盛放木炭。
Ⅰ.先在A处通入氮气一段时间后,在B处加热,B、C处没有明显变化;
Ⅱ.待B处冷却至室温,在A处通入氧气一段时间后,B、C处没有明显变化;
Ⅲ.在A处继续通入氧气,然后在B处加热,发现木炭燃烧,C处变浑浊。
(2)模拟工业炼铁:若B处盛放氧化铁粉末。在A处通入一氧化碳一段时间后,B处下方用酒精喷灯加热。下列说法中正确的是( )
①Ⅰ和Ⅲ对比,说明燃烧需要可燃物与氧气接触
②Ⅰ和Ⅲ对比,说明O2的化学性质比氮气活泼
③Ⅱ与Ⅲ对比,说明燃烧需要温度超过可燃物的着火点
④该实验还能证明燃烧需要可燃物
⑤实验(2)中缺乏尾气处理装置
⑥实验(2)中玻璃管内物质的质量在反应前后的减少量可能等于C中反应前后物质的质量的增加量。
A.①②③④⑤⑥
B.①②③④⑤
C.①②⑤⑥
D.①②⑤
2.将苯(C6H6)和氧气置于密闭容器中引燃,反应后生成CO2、H2O和X。已知反应前后各物质的质量如下表。下列说法正确的是( )
物质
C6H6
O2
CO2
H2O
X
反应前质量(g)
1.3
3.2
0
0
0
反应后质量(g)
0
0
2.2
0.9
W
A.W的质量等于1.5g
B.X由碳、氢两种元素组成
C.X由碳、氧两种元素组成
D.CO2和H2O分子个数比为2:1
3.将一定量的NaOH和NaHCO3的混合物,放在密闭容器中加热充分反应,冷却到室温后测得容器内CO2的质量为ag,再将反应后的固体残渣与足量稀盐酸反应,又生成bg
CO2,下列有关CO2质量的分析正确的是( )
A.a>b
B.a=b
C.a<b
D.均有可能
4.下列说法错误的是( )
A.化学反应中,反应物的总质量等于生成物的总质量
B.镁条燃烧后,生成物质量大于镁条质量
C.反应物和生成物分子个数一定相等
D.化学反应前后,元素种类没变
5.洁厕灵和“84消毒液“混合使用时会生成有毒气体Cl2,即NaClO+2HCl═NaCl+Cl2↑+H2O,下列说法错误的是( )
A.NaCl的名称为氯化钠
B.该反应常温下就可以进行
C.Cl2属于单质
D.NaClO中钠、氧、氯元素的质量比为1:1:1
6.有关2H2+O22H2O的叙述正确的是( )
A.两个氢分子加一个氧分子等于两个水分子
B.氢气和氧气在点燃条件下反应生成水
C.氢气加氧气点燃等于水
D.2g氢气和lg氧气反应生成2g水
7.北京2008年奥运会火炬“祥云”使用的燃料是丙烷(C3H8),其燃烧的化学方程式为:C3H8+xO2yCO2+4H2O,其中x、y分别是( )
A.5;3
B.7;3
C.1;3
D.1;5
8.化学方程式aC2H2
+bO2cH2O+dCO2配平后a、b、c、d之和为( )
A.15
B.14
C.13
D.10
9.已知同温、同压下相同体积的任何气体都含有相同的分子数.工业制HNO3的尾气中含有的NO2和NO常用NaOH溶液吸收,反应的化学方程式为:NO+NO2+2NaOH=2NaNO2+H2O,2NO2+2NaOH=NaNO2+NaNO3+H2O,NO不能被NaOH溶液吸收.同温、同压下NO2与NO的体积比如下,其中不能被NaOH溶液完全吸收的是( )
A.1:1
B.1:3
C.2:l
D.3:1
10.将15克A物质、24克B物质、8克C物质混合加热,充分发生化学反应,经分析得知反应后的混合物中,含有A8克,C30克,还有一种物质D.若A、B、C、D的相对分子质量依次为28、32、44、18,则它们之间所发生的化学方程式为( )
A.A+B=C+D
B.A+2B=2C+D
C.A+3B=C+2D
D.A+3B=2C+2D
二.填空题(共5小题)
11.某兴趣小组活动中,同学们按图1装置对“可燃物燃烧的条件”进行探究。探究过程中,大家对磷燃烧生成的大量白烟是否危害人体健康提出疑问。
[查阅资料]白磷的着火点是40℃,红磷的着火点是240℃,…燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3)。
[交流与讨论]白烟对人体健康有害,该实验装置必须改进。
[改进与实验]同学们按改进后的图2装置进行实验。
请你帮助他们将下表补充完整。
现象
解释
a试管中白磷燃烧,热水中白磷没有燃烧b试管中红磷没有燃烧
b试管中红磷、热水中白磷都没有燃烧的原因是①
;②
。
[反思与评价](1)改进后的图2装置与图1装置比较,优点是
(2)小林同学指出图2装置仍有不足之处,并设计了图3装置,其中气球的作用是
[拓展与迁移]实验小结时,小朱同学说:“待a试管冷却后,如果将试管口紧贴水面(室温下)。并取下橡皮塞,将看到液体进入试管。”这一说法得到大家的一致认同。
小晶问:“如果不考虑橡皮塞占试管的容积,进入a试管内液体的体积会是多少呢?大家争论后,出现两种预测。
甲:接近试管容积的;
乙:不一定接近试管容积的.你赞同的预测是
(填“甲”或“乙”),理由是
。
12.同学们为了验证质量守恒定律,进行了如图实验:
(1)甲实验玻璃管的作用是
,化学方程式为
。
(2)实验乙反应前天平平衡,反应过程中实验现象为
。
(3)实验丙中,称量镁条和石棉网的质量后,点燃镁条,观察到镁条剧烈燃烧,产生大量白烟,反应结束,将所得物质与石棉网一起再次称量,发现质量减轻了,其原因是
。
13.根据化学方程式4Al+3O2═2Al2O3,反应物是
和
,每
份质量的
和
份质量的
反应生成
份质量的
。
14.配平下列反应的化学方程式:
(1)
Fe2O3+
C
Fe+
CO2↑
(2)
NH3+
O2
NO+
H2O;
(3)
C6H6+
O2═
CO2+
H2O;
(4)
Cl2+
Ca(OH)2═
Ca(ClO)2+
H2O+
CaCl2
15.在化学反应2H2+O22H2O中、H2、O2、H2O的质量比为:
.
三.解答题(共5小题)
16.如图中的甲、乙两套装置都可以用来探究可燃物燃烧的条件.
(1)某同学用甲图所示的装置进行探究实验,观察到的现象是
,该反应属于
(填“化合”或“分解”)反应.
(2)另一同学用乙图所示的装置进行了探究实验,得出了以下四个实验事实:
①不通空气,热水中的白磷不能燃烧
②不通空气,冷水中的白磷不能燃烧
③通空气,热水中的白磷能燃烧
④通空气,冷水中的白磷不能燃烧
比较
(填序号)两个实验可以得出“可燃物燃烧需要与空气接触”的结论;比较
(填序号)两个实验可以得出“可燃物燃烧需要达到一定温度(着火点)”的结论.
(3)甲图与乙图所示实验相比,
(填“甲”或“乙”)更体现了化学实验的绿色化追求.
(4)同学们查阅资料获取到这样一条信息:“点燃的镁带可以在二氧化碳气体中继续剧烈燃烧,生成碳和氧化镁”.
请写出该反应的化学方程式:
你对燃烧或灭火有什么新的认识
.
17.“喝酒不开车,开车不喝酒”。酒中含有乙醇(C2H6O),交通警察执法时让开车者对着便携式酒精检查仪吹气,便携式酒精检查仪内部发生反应的原理为:2K2Cr2O7(橙色)+3C2H6O+8H2SO4
═2Cr2(SO4)3(蓝绿色)+3C2H4O2+2K2SO4+11X
根据该反应回答下列问题:
(1)如果司机饮了酒,交警观察到仪器内部药品发生反应的现象是
。
(2)便携式酒精检查仪中的铬(Cr)元素在检查前后的质量
(填“增加”、“减少”、“不变”)。
(3)该反应生成物中X的化学式为
。
(4)Cr元素的化合价在反应前后的变化是
(填由多少价变到多少价)。
(5)乙醇也是一种燃料,在空气中完全燃烧生成水和二氧化碳。乙醇在空气中完全燃烧的化学方程式为
。
18.S+O2SO2能表示的意义是:
(1)微观:表示
。
(2)宏观①质的关系:
;
②量的关系:
。
19.配平化学方程式:
(1)
C2H6+
O2
CO2+
H2O
(2)
Al+
Fe3O4
Al2O3+
Fe
20.请用化学方程式表示下列反应原理.
(1)铁在氧气中燃烧:
.
(2)乙醇(化学式为C2H5OH)用作燃料:
.
(3)干粉灭火器中的干粉(主要成分是NaHCO3)受热时分解生成碳酸钠、水和二氧化碳:
.
参考答案
一.选择题(共10小题)
1.D;
2.C;
3.C;
4.C;
5.D;
6.B;
7.A;
8.C;
9.B;
10.D;
二.填空题(共5小题)
11.温度未达到红磷的着火点;热水中的白磷没有与氧气(或空气)接触;防止白磷燃烧产生的五氧化二磷扩散,污染环境和危害人体健康;避免橡皮塞因试管内气体热膨胀飞出,造成安全事故;甲;空气中氧气的体积约占空气体积的,且上述实验白磷足量、气密性良好,所以进入a试管内液体的体积能接近试管容积的;
12.导热来让红磷在密闭体系中点燃;4P+5O22P2O5;天平指针向右偏转;镁条在燃烧时产生大量的白烟,其实是生成的氧化镁部分散失到空气中;
13.铝;氧气;108;铝;96;氧气;204;氧化铝;
14.2;3;4;3;4;5;4;6;2;
15;12;6;2;2;1;2;1;
15.1:8:9;
三.解答题(共5小题)
16.在铜片上的白磷剧烈燃烧,产生大量白烟,放出热量,生成白色固体;红磷及水中的白磷没有变化;化合;①③;③④;乙;2Mg+CO2C+2MgO;燃烧不一定有氧气参加;
17.仪器显示蓝绿色或仪器显示的颜色由橙色变为蓝绿色;不变;H2O;+6变为+3;C2H6O+3O22CO2+3H2O;
18.一个硫原子和一个氧分子在点燃的条件下生成一个二氧化硫分子;硫和氧气在点燃的条件下生成二氧化硫;每32份质量的硫和32份质量的氧气在点燃的条件下生成64份质量的二氧化硫;
19.2;7;4;6;8;3;4;9;
20.3Fe+2O2Fe3O4;C2H5OH+3O22CO2+3H2O;;
2NaHCO3Na2CO3+H2O+CO2↑;
第1页(共1页)
《定量研究化学反应》高频易错题集1带答案
一.选择题(共10小题)
1.用如图装置完成以下试验:
(1)探究燃烧条件:若B处盛放木炭。
Ⅰ.先在A处通入氮气一段时间后,在B处加热,B、C处没有明显变化;
Ⅱ.待B处冷却至室温,在A处通入氧气一段时间后,B、C处没有明显变化;
Ⅲ.在A处继续通入氧气,然后在B处加热,发现木炭燃烧,C处变浑浊。
(2)模拟工业炼铁:若B处盛放氧化铁粉末。在A处通入一氧化碳一段时间后,B处下方用酒精喷灯加热。下列说法中正确的是( )
①Ⅰ和Ⅲ对比,说明燃烧需要可燃物与氧气接触
②Ⅰ和Ⅲ对比,说明O2的化学性质比氮气活泼
③Ⅱ与Ⅲ对比,说明燃烧需要温度超过可燃物的着火点
④该实验还能证明燃烧需要可燃物
⑤实验(2)中缺乏尾气处理装置
⑥实验(2)中玻璃管内物质的质量在反应前后的减少量可能等于C中反应前后物质的质量的增加量。
A.①②③④⑤⑥
B.①②③④⑤
C.①②⑤⑥
D.①②⑤
2.将苯(C6H6)和氧气置于密闭容器中引燃,反应后生成CO2、H2O和X。已知反应前后各物质的质量如下表。下列说法正确的是( )
物质
C6H6
O2
CO2
H2O
X
反应前质量(g)
1.3
3.2
0
0
0
反应后质量(g)
0
0
2.2
0.9
W
A.W的质量等于1.5g
B.X由碳、氢两种元素组成
C.X由碳、氧两种元素组成
D.CO2和H2O分子个数比为2:1
3.将一定量的NaOH和NaHCO3的混合物,放在密闭容器中加热充分反应,冷却到室温后测得容器内CO2的质量为ag,再将反应后的固体残渣与足量稀盐酸反应,又生成bg
CO2,下列有关CO2质量的分析正确的是( )
A.a>b
B.a=b
C.a<b
D.均有可能
4.下列说法错误的是( )
A.化学反应中,反应物的总质量等于生成物的总质量
B.镁条燃烧后,生成物质量大于镁条质量
C.反应物和生成物分子个数一定相等
D.化学反应前后,元素种类没变
5.洁厕灵和“84消毒液“混合使用时会生成有毒气体Cl2,即NaClO+2HCl═NaCl+Cl2↑+H2O,下列说法错误的是( )
A.NaCl的名称为氯化钠
B.该反应常温下就可以进行
C.Cl2属于单质
D.NaClO中钠、氧、氯元素的质量比为1:1:1
6.有关2H2+O22H2O的叙述正确的是( )
A.两个氢分子加一个氧分子等于两个水分子
B.氢气和氧气在点燃条件下反应生成水
C.氢气加氧气点燃等于水
D.2g氢气和lg氧气反应生成2g水
7.北京2008年奥运会火炬“祥云”使用的燃料是丙烷(C3H8),其燃烧的化学方程式为:C3H8+xO2yCO2+4H2O,其中x、y分别是( )
A.5;3
B.7;3
C.1;3
D.1;5
8.化学方程式aC2H2
+bO2cH2O+dCO2配平后a、b、c、d之和为( )
A.15
B.14
C.13
D.10
9.已知同温、同压下相同体积的任何气体都含有相同的分子数.工业制HNO3的尾气中含有的NO2和NO常用NaOH溶液吸收,反应的化学方程式为:NO+NO2+2NaOH=2NaNO2+H2O,2NO2+2NaOH=NaNO2+NaNO3+H2O,NO不能被NaOH溶液吸收.同温、同压下NO2与NO的体积比如下,其中不能被NaOH溶液完全吸收的是( )
A.1:1
B.1:3
C.2:l
D.3:1
10.将15克A物质、24克B物质、8克C物质混合加热,充分发生化学反应,经分析得知反应后的混合物中,含有A8克,C30克,还有一种物质D.若A、B、C、D的相对分子质量依次为28、32、44、18,则它们之间所发生的化学方程式为( )
A.A+B=C+D
B.A+2B=2C+D
C.A+3B=C+2D
D.A+3B=2C+2D
二.填空题(共5小题)
11.某兴趣小组活动中,同学们按图1装置对“可燃物燃烧的条件”进行探究。探究过程中,大家对磷燃烧生成的大量白烟是否危害人体健康提出疑问。
[查阅资料]白磷的着火点是40℃,红磷的着火点是240℃,…燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3)。
[交流与讨论]白烟对人体健康有害,该实验装置必须改进。
[改进与实验]同学们按改进后的图2装置进行实验。
请你帮助他们将下表补充完整。
现象
解释
a试管中白磷燃烧,热水中白磷没有燃烧b试管中红磷没有燃烧
b试管中红磷、热水中白磷都没有燃烧的原因是①
;②
。
[反思与评价](1)改进后的图2装置与图1装置比较,优点是
(2)小林同学指出图2装置仍有不足之处,并设计了图3装置,其中气球的作用是
[拓展与迁移]实验小结时,小朱同学说:“待a试管冷却后,如果将试管口紧贴水面(室温下)。并取下橡皮塞,将看到液体进入试管。”这一说法得到大家的一致认同。
小晶问:“如果不考虑橡皮塞占试管的容积,进入a试管内液体的体积会是多少呢?大家争论后,出现两种预测。
甲:接近试管容积的;
乙:不一定接近试管容积的.你赞同的预测是
(填“甲”或“乙”),理由是
。
12.同学们为了验证质量守恒定律,进行了如图实验:
(1)甲实验玻璃管的作用是
,化学方程式为
。
(2)实验乙反应前天平平衡,反应过程中实验现象为
。
(3)实验丙中,称量镁条和石棉网的质量后,点燃镁条,观察到镁条剧烈燃烧,产生大量白烟,反应结束,将所得物质与石棉网一起再次称量,发现质量减轻了,其原因是
。
13.根据化学方程式4Al+3O2═2Al2O3,反应物是
和
,每
份质量的
和
份质量的
反应生成
份质量的
。
14.配平下列反应的化学方程式:
(1)
Fe2O3+
C
Fe+
CO2↑
(2)
NH3+
O2
NO+
H2O;
(3)
C6H6+
O2═
CO2+
H2O;
(4)
Cl2+
Ca(OH)2═
Ca(ClO)2+
H2O+
CaCl2
15.在化学反应2H2+O22H2O中、H2、O2、H2O的质量比为:
.
三.解答题(共5小题)
16.如图中的甲、乙两套装置都可以用来探究可燃物燃烧的条件.
(1)某同学用甲图所示的装置进行探究实验,观察到的现象是
,该反应属于
(填“化合”或“分解”)反应.
(2)另一同学用乙图所示的装置进行了探究实验,得出了以下四个实验事实:
①不通空气,热水中的白磷不能燃烧
②不通空气,冷水中的白磷不能燃烧
③通空气,热水中的白磷能燃烧
④通空气,冷水中的白磷不能燃烧
比较
(填序号)两个实验可以得出“可燃物燃烧需要与空气接触”的结论;比较
(填序号)两个实验可以得出“可燃物燃烧需要达到一定温度(着火点)”的结论.
(3)甲图与乙图所示实验相比,
(填“甲”或“乙”)更体现了化学实验的绿色化追求.
(4)同学们查阅资料获取到这样一条信息:“点燃的镁带可以在二氧化碳气体中继续剧烈燃烧,生成碳和氧化镁”.
请写出该反应的化学方程式:
你对燃烧或灭火有什么新的认识
.
17.“喝酒不开车,开车不喝酒”。酒中含有乙醇(C2H6O),交通警察执法时让开车者对着便携式酒精检查仪吹气,便携式酒精检查仪内部发生反应的原理为:2K2Cr2O7(橙色)+3C2H6O+8H2SO4
═2Cr2(SO4)3(蓝绿色)+3C2H4O2+2K2SO4+11X
根据该反应回答下列问题:
(1)如果司机饮了酒,交警观察到仪器内部药品发生反应的现象是
。
(2)便携式酒精检查仪中的铬(Cr)元素在检查前后的质量
(填“增加”、“减少”、“不变”)。
(3)该反应生成物中X的化学式为
。
(4)Cr元素的化合价在反应前后的变化是
(填由多少价变到多少价)。
(5)乙醇也是一种燃料,在空气中完全燃烧生成水和二氧化碳。乙醇在空气中完全燃烧的化学方程式为
。
18.S+O2SO2能表示的意义是:
(1)微观:表示
。
(2)宏观①质的关系:
;
②量的关系:
。
19.配平化学方程式:
(1)
C2H6+
O2
CO2+
H2O
(2)
Al+
Fe3O4
Al2O3+
Fe
20.请用化学方程式表示下列反应原理.
(1)铁在氧气中燃烧:
.
(2)乙醇(化学式为C2H5OH)用作燃料:
.
(3)干粉灭火器中的干粉(主要成分是NaHCO3)受热时分解生成碳酸钠、水和二氧化碳:
.
参考答案
一.选择题(共10小题)
1.D;
2.C;
3.C;
4.C;
5.D;
6.B;
7.A;
8.C;
9.B;
10.D;
二.填空题(共5小题)
11.温度未达到红磷的着火点;热水中的白磷没有与氧气(或空气)接触;防止白磷燃烧产生的五氧化二磷扩散,污染环境和危害人体健康;避免橡皮塞因试管内气体热膨胀飞出,造成安全事故;甲;空气中氧气的体积约占空气体积的,且上述实验白磷足量、气密性良好,所以进入a试管内液体的体积能接近试管容积的;
12.导热来让红磷在密闭体系中点燃;4P+5O22P2O5;天平指针向右偏转;镁条在燃烧时产生大量的白烟,其实是生成的氧化镁部分散失到空气中;
13.铝;氧气;108;铝;96;氧气;204;氧化铝;
14.2;3;4;3;4;5;4;6;2;
15;12;6;2;2;1;2;1;
15.1:8:9;
三.解答题(共5小题)
16.在铜片上的白磷剧烈燃烧,产生大量白烟,放出热量,生成白色固体;红磷及水中的白磷没有变化;化合;①③;③④;乙;2Mg+CO2C+2MgO;燃烧不一定有氧气参加;
17.仪器显示蓝绿色或仪器显示的颜色由橙色变为蓝绿色;不变;H2O;+6变为+3;C2H6O+3O22CO2+3H2O;
18.一个硫原子和一个氧分子在点燃的条件下生成一个二氧化硫分子;硫和氧气在点燃的条件下生成二氧化硫;每32份质量的硫和32份质量的氧气在点燃的条件下生成64份质量的二氧化硫;
19.2;7;4;6;8;3;4;9;
20.3Fe+2O2Fe3O4;C2H5OH+3O22CO2+3H2O;;
2NaHCO3Na2CO3+H2O+CO2↑;
第1页(共1页)
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
