1.2《共价键》课件(苏教版必修2)
图片预览





文档简介
(共17张PPT)
共价键
请指出19、35号元素在元素周期表中的位置?
19号元素:第四周期,第ⅠA族
35号元素:第四周期,第ⅦA族
想一想这两种元素可能具有怎样的性质,为什么?
电子式
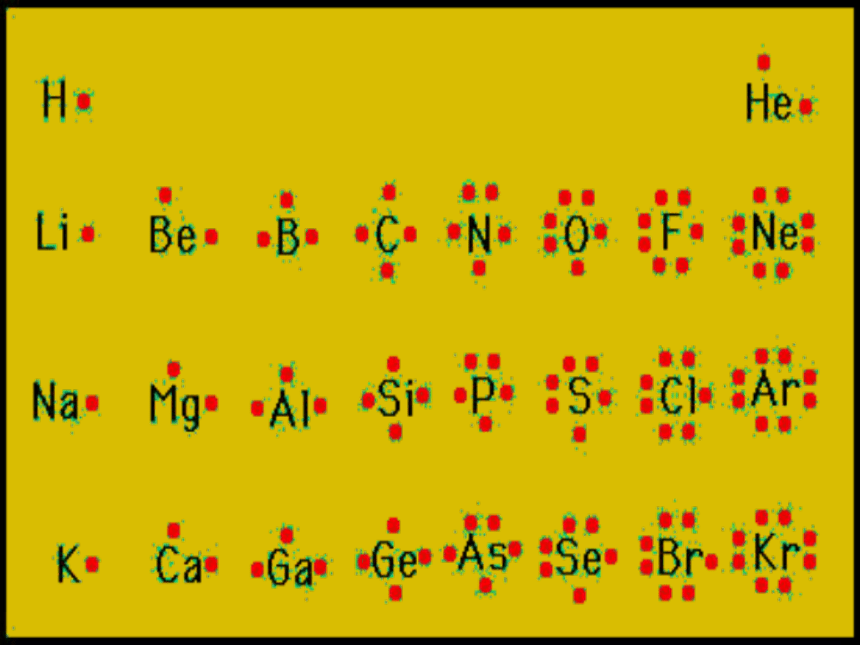
在元素符号周围用(·或×)来表示原子的最外层电子,这种式子 叫做电子式。
原子的电子式:尽量分散到四个方向上
氢原子,氦原子, 溴原子,氧原子
·o·
··
··
Br ·
··
··
··
·He·
·H
讨论
我们知道氦是单原子分子,而氢气是双原子分子,这是为什么呢?
分析氯化氢的形成过程
原子之间通过共用电子对所形成的强烈的相互作用,叫做共价键。象HCl这样以共用电子对形成分子的化合物就叫做共价化合物
1、成键微粒:
2、相互作用:
3、成键元素:同种或不同种非金属元素或非金属和活泼性不强的金属元素
共价键
原子
共用电子对
用电子式表示下列分子
H2O NH3 Cl2
练习
N2 HClO CO2
注意:在用电子式表示共价分子时,首先需分析所涉及的原子最外层有几个电子,则这个原子所需要的共用电子对数即为8-n(氢只需共用一对)
结构式
在化学上常用一根短线来表示一对共用电子,这样得到的式子又叫结构式
CH4 C2H4 C2H2
活动
用电子式表示共价键的形成过程
用电子式表示下列共价化合物的形成过程
CO2 NH3 CH4
拓展与延伸
共价键
请指出19、35号元素在元素周期表中的位置?
19号元素:第四周期,第ⅠA族
35号元素:第四周期,第ⅦA族
想一想这两种元素可能具有怎样的性质,为什么?
电子式
在元素符号周围用(·或×)来表示原子的最外层电子,这种式子 叫做电子式。
原子的电子式:尽量分散到四个方向上
氢原子,氦原子, 溴原子,氧原子
·o·
··
··
Br ·
··
··
··
·He·
·H
讨论
我们知道氦是单原子分子,而氢气是双原子分子,这是为什么呢?
分析氯化氢的形成过程
原子之间通过共用电子对所形成的强烈的相互作用,叫做共价键。象HCl这样以共用电子对形成分子的化合物就叫做共价化合物
1、成键微粒:
2、相互作用:
3、成键元素:同种或不同种非金属元素或非金属和活泼性不强的金属元素
共价键
原子
共用电子对
用电子式表示下列分子
H2O NH3 Cl2
练习
N2 HClO CO2
注意:在用电子式表示共价分子时,首先需分析所涉及的原子最外层有几个电子,则这个原子所需要的共用电子对数即为8-n(氢只需共用一对)
结构式
在化学上常用一根短线来表示一对共用电子,这样得到的式子又叫结构式
CH4 C2H4 C2H2
活动
用电子式表示共价键的形成过程
用电子式表示下列共价化合物的形成过程
CO2 NH3 CH4
拓展与延伸
