2020-2021学年华师版科学七年级下册第1章 水 单元测试 (含解析 无分值)
文档属性
| 名称 | 2020-2021学年华师版科学七年级下册第1章 水 单元测试 (含解析 无分值) |

|
|
| 格式 | docx | ||
| 文件大小 | 113.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-04-10 00:00:00 | ||
图片预览



文档简介
(
…………○…………外…………○…………装…………○…………订…………○…………线…………○…………
)
(
※※请※※不※※要※※在※※装※※订※※线※※内※※答※※题※※
)
(
…………○…………内…………○…………装…………○…………订…………○…………线…………○…………
)
第1章
水
单元测试
姓名:__________
班级:__________考号:__________
一、单选题
1.地球上的水以各种形式分布在不同区域,下图为水的分布图,图中代表海洋水的是(
?)
A.?①?????????????????????????????????????????B.?②?????????????????????????????????????????C.?③?????????????????????????????????????????D.?④
2.下列有关水的说法正确的是(
??)
A.?明矾可促进水中悬浮杂质的沉降
B.?生活中常用蒸馏的方法降低水的硬度
C.?地球上总水储量很大,水资源不会短缺
D.?经自来水厂净化处理过的生活用水一定是软水
3.我国东部地区人均水资源拥有量随纬度变化情况如图所示。据此信息,下列有关该地区人均水资源拥有量的说法不正确的是(
??)
A.?低纬度地区较多???????B.?北纬40°附近最少???????C.?在空间上分布不均匀???????D.?随着纬度的升高而减少
4.杭州正在修建地铁,在它的四周围栏上而安装了大量的喷雾装置,可见很多的“白汽”,如图。这些“白汽”不断喷洒,不断消失,有关“白汽”的分析正确的是(????
)
A.?“白汽”是水蒸气?????B.?“消失”是汽化现象?????C.?“喷洒”是升华现象?????D.?“消失”时需要放热
5.下面叙述的四种产生“白气”的现象中,有一种“白气”产生的原因与其他几种都不一样,这一种“白气”是(????
)。
A.?夏天打开冰棒包装纸,常常会看到冰棒在冒“白气”
B.?冬天,户外的人嘴里不断冒出“白气”
C.?吸烟时,
嘴里喷出的“白气”
D.?夏天打开冰箱冷冻室的门,会冒出一股“白气”
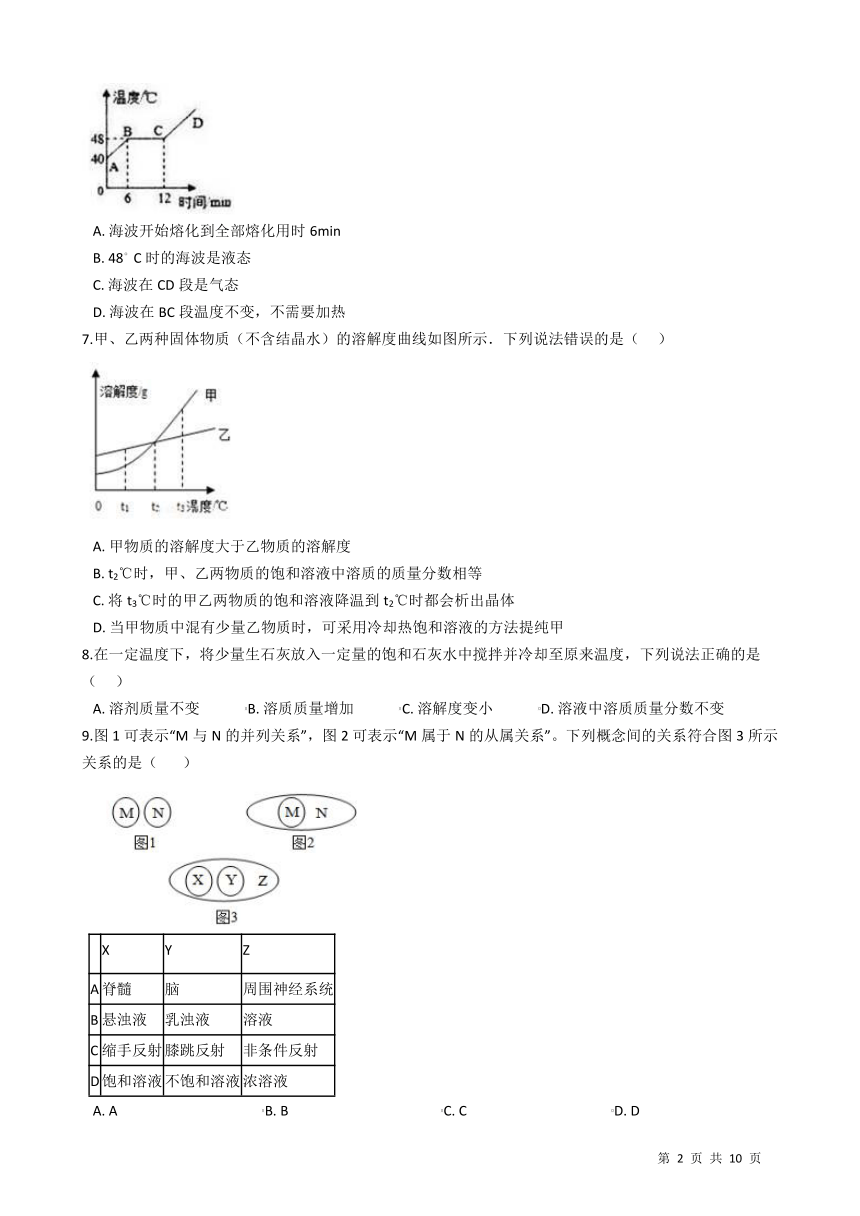
6.如图所示为海波的熔化图像,根据图像,下列说法正确的是(?
)。
A.?海波开始熔化到全部熔化用时6min
B.?48?C时的海波是液态
C.?海波在CD段是气态
D.?海波在BC段温度不变,不需要加热
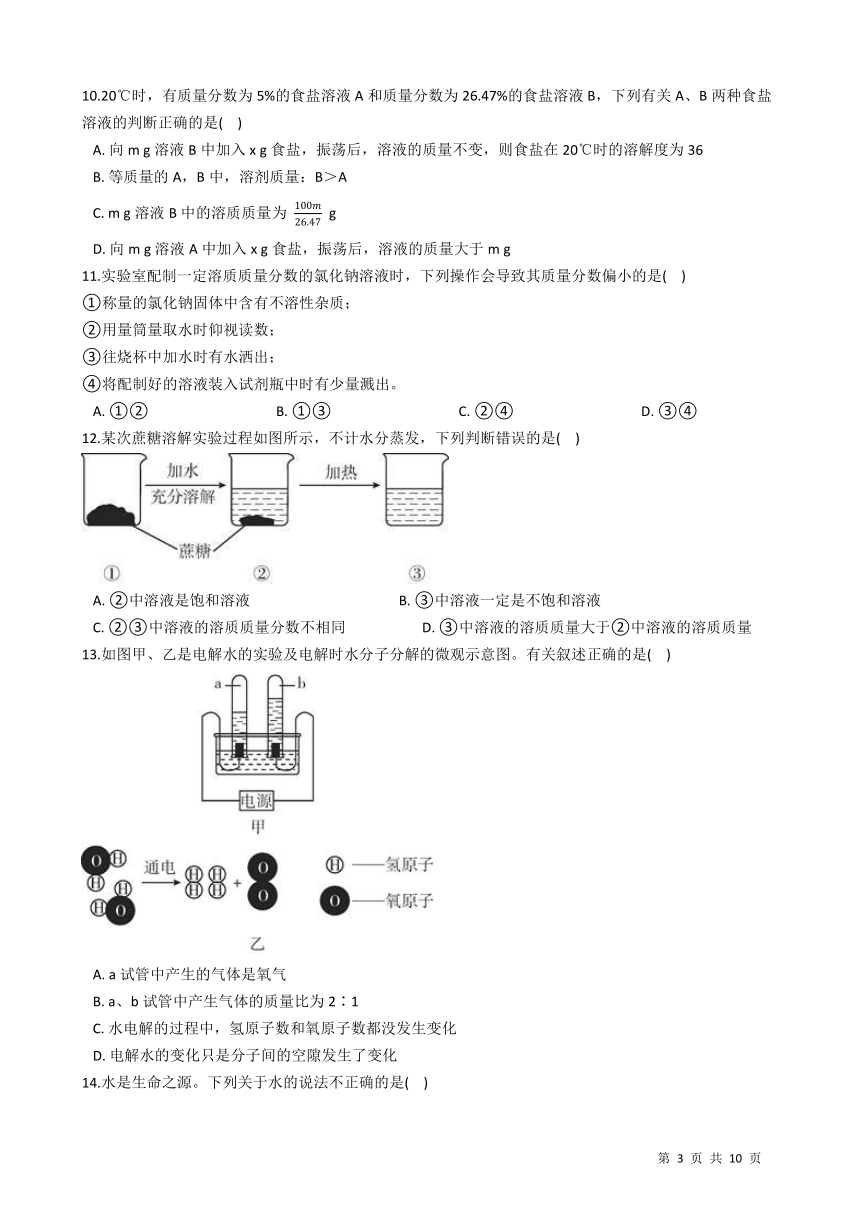
7.甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示.下列说法错误的是(???
)
A.?甲物质的溶解度大于乙物质的溶解度
B.?t2℃时,甲、乙两物质的饱和溶液中溶质的质量分数相等
C.?将t3℃时的甲乙两物质的饱和溶液降温到t2℃时都会析出晶体
D.?当甲物质中混有少量乙物质时,可采用冷却热饱和溶液的方法提纯甲
8.在一定温度下,将少量生石灰放入一定量的饱和石灰水中搅拌并冷却至原来温度,下列说法正确的是(???
)
A.?溶剂质量不变?????????????B.?溶质质量增加?????????????C.?溶解度变小?????????????D.?溶液中溶质质量分数不变
9.图1可表示“M与N的并列关系”,图2可表示“M属于N的从属关系”。下列概念间的关系符合图3所示关系的是(?????
)
X
Y
Z
A
脊髓
脑
周围神经系统
B
悬浊液
乳浊液
溶液
C
缩手反射
膝跳反射
非条件反射
D
饱和溶液
不饱和溶液
浓溶液
A.?A??????????????????????????????????????????B.?B
??????????????????????????????????????????C.?C??????????????????????????????????????????D.?D
10.20℃时,有质量分数为5%的食盐溶液A和质量分数为26.47%的食盐溶液B,下列有关A、B两种食盐溶液的判断正确的是(
??)
A.?向m
g溶液B中加入x
g食盐,振荡后,溶液的质量不变,则食盐在20℃时的溶解度为36
B.?等质量的A,B中,溶剂质量:B>A
C.?m
g溶液B中的溶质质量为
g
D.?向m
g溶液A中加入x
g食盐,振荡后,溶液的质量大于m
g
11.实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致其质量分数偏小的是(
??)
①称量的氯化钠固体中含有不溶性杂质;
②用量筒量取水时仰视读数;
③往烧杯中加水时有水洒出;
④将配制好的溶液装入试剂瓶中时有少量溅出。
A.?①②?????????????????????????????????????B.?①③?????????????????????????????????????C.?②④?????????????????????????????????????D.?③④
12.某次蔗糖溶解实验过程如图所示,不计水分蒸发,下列判断错误的是(
??)
A.?②中溶液是饱和溶液???????????????????????????????????????????B.?③中溶液一定是不饱和溶液
C.?②③中溶液的溶质质量分数不相同??????????????????????D.?③中溶液的溶质质量大于②中溶液的溶质质量
13.如图甲、乙是电解水的实验及电解时水分子分解的微观示意图。有关叙述正确的是(??
)
A.?a试管中产生的气体是氧气
B.?a、b试管中产生气体的质量比为2∶1
C.?水电解的过程中,氢原子数和氧原子数都没发生变化
D.?电解水的变化只是分子间的空隙发生了变化
14.水是生命之源。下列关于水的说法不正确的是(??
)
A.?水是一种化学资源??????????????????????????????????????????????B.?水是一种常用溶剂
C.?活性炭在净水过程中起着吸附和消毒作用???????????D.?水在通电的条件下分解得到两种新的物质
15.同学们对水进行研究,其中能确定水由氢和氧组成的是(
??)
A.?水的蒸发???????????????????????????B.?水的电解???????????????????????????C.?水的凝固???????????????????????????D.?水的沸腾
二、填空题
16.请你运用所学的科学知识回答生活中的问题。
(1)在十燥的天气里,用塑料梳子梳头,发现头发越梳越蓬松,这是因为梳头后头发带________(填“同”或“异”)种电荷。
(2)夏天的鱼塘里,常常出现鱼缺氧而“浮头”的现象,夏天水中缺氧的原因是________。
三、解答题
17.现有硝酸钾(KNO3)和氯化钠(NaCl)两种物质的溶解度数据如下表:
温度/℃
0
10
20
30
40
50
60
70
溶解度/g
NaCl
35.7
35.8
36.0
36.3
36.6
37.0
37.3
37.8
KNO3
13.3
20.9
31.6
45.8
45.8
85.5
110
138
(1)20℃时,能否制得溶质质量分数为30%的氯化钠溶液?请计算后说明。
(2)人们把海水引入盐田,风吹日晒后,食盐就会结晶析出。这种从溶液中得到体的方法叫________(填“蒸发溶剂”或“冷却热饱和溶液”)。
(3)有硝酸钾和氯化钠的饱和溶液各一杯,它们的温度、溶质质量分数都相同,则由表可知这两杯溶液的温度的最小范围是________。
答案解析部分
一、单选题
1.【答案】
A
【解析】【分析】地球上最多的水是海洋水,但海洋水不能食用,目前我国可直接利用的淡水资源,主要是江河、湖泊水和浅层地下水,应保护水资源。
【解答】海洋水在地球上所占比例为96.53%,A符合题意。
故答案为:A
?
2.【答案】
A
【解析】【分析】(1)根据水的净化的知识分析;
(2)根据蒸馏的作用分析;
(4)根据水资源的分布情况判断;
(4)根据硬水和软水的区别分析。
【解答】A.明矾溶于水形成的胶体具有吸附性,能将水中不溶性固体杂质吸附在其表面形成大颗粒,易于沉降,故A正确;
B.生活中常用加热煮沸的方法降低水的硬度,而不是蒸馏,故B错误;
C.地球上水的总储量很大,但是淡水储量很少,且分布不均匀,有些国家和地区水资源极度匮乏,故C错误;
D.经过自来水厂处理过的生活用水,其中可溶性的物质的量并没有多大变化,因此对水的硬度没有太大影响,故D错误。
故选A。
3.【答案】
D
【解析】【分析】条形图越高,说明人均水量越大;条形图越低,说明人均水量越少,据此分析判断。
【解答】A.根据图片可知,低纬度地区的条形图都比较高,即低纬度地区人均水资源拥有量较多,故A正确不合题意;?
B.北纬40°时条形图的高度最小,因此北纬40°附近人均水资源拥有量最少,故B正确不合题意;?
C.根据图像可知,人均水资源拥有量随纬度的不同而变化,因此在空间上分布不均匀,故C正确不合题意;
D.根据图片可知,人均水资源拥有量随着纬度的升高先减小后增大,故D错误符合题意。
故选D。
4.【答案】
B
【解析】【分析】物质由液态变成气态叫汽化,汽化需要吸热,据此分析判断。
【解答】“白汽”是小水珠,在空气中吸热后变成气态的水蒸气而消失,这是汽化现象,故B正确,而A、C、D错误。
故选B。
5.【答案】
C
【解析】【分析】从物态变化的角度对“白气”的成因进行分析即可。
【解答】A.夏天,冰棒的温度很低,水蒸气在冰棒周围放热,由气态变成液态的水发生液化现象,“白气”就是液化而成的小水珠;
B.冬天,人嘴里呼出的水蒸气温度较高,而户外的空气温度很低,此时水蒸气放热由气态变成液态的水发生液化现象,“白气”就是液化而成的小水珠;?
C.吸烟时,从嘴里冒出的“白气”是没有完全燃烧的固态小颗粒;?
D.夏天,打开冰箱门,里面的空气温度很低,而外面的空气温度很高,外面的水蒸气在冰箱门附近放热,由气态变成液态的水发生液化现象,而“白气”就是液化而成的小水珠。
那么与其它三个不同的是C。
故选C。
6.【答案】
A
【解析】【分析】(1)图像中横线对应的时间就是熔化时间;
(2)根据晶体在熔点时的状态分析;
(3)根据图像确定各个阶段海波的状态;
(4)根据晶体熔化的条件判断。
【解答】A.根据图像可知,海波6min时开始熔化,12min时熔化结束,那么熔化用的时间为:12min-6min=6min,故A正确;
B.48℃时海波的温度保持不变,那么这就是海波的熔点。如果熔化刚刚开始,那么海波为固态;如果熔化已经结束,那么海波为液态;如果熔化正在进行,那么海波为固液混合态,故B错误;
C.海波在AB段为固态,BC段为固液混合态,CD段为液态,故C错误;
D.海波在BC段温度不变,正在熔化,仍然需要不断加热,故D错误。
故选A。
7.【答案】
A
【解析】【分析】(1)谈到溶解度就必须说明温度,否则溶解度就没有意义;
(2)饱和溶液的溶质质量分数=;
(3)根据两种物质温度降低时溶解度的变化分析即可;
(4)如果物质的溶解度随温度变化明显,那么可以使用冷却热饱和溶液的方式结晶提纯。
【解答】A.温度低于t2时,甲的溶解度小于乙;温度高于t2时,甲的溶解度大于乙,故A错误符合题意;
B.t2℃时,甲和乙的溶解度相等,根据溶质质量分数=可知,二者的饱和溶液的溶质质量分数相等,故B正确不合题意;
C.甲和乙的溶解度都随温度的降低而减小,因此降温时二者的饱和溶液都有晶体析出,故C正确不合题意;
D.甲的溶解度随温度的变化十分明显,而乙的溶解度受温度的影响变化很小,因此利用冷却热饱和溶液的方法提纯甲,故D正确不合题意。
故选A。
8.【答案】
D
【解析】【分析】生石灰中的氧化钙与水反应,生成氢氧化钙;当温度不变时,同种物质的溶解度保持不变,那么饱和溶液的溶质质量分数保持不变,据此分析判断。
【解答】在一定温度下,将少量生石灰放入一定量的饱和石灰水中搅拌并冷却至原来温度。由于生石灰与水反应生成氢氧化钙,所以溶剂水的质量减小,故A错误;
石灰水原来就是饱和的,当溶剂质量减少时,肯定会有氢氧化钙析出,故B错误;
温度保持不变,那么石灰水的溶解度保持不变,故C错误;
因为石灰水的溶解度保持不变,且石灰水仍然饱和,那么溶液中溶质质量分数不变,故D正确。
故选D。
9.【答案】
C
【解析】【分析】非条件反射,是外界刺激与有机体反应之间与生俱来的固定神经联系。或在出生后发挥作用,或随着有机体的生长发育而出现。反射弧完整,在相应的刺激下,不需要后天的训练就能引起反射性反应,这类反射叫作非条件反射。
【解答】由图可知,X与Y是并列关系;X和Y都属于Z;
A、脊髓和脑是并列关系,但不属于周围神经系统;故A错误;
B、悬浊液和乳浊液是并列关系,但不属于溶液;故B错误;
C、缩手反射和膝跳反射是并列关系,都属于非条件反射;故C正确;
D、饱和溶液和不饱和溶液是并列关系,但不一定属于浓溶液;故D错误;
故答案为:C。
10.【答案】
D
【解析】【分析】(1)加入食盐后,溶液质量不变,说明加入的食盐没有溶解,即此时溶液饱和,然后根据饱和溶液的溶质质量分数=计算溶解度;
(2)根据溶液质量×溶质质量分数计算出溶质质量大小,再根据溶剂质量=溶液质量-溶剂质量比较即可;
(3)根据液质量×溶质质量分数计算出溶质质量大小;
(4)将两个溶液的溶质质量分数比较,确定A是否饱和,进而判断加入食盐后溶质质量是否会增大。
【解答】A.向m
g溶液B中加入x
g食盐,振荡后,溶液的质量不变,说明加入的x
g食盐没有溶解,溶液B是饱和溶液。设20℃时的食盐溶解度为S,
×100%=26.47%,解得S≈36g,则食盐在20℃时的溶解度为36g,不是36,故A错误;
B.因为A的浓度小于B,所以等质量的A、B中的溶剂质量:B<A,故B错误;
C.mg溶液B中的溶质质量为:?
,
故C错误;
D.溶液A不是饱和溶液,向m
g溶液A中加入x
g食盐,振荡后,会有食盐继续溶解,所以溶液的质量>m
g,故D正确。
故选D。
11.【答案】
A
【解析】【分析】根据溶质质量分数=可知,溶质质量偏小,要么是溶质质量偏小,要么是溶剂质量偏大,据此分析判断。
【解答】①称量的氯化钠固体中含有不溶性杂质,导致溶质质量偏小,故①符合题意;
②用量筒量取水时仰视读数,根据“俯视大仰视小”可知,读出的示数偏小,而实际量取的偏大,故②符合题意;
③往烧杯中加水时有水洒出,会导致溶剂质量偏小,溶质质量分数偏大,故③不合题意;
④将配制好的溶液装入试剂瓶中时有少量溅出,由于溶液均一稳定,所以不会影响溶质质量分数,故④不合题意。
那么导致溶质质量分数偏小的是①②。
故选A。
12.【答案】
B
【解析】【分析】(1)(2)如果溶液中出现未溶的固体,那么溶液肯定饱和;如果没有未溶的固体,那么溶液是否饱和无法判断;
(3)根据溶质质量分数=分析;
(4)剩余的固体越少,溶质质量越大。
【解答】根据图片可知,②中出现未溶的固体,那么肯定是饱和溶液;③中没有未溶的固体,那么是否饱和无法判断,故A正确不合题意,而B错误符合题意;
②中蔗糖有剩余,③中蔗糖完全溶解,那么溶质质量③>②,而溶剂质量相等,根据溶质质量分数=
,
二者的溶质质量分数不同,故C、D正确不合题意。
故选B。
?
13.【答案】
C
【解析】【分析】(1)在电解水的实验中,生成气体的体积是氧气体积的2倍;
(2)根据电解水的实验现象判断;
(3)根据图片确定反应前后原子的种类和个数是否改变;
(4)根据化学变化的本质判断。
【解答】A.根据图片可知,a试管内气体的体积大于b试管内气体体积,因此a气体为氢气,故A错误;
B.a、b试管中氢气和氧气的体积之比为2:1,故B错误;
C.根据示意图可知,水电解前后,氢原子都是4个,而氧原子都是2个,因此氢和氧原子的个数都没有变化,故C正确;
D.电解水的变化,其实是水分子分解为氢原子和氧原子,然后再结合成氢分子和氧分子的过程,故D错误。
故选C。
14.【答案】
C
【解析】【分析】根据水的组成、净化等知识分析判断。
【解答】A.电解水可以制取氢气和氧气,还可以利用水制取重水,重水是一种重要的核原料,因此水是一种化学资源,故A正确不合题意;
B.很多物质都能溶解在水中,因此水是一种常用溶剂,故B正确不合题意;
C.活性炭具有吸附性,在净水过程中起着吸附作用,不能消毒,故C错误符合题意;
D.水在通电的条件下分解得到两种新的物质,即氢气和氧气,故D正确不合题意。
故选C。
15.【答案】
B
【解析】【分析】根据化学反应前后元素种类不变分析即可。
【解答】水的蒸发、凝固和沸腾,都是水分子之间的间隙发生改变,而水分子本身没有发变化,无法证明水由氢和氧两种元素组成,故A、C、D错误;
水电解生成氢气和氧气,根据化学反应前后元素种类不变可知,水由氢和氧两种元素组成,故B正确。
故选B。
二、填空题
16.【答案】
(1)同
(2)气体溶解度随问温度的升高而减小
【解析】【分析】(1)根据电荷之间的相互作用规律分析解答;
(2)根据气体溶解度随温度变化的规律分析解答。
【解答】(1)在十燥的天气里,用塑料梳子梳头,发现头发越梳越蓬松,根据“同种电荷相互排斥”可知,这是因为梳头后头发带同种电荷。
(2)夏天的鱼塘里,常常出现鱼缺氧而“浮头”的现象,夏天水中缺氧的原因是:气体溶解度随温度的升高而减小?
。?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
三、解答题
17.【答案】
(1)由表可知,20℃对应的氯化钠溶液溶解度为36.0g,可计算得出该温度下饱和氯化纳溶液的济质质任分数为
所以该温度下不能制得溶质质量分数为30%的氯化钠溶液。
(2)蒸发溶剂
(3)20~30℃
【解析】【分析】(1)查表找到20℃时氯化钠的溶解度,然后根据计算出饱和溶液的溶质质量分数,最后与30%进行比较即可。
(2)海水经过风吹日晒后,其中的溶剂水会越来越少,当海水饱和时,其中的氯化钠就会结晶,据此分析结晶的方法;
(3)根据表格数据,分析哪两个温度之间二者的溶解度可能有重叠即可。
【解答】(1)由表可知,20℃对应的氯化钠溶液溶解度为36.0g,
该温度下饱和氯化纳溶液的济质质量分数为:??
?
;
所以该温度下不能制得溶质质量分数为30%的氯化钠溶液。
(2)人们把海水引入盐田,风吹日晒后,食盐就会结晶析出。这种从溶液中得到体的方法叫蒸发溶剂;
(3)根据表格可知,当温度低于20℃时,硝酸钾的溶解度大于氯化钠;当温度高于30℃时,硝酸钾的溶解度大于氯化钠,那么二者溶质质量分数可能相等的温度范围为:20~30℃。
(
第
1
页
共
3
页
)
…………○…………外…………○…………装…………○…………订…………○…………线…………○…………
)
(
※※请※※不※※要※※在※※装※※订※※线※※内※※答※※题※※
)
(
…………○…………内…………○…………装…………○…………订…………○…………线…………○…………
)
第1章
水
单元测试
姓名:__________
班级:__________考号:__________
一、单选题
1.地球上的水以各种形式分布在不同区域,下图为水的分布图,图中代表海洋水的是(
?)
A.?①?????????????????????????????????????????B.?②?????????????????????????????????????????C.?③?????????????????????????????????????????D.?④
2.下列有关水的说法正确的是(
??)
A.?明矾可促进水中悬浮杂质的沉降
B.?生活中常用蒸馏的方法降低水的硬度
C.?地球上总水储量很大,水资源不会短缺
D.?经自来水厂净化处理过的生活用水一定是软水
3.我国东部地区人均水资源拥有量随纬度变化情况如图所示。据此信息,下列有关该地区人均水资源拥有量的说法不正确的是(
??)
A.?低纬度地区较多???????B.?北纬40°附近最少???????C.?在空间上分布不均匀???????D.?随着纬度的升高而减少
4.杭州正在修建地铁,在它的四周围栏上而安装了大量的喷雾装置,可见很多的“白汽”,如图。这些“白汽”不断喷洒,不断消失,有关“白汽”的分析正确的是(????
)
A.?“白汽”是水蒸气?????B.?“消失”是汽化现象?????C.?“喷洒”是升华现象?????D.?“消失”时需要放热
5.下面叙述的四种产生“白气”的现象中,有一种“白气”产生的原因与其他几种都不一样,这一种“白气”是(????
)。
A.?夏天打开冰棒包装纸,常常会看到冰棒在冒“白气”
B.?冬天,户外的人嘴里不断冒出“白气”
C.?吸烟时,
嘴里喷出的“白气”
D.?夏天打开冰箱冷冻室的门,会冒出一股“白气”
6.如图所示为海波的熔化图像,根据图像,下列说法正确的是(?
)。
A.?海波开始熔化到全部熔化用时6min
B.?48?C时的海波是液态
C.?海波在CD段是气态
D.?海波在BC段温度不变,不需要加热
7.甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示.下列说法错误的是(???
)
A.?甲物质的溶解度大于乙物质的溶解度
B.?t2℃时,甲、乙两物质的饱和溶液中溶质的质量分数相等
C.?将t3℃时的甲乙两物质的饱和溶液降温到t2℃时都会析出晶体
D.?当甲物质中混有少量乙物质时,可采用冷却热饱和溶液的方法提纯甲
8.在一定温度下,将少量生石灰放入一定量的饱和石灰水中搅拌并冷却至原来温度,下列说法正确的是(???
)
A.?溶剂质量不变?????????????B.?溶质质量增加?????????????C.?溶解度变小?????????????D.?溶液中溶质质量分数不变
9.图1可表示“M与N的并列关系”,图2可表示“M属于N的从属关系”。下列概念间的关系符合图3所示关系的是(?????
)
X
Y
Z
A
脊髓
脑
周围神经系统
B
悬浊液
乳浊液
溶液
C
缩手反射
膝跳反射
非条件反射
D
饱和溶液
不饱和溶液
浓溶液
A.?A??????????????????????????????????????????B.?B
??????????????????????????????????????????C.?C??????????????????????????????????????????D.?D
10.20℃时,有质量分数为5%的食盐溶液A和质量分数为26.47%的食盐溶液B,下列有关A、B两种食盐溶液的判断正确的是(
??)
A.?向m
g溶液B中加入x
g食盐,振荡后,溶液的质量不变,则食盐在20℃时的溶解度为36
B.?等质量的A,B中,溶剂质量:B>A
C.?m
g溶液B中的溶质质量为
g
D.?向m
g溶液A中加入x
g食盐,振荡后,溶液的质量大于m
g
11.实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致其质量分数偏小的是(
??)
①称量的氯化钠固体中含有不溶性杂质;
②用量筒量取水时仰视读数;
③往烧杯中加水时有水洒出;
④将配制好的溶液装入试剂瓶中时有少量溅出。
A.?①②?????????????????????????????????????B.?①③?????????????????????????????????????C.?②④?????????????????????????????????????D.?③④
12.某次蔗糖溶解实验过程如图所示,不计水分蒸发,下列判断错误的是(
??)
A.?②中溶液是饱和溶液???????????????????????????????????????????B.?③中溶液一定是不饱和溶液
C.?②③中溶液的溶质质量分数不相同??????????????????????D.?③中溶液的溶质质量大于②中溶液的溶质质量
13.如图甲、乙是电解水的实验及电解时水分子分解的微观示意图。有关叙述正确的是(??
)
A.?a试管中产生的气体是氧气
B.?a、b试管中产生气体的质量比为2∶1
C.?水电解的过程中,氢原子数和氧原子数都没发生变化
D.?电解水的变化只是分子间的空隙发生了变化
14.水是生命之源。下列关于水的说法不正确的是(??
)
A.?水是一种化学资源??????????????????????????????????????????????B.?水是一种常用溶剂
C.?活性炭在净水过程中起着吸附和消毒作用???????????D.?水在通电的条件下分解得到两种新的物质
15.同学们对水进行研究,其中能确定水由氢和氧组成的是(
??)
A.?水的蒸发???????????????????????????B.?水的电解???????????????????????????C.?水的凝固???????????????????????????D.?水的沸腾
二、填空题
16.请你运用所学的科学知识回答生活中的问题。
(1)在十燥的天气里,用塑料梳子梳头,发现头发越梳越蓬松,这是因为梳头后头发带________(填“同”或“异”)种电荷。
(2)夏天的鱼塘里,常常出现鱼缺氧而“浮头”的现象,夏天水中缺氧的原因是________。
三、解答题
17.现有硝酸钾(KNO3)和氯化钠(NaCl)两种物质的溶解度数据如下表:
温度/℃
0
10
20
30
40
50
60
70
溶解度/g
NaCl
35.7
35.8
36.0
36.3
36.6
37.0
37.3
37.8
KNO3
13.3
20.9
31.6
45.8
45.8
85.5
110
138
(1)20℃时,能否制得溶质质量分数为30%的氯化钠溶液?请计算后说明。
(2)人们把海水引入盐田,风吹日晒后,食盐就会结晶析出。这种从溶液中得到体的方法叫________(填“蒸发溶剂”或“冷却热饱和溶液”)。
(3)有硝酸钾和氯化钠的饱和溶液各一杯,它们的温度、溶质质量分数都相同,则由表可知这两杯溶液的温度的最小范围是________。
答案解析部分
一、单选题
1.【答案】
A
【解析】【分析】地球上最多的水是海洋水,但海洋水不能食用,目前我国可直接利用的淡水资源,主要是江河、湖泊水和浅层地下水,应保护水资源。
【解答】海洋水在地球上所占比例为96.53%,A符合题意。
故答案为:A
?
2.【答案】
A
【解析】【分析】(1)根据水的净化的知识分析;
(2)根据蒸馏的作用分析;
(4)根据水资源的分布情况判断;
(4)根据硬水和软水的区别分析。
【解答】A.明矾溶于水形成的胶体具有吸附性,能将水中不溶性固体杂质吸附在其表面形成大颗粒,易于沉降,故A正确;
B.生活中常用加热煮沸的方法降低水的硬度,而不是蒸馏,故B错误;
C.地球上水的总储量很大,但是淡水储量很少,且分布不均匀,有些国家和地区水资源极度匮乏,故C错误;
D.经过自来水厂处理过的生活用水,其中可溶性的物质的量并没有多大变化,因此对水的硬度没有太大影响,故D错误。
故选A。
3.【答案】
D
【解析】【分析】条形图越高,说明人均水量越大;条形图越低,说明人均水量越少,据此分析判断。
【解答】A.根据图片可知,低纬度地区的条形图都比较高,即低纬度地区人均水资源拥有量较多,故A正确不合题意;?
B.北纬40°时条形图的高度最小,因此北纬40°附近人均水资源拥有量最少,故B正确不合题意;?
C.根据图像可知,人均水资源拥有量随纬度的不同而变化,因此在空间上分布不均匀,故C正确不合题意;
D.根据图片可知,人均水资源拥有量随着纬度的升高先减小后增大,故D错误符合题意。
故选D。
4.【答案】
B
【解析】【分析】物质由液态变成气态叫汽化,汽化需要吸热,据此分析判断。
【解答】“白汽”是小水珠,在空气中吸热后变成气态的水蒸气而消失,这是汽化现象,故B正确,而A、C、D错误。
故选B。
5.【答案】
C
【解析】【分析】从物态变化的角度对“白气”的成因进行分析即可。
【解答】A.夏天,冰棒的温度很低,水蒸气在冰棒周围放热,由气态变成液态的水发生液化现象,“白气”就是液化而成的小水珠;
B.冬天,人嘴里呼出的水蒸气温度较高,而户外的空气温度很低,此时水蒸气放热由气态变成液态的水发生液化现象,“白气”就是液化而成的小水珠;?
C.吸烟时,从嘴里冒出的“白气”是没有完全燃烧的固态小颗粒;?
D.夏天,打开冰箱门,里面的空气温度很低,而外面的空气温度很高,外面的水蒸气在冰箱门附近放热,由气态变成液态的水发生液化现象,而“白气”就是液化而成的小水珠。
那么与其它三个不同的是C。
故选C。
6.【答案】
A
【解析】【分析】(1)图像中横线对应的时间就是熔化时间;
(2)根据晶体在熔点时的状态分析;
(3)根据图像确定各个阶段海波的状态;
(4)根据晶体熔化的条件判断。
【解答】A.根据图像可知,海波6min时开始熔化,12min时熔化结束,那么熔化用的时间为:12min-6min=6min,故A正确;
B.48℃时海波的温度保持不变,那么这就是海波的熔点。如果熔化刚刚开始,那么海波为固态;如果熔化已经结束,那么海波为液态;如果熔化正在进行,那么海波为固液混合态,故B错误;
C.海波在AB段为固态,BC段为固液混合态,CD段为液态,故C错误;
D.海波在BC段温度不变,正在熔化,仍然需要不断加热,故D错误。
故选A。
7.【答案】
A
【解析】【分析】(1)谈到溶解度就必须说明温度,否则溶解度就没有意义;
(2)饱和溶液的溶质质量分数=;
(3)根据两种物质温度降低时溶解度的变化分析即可;
(4)如果物质的溶解度随温度变化明显,那么可以使用冷却热饱和溶液的方式结晶提纯。
【解答】A.温度低于t2时,甲的溶解度小于乙;温度高于t2时,甲的溶解度大于乙,故A错误符合题意;
B.t2℃时,甲和乙的溶解度相等,根据溶质质量分数=可知,二者的饱和溶液的溶质质量分数相等,故B正确不合题意;
C.甲和乙的溶解度都随温度的降低而减小,因此降温时二者的饱和溶液都有晶体析出,故C正确不合题意;
D.甲的溶解度随温度的变化十分明显,而乙的溶解度受温度的影响变化很小,因此利用冷却热饱和溶液的方法提纯甲,故D正确不合题意。
故选A。
8.【答案】
D
【解析】【分析】生石灰中的氧化钙与水反应,生成氢氧化钙;当温度不变时,同种物质的溶解度保持不变,那么饱和溶液的溶质质量分数保持不变,据此分析判断。
【解答】在一定温度下,将少量生石灰放入一定量的饱和石灰水中搅拌并冷却至原来温度。由于生石灰与水反应生成氢氧化钙,所以溶剂水的质量减小,故A错误;
石灰水原来就是饱和的,当溶剂质量减少时,肯定会有氢氧化钙析出,故B错误;
温度保持不变,那么石灰水的溶解度保持不变,故C错误;
因为石灰水的溶解度保持不变,且石灰水仍然饱和,那么溶液中溶质质量分数不变,故D正确。
故选D。
9.【答案】
C
【解析】【分析】非条件反射,是外界刺激与有机体反应之间与生俱来的固定神经联系。或在出生后发挥作用,或随着有机体的生长发育而出现。反射弧完整,在相应的刺激下,不需要后天的训练就能引起反射性反应,这类反射叫作非条件反射。
【解答】由图可知,X与Y是并列关系;X和Y都属于Z;
A、脊髓和脑是并列关系,但不属于周围神经系统;故A错误;
B、悬浊液和乳浊液是并列关系,但不属于溶液;故B错误;
C、缩手反射和膝跳反射是并列关系,都属于非条件反射;故C正确;
D、饱和溶液和不饱和溶液是并列关系,但不一定属于浓溶液;故D错误;
故答案为:C。
10.【答案】
D
【解析】【分析】(1)加入食盐后,溶液质量不变,说明加入的食盐没有溶解,即此时溶液饱和,然后根据饱和溶液的溶质质量分数=计算溶解度;
(2)根据溶液质量×溶质质量分数计算出溶质质量大小,再根据溶剂质量=溶液质量-溶剂质量比较即可;
(3)根据液质量×溶质质量分数计算出溶质质量大小;
(4)将两个溶液的溶质质量分数比较,确定A是否饱和,进而判断加入食盐后溶质质量是否会增大。
【解答】A.向m
g溶液B中加入x
g食盐,振荡后,溶液的质量不变,说明加入的x
g食盐没有溶解,溶液B是饱和溶液。设20℃时的食盐溶解度为S,
×100%=26.47%,解得S≈36g,则食盐在20℃时的溶解度为36g,不是36,故A错误;
B.因为A的浓度小于B,所以等质量的A、B中的溶剂质量:B<A,故B错误;
C.mg溶液B中的溶质质量为:?
,
故C错误;
D.溶液A不是饱和溶液,向m
g溶液A中加入x
g食盐,振荡后,会有食盐继续溶解,所以溶液的质量>m
g,故D正确。
故选D。
11.【答案】
A
【解析】【分析】根据溶质质量分数=可知,溶质质量偏小,要么是溶质质量偏小,要么是溶剂质量偏大,据此分析判断。
【解答】①称量的氯化钠固体中含有不溶性杂质,导致溶质质量偏小,故①符合题意;
②用量筒量取水时仰视读数,根据“俯视大仰视小”可知,读出的示数偏小,而实际量取的偏大,故②符合题意;
③往烧杯中加水时有水洒出,会导致溶剂质量偏小,溶质质量分数偏大,故③不合题意;
④将配制好的溶液装入试剂瓶中时有少量溅出,由于溶液均一稳定,所以不会影响溶质质量分数,故④不合题意。
那么导致溶质质量分数偏小的是①②。
故选A。
12.【答案】
B
【解析】【分析】(1)(2)如果溶液中出现未溶的固体,那么溶液肯定饱和;如果没有未溶的固体,那么溶液是否饱和无法判断;
(3)根据溶质质量分数=分析;
(4)剩余的固体越少,溶质质量越大。
【解答】根据图片可知,②中出现未溶的固体,那么肯定是饱和溶液;③中没有未溶的固体,那么是否饱和无法判断,故A正确不合题意,而B错误符合题意;
②中蔗糖有剩余,③中蔗糖完全溶解,那么溶质质量③>②,而溶剂质量相等,根据溶质质量分数=
,
二者的溶质质量分数不同,故C、D正确不合题意。
故选B。
?
13.【答案】
C
【解析】【分析】(1)在电解水的实验中,生成气体的体积是氧气体积的2倍;
(2)根据电解水的实验现象判断;
(3)根据图片确定反应前后原子的种类和个数是否改变;
(4)根据化学变化的本质判断。
【解答】A.根据图片可知,a试管内气体的体积大于b试管内气体体积,因此a气体为氢气,故A错误;
B.a、b试管中氢气和氧气的体积之比为2:1,故B错误;
C.根据示意图可知,水电解前后,氢原子都是4个,而氧原子都是2个,因此氢和氧原子的个数都没有变化,故C正确;
D.电解水的变化,其实是水分子分解为氢原子和氧原子,然后再结合成氢分子和氧分子的过程,故D错误。
故选C。
14.【答案】
C
【解析】【分析】根据水的组成、净化等知识分析判断。
【解答】A.电解水可以制取氢气和氧气,还可以利用水制取重水,重水是一种重要的核原料,因此水是一种化学资源,故A正确不合题意;
B.很多物质都能溶解在水中,因此水是一种常用溶剂,故B正确不合题意;
C.活性炭具有吸附性,在净水过程中起着吸附作用,不能消毒,故C错误符合题意;
D.水在通电的条件下分解得到两种新的物质,即氢气和氧气,故D正确不合题意。
故选C。
15.【答案】
B
【解析】【分析】根据化学反应前后元素种类不变分析即可。
【解答】水的蒸发、凝固和沸腾,都是水分子之间的间隙发生改变,而水分子本身没有发变化,无法证明水由氢和氧两种元素组成,故A、C、D错误;
水电解生成氢气和氧气,根据化学反应前后元素种类不变可知,水由氢和氧两种元素组成,故B正确。
故选B。
二、填空题
16.【答案】
(1)同
(2)气体溶解度随问温度的升高而减小
【解析】【分析】(1)根据电荷之间的相互作用规律分析解答;
(2)根据气体溶解度随温度变化的规律分析解答。
【解答】(1)在十燥的天气里,用塑料梳子梳头,发现头发越梳越蓬松,根据“同种电荷相互排斥”可知,这是因为梳头后头发带同种电荷。
(2)夏天的鱼塘里,常常出现鱼缺氧而“浮头”的现象,夏天水中缺氧的原因是:气体溶解度随温度的升高而减小?
。?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
三、解答题
17.【答案】
(1)由表可知,20℃对应的氯化钠溶液溶解度为36.0g,可计算得出该温度下饱和氯化纳溶液的济质质任分数为
所以该温度下不能制得溶质质量分数为30%的氯化钠溶液。
(2)蒸发溶剂
(3)20~30℃
【解析】【分析】(1)查表找到20℃时氯化钠的溶解度,然后根据计算出饱和溶液的溶质质量分数,最后与30%进行比较即可。
(2)海水经过风吹日晒后,其中的溶剂水会越来越少,当海水饱和时,其中的氯化钠就会结晶,据此分析结晶的方法;
(3)根据表格数据,分析哪两个温度之间二者的溶解度可能有重叠即可。
【解答】(1)由表可知,20℃对应的氯化钠溶液溶解度为36.0g,
该温度下饱和氯化纳溶液的济质质量分数为:??
?
;
所以该温度下不能制得溶质质量分数为30%的氯化钠溶液。
(2)人们把海水引入盐田,风吹日晒后,食盐就会结晶析出。这种从溶液中得到体的方法叫蒸发溶剂;
(3)根据表格可知,当温度低于20℃时,硝酸钾的溶解度大于氯化钠;当温度高于30℃时,硝酸钾的溶解度大于氯化钠,那么二者溶质质量分数可能相等的温度范围为:20~30℃。
(
第
1
页
共
3
页
)
同课章节目录
- 第1章 水
- 1 地球上的水
- 2 水的三态变化
- 3 水是常用的溶剂
- 4 配制溶液
- 5 水的组成
- 6 水资源的利用和保护
- 第2章 空气
- 1 空气的存在
- 2 空气的成分
- 3 氧气
- 4 二氧化碳
- 5 保护大气圈
- 第3章 阳光
- 1 太阳辐射能
- 2 阳光的传播
- 3 阳光的组成
- 第4章 土壤
- 1 土壤的组成和性状
- 2 土壤与植物
- 3 人类活动与土壤
- 第5章 生态系统
- 1 种群和群落
- 2 生态系统
- 3 生物圈
- 第6章 动物和人的生殖与发育
- 1 动物的生殖与发育
- 2 人的生殖与发育
- 第7章 植物和微生物的生殖与发育
- 1 绿色开花植物的有性生殖和发育
- 2 种子的萌发和幼苗形成
- 3 植物的无性生殖
- 4 细菌和真菌的繁殖
