3-4 离子晶体(1)离子晶体 课件(38张ppt) 2020-2021学年人教版高二化学选修3
文档属性
| 名称 | 3-4 离子晶体(1)离子晶体 课件(38张ppt) 2020-2021学年人教版高二化学选修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-12 00:00:00 | ||
图片预览





文档简介
晶体结构与性质
W:2021.4
第三章
学习
目标
2.了解离子晶体中离子晶体配位数及其影响因素
3.了解决定离子晶体结构的重要因素
重难点:
离子晶体配位数及其影响因素;
第四节 离子晶体
1.理解离子晶体的结构模型及其性质的一般特点
知识
回顾
1、什么是离子键?成键粒子是?
本质是静电作用;特点是没有方向性与饱和性,这是因为在静电作用能够达到的范围内,只要空间条件允许,一个离子可以同时吸引多个带相反电荷的离子。
活泼的金属元素和非金属元素间容易形成离子键;形成化合物的元素的电负性之差>1.7
2、离子键的本质和特点是什么?
相反电荷离子间的相互作用;成键粒子是阴离子和阳离子。
3、离子键的形成条件是什么?从电负性角度考虑,如何能形成离子键
晶体
氯化钠
干冰
金刚石
熔 点
(℃)
801
-56.2
3550
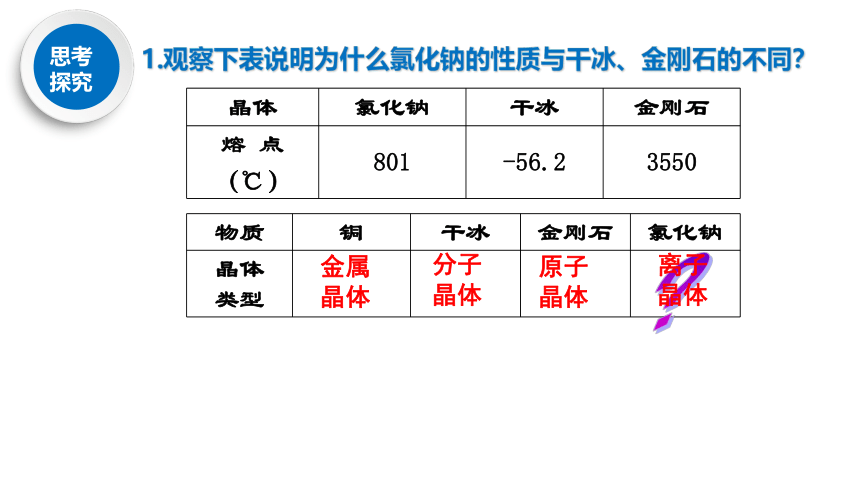
1.观察下表说明为什么氯化钠的性质与干冰、金刚石的不同?
思考探究
物质
铜
干冰
金刚石
氯化钠
晶体
类型
金属
晶体
分子
晶体
原子
晶体
?
离子晶体
2Na + Cl2 == 2NaCl
+11
+17
+17
+11
Na+ Cl-
Na
Cl
Cl-
Na+
观察
学习
1、离子晶体的定义
由阴、阳离子通过离子键结合而成的晶体
阴、阳离子
(1)构成微粒
阴、阳离子间是离子键,离子内可能有共价键或者配位键,如NaOH、NH4Cl
(2)微粒间相互作用
一、 离子晶体
2、离子晶体的结构特征
离子键无饱和性和方向性,在离子晶体中阴、阳离子尽可能与带相反电荷的离子接触采用最密堆积。
离子晶体无单个分子,其化学式表示阴、阳离子最简整数比,而不是分子组成,能把化学式称作分子式的只有分子晶体。
1.下列叙述中正确的是( )
A.带相反电荷离子之间的相互吸引称为离子键
B.金属元素与非金属元素化合时,不一定形成离子键
C.某元素的原子最外层只有一个电子,它跟卤素结合时所形成的化学键不一定是离子键
D.非金属原子间不可能形成离子键,只含有非金属元素的化合物不可能是离子化合物
E.离子化合物中一定含有金属元素,含金属元素的化合物一定是离子化合物
F.离子键只存在于离子化合物中,离子化合物中一定含有离子键不可能含有非极性键
G.离子化合物受热熔化破坏化学键,吸收热量,属于化学变化。
BC
课堂
练习
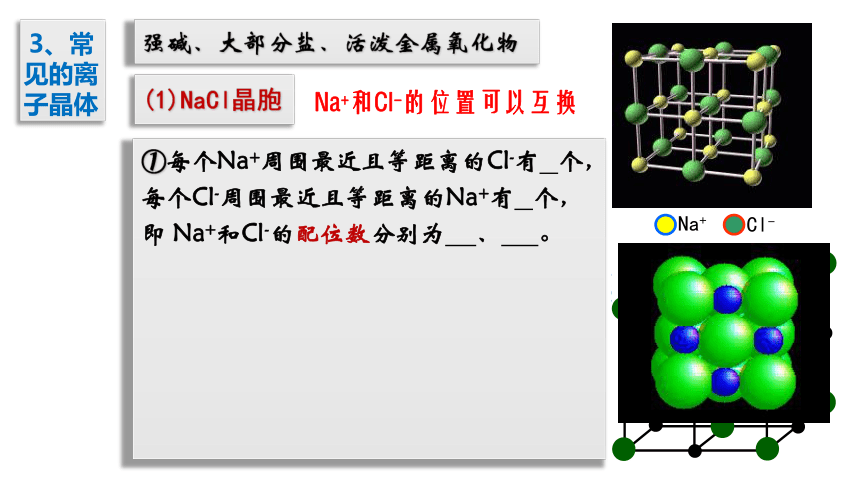
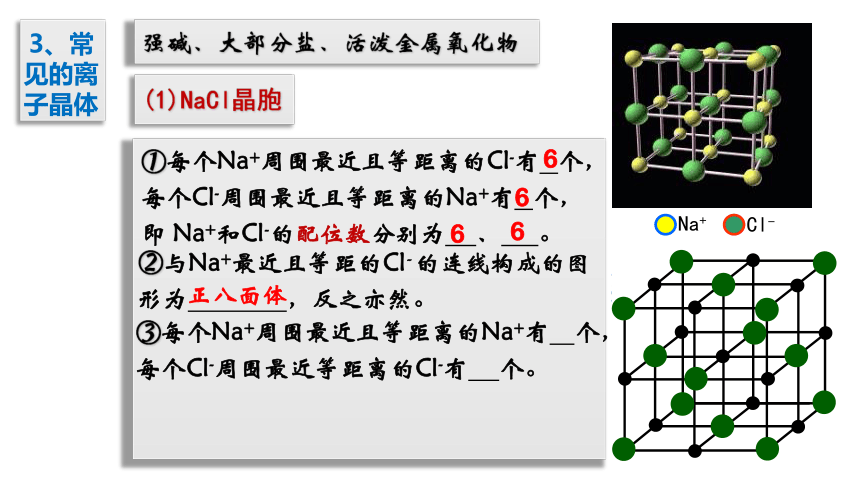
3、常见的离子晶体
强碱、大部分盐、活泼金属氧化物
(1)NaCl晶胞
Na+
Cl-
①每个Na+周围最近且等距离的Cl-有 个,每个Cl-周围最近且等距离的Na+有 个,即 Na+和Cl-的配位数分别为 、 。
思考:模型中Na+和Cl-各在什么位置?
Cl-:体心和棱上;
Na+:面心和顶点.
Na+和Cl-的位置可以互换
---Cl-
--- Na+
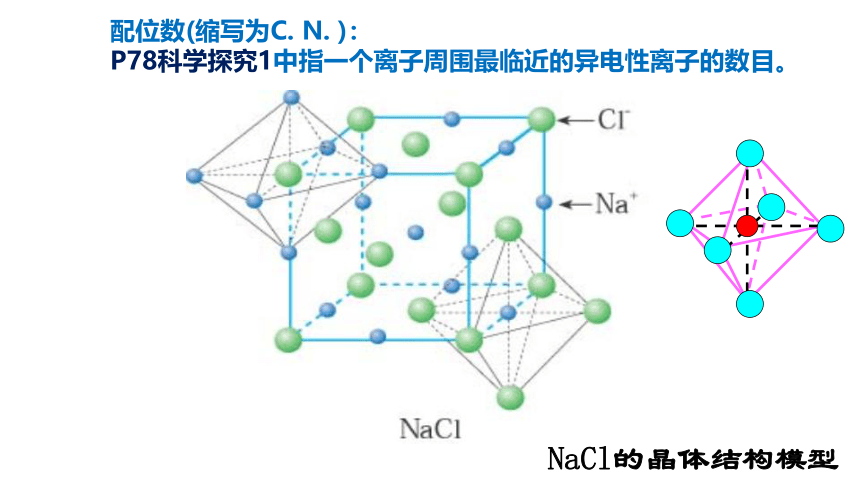
NaCl的晶体结构模型
配位数(缩写为C. N. ):
P78科学探究1中指一个离子周围最临近的异电性离子的数目。
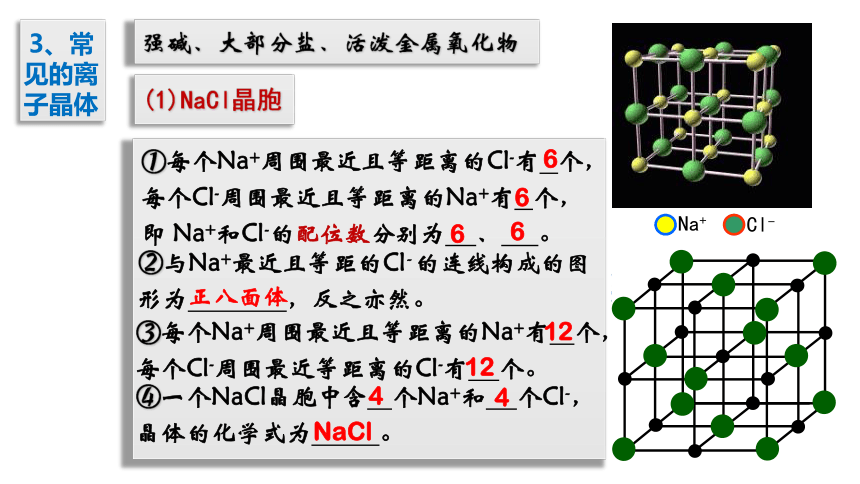
3、常见的离子晶体
强碱、大部分盐、活泼金属氧化物
(1)NaCl晶胞
Na+
Cl-
①每个Na+周围最近且等距离的Cl-有 个,每个Cl-周围最近且等距离的Na+有 个,即 Na+和Cl-的配位数分别为 、 。
思考:模型中Na+和Cl-各在什么位置?
Cl-:体心和棱上;
Na+:面心和顶点.
6
6
6
6
②与Na+最近且等距的Cl- 的连线构成的图形为 ,反之亦然。
正八面体
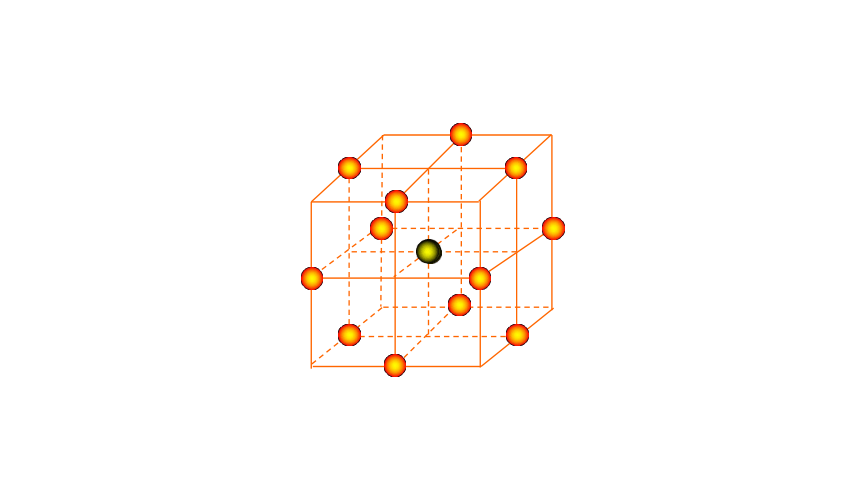
③每个Na+周围最近且等距离的Na+有 个,每个Cl-周围最近等距离的Cl-有 个。
3、常见的离子晶体
强碱、大部分盐、活泼金属氧化物
(1)NaCl晶胞
Na+
Cl-
①每个Na+周围最近且等距离的Cl-有 个,每个Cl-周围最近且等距离的Na+有 个,即 Na+和Cl-的配位数分别为 、 。
思考:模型中Na+和Cl-各在什么位置?
Cl-:体心和棱上;
Na+:面心和顶点.
6
6
6
6
②与Na+最近且等距的Cl- 的连线构成的图形为 ,反之亦然。
正八面体
③每个Na+周围最近且等距离的Na+有 个,每个Cl-周围最近等距离的Cl-有 个。
12
12
④一个NaCl晶胞中含 个Na+和 个Cl-, 晶体的化学式为 。
4
4
NaCl
3、常见的离子晶体
(2)CsCl晶胞
①每个Cs+周围最近且等距离的Cl-有 个,每个Cl-周围最近且等距离的Cs+有 个,即 Cs+和Cl-的配位数分别为 、 。
Cl-
Cs+
Cs+和Cl-的位置可以互换
---Cs+
---Cl-
CsCl的晶体结构及晶胞构示意图
3、常见的离子晶体
(2)CsCl晶胞
①每个Cs+周围最近且等距离的Cl-有 个,每个Cl-周围最近且等距离的Cs+有 个,即 Cs+和Cl-的配位数分别为 、 。
8
8
8
8
②每个Cs+周围最近且等距离的Cs+有 个,每个Cl-周围最近等距离的Cl-有 个。
Cl-
Cs+
3、常见的离子晶体
(2)CsCl晶胞
①每个Cs+周围最近且等距离的Cl-有 个,每个Cl-周围最近且等距离的Cs+有 个,即 Cs+和Cl-的配位数分别为 、 。
8
8
8
8
②每个Cs+周围最近且等距离的Cs+有 个,每个Cl-周围最近等距离的Cl-有 个。
6
6
③一个CsCl晶胞中含 个Cs+和 个Cl-, 晶体的化学式为 。
1
1
CsCl
Cl-
Cs+
3、常见的离子晶体
(3)CaF2(萤石)晶胞
3、常见的离子晶体
(3)CaF2(萤石)晶胞
①每个Ca2+周围最近且等距离的F-有 个,每个F-周围最近且等距离的Ca2+有 个,即 Ca2+和F-的配位数分别为 、 。
8
4
8
4
②每个Ca2+周围最近且等距离的Ca2+有 个,每个F-周围最近等距离的F-有 个。
12
6
③一个CaF2晶胞中含 个Ca2+和 个F-, 晶体的化学式为 。
4
8
CaF2
Ca2+
F-
白色的为Zn2+ 黑色的为S2-
3、常见的离子晶体
(4)ZnS 晶胞
①Zn2+和S2-的配位数分别为 、 。
4
4
②一个ZnS晶胞中含 个Zn2+和 个S2-。
4
4
配位数
4
6
8
离子晶体
ZnS
NaCl
CsCl
半径比
0.2~0.4
0.4~0.7
0.7~1.0
3. 根据教材79页表3-5、表3-6和以上数据,你得出影响离子晶体结构的因素是什么?这个因素对离子晶体的配位数有何影响?
2.在氯化钠、氯化铯、硫化锌晶体中阳离子和阴离子的个数比都是1:1,它们的晶胞结构是否相同?阴、阳离子的配位数分别为多少?
思考探究
结论:晶体中正负离子的的半径比(r+/r-)是决定离子晶体结构的重要因素,简称几何因素。
一般情况下:正负离子的半径比越大,配位数越多.
4.阅读教材79页除开科学视野倒数第2段:为什么在氯化钠、氯化铯、硫化锌晶体阴、阳离子的配位数分别是相同的?为什么在氟化钙中阴离子和阳离子的配位数不同?
4、决定离子晶体结构的因素
晶体中正负离子的半径比(r+/r-),一般半径比越大,配位数越多。
(1)几何因素
思考探究
晶体中正负离子的电荷相同,配位数就相同,晶体中正负离子的电荷数不同,配位数就不会相同。
(2)电荷因素
正负离子电荷比=正负离子配位数比
=正负离子数目反比
离子键的纯粹程度。
(3)键性因素
5、离子晶体的性质
离子晶体熔化时破坏的作用力是 。
(1)熔沸点较高,硬度较大,难挥发,难压缩
5.阅读课本79页最后一段(即科学视野之前的一段),结合学过的离子晶体的结构,你认为离子晶体物理性质有何特点?
思考探究
离子键
大多数离子晶体易溶于极性溶剂如水,难溶于非极性溶剂。
(2)溶解性
固态不导电,熔融状态或者溶于水能导电。
(3)导电性
为什么?
离子晶体内无自由移动的离子,熔化或溶于水后阴阳离子能自由移动
如何比较离子晶体熔沸点的高低?
离子半径越小,离子电荷越多,离子键越强,离子晶体的熔沸点越高。
2.离子晶体不可能具有的性质是( )
A.较高的熔、沸点 B.良好的导电性
C.溶于极性溶剂 D.坚硬而易粉碎
B
课堂
练习
3.下列变化不需要破坏化学键的是( )
A.加热氯化铵 B.干冰升华
C.水通电分解 D.硫酸钠溶于水
B
4.下列性质适合于离子晶体的是( )
A.熔点1070℃,易溶于水,水溶液能导电
B.熔点10.31℃,液态不导电,水溶液导电
C.能溶于CS2,熔点112.8℃,沸点444.6℃
D.熔点97.81℃,质软,导电,密度0.97g/cm3
A
各类型离子晶体晶胞的比较
晶体类型
晶胞类型
晶胞结构示意图
配位数
距离最近且相等的同种离子
每个晶胞含有离子数
实例
NaCl型
AB
CsCl型
ZnS型
AB2
CaF2型
Na+:
6
Cl-:
6
Cs+:
Cl-:
8
8
Zn2+:
S2-:
4
4
Ca2+:
F-:
4
8
Na+:
Cl-:
Cs+:
Cl-:
Ca2+:
F-:
Na+:
Cl-:
Cs+:
Cl-:
Zn2+:
S2-:
Ca2+:
F-:
12
12
6
6
6
12
4
4
1
1
4
4
8
4
KBr AgCl、MgO、CaS、BaSe
ZnS、AgI、
BeO
CsCl、CsBr、CsI、TlCl
碱土金属卤化物、碱金属氧化物。
课堂
小结
离子晶体
原子晶体
分子晶体
金属晶体
存在微粒
阴阳离子
原子
分子
金属离子、自由电子
微粒间作用
离子键
共价键
范德华力
金属键
主要性质
硬而脆,易溶于极性溶剂,熔化时能够导电,溶沸点高
质地硬,不溶于大多数溶剂,导电性差,熔沸点很高
硬度小,水溶液能够导电,溶沸点低
金属光泽,是电和热的良导体,熔沸点高或低
实例
食盐晶体
金刚石
氨、氯化氢
镁、铝
各种晶体类型的比较
课堂
小结
5、下列各指定微粒的数目之比不是1:1的是( )
A、Na2O2晶体中的阴离子和阳离子
B、NaHCO3晶体中的钠离子和碳酸氢根离子
C、 离子中的质子和中子
D、氟化钙晶胞中阴、阳离子配位数之比
A
课堂
练习
6、在氯化钠晶体中,与每个Na+等距离且最近的几个Cl-所围成的空间几何构型( )
A、十二面体 B、正八面体
C、正六面体 D、正四面体
B
D
7、离子晶体中一定不存在的相互作用力是( )
A.离子键 B.极性键
C.非极性键 D.范德华力
B
课堂
练习
9、下列晶体中,熔点最高的是( )
A.KF B.MgO
C.CaO D.NaCl
B
8、 ①NaF ②NaI ③MgO均为离子化合物,根据以下数据,推知这三种化合物的熔点的高低顺序是( )
物质
①
②
③
离子电荷数
1
1
2
键长(10-10m)
2.31
3.18
2.10
A.①>②>③ B.③>①>②
C.③>②>① D.②>①>③
10、下面图像是从NaCl或CsCl晶体结构图中分割出来的部分结构图,试判断属于NaCl晶体结构的是( )
(1) (2)
(3) (4)
A.①和③ B.②和③
C.①和④ D.只有①
C
课堂
练习
课堂
练习
[Ar]3d10
sp、sp2
3
4
(3)CaC2晶体的晶胞结构与NaCl晶体的相似(如右图所示),但CaC2晶体中含有的中哑铃形C22-的存在,使晶胞沿一个方向拉长.CaC2晶体中1个Ca2+周围距离最近的C22-数目为___.
11、乙炔是有机合成工业的一种原料.工业上曾用CaC2与水反应生成乙炔.
(1)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀.Cu+基态核外电子排布式为______.
(2)乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N).丙烯腈分子中碳原子轨道杂化类型是______;分子中处于同一直线上的原子数目最多为____.
1
2
3
4
5
6
8
7
8
12、中学教材上图示的NaCl晶体结构,它向三维空间延伸得到完美晶体。NiO晶体结构与NaCl相同,Ni2+与邻近的O2-核间距为a×10-8 ㎝,计算NiO晶体密度(已知NiO摩尔质量为74.7g·mol-1)
解:在该晶体中最小正方体中所含的
Ni2+、O2-个数均为:
即晶体中每个小正方体中平均含有1/2个
NiO.其质量为:
而此小正方体体积为(a×10-8㎝)3
故NiO晶体密度为:
74.7g
6.02×1023
×
1
2
(个)
1
2
4×
1
8
=
74.7g
6.02×1023
×
1
2
(a×10-8㎝)3
g. ㎝-3
62.0
a3
=
课堂
练习
13、(1)NiO晶体结构与NaCl相同,设NiO的摩尔质量M g/mol,密度为ρg/mL,阿伏加德罗常数为NA,求晶胞中两个距离最近的氧离子中心间的距离为多少cm?
解题思路:(1)每个晶胞中含NiO的个数(2)一个晶胞的质量(3)一个晶胞的体积(4)晶胞的边长(5)晶胞中任一个面对角线长度的一半
课堂
练习
(2)天然的和大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在以下缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代。其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。某氧化镍样品组成为Ni0.97O,试计算该晶体中Ni3+与Ni2+的离子数之比。
参考答案: Ni3+ :Ni2+=6 :91
分析:本题命题角度较新颖,实际上难度不大,第(2)题所提供的Ni0.97O信息,实际上是一种“平均化学式”。尽管题给示意图及题目叙述中提到了有“Ni2+”空缺,但“Ni0.97O”的平均化学式与所述的“空缺”无关,它只是遵循着电中性原则,即由于掺杂多带一个电荷的Ni3+代替了部分Ni2+ ,才使“NiO”变成了“Ni0.97O”。
课堂
练习
(2)0.97 mol的镍离子的平均带电量为2,那么1 mol镍离子的平均带电量为2/0.97,这是+2和+3价的镍离子的共同电量,由此可列方程式。不同于上解的是,这种做法将0.97 mol镍离子化为1 mol镍离子来计算。
解法一:
设1molNi中含Ni2+ x mol,则含Ni3+(1-x)mol,
根据电荷守恒: 2x+3(1-x)=2/0.97
x=91/97
n(Ni3+): n(Ni2+)=(1-91/97)∶91/97=6∶91
解法二:因为中Nio.97O中既有+2价的离子又有+3价的镍离子,所以可写成xNiO·yNi2O3的复合形式,该形式中很容易看出镍离子的总和为x+2y,氧离子的总和为x+3y,因此可列方程如下:
(1):x+2y=0.97 镍离子个数守恒
x+3y=1 氧离子个数守恒
(2):(x+2y )/(x+3y)=0.97/1 同样可以求出三价镍与二价镍离子数目之比。
课堂
练习
演示结束. 感谢聆听
2021
W:2021.4
第三章
学习
目标
2.了解离子晶体中离子晶体配位数及其影响因素
3.了解决定离子晶体结构的重要因素
重难点:
离子晶体配位数及其影响因素;
第四节 离子晶体
1.理解离子晶体的结构模型及其性质的一般特点
知识
回顾
1、什么是离子键?成键粒子是?
本质是静电作用;特点是没有方向性与饱和性,这是因为在静电作用能够达到的范围内,只要空间条件允许,一个离子可以同时吸引多个带相反电荷的离子。
活泼的金属元素和非金属元素间容易形成离子键;形成化合物的元素的电负性之差>1.7
2、离子键的本质和特点是什么?
相反电荷离子间的相互作用;成键粒子是阴离子和阳离子。
3、离子键的形成条件是什么?从电负性角度考虑,如何能形成离子键
晶体
氯化钠
干冰
金刚石
熔 点
(℃)
801
-56.2
3550
1.观察下表说明为什么氯化钠的性质与干冰、金刚石的不同?
思考探究
物质
铜
干冰
金刚石
氯化钠
晶体
类型
金属
晶体
分子
晶体
原子
晶体
?
离子晶体
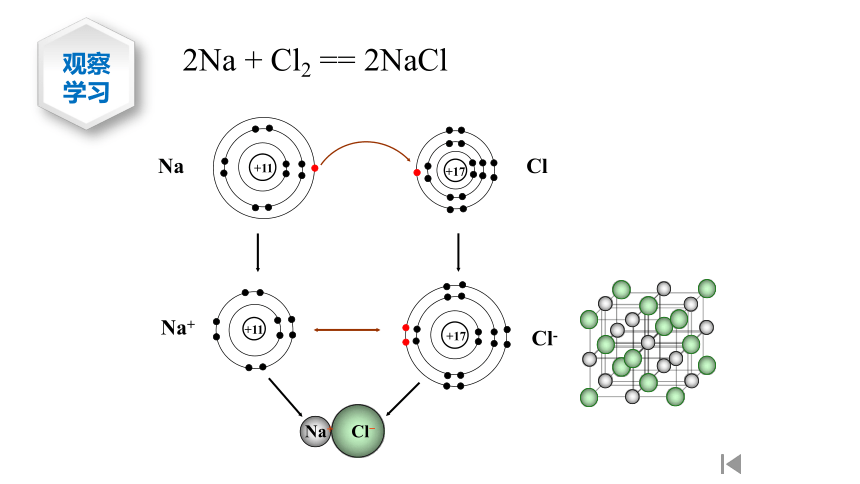
2Na + Cl2 == 2NaCl
+11
+17
+17
+11
Na+ Cl-
Na
Cl
Cl-
Na+
观察
学习
1、离子晶体的定义
由阴、阳离子通过离子键结合而成的晶体
阴、阳离子
(1)构成微粒
阴、阳离子间是离子键,离子内可能有共价键或者配位键,如NaOH、NH4Cl
(2)微粒间相互作用
一、 离子晶体
2、离子晶体的结构特征
离子键无饱和性和方向性,在离子晶体中阴、阳离子尽可能与带相反电荷的离子接触采用最密堆积。
离子晶体无单个分子,其化学式表示阴、阳离子最简整数比,而不是分子组成,能把化学式称作分子式的只有分子晶体。
1.下列叙述中正确的是( )
A.带相反电荷离子之间的相互吸引称为离子键
B.金属元素与非金属元素化合时,不一定形成离子键
C.某元素的原子最外层只有一个电子,它跟卤素结合时所形成的化学键不一定是离子键
D.非金属原子间不可能形成离子键,只含有非金属元素的化合物不可能是离子化合物
E.离子化合物中一定含有金属元素,含金属元素的化合物一定是离子化合物
F.离子键只存在于离子化合物中,离子化合物中一定含有离子键不可能含有非极性键
G.离子化合物受热熔化破坏化学键,吸收热量,属于化学变化。
BC
课堂
练习
3、常见的离子晶体
强碱、大部分盐、活泼金属氧化物
(1)NaCl晶胞
Na+
Cl-
①每个Na+周围最近且等距离的Cl-有 个,每个Cl-周围最近且等距离的Na+有 个,即 Na+和Cl-的配位数分别为 、 。
思考:模型中Na+和Cl-各在什么位置?
Cl-:体心和棱上;
Na+:面心和顶点.
Na+和Cl-的位置可以互换
---Cl-
--- Na+
NaCl的晶体结构模型
配位数(缩写为C. N. ):
P78科学探究1中指一个离子周围最临近的异电性离子的数目。
3、常见的离子晶体
强碱、大部分盐、活泼金属氧化物
(1)NaCl晶胞
Na+
Cl-
①每个Na+周围最近且等距离的Cl-有 个,每个Cl-周围最近且等距离的Na+有 个,即 Na+和Cl-的配位数分别为 、 。
思考:模型中Na+和Cl-各在什么位置?
Cl-:体心和棱上;
Na+:面心和顶点.
6
6
6
6
②与Na+最近且等距的Cl- 的连线构成的图形为 ,反之亦然。
正八面体
③每个Na+周围最近且等距离的Na+有 个,每个Cl-周围最近等距离的Cl-有 个。
3、常见的离子晶体
强碱、大部分盐、活泼金属氧化物
(1)NaCl晶胞
Na+
Cl-
①每个Na+周围最近且等距离的Cl-有 个,每个Cl-周围最近且等距离的Na+有 个,即 Na+和Cl-的配位数分别为 、 。
思考:模型中Na+和Cl-各在什么位置?
Cl-:体心和棱上;
Na+:面心和顶点.
6
6
6
6
②与Na+最近且等距的Cl- 的连线构成的图形为 ,反之亦然。
正八面体
③每个Na+周围最近且等距离的Na+有 个,每个Cl-周围最近等距离的Cl-有 个。
12
12
④一个NaCl晶胞中含 个Na+和 个Cl-, 晶体的化学式为 。
4
4
NaCl
3、常见的离子晶体
(2)CsCl晶胞
①每个Cs+周围最近且等距离的Cl-有 个,每个Cl-周围最近且等距离的Cs+有 个,即 Cs+和Cl-的配位数分别为 、 。
Cl-
Cs+
Cs+和Cl-的位置可以互换
---Cs+
---Cl-
CsCl的晶体结构及晶胞构示意图
3、常见的离子晶体
(2)CsCl晶胞
①每个Cs+周围最近且等距离的Cl-有 个,每个Cl-周围最近且等距离的Cs+有 个,即 Cs+和Cl-的配位数分别为 、 。
8
8
8
8
②每个Cs+周围最近且等距离的Cs+有 个,每个Cl-周围最近等距离的Cl-有 个。
Cl-
Cs+
3、常见的离子晶体
(2)CsCl晶胞
①每个Cs+周围最近且等距离的Cl-有 个,每个Cl-周围最近且等距离的Cs+有 个,即 Cs+和Cl-的配位数分别为 、 。
8
8
8
8
②每个Cs+周围最近且等距离的Cs+有 个,每个Cl-周围最近等距离的Cl-有 个。
6
6
③一个CsCl晶胞中含 个Cs+和 个Cl-, 晶体的化学式为 。
1
1
CsCl
Cl-
Cs+
3、常见的离子晶体
(3)CaF2(萤石)晶胞
3、常见的离子晶体
(3)CaF2(萤石)晶胞
①每个Ca2+周围最近且等距离的F-有 个,每个F-周围最近且等距离的Ca2+有 个,即 Ca2+和F-的配位数分别为 、 。
8
4
8
4
②每个Ca2+周围最近且等距离的Ca2+有 个,每个F-周围最近等距离的F-有 个。
12
6
③一个CaF2晶胞中含 个Ca2+和 个F-, 晶体的化学式为 。
4
8
CaF2
Ca2+
F-
白色的为Zn2+ 黑色的为S2-
3、常见的离子晶体
(4)ZnS 晶胞
①Zn2+和S2-的配位数分别为 、 。
4
4
②一个ZnS晶胞中含 个Zn2+和 个S2-。
4
4
配位数
4
6
8
离子晶体
ZnS
NaCl
CsCl
半径比
0.2~0.4
0.4~0.7
0.7~1.0
3. 根据教材79页表3-5、表3-6和以上数据,你得出影响离子晶体结构的因素是什么?这个因素对离子晶体的配位数有何影响?
2.在氯化钠、氯化铯、硫化锌晶体中阳离子和阴离子的个数比都是1:1,它们的晶胞结构是否相同?阴、阳离子的配位数分别为多少?
思考探究
结论:晶体中正负离子的的半径比(r+/r-)是决定离子晶体结构的重要因素,简称几何因素。
一般情况下:正负离子的半径比越大,配位数越多.
4.阅读教材79页除开科学视野倒数第2段:为什么在氯化钠、氯化铯、硫化锌晶体阴、阳离子的配位数分别是相同的?为什么在氟化钙中阴离子和阳离子的配位数不同?
4、决定离子晶体结构的因素
晶体中正负离子的半径比(r+/r-),一般半径比越大,配位数越多。
(1)几何因素
思考探究
晶体中正负离子的电荷相同,配位数就相同,晶体中正负离子的电荷数不同,配位数就不会相同。
(2)电荷因素
正负离子电荷比=正负离子配位数比
=正负离子数目反比
离子键的纯粹程度。
(3)键性因素
5、离子晶体的性质
离子晶体熔化时破坏的作用力是 。
(1)熔沸点较高,硬度较大,难挥发,难压缩
5.阅读课本79页最后一段(即科学视野之前的一段),结合学过的离子晶体的结构,你认为离子晶体物理性质有何特点?
思考探究
离子键
大多数离子晶体易溶于极性溶剂如水,难溶于非极性溶剂。
(2)溶解性
固态不导电,熔融状态或者溶于水能导电。
(3)导电性
为什么?
离子晶体内无自由移动的离子,熔化或溶于水后阴阳离子能自由移动
如何比较离子晶体熔沸点的高低?
离子半径越小,离子电荷越多,离子键越强,离子晶体的熔沸点越高。
2.离子晶体不可能具有的性质是( )
A.较高的熔、沸点 B.良好的导电性
C.溶于极性溶剂 D.坚硬而易粉碎
B
课堂
练习
3.下列变化不需要破坏化学键的是( )
A.加热氯化铵 B.干冰升华
C.水通电分解 D.硫酸钠溶于水
B
4.下列性质适合于离子晶体的是( )
A.熔点1070℃,易溶于水,水溶液能导电
B.熔点10.31℃,液态不导电,水溶液导电
C.能溶于CS2,熔点112.8℃,沸点444.6℃
D.熔点97.81℃,质软,导电,密度0.97g/cm3
A
各类型离子晶体晶胞的比较
晶体类型
晶胞类型
晶胞结构示意图
配位数
距离最近且相等的同种离子
每个晶胞含有离子数
实例
NaCl型
AB
CsCl型
ZnS型
AB2
CaF2型
Na+:
6
Cl-:
6
Cs+:
Cl-:
8
8
Zn2+:
S2-:
4
4
Ca2+:
F-:
4
8
Na+:
Cl-:
Cs+:
Cl-:
Ca2+:
F-:
Na+:
Cl-:
Cs+:
Cl-:
Zn2+:
S2-:
Ca2+:
F-:
12
12
6
6
6
12
4
4
1
1
4
4
8
4
KBr AgCl、MgO、CaS、BaSe
ZnS、AgI、
BeO
CsCl、CsBr、CsI、TlCl
碱土金属卤化物、碱金属氧化物。
课堂
小结
离子晶体
原子晶体
分子晶体
金属晶体
存在微粒
阴阳离子
原子
分子
金属离子、自由电子
微粒间作用
离子键
共价键
范德华力
金属键
主要性质
硬而脆,易溶于极性溶剂,熔化时能够导电,溶沸点高
质地硬,不溶于大多数溶剂,导电性差,熔沸点很高
硬度小,水溶液能够导电,溶沸点低
金属光泽,是电和热的良导体,熔沸点高或低
实例
食盐晶体
金刚石
氨、氯化氢
镁、铝
各种晶体类型的比较
课堂
小结
5、下列各指定微粒的数目之比不是1:1的是( )
A、Na2O2晶体中的阴离子和阳离子
B、NaHCO3晶体中的钠离子和碳酸氢根离子
C、 离子中的质子和中子
D、氟化钙晶胞中阴、阳离子配位数之比
A
课堂
练习
6、在氯化钠晶体中,与每个Na+等距离且最近的几个Cl-所围成的空间几何构型( )
A、十二面体 B、正八面体
C、正六面体 D、正四面体
B
D
7、离子晶体中一定不存在的相互作用力是( )
A.离子键 B.极性键
C.非极性键 D.范德华力
B
课堂
练习
9、下列晶体中,熔点最高的是( )
A.KF B.MgO
C.CaO D.NaCl
B
8、 ①NaF ②NaI ③MgO均为离子化合物,根据以下数据,推知这三种化合物的熔点的高低顺序是( )
物质
①
②
③
离子电荷数
1
1
2
键长(10-10m)
2.31
3.18
2.10
A.①>②>③ B.③>①>②
C.③>②>① D.②>①>③
10、下面图像是从NaCl或CsCl晶体结构图中分割出来的部分结构图,试判断属于NaCl晶体结构的是( )
(1) (2)
(3) (4)
A.①和③ B.②和③
C.①和④ D.只有①
C
课堂
练习
课堂
练习
[Ar]3d10
sp、sp2
3
4
(3)CaC2晶体的晶胞结构与NaCl晶体的相似(如右图所示),但CaC2晶体中含有的中哑铃形C22-的存在,使晶胞沿一个方向拉长.CaC2晶体中1个Ca2+周围距离最近的C22-数目为___.
11、乙炔是有机合成工业的一种原料.工业上曾用CaC2与水反应生成乙炔.
(1)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀.Cu+基态核外电子排布式为______.
(2)乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N).丙烯腈分子中碳原子轨道杂化类型是______;分子中处于同一直线上的原子数目最多为____.
1
2
3
4
5
6
8
7
8
12、中学教材上图示的NaCl晶体结构,它向三维空间延伸得到完美晶体。NiO晶体结构与NaCl相同,Ni2+与邻近的O2-核间距为a×10-8 ㎝,计算NiO晶体密度(已知NiO摩尔质量为74.7g·mol-1)
解:在该晶体中最小正方体中所含的
Ni2+、O2-个数均为:
即晶体中每个小正方体中平均含有1/2个
NiO.其质量为:
而此小正方体体积为(a×10-8㎝)3
故NiO晶体密度为:
74.7g
6.02×1023
×
1
2
(个)
1
2
4×
1
8
=
74.7g
6.02×1023
×
1
2
(a×10-8㎝)3
g. ㎝-3
62.0
a3
=
课堂
练习
13、(1)NiO晶体结构与NaCl相同,设NiO的摩尔质量M g/mol,密度为ρg/mL,阿伏加德罗常数为NA,求晶胞中两个距离最近的氧离子中心间的距离为多少cm?
解题思路:(1)每个晶胞中含NiO的个数(2)一个晶胞的质量(3)一个晶胞的体积(4)晶胞的边长(5)晶胞中任一个面对角线长度的一半
课堂
练习
(2)天然的和大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在以下缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代。其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。某氧化镍样品组成为Ni0.97O,试计算该晶体中Ni3+与Ni2+的离子数之比。
参考答案: Ni3+ :Ni2+=6 :91
分析:本题命题角度较新颖,实际上难度不大,第(2)题所提供的Ni0.97O信息,实际上是一种“平均化学式”。尽管题给示意图及题目叙述中提到了有“Ni2+”空缺,但“Ni0.97O”的平均化学式与所述的“空缺”无关,它只是遵循着电中性原则,即由于掺杂多带一个电荷的Ni3+代替了部分Ni2+ ,才使“NiO”变成了“Ni0.97O”。
课堂
练习
(2)0.97 mol的镍离子的平均带电量为2,那么1 mol镍离子的平均带电量为2/0.97,这是+2和+3价的镍离子的共同电量,由此可列方程式。不同于上解的是,这种做法将0.97 mol镍离子化为1 mol镍离子来计算。
解法一:
设1molNi中含Ni2+ x mol,则含Ni3+(1-x)mol,
根据电荷守恒: 2x+3(1-x)=2/0.97
x=91/97
n(Ni3+): n(Ni2+)=(1-91/97)∶91/97=6∶91
解法二:因为中Nio.97O中既有+2价的离子又有+3价的镍离子,所以可写成xNiO·yNi2O3的复合形式,该形式中很容易看出镍离子的总和为x+2y,氧离子的总和为x+3y,因此可列方程如下:
(1):x+2y=0.97 镍离子个数守恒
x+3y=1 氧离子个数守恒
(2):(x+2y )/(x+3y)=0.97/1 同样可以求出三价镍与二价镍离子数目之比。
课堂
练习
演示结束. 感谢聆听
2021
