3.1物质的转化(第三课时)
图片预览






文档简介
(共19张PPT)
第三章 物质的转化和
元素的循环
&1.物质的转化
复习回忆
写出下列有关化学方程式:
1、铜丝在空气中加热
2、氢气还原氧化铜
3、铁矿石冶炼原理
4、铁丝燃烧
2Cu+O2 = 2CuO
H2 + CuO= Cu+ H2O
Fe2O3+3CO = 2Fe+3CO2
3Fe+2O2 = Fe3O4
高温
点燃
想一想:
金属能被氧化成为氧化物,而金属氧化物又能被还原剂还原成金属单质,那么非金属是否能转化为其他物质呢?
一、非金属单质与其化合物的转化
实验:
1、在燃烧匙里放入少量硫粉,加热,直至燃烧,看到的现象是________________,然后把燃着硫的燃烧匙伸入盛有氧气的集气瓶,看到_________________。燃烧停止后,小心闻一下气体。有_______气味。
2、立即向瓶内倒入少量水,振荡,加入几滴石蕊试液,看到石蕊试液变__色,说明溶液为___。
实验步骤:
红
酸性
刺激性
发出微弱的淡蓝色火焰
明亮的蓝紫色火焰
酸雨形成的模拟实验.swf
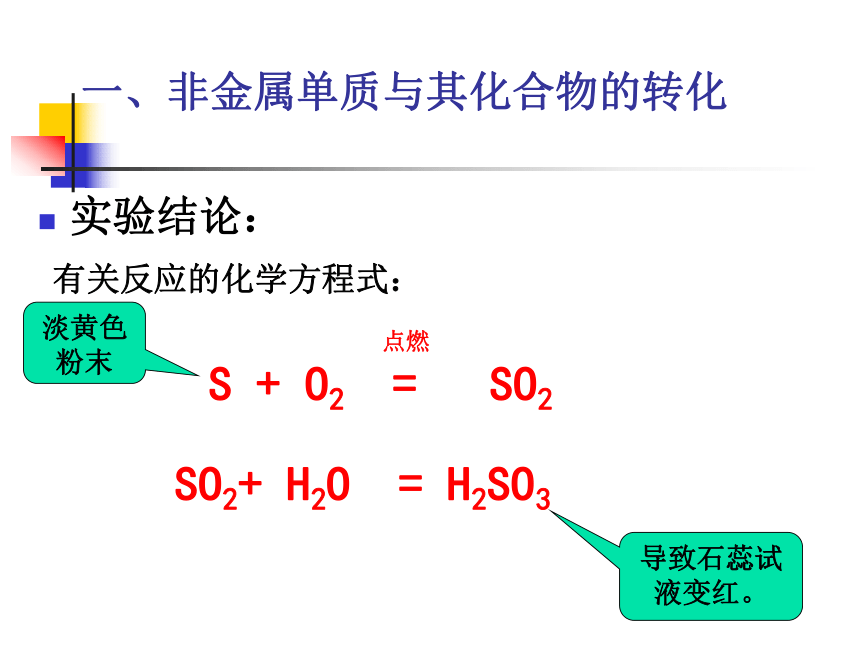
实验结论:
有关反应的化学方程式:
一、非金属单质与其化合物的转化
S + O2 = SO2
点燃
SO2+ H2O = H2SO3
导致石蕊试液变红。
淡黄色粉末
二、酸雨
当雨水被二氧化碳饱和时,略呈酸性,pH值为5.6。当大气被酸性气体污染时,pH值小于5.6的雨叫酸雨;pH值小于5.6的雪叫酸雪;在高空或高山上弥漫的雾,pH值小于5.6时叫酸雾。
想一想:
1、天然降水显酸性还是碱性?
由于空气中的CO2与水反应生成H2CO3,因而天然降水显弱酸性。
2、形成酸雨的主要污染物:
空气中的二氧化硫和氮氧化合物。
污染物的来源:
主要来源于煤和石油制品的燃烧。
3、酸雨形成的原因:
主要反应的化学方程式:
一、非金属单质与其化合物的转化
S + O2 = SO2
点燃
SO2+ H2O = H2SO3
空气中的二氧化硫和氮氧化合物在降水时溶解在水中生成了相应的酸。
2H2S03 + 02 = 2H2SO4
导致雨水PH降低。
想一想:
4、酸雨的危害?
(1)酸雨直接危害人类健康。
(2)使水体、土壤酸化,影响农业和渔业。
(3)腐蚀建筑物、工厂设备和文物古迹。
煤中的硫燃烧生成_______,它在粉尘的催化作用下跟O2反应生成________,再与雨水结合生成硫酸。相关的化学方程式是:
酸雨的形成
SO2
SO3
S + O2 = SO2
点燃
2SO2 + O2 = 2SO3
催化剂
SO3+ H2O = H2SO4
怎样用化学方程式表示下列物质的转化?
C→CO2→H2CO3
①
②
非金属单质与其化合物的转化规律
非金属单质
非金属氧化物
酸
→
→
O2
H2O
讨论:
SiO2不与水直接反应生成硅酸。
P P2O5 H3PO4
③
④
你能用化学方程式来表示下列物质之间的转化吗?
非金属单质
非金属氧化物
酸
→
→
O2
H2O
练一练:
我们能否由非金属、非金属氧化物与对应的酸之间的转化规律推测金属、金属氧化物和对应的碱之间的转化规律呢?
非金属单质
非金属氧化物
酸
→
→
O2
H2O
想一想:
钾钙钠的氧化物+水→碱
K 2 O + H2O= 2KOH
其他金属氧化物不溶于水,跟水不反应
Ca O + H2O= Ca(OH)2
Na 2 O + H2O= 2NaOH
+ O2
+ H2O
金属氧化物
→
金属
碱
→
只限于钾钙钠
Cu CuO Cu(OH)2
2Cu + O2 = 2CuO
△
金属的氧化
CuO + H2SO4 = CuSO4 + H2O
CuSO4 +2NaOH = Cu(OH)2 ↓+Na2SO4
金属氧化物
→
金属
盐
→
+ O2
+ 酸
碱
→
+ 可溶性的碱
想一想:
可溶性的碱
1.Ca→CaO→Ca(OH)2 →CaCO3
2)CaO + H2O = Ca(OH)2
3)Ca(OH)2 + CO2 = CaCO3 + H2O
1)
2)
3)
讨论:分析下列物质的变化
1)C + O2 = CO2
点燃
讨论:分析下列物质的变化
2.C→CO2→H2CO3 →Na2CO3
1)
2)
3)
2)CO2 + H2O = H2CO3
3)H2CO3 + 2NaOH = Na2CO3 + H2O
1)C + O2 = CO2
点燃
1.Zn + 2HCl = ZnCl2 + H2↑
2.Zn + Cl2 = ZnCl2
3.2Zn + O2 = 2ZnO
ZnO + 2HCl = ZnCl2 + H2O ↑
试设计由锌为原料制取氯化锌的实验方案。书P63。
方案1比较好,不但操作简单,并还可以回收氢气
加热
加热
方案2使用了氯气,可能会漏出氯气对环境造成污染
第三章 物质的转化和
元素的循环
&1.物质的转化
复习回忆
写出下列有关化学方程式:
1、铜丝在空气中加热
2、氢气还原氧化铜
3、铁矿石冶炼原理
4、铁丝燃烧
2Cu+O2 = 2CuO
H2 + CuO= Cu+ H2O
Fe2O3+3CO = 2Fe+3CO2
3Fe+2O2 = Fe3O4
高温
点燃
想一想:
金属能被氧化成为氧化物,而金属氧化物又能被还原剂还原成金属单质,那么非金属是否能转化为其他物质呢?
一、非金属单质与其化合物的转化
实验:
1、在燃烧匙里放入少量硫粉,加热,直至燃烧,看到的现象是________________,然后把燃着硫的燃烧匙伸入盛有氧气的集气瓶,看到_________________。燃烧停止后,小心闻一下气体。有_______气味。
2、立即向瓶内倒入少量水,振荡,加入几滴石蕊试液,看到石蕊试液变__色,说明溶液为___。
实验步骤:
红
酸性
刺激性
发出微弱的淡蓝色火焰
明亮的蓝紫色火焰
酸雨形成的模拟实验.swf
实验结论:
有关反应的化学方程式:
一、非金属单质与其化合物的转化
S + O2 = SO2
点燃
SO2+ H2O = H2SO3
导致石蕊试液变红。
淡黄色粉末
二、酸雨
当雨水被二氧化碳饱和时,略呈酸性,pH值为5.6。当大气被酸性气体污染时,pH值小于5.6的雨叫酸雨;pH值小于5.6的雪叫酸雪;在高空或高山上弥漫的雾,pH值小于5.6时叫酸雾。
想一想:
1、天然降水显酸性还是碱性?
由于空气中的CO2与水反应生成H2CO3,因而天然降水显弱酸性。
2、形成酸雨的主要污染物:
空气中的二氧化硫和氮氧化合物。
污染物的来源:
主要来源于煤和石油制品的燃烧。
3、酸雨形成的原因:
主要反应的化学方程式:
一、非金属单质与其化合物的转化
S + O2 = SO2
点燃
SO2+ H2O = H2SO3
空气中的二氧化硫和氮氧化合物在降水时溶解在水中生成了相应的酸。
2H2S03 + 02 = 2H2SO4
导致雨水PH降低。
想一想:
4、酸雨的危害?
(1)酸雨直接危害人类健康。
(2)使水体、土壤酸化,影响农业和渔业。
(3)腐蚀建筑物、工厂设备和文物古迹。
煤中的硫燃烧生成_______,它在粉尘的催化作用下跟O2反应生成________,再与雨水结合生成硫酸。相关的化学方程式是:
酸雨的形成
SO2
SO3
S + O2 = SO2
点燃
2SO2 + O2 = 2SO3
催化剂
SO3+ H2O = H2SO4
怎样用化学方程式表示下列物质的转化?
C→CO2→H2CO3
①
②
非金属单质与其化合物的转化规律
非金属单质
非金属氧化物
酸
→
→
O2
H2O
讨论:
SiO2不与水直接反应生成硅酸。
P P2O5 H3PO4
③
④
你能用化学方程式来表示下列物质之间的转化吗?
非金属单质
非金属氧化物
酸
→
→
O2
H2O
练一练:
我们能否由非金属、非金属氧化物与对应的酸之间的转化规律推测金属、金属氧化物和对应的碱之间的转化规律呢?
非金属单质
非金属氧化物
酸
→
→
O2
H2O
想一想:
钾钙钠的氧化物+水→碱
K 2 O + H2O= 2KOH
其他金属氧化物不溶于水,跟水不反应
Ca O + H2O= Ca(OH)2
Na 2 O + H2O= 2NaOH
+ O2
+ H2O
金属氧化物
→
金属
碱
→
只限于钾钙钠
Cu CuO Cu(OH)2
2Cu + O2 = 2CuO
△
金属的氧化
CuO + H2SO4 = CuSO4 + H2O
CuSO4 +2NaOH = Cu(OH)2 ↓+Na2SO4
金属氧化物
→
金属
盐
→
+ O2
+ 酸
碱
→
+ 可溶性的碱
想一想:
可溶性的碱
1.Ca→CaO→Ca(OH)2 →CaCO3
2)CaO + H2O = Ca(OH)2
3)Ca(OH)2 + CO2 = CaCO3 + H2O
1)
2)
3)
讨论:分析下列物质的变化
1)C + O2 = CO2
点燃
讨论:分析下列物质的变化
2.C→CO2→H2CO3 →Na2CO3
1)
2)
3)
2)CO2 + H2O = H2CO3
3)H2CO3 + 2NaOH = Na2CO3 + H2O
1)C + O2 = CO2
点燃
1.Zn + 2HCl = ZnCl2 + H2↑
2.Zn + Cl2 = ZnCl2
3.2Zn + O2 = 2ZnO
ZnO + 2HCl = ZnCl2 + H2O ↑
试设计由锌为原料制取氯化锌的实验方案。书P63。
方案1比较好,不但操作简单,并还可以回收氢气
加热
加热
方案2使用了氯气,可能会漏出氯气对环境造成污染
同课章节目录
- 第一章 宇宙的起源与演化
- 1 我们的宇宙
- 2 热大爆炸宇宙模型
- 3 恒星的一生
- 4 星际航行和空间技术
- 第二章 地球的演化和生物圈的形成
- 1 地球的演化
- 2 生命起源
- 3 生物进化
- 4 生态平衡
- 第三章 物质的转化和元素的循环
- 1 物质的转化
- 2 自然界中的碳循环和氧循环
- 3 自然界中的氮循环
- 第四章 健康与保健
- 1 健康、亚健康和疾病
- 2 运动与健康
- 3 免疫与健康
- 4 营养与健康
- 5 卫生与健康
- 6 环境与健康
- 第五章 生物的遗传和变异
- 1 生物的遗传
- 2 生物的变异
- 第六章 能源与社会
- 1 能源和能源的分类
- 2 太阳能的利用
- 3 核能的开发与放射性防护
- 4 新能源与可持续发展
- 第七章 科学与社会发展
- 1 科学就是力量
- 2 科学推动技术发展
- 3 科学技术推动经济增长
- 4 科学技术与可持续发展
