7.1 认识有机化合物(第二课时烷烃的性质)课件(30张ppt)【新教材】2020-2021学年人教版(2019)高一化学必修二
文档属性
| 名称 | 7.1 认识有机化合物(第二课时烷烃的性质)课件(30张ppt)【新教材】2020-2021学年人教版(2019)高一化学必修二 |

|
|
| 格式 | pptx | ||
| 文件大小 | 109.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-15 00:00:00 | ||
图片预览










文档简介
认识有机化合物
第二课时 烷烃
常德芷兰实验学校
烷烃的存在
天然气
油田气
煤层气
沼气
CH4——天然气,沼气,煤层气的主要成分
含碳个数较多的烷烃——护肤品、医用软膏中的“凡士林”,蜡笔中的石蜡
请结合生活经验和初中化学的有关知识,想一想烷烃可能具有哪些性质。
烷烃的物理性质
1.甲烷的物理性质:
2.烷烃的物理性质:
无色、无味、极难溶于水的气体
熔点:-182℃
沸点:-164℃
密度:0.717g/L(标准状况下)
烷烃都不溶于水,可溶于有机溶剂(汽油,苯等)
随着碳原子数增多,熔沸点升高,室温时C1-C4气态,C5-C17液态,C18以上固态。
随着碳原子增多,密度增大,都小于水的密度
稳定性:在通常情况下,烷烃比较稳定。
与强酸、强碱或高锰酸钾等强氧化剂不发生反应。
1、可燃性:烷烃都能燃烧
二、烷烃的化学性质
注意:有机反应式通常用箭头!
CH4燃烧方程式:_________________________。
C3H8燃烧方程式:___________________________。
链状烷烃燃烧通式:______________________________________。
实验室常用燃烧法测定有机物的组成元素,先通过定性研究,初步得出有机物的元素组成,再通过定性、定量结合的方法,测定并推断有机物是否含有其他元素。
甲烷的爆炸实验
CH4在空气中的爆炸极限5%~15.4%(V/V)
甲烷点燃前一定要验纯!
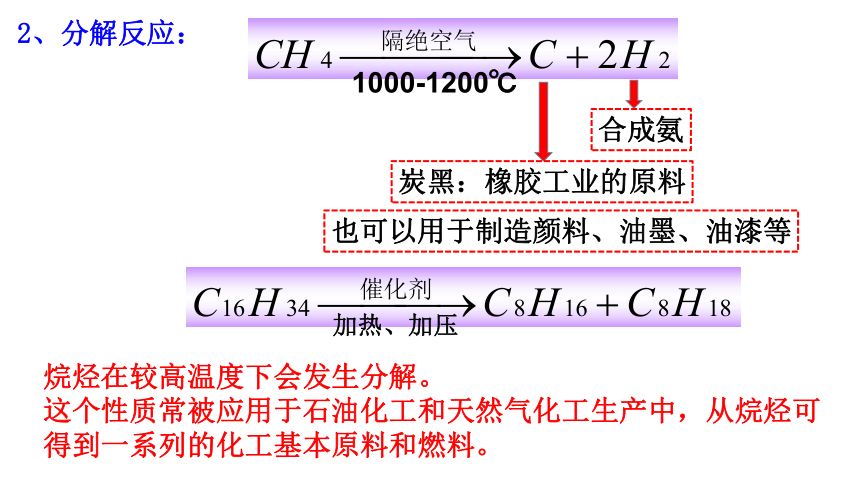
2、分解反应:
1000-1200℃
加热、加压
炭黑:橡胶工业的原料
也可以用于制造颜料、油墨、油漆等
合成氨
烷烃在较高温度下会发生分解。
这个性质常被应用于石油化工和天然气化工生产中,从烷烃可得到一系列的化工基本原料和燃料。
(2)在通常条件下,烷烃和硫酸、氢氧化钠不反应,和酸性KMnO4溶液也不反应( )
(3)在做甲烷、乙烷燃烧试验前,气体一定要验纯( )
(1)常温常压下,CH4、C2H6和C3H8为气体,C4H10、C6H14呈液态( )
×
√
√
提示 常温常压下,分子中碳原子数n≤4的烷烃为气态,故C4H10为气态。
提示 等体积的CH4和C4H10,C4H10用的氧气更多,如不减小进气量(或增大进风量),则C4H10燃烧不充分,会产生CO等有毒气体。
(4)使用天然气(主要成分为CH4)的燃气灶,改用液化石油气(主要成分为C4H10),应减小进气量或增大进风量( )
√
练习
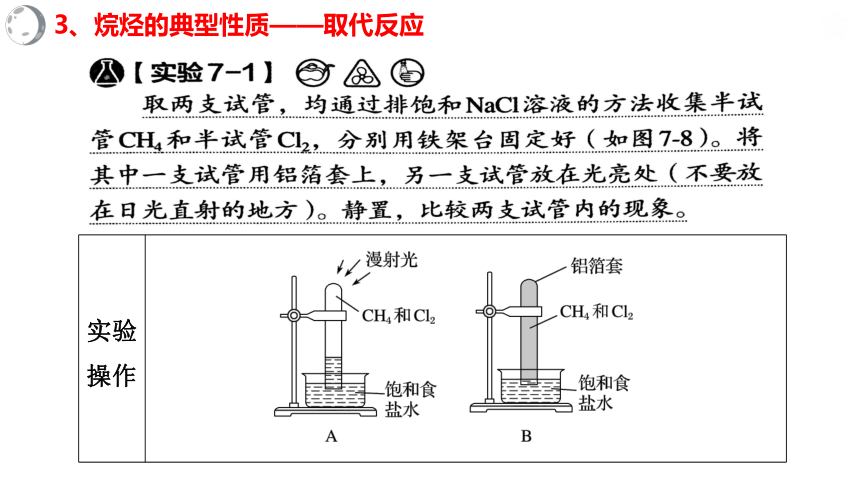
实验
操作
?
3、烷烃的典型性质——取代反应
实验现象
CH4与Cl2混合,光照条件下:
试管内黄绿色逐渐变浅;
试管内液面上升,试管内有白雾;
试管壁出现油状液滴。
Cl2发生反应
气体体积减小
生成难溶于水的物质
注意:暗处不反应,强光直射会爆炸
结论:光照条件下,甲烷与氯气发生了反应
一氯甲烷(气体)
二氯甲烷(液态)
三氯甲烷(液态)俗称:氯仿
四氯甲烷(液态)四氯化碳
取代反应:有机物分子里的某些原子或原子团被其他 原子或原子团所替代的反应
无色油
状液滴
Cl
H
Cl
H
C
两种写法表示同一物质
H
Cl
Cl
H
C
同一物质不同投影方式
取代反应
2.反应条件为光照(室温或阴暗处不反应)
3.烷烃和卤素的气态单质反应,溶液不反应(例如甲烷和溴水,溴的CCl4溶液不反应)
4.反应一旦发生,不会停留在某一步,即使氯气不足量,产物依然是五种物质的混合物
5.有机物参加的反应往往比较复杂,有副产物生成,因此有机方程式中用箭头而不用等号
1.“一上一下,取而代之”,用一个卤素原子代替一个氢原子,下来的氢原子与卤素原子形成卤化氢。
问1:CH4和Cl2取代反应的产物中物质的量最多的是什么?
它与Cl2在量上有什么关系?
HCl,反应生成的HCl与反应消耗的Cl2的物质的量相等。
问2:能否用CH4和Cl2按1∶1的体积比混合来制取纯净的CH3Cl ?
问3:1 mol甲烷和Cl2恰好完全发生反应,并生成相同物质的量的4种有机物,则需Cl2的物质的量是多少?
根据取代反应的特点, 需要Cl2的物质的量等于被取代的氢原子的物质的量,即0.25 mol×(1+2+3+4)=2.5 mol。
CH4和Cl2的反应是连锁反应,不可能只发生第一步取代反应,生成物为混合物。
解析 因Cl2足量,若充分反应,则CH4中的四个H原子可完全被取代,生成CCl4和HCl,即化学方程式为CH4+4Cl2 CCl4+4HCl。
1.某课外活动小组利用如图所示装置探
究CH4和Cl2的反应,据题意,回答下列
问题:
(1)CH4和Cl2发生反应条件是________,
若用日光直射,可能会引起______,假
设甲烷与氯气反应充分,且只产生一种
有机物,请写出化学方程式:__________________________。
漫射光
爆炸
典型例题
(2)若题目中甲烷与氯气的体积之比为
1∶1,则得到的产物为___(填字母)。
A.CH3Cl HCl
B.CCl4 HCl
C.CH3Cl CH2Cl2
D.CH3Cl CH2Cl2 CHCl3 CCl4 HCl
D
解析 甲烷与氯气的取代反应,是四步反应同时发生,故得到四种氯代产物和HCl。
(3)经过几个小时的反应后,U形管右
端的水柱变化是____(填字母)。
A.升高
B.降低
C.不变
D.无法确定
B
解析 甲烷和氯气在光照的条件下发生取代反应,U形管左端生成的氯化氢气体易溶于水,压强减小,U形管右端液面下降,左端液面上升。
(4)若水中含有Na2SiO3,则在U形管左端会观察到____________________。
有白色胶状沉淀生成
解析 因左端生成HCl溶于水后发生反应2HCl+Na2SiO3===H2SiO3↓+2NaCl,所以观察到有白色胶状沉淀生成。
(5)右端玻璃管的作用是__________。
平衡气压
解析 为了平衡气压,在U形管右端插一个玻璃管。
2.下列反应属于取代反应的是________(填序号)。
①CH4 C+2H2 ②CuSO4+Fe===FeSO4+Cu
③CH3Cl+Cl2 CH2Cl2+HCl ④2NaBr+Cl2===2NaCl+Br2
⑤CH3OH+HCl CH3Cl+H2O
⑥CH3CH2Br+H2O CH3CH2OH+HBr
⑦CH4+2O2 CO2+2H2O
解析 ①为CH4在高温下的分解反应;
②和④为无机反应中的置换反应,也为氧化还原反应;
⑦为CH4的燃烧,属于氧化反应,③⑤⑥属于有机反应中的取代反应。
③⑤⑥
小结:烷烃的性质归纳
1.烷烃的结构与通式
C原子都以C—C相连,其余的价键均用于与H原子结合,达到“饱和”的一系列化合物,也叫“饱和烃”。
分子式通式:
CnH2n+2 (n为整数)
2.烷烃的性质(与甲烷类似)
(1)物理性质:熔点低,难溶于水,易溶于有机溶剂,熔沸点随C原子数增多而升高
(2)化学性质:整体稳定,不与强酸、强碱、高锰酸钾溶液反应
典型反应:a.燃烧,b.受热分解c.取代反应
有机物的通性:
1.大多数有机物的熔点比较低,且难溶于水,易溶于有机溶剂(汽油,乙醇,苯等)。
相似相溶原理
2.大多数有机物容易燃烧,受热会发生分解。
3.有机化学反应比较复杂,常有副反应。
1、有机物 与氯气发生取代反应,生成的一氯代物有( )
A.1种 B.2种 C.3种 D.4种
2、进行一氯取代反应后,只能生成三种沸点不同的产物的烷烃是 ( )
B.
C.
D.
A.
3、某烃具有同分异构体,且各同分异构体的一氯代物的种数相同,该烃的分子式是 ( )
A. CH4 B. C3H8 C. C4H10 D. C5H12
-C-
H
H
H
H
C
-C-
H
H
H
H
H
H
-C-
CH3
CH3
CH3
CH3
同一个碳原子上的氢是等效氢
同一个碳原子上的甲基上的氢是等效氢
处于分子中对称位置的碳上的氢原子是等效氢
判断“等效氢”的三条原则是:
补充:烃的一元取代产物同分异构体数目的判断---等效氢法
方法:找出有多少种不同的氢原子
关键:对称氢原子的确定
烃或烃的衍生物的一元取代物分子中,等效氢原子种类有多少,则其一元取代物种类就有多少。
判断某种烃的一氯代物种类
下面烷烃一氯代物有___________种同分异构体.
CH3—CH—CH—CH—CH3
l l l
CH3 CH3 CH3
1
4
4
2 3
——找准称轴、点、面
CH3CH2CH2CH2CH3
对称轴
③ ② ① ② ③
CH3-CH2-CH-CH2-CH3
CH2
CH3
对称点
①
②
②
②
③
③
③
CH3
CH3 – C – CH2- CH3
CH3
③
对称点
对称面
①
②
①
①
等效氢法
b
b
b
b
a
a
a
a
2、烃的二元取代物的同分异构体数目判断
——“定一移一法”
如:C3H8
第二课时 烷烃
常德芷兰实验学校
烷烃的存在
天然气
油田气
煤层气
沼气
CH4——天然气,沼气,煤层气的主要成分
含碳个数较多的烷烃——护肤品、医用软膏中的“凡士林”,蜡笔中的石蜡
请结合生活经验和初中化学的有关知识,想一想烷烃可能具有哪些性质。
烷烃的物理性质
1.甲烷的物理性质:
2.烷烃的物理性质:
无色、无味、极难溶于水的气体
熔点:-182℃
沸点:-164℃
密度:0.717g/L(标准状况下)
烷烃都不溶于水,可溶于有机溶剂(汽油,苯等)
随着碳原子数增多,熔沸点升高,室温时C1-C4气态,C5-C17液态,C18以上固态。
随着碳原子增多,密度增大,都小于水的密度
稳定性:在通常情况下,烷烃比较稳定。
与强酸、强碱或高锰酸钾等强氧化剂不发生反应。
1、可燃性:烷烃都能燃烧
二、烷烃的化学性质
注意:有机反应式通常用箭头!
CH4燃烧方程式:_________________________。
C3H8燃烧方程式:___________________________。
链状烷烃燃烧通式:______________________________________。
实验室常用燃烧法测定有机物的组成元素,先通过定性研究,初步得出有机物的元素组成,再通过定性、定量结合的方法,测定并推断有机物是否含有其他元素。
甲烷的爆炸实验
CH4在空气中的爆炸极限5%~15.4%(V/V)
甲烷点燃前一定要验纯!
2、分解反应:
1000-1200℃
加热、加压
炭黑:橡胶工业的原料
也可以用于制造颜料、油墨、油漆等
合成氨
烷烃在较高温度下会发生分解。
这个性质常被应用于石油化工和天然气化工生产中,从烷烃可得到一系列的化工基本原料和燃料。
(2)在通常条件下,烷烃和硫酸、氢氧化钠不反应,和酸性KMnO4溶液也不反应( )
(3)在做甲烷、乙烷燃烧试验前,气体一定要验纯( )
(1)常温常压下,CH4、C2H6和C3H8为气体,C4H10、C6H14呈液态( )
×
√
√
提示 常温常压下,分子中碳原子数n≤4的烷烃为气态,故C4H10为气态。
提示 等体积的CH4和C4H10,C4H10用的氧气更多,如不减小进气量(或增大进风量),则C4H10燃烧不充分,会产生CO等有毒气体。
(4)使用天然气(主要成分为CH4)的燃气灶,改用液化石油气(主要成分为C4H10),应减小进气量或增大进风量( )
√
练习
实验
操作
?
3、烷烃的典型性质——取代反应
实验现象
CH4与Cl2混合,光照条件下:
试管内黄绿色逐渐变浅;
试管内液面上升,试管内有白雾;
试管壁出现油状液滴。
Cl2发生反应
气体体积减小
生成难溶于水的物质
注意:暗处不反应,强光直射会爆炸
结论:光照条件下,甲烷与氯气发生了反应
一氯甲烷(气体)
二氯甲烷(液态)
三氯甲烷(液态)俗称:氯仿
四氯甲烷(液态)四氯化碳
取代反应:有机物分子里的某些原子或原子团被其他 原子或原子团所替代的反应
无色油
状液滴
Cl
H
Cl
H
C
两种写法表示同一物质
H
Cl
Cl
H
C
同一物质不同投影方式
取代反应
2.反应条件为光照(室温或阴暗处不反应)
3.烷烃和卤素的气态单质反应,溶液不反应(例如甲烷和溴水,溴的CCl4溶液不反应)
4.反应一旦发生,不会停留在某一步,即使氯气不足量,产物依然是五种物质的混合物
5.有机物参加的反应往往比较复杂,有副产物生成,因此有机方程式中用箭头而不用等号
1.“一上一下,取而代之”,用一个卤素原子代替一个氢原子,下来的氢原子与卤素原子形成卤化氢。
问1:CH4和Cl2取代反应的产物中物质的量最多的是什么?
它与Cl2在量上有什么关系?
HCl,反应生成的HCl与反应消耗的Cl2的物质的量相等。
问2:能否用CH4和Cl2按1∶1的体积比混合来制取纯净的CH3Cl ?
问3:1 mol甲烷和Cl2恰好完全发生反应,并生成相同物质的量的4种有机物,则需Cl2的物质的量是多少?
根据取代反应的特点, 需要Cl2的物质的量等于被取代的氢原子的物质的量,即0.25 mol×(1+2+3+4)=2.5 mol。
CH4和Cl2的反应是连锁反应,不可能只发生第一步取代反应,生成物为混合物。
解析 因Cl2足量,若充分反应,则CH4中的四个H原子可完全被取代,生成CCl4和HCl,即化学方程式为CH4+4Cl2 CCl4+4HCl。
1.某课外活动小组利用如图所示装置探
究CH4和Cl2的反应,据题意,回答下列
问题:
(1)CH4和Cl2发生反应条件是________,
若用日光直射,可能会引起______,假
设甲烷与氯气反应充分,且只产生一种
有机物,请写出化学方程式:__________________________。
漫射光
爆炸
典型例题
(2)若题目中甲烷与氯气的体积之比为
1∶1,则得到的产物为___(填字母)。
A.CH3Cl HCl
B.CCl4 HCl
C.CH3Cl CH2Cl2
D.CH3Cl CH2Cl2 CHCl3 CCl4 HCl
D
解析 甲烷与氯气的取代反应,是四步反应同时发生,故得到四种氯代产物和HCl。
(3)经过几个小时的反应后,U形管右
端的水柱变化是____(填字母)。
A.升高
B.降低
C.不变
D.无法确定
B
解析 甲烷和氯气在光照的条件下发生取代反应,U形管左端生成的氯化氢气体易溶于水,压强减小,U形管右端液面下降,左端液面上升。
(4)若水中含有Na2SiO3,则在U形管左端会观察到____________________。
有白色胶状沉淀生成
解析 因左端生成HCl溶于水后发生反应2HCl+Na2SiO3===H2SiO3↓+2NaCl,所以观察到有白色胶状沉淀生成。
(5)右端玻璃管的作用是__________。
平衡气压
解析 为了平衡气压,在U形管右端插一个玻璃管。
2.下列反应属于取代反应的是________(填序号)。
①CH4 C+2H2 ②CuSO4+Fe===FeSO4+Cu
③CH3Cl+Cl2 CH2Cl2+HCl ④2NaBr+Cl2===2NaCl+Br2
⑤CH3OH+HCl CH3Cl+H2O
⑥CH3CH2Br+H2O CH3CH2OH+HBr
⑦CH4+2O2 CO2+2H2O
解析 ①为CH4在高温下的分解反应;
②和④为无机反应中的置换反应,也为氧化还原反应;
⑦为CH4的燃烧,属于氧化反应,③⑤⑥属于有机反应中的取代反应。
③⑤⑥
小结:烷烃的性质归纳
1.烷烃的结构与通式
C原子都以C—C相连,其余的价键均用于与H原子结合,达到“饱和”的一系列化合物,也叫“饱和烃”。
分子式通式:
CnH2n+2 (n为整数)
2.烷烃的性质(与甲烷类似)
(1)物理性质:熔点低,难溶于水,易溶于有机溶剂,熔沸点随C原子数增多而升高
(2)化学性质:整体稳定,不与强酸、强碱、高锰酸钾溶液反应
典型反应:a.燃烧,b.受热分解c.取代反应
有机物的通性:
1.大多数有机物的熔点比较低,且难溶于水,易溶于有机溶剂(汽油,乙醇,苯等)。
相似相溶原理
2.大多数有机物容易燃烧,受热会发生分解。
3.有机化学反应比较复杂,常有副反应。
1、有机物 与氯气发生取代反应,生成的一氯代物有( )
A.1种 B.2种 C.3种 D.4种
2、进行一氯取代反应后,只能生成三种沸点不同的产物的烷烃是 ( )
B.
C.
D.
A.
3、某烃具有同分异构体,且各同分异构体的一氯代物的种数相同,该烃的分子式是 ( )
A. CH4 B. C3H8 C. C4H10 D. C5H12
-C-
H
H
H
H
C
-C-
H
H
H
H
H
H
-C-
CH3
CH3
CH3
CH3
同一个碳原子上的氢是等效氢
同一个碳原子上的甲基上的氢是等效氢
处于分子中对称位置的碳上的氢原子是等效氢
判断“等效氢”的三条原则是:
补充:烃的一元取代产物同分异构体数目的判断---等效氢法
方法:找出有多少种不同的氢原子
关键:对称氢原子的确定
烃或烃的衍生物的一元取代物分子中,等效氢原子种类有多少,则其一元取代物种类就有多少。
判断某种烃的一氯代物种类
下面烷烃一氯代物有___________种同分异构体.
CH3—CH—CH—CH—CH3
l l l
CH3 CH3 CH3
1
4
4
2 3
——找准称轴、点、面
CH3CH2CH2CH2CH3
对称轴
③ ② ① ② ③
CH3-CH2-CH-CH2-CH3
CH2
CH3
对称点
①
②
②
②
③
③
③
CH3
CH3 – C – CH2- CH3
CH3
③
对称点
对称面
①
②
①
①
等效氢法
b
b
b
b
a
a
a
a
2、烃的二元取代物的同分异构体数目判断
——“定一移一法”
如:C3H8
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
