氯气
图片预览








文档简介
(共23张PPT)
氯气
第一节 Cl2
[教学目的]
知识目标:掌握氯气的实验室制法及化学性质。
能力目标:通过引导学生观察、分析演示实验的现象,培养学生的观察和分析问题的能力。
品质目标:培养学生热爱科学思想,对学生进行环境保护教育
一、氯气的实验室制备方法
问题:1、 一套完整的制取气体的装置包括哪几个环节
1、气体发生装置
2、净化装置
3、收集气体的方法
4、尾气吸收装置
氯气
黄绿色、有毒、密度比空气大、能溶于水(1:2)的气体,并能与NaOH溶液反应。
实验室制取氯气常用MnO2和浓盐酸为原料(反应需加热)
MnO2+4HCl(浓) = MnCl2+2H2O+Cl2↑
1、实验原理:
MnO2+4HCl(浓) = MnCl2+2H2O+Cl2↑
2、Cl2中可能含的杂质:
3、除杂试剂:
4、收集方法:
5、尾气吸收试剂:
浓氢氧化钠溶液
饱和食盐水、浓硫酸
向上排空气法或排饱和食盐水法
HCl H2O
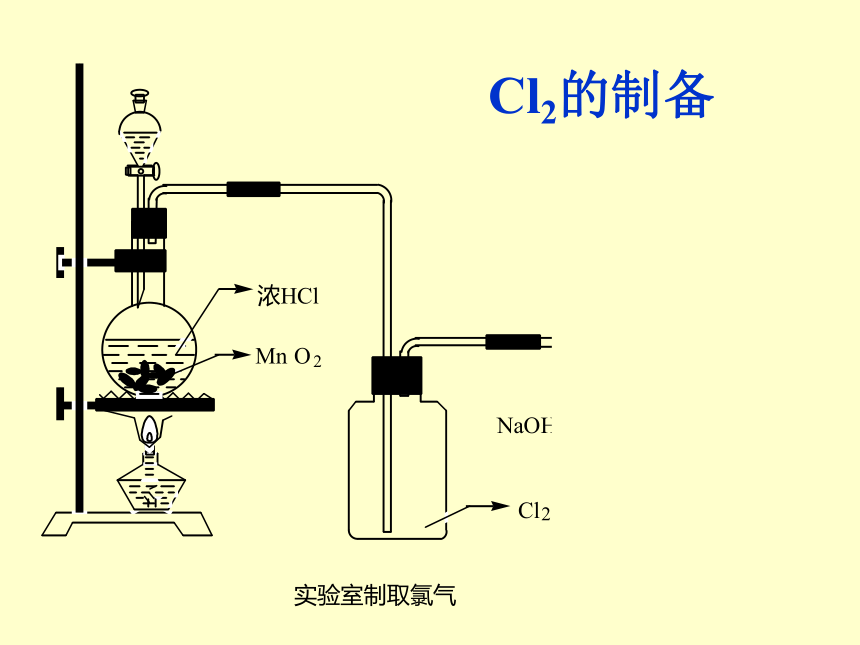
Cl2的制备
Cl2的制备
Cl2的制备
Cl2中混有HCl和H2O(g)
Cl2的制备、提纯、吸收
①连接好装置,检查气密性
②在烧瓶中加入二氧化锰粉末
③往分液漏斗中加入浓盐酸,
再缓缓滴入烧瓶中
④缓缓加热,加快反应,使气体均匀逸出
⑤用向上排空气法收集氯气,
尾气导入吸收剂中
实验步骤
1、下图是实验室用来制取干燥、纯净氯气的装置;由于装置和使用药品有错误而未能在D瓶中收集到Cl2;请指出装置中的错误
①长颈漏斗应改为分液漏斗.
②烧瓶下应垫石棉网.
③应用酒精灯加热.
④稀盐酸应改为浓盐酸.
⑤多余Cl2应通入NaOH溶液中
二、氯气的化学性质
1、氯气与水的反应
3、怎样证明氯气与水发生了化学反应。
4、能不能设计一实验证明起漂白性作
用的是HClO而不是Cl2、盐酸。
问题:
问题:
6、Cl2溶于水后是否完全与水反应了,怎样用实验证明?
7、新制(久置)的氯水中存在哪些微粒?如何保存氯水?
5、HClO有哪些重要的性质和用途?
二、氯气的化学性质
2、氯气与氢氧化钠溶液的反应
问题:
8、工业上如何制漂粉精?
9、HClO有漂白作用,为什么不直接用HClO漂白,而要转化成次氯酸盐,其漂白原理是什么?
10、Ca(ClO)2能否与稀盐酸反应?如何保存漂粉精?
1、下列气体发生装置相同的是( )
A 氯气和氢气 B 氯气和氧气
C 氢气和二氧化碳 D 氧气和二氧化碳
2、实验室制氯气时,二氧化锰的作用是 ( )
A 催化剂 B 氧化剂
C 还原剂 D 反应物
3.在空气中能稳定存在的物质是( )
A 石灰水 B 氯水
C 次氯酸钙 D 食盐水
C
BD
D
1、实验室 制氯气为何不用氢氧化钙溶液吸收尾气?
2、下列物质能使干燥的蓝色石蕊试纸先变红后褪
色的是①氯气②液氯③新制的氯水④盐酸⑤盐酸酸
化的漂白粉溶液
思考
实验室还可用KMnO4或KClO3代替MnO2与浓盐酸反应制氯气
2KMnO4+16HCl=2KCl+2MnCl2+8H2O+5Cl2 ↑
KClO3+6HCl=KCl+3H2O+3Cl2 ↑
讨论
1、使浓盐酸与足量的MnO2共热制Cl2、实际产生的Cl2总比理论值低,其主要原因是什么?
稀盐酸与MnO2不反应,随着反应的进行,浓盐酸的浓度逐渐变小。
再 见
氯气
第一节 Cl2
[教学目的]
知识目标:掌握氯气的实验室制法及化学性质。
能力目标:通过引导学生观察、分析演示实验的现象,培养学生的观察和分析问题的能力。
品质目标:培养学生热爱科学思想,对学生进行环境保护教育
一、氯气的实验室制备方法
问题:1、 一套完整的制取气体的装置包括哪几个环节
1、气体发生装置
2、净化装置
3、收集气体的方法
4、尾气吸收装置
氯气
黄绿色、有毒、密度比空气大、能溶于水(1:2)的气体,并能与NaOH溶液反应。
实验室制取氯气常用MnO2和浓盐酸为原料(反应需加热)
MnO2+4HCl(浓) = MnCl2+2H2O+Cl2↑
1、实验原理:
MnO2+4HCl(浓) = MnCl2+2H2O+Cl2↑
2、Cl2中可能含的杂质:
3、除杂试剂:
4、收集方法:
5、尾气吸收试剂:
浓氢氧化钠溶液
饱和食盐水、浓硫酸
向上排空气法或排饱和食盐水法
HCl H2O
Cl2的制备
Cl2的制备
Cl2的制备
Cl2中混有HCl和H2O(g)
Cl2的制备、提纯、吸收
①连接好装置,检查气密性
②在烧瓶中加入二氧化锰粉末
③往分液漏斗中加入浓盐酸,
再缓缓滴入烧瓶中
④缓缓加热,加快反应,使气体均匀逸出
⑤用向上排空气法收集氯气,
尾气导入吸收剂中
实验步骤
1、下图是实验室用来制取干燥、纯净氯气的装置;由于装置和使用药品有错误而未能在D瓶中收集到Cl2;请指出装置中的错误
①长颈漏斗应改为分液漏斗.
②烧瓶下应垫石棉网.
③应用酒精灯加热.
④稀盐酸应改为浓盐酸.
⑤多余Cl2应通入NaOH溶液中
二、氯气的化学性质
1、氯气与水的反应
3、怎样证明氯气与水发生了化学反应。
4、能不能设计一实验证明起漂白性作
用的是HClO而不是Cl2、盐酸。
问题:
问题:
6、Cl2溶于水后是否完全与水反应了,怎样用实验证明?
7、新制(久置)的氯水中存在哪些微粒?如何保存氯水?
5、HClO有哪些重要的性质和用途?
二、氯气的化学性质
2、氯气与氢氧化钠溶液的反应
问题:
8、工业上如何制漂粉精?
9、HClO有漂白作用,为什么不直接用HClO漂白,而要转化成次氯酸盐,其漂白原理是什么?
10、Ca(ClO)2能否与稀盐酸反应?如何保存漂粉精?
1、下列气体发生装置相同的是( )
A 氯气和氢气 B 氯气和氧气
C 氢气和二氧化碳 D 氧气和二氧化碳
2、实验室制氯气时,二氧化锰的作用是 ( )
A 催化剂 B 氧化剂
C 还原剂 D 反应物
3.在空气中能稳定存在的物质是( )
A 石灰水 B 氯水
C 次氯酸钙 D 食盐水
C
BD
D
1、实验室 制氯气为何不用氢氧化钙溶液吸收尾气?
2、下列物质能使干燥的蓝色石蕊试纸先变红后褪
色的是①氯气②液氯③新制的氯水④盐酸⑤盐酸酸
化的漂白粉溶液
思考
实验室还可用KMnO4或KClO3代替MnO2与浓盐酸反应制氯气
2KMnO4+16HCl=2KCl+2MnCl2+8H2O+5Cl2 ↑
KClO3+6HCl=KCl+3H2O+3Cl2 ↑
讨论
1、使浓盐酸与足量的MnO2共热制Cl2、实际产生的Cl2总比理论值低,其主要原因是什么?
稀盐酸与MnO2不反应,随着反应的进行,浓盐酸的浓度逐渐变小。
再 见
