7.1.1有机化合物中碳原子的成键特点 课件(34张ppt)【新教材】2020-2021学年人教版(2019)高一化学必修二
文档属性
| 名称 | 7.1.1有机化合物中碳原子的成键特点 课件(34张ppt)【新教材】2020-2021学年人教版(2019)高一化学必修二 |
|
|
| 格式 | pptx | ||
| 文件大小 | 3.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-16 00:00:00 | ||
图片预览




文档简介
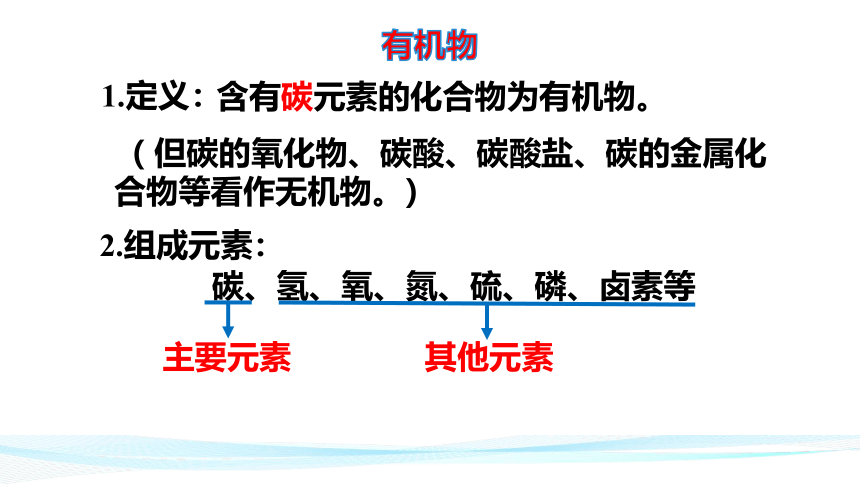
第七章 有机化合物
第一节 认识有机化合物
第1课时 有机化合物中碳原子的成键特点
1.定义:
含有碳元素的化合物为有机物。
( 但碳的氧化物、碳酸、碳酸盐、碳的金属化合物等看作无机物。)
2.组成元素:
碳、氢、氧、氮、硫、磷、卤素等
主要元素
其他元素
有机物
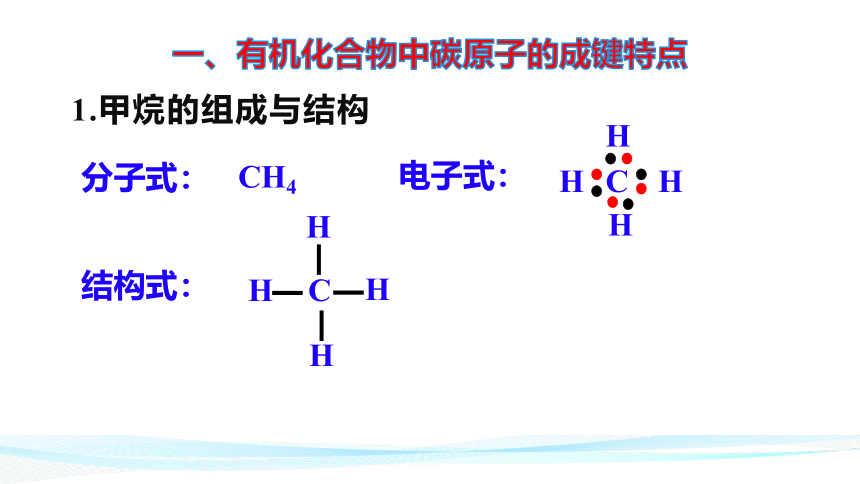
1.甲烷的组成与结构
分子式:
CH4
电子式:
H
H
H
C
H
结构式:
C
H
H
H
H
一、有机化合物中碳原子的成键特点
(1)碳原子的最外层有4个电子,可与其他原子形成4个共价键,而且碳碳原子之间也能相互形成共价键。
(2)碳原子与碳原子之间不仅可以形成单键,还可以形成双键或三键。
单键( )、双键( )、三键(—C≡C—)
2.有机化合物中碳原子的成键特点
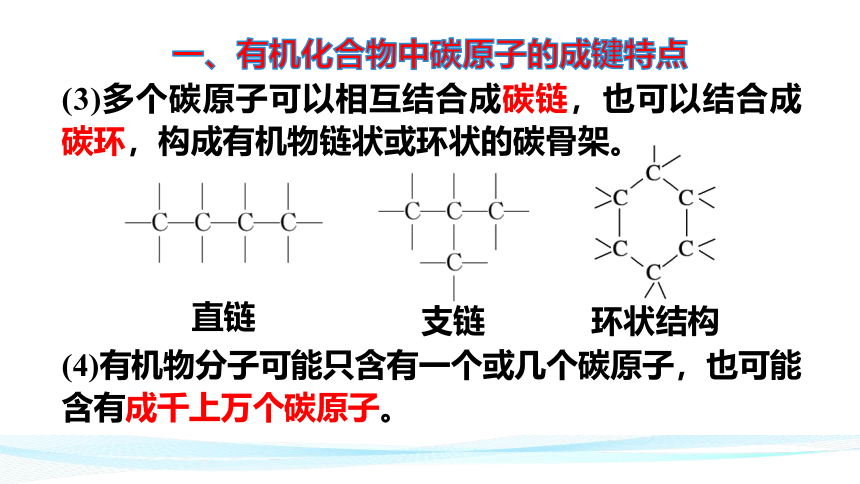
一、有机化合物中碳原子的成键特点
(3)多个碳原子可以相互结合成碳链,也可以结合成碳环,构成有机物链状或环状的碳骨架。
直链
支链
环状结构
(4)有机物分子可能只含有一个或几个碳原子,也可能含有成千上万个碳原子。
一、有机化合物中碳原子的成键特点
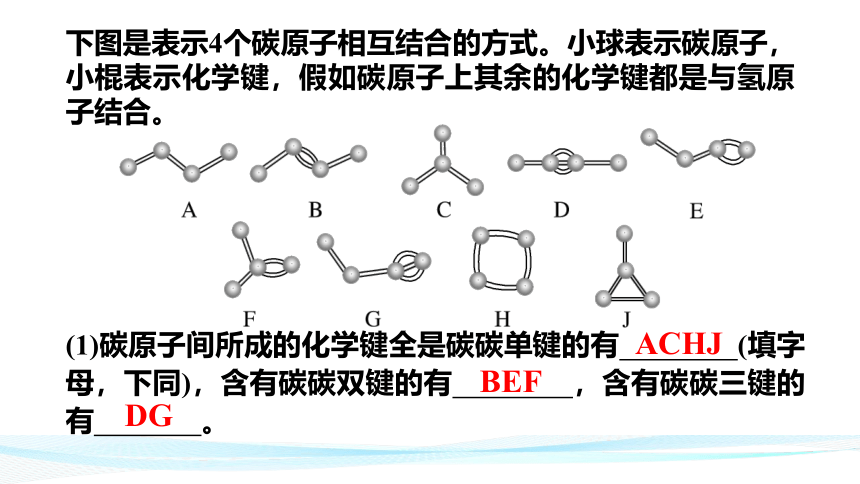
下图是表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢原子结合。
(1)碳原子间所成的化学键全是碳碳单键的有 (填字母,下同),含有碳碳双键的有 ,含有碳碳三键的有 。
ACHJ
BEF
DG
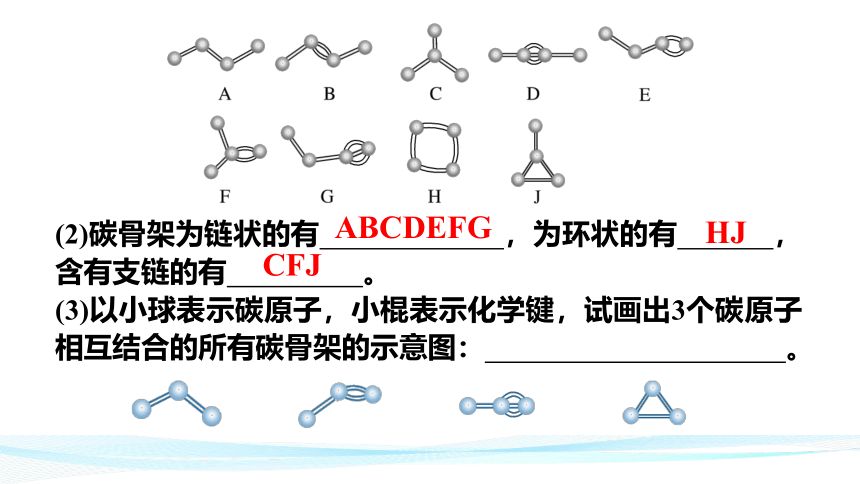
(2)碳骨架为链状的有 ,为环状的有 ,含有支链的有 。
(3)以小球表示碳原子,小棍表示化学键,试画出3个碳原子相互结合的所有碳骨架的示意图: 。
ABCDEFG
HJ
CFJ
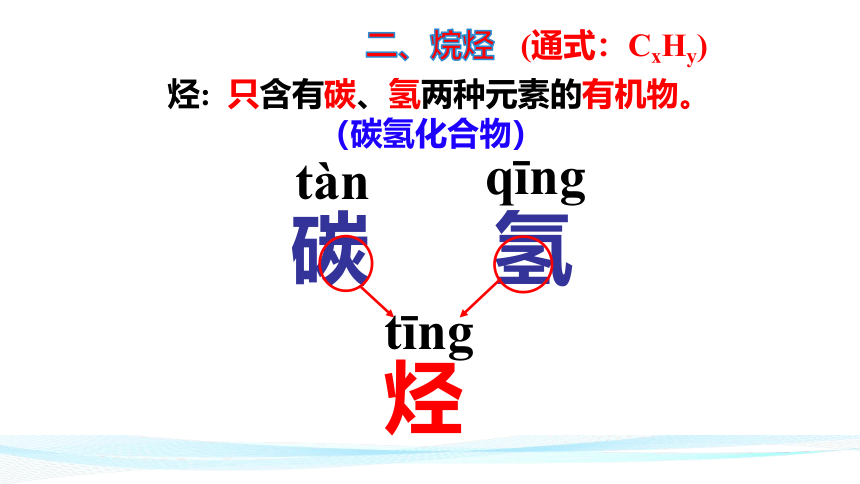
烃:
(碳氢化合物)
只含有碳、氢两种元素的有机物。
二、烷烃
(通式:CxHy)
碳
tàn
氢
qīng
烃
tīng
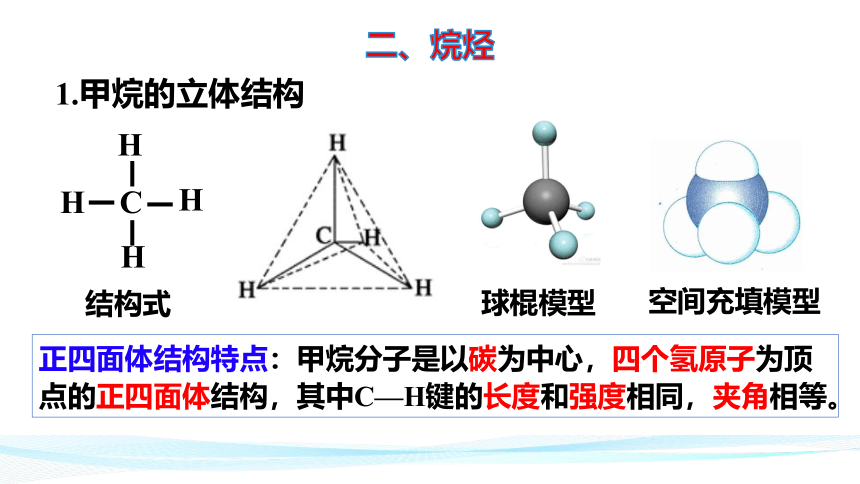
1.甲烷的立体结构
C
H
H
H
H
结构式
正四面体结构特点:甲烷分子是以碳为中心,四个氢原子为顶点的正四面体结构,其中C—H键的长度和强度相同,夹角相等。
球棍模型
空间充填模型
二、烷烃
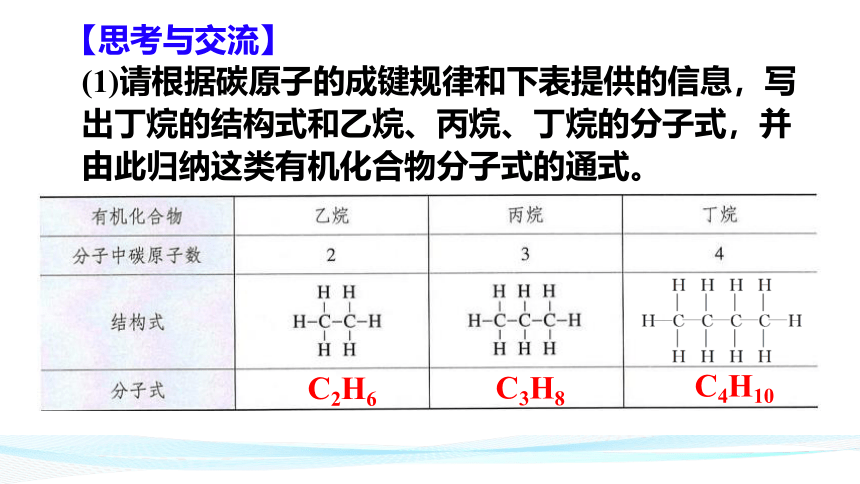
【思考与交流】
(1)请根据碳原子的成键规律和下表提供的信息,写出丁烷的结构式和乙烷、丙烷、丁烷的分子式,并由此归纳这类有机化合物分子式的通式。
C2H6
C3H8
C4H10
(2)与同学交流,比较大家写出的丁烷的结构式是否相同,思考产生这种现象的可能原因。
(3)结合图7-6中的分子结构模型,总结这类有机化合物的组成和分子结构特点。
只含碳和氢两种元素,分子中的碳原子之间都以单键结合,碳原子的剩余价键均与氢原子结合,使碳原子的化合价都达到“饱和”。
【思考与交流】
2.烷烃的结构
(1)概念:碳原子之间都以碳碳单键结合,剩余的价键均与氢原子结合,使碳原子的化合价都达到“饱和”。这样的一类有机化合物称为饱和烃,也称为烷烃。——饱和链状烃
饱和碳原子:四个共价键分别连接4个原子。
二、烷烃
(2)烷烃结构、组成特征
①碳原子间都以C-C相连、其余都是C-H键;
②每个C原子都连有4个原子,都为饱和碳原子;
③除乙烷外,其余烷烃的碳链均为非直线型,呈锯齿状;
④单键可以转动;
⑤相同碳原子数的有机物分子里,链状烷烃的含氢量最大。
二、烷烃
(3)烷烃的习惯命名
碳原子数(n)及表示
n≤10
1
2
3
4
5
6
7
8
9
10
甲烷
乙烷
丙烷
丁烷
戊烷
烷
烷
烷
烷
烷
n>10
己
庚
辛
壬
癸
相应汉字数字+烷
二、烷烃
【练一练】
写出下列烷烃的名称
C
H
H
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
H
C
H
H
C
H
H
壬烷
十一烷
烷烃的分子通式:
CnH2n+2(n≥1)
【练习 】写出下列烷烃的分子式:
(1)含有20个碳原子的烷烃
(2)含有20个氢原子的烷烃
C20H42
C9H20
丙烷
乙烷
丁烷
结构式:
结构简式:
省略C—H键
把同一C上的H合并
省略横线上C—C键
CH3-CH3
CH3CH3
CH3-CH2-CH3
CH3CH2CH3
CH3-CH2-CH2-CH3
CH3CH2CH2CH3
C2H6
C3H8
C4H10
分子式:
定义:结构相似、分子组成上相差一个或若干个CH2原子团的物质互相称为同系物。
3.同系物
化学性质相似,物理性质不同
丙烷
乙烷
丁烷
C2H6
C3H8
C4H10
二、烷烃
同:
差:
同类物质,通式同,组成元素同
组成上相差n个CH2原子团
①碳原子数不同
②分子式不同
③相对分子质量相差14n
似:
结构相似(化学键类型相似)
3.同系物
二、烷烃
【练习】
下列物质中属于同系物的是_________。
① CH2=CH-CH3 ②CH4 ③CH3CH2CH3 ④CH3(CH2)5CH(CH3)CH3 ⑤
CH2—CH2
CH2—CH2
②③④
4.同分异构现象和同分异构体
(1)同分异构现象
化合物具有相同的分子式,但具有不同的结构现象,叫做同分异构体现象。
(2)同分异构体
具有同分异构体现象的化合物互称为同分异构体。
二、烷烃
正丁烷
异丁烷
三同
分子式相同
分子组成相同
分子量相同
两不同
结构不同、性质不同
4.同分异构现象和同分异构体
二、烷烃
正戊烷
CH3CH2CH2CH2CH3
异戊烷
CH3CHCH2CH3
CH3
新戊烷
CH3
CH3CCH3
CH3
戊烷的同分异构体
以下是不是丁烷的同分异构体呢?
判断下列物质中属于同分异构体的有 。
①CH3—CH2—CH—CH3
CH3
②CH3CH2CH3
③CH3—CH—CH3
CH3
④CH3—CH2—CH2
CH3
⑥CH3—CH—CH3
CH2
CH3
CH—CH2
H3C
H3C
⑤
③和④
④和⑤
【练习】
名 称
熔点/℃
沸点/℃
相对密度
正丁烷
-138.4
-0.5
0.5788
异丁烷
-159.6
-11.7
0.557
(3) 同分异构体性质
物理性质:
支链越多,熔沸点越低,密度越小
化学性质:
不一定相同
4.同分异构现象和同分异构体
二、烷烃
正丁烷和异丁烷的某些物理性质
同分异构体的书写
书写方法:“碳链缩短法”
步骤:先写最长的碳链,然后逐个减少碳原子,把减少的碳原子作为支链连在主链上
可概括为“两注意,四句话”:
两注意:①选择最长的碳链为主链;②找出中心对称线。
四句话:①主链由长到短;②支链由整到散;③位置由心到边;④排布由对-邻-间。
有机物
碳原子成键特点
烷烃结构
烷烃的习惯命名法
同系物
同分异构
分子式相同,结构不同
甲烷正四面体
结构相似,分子式相差1个或n个CH2原子团
【小结】
概念
内 涵
比较对象
实例
同位素
同素异形体
同系物
同分异构体
质子数等,中子数
不等,原子之间
原子
氕、氚
同一元素形成的不同单质
单质
O2、O3
结构相似,组成上差一个或n个CH2
有机物
C2H6、C4H10
相同分子式,不同结构的化合物
有机物
CH3(CH2)3CH3、
C(CH3)4
【小结】
1.下列分子只表示一种物质的是( )
A.C3H7Cl B.C3H8 C.C5H12 D.C4H10
B
【课堂练习】
2.已知碳原子可以成4个价键,氢原子可以成1个价键,氧原子可以成2个价键,下列分子式或结构简式书写正确的是( )
A. CH3 B. C2H6 C. D.
B
3.下列关于同系物的说法中错误的是( )
A.同系物具有相同的最简式
B.同系物能符合同一通式
C.同系物中,相邻的同系物彼此在组成上相差一个“CH2”原子团
D.同系物的化学性质基本相似,物理性质随碳原子数增加而呈规律性变化
A
【课堂练习】
4.下列关于CH4 和 的叙述 中正确的是( )
A.均能用组成通式CnH2n+2来表示
B.与所有烷烃互为同素异形体
C.因为它们结构相似,所以它们的化学性质相似,物理性质相同
D.通常情况下它们都是气态烷烃
A
【课堂练习】
5.下列有机物中和甲烷互为同系物的为_______(填序号,下同),和CH2=CH2互为同系物的为_____,和
互为同分异构体的为______。
①CH3CH2CH3 ② ③CH2=CH—CH3
④ ⑤ ⑥
①②④
③⑥
③
【课堂练习】
有同分异构体的烷烃的命名:正、异、新
1.无支链称“正”某烷 如:
2.含 称“异”某烷
CH3—CH—
CH3
3.含 称“新”某烷
CH3—C—
CH3
CH3
CH3CH2CH2CH3
CH3—CH—CH2
CH3
第一节 认识有机化合物
第1课时 有机化合物中碳原子的成键特点
1.定义:
含有碳元素的化合物为有机物。
( 但碳的氧化物、碳酸、碳酸盐、碳的金属化合物等看作无机物。)
2.组成元素:
碳、氢、氧、氮、硫、磷、卤素等
主要元素
其他元素
有机物
1.甲烷的组成与结构
分子式:
CH4
电子式:
H
H
H
C
H
结构式:
C
H
H
H
H
一、有机化合物中碳原子的成键特点
(1)碳原子的最外层有4个电子,可与其他原子形成4个共价键,而且碳碳原子之间也能相互形成共价键。
(2)碳原子与碳原子之间不仅可以形成单键,还可以形成双键或三键。
单键( )、双键( )、三键(—C≡C—)
2.有机化合物中碳原子的成键特点
一、有机化合物中碳原子的成键特点
(3)多个碳原子可以相互结合成碳链,也可以结合成碳环,构成有机物链状或环状的碳骨架。
直链
支链
环状结构
(4)有机物分子可能只含有一个或几个碳原子,也可能含有成千上万个碳原子。
一、有机化合物中碳原子的成键特点
下图是表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢原子结合。
(1)碳原子间所成的化学键全是碳碳单键的有 (填字母,下同),含有碳碳双键的有 ,含有碳碳三键的有 。
ACHJ
BEF
DG
(2)碳骨架为链状的有 ,为环状的有 ,含有支链的有 。
(3)以小球表示碳原子,小棍表示化学键,试画出3个碳原子相互结合的所有碳骨架的示意图: 。
ABCDEFG
HJ
CFJ
烃:
(碳氢化合物)
只含有碳、氢两种元素的有机物。
二、烷烃
(通式:CxHy)
碳
tàn
氢
qīng
烃
tīng
1.甲烷的立体结构
C
H
H
H
H
结构式
正四面体结构特点:甲烷分子是以碳为中心,四个氢原子为顶点的正四面体结构,其中C—H键的长度和强度相同,夹角相等。
球棍模型
空间充填模型
二、烷烃
【思考与交流】
(1)请根据碳原子的成键规律和下表提供的信息,写出丁烷的结构式和乙烷、丙烷、丁烷的分子式,并由此归纳这类有机化合物分子式的通式。
C2H6
C3H8
C4H10
(2)与同学交流,比较大家写出的丁烷的结构式是否相同,思考产生这种现象的可能原因。
(3)结合图7-6中的分子结构模型,总结这类有机化合物的组成和分子结构特点。
只含碳和氢两种元素,分子中的碳原子之间都以单键结合,碳原子的剩余价键均与氢原子结合,使碳原子的化合价都达到“饱和”。
【思考与交流】
2.烷烃的结构
(1)概念:碳原子之间都以碳碳单键结合,剩余的价键均与氢原子结合,使碳原子的化合价都达到“饱和”。这样的一类有机化合物称为饱和烃,也称为烷烃。——饱和链状烃
饱和碳原子:四个共价键分别连接4个原子。
二、烷烃
(2)烷烃结构、组成特征
①碳原子间都以C-C相连、其余都是C-H键;
②每个C原子都连有4个原子,都为饱和碳原子;
③除乙烷外,其余烷烃的碳链均为非直线型,呈锯齿状;
④单键可以转动;
⑤相同碳原子数的有机物分子里,链状烷烃的含氢量最大。
二、烷烃
(3)烷烃的习惯命名
碳原子数(n)及表示
n≤10
1
2
3
4
5
6
7
8
9
10
甲烷
乙烷
丙烷
丁烷
戊烷
烷
烷
烷
烷
烷
n>10
己
庚
辛
壬
癸
相应汉字数字+烷
二、烷烃
【练一练】
写出下列烷烃的名称
C
H
H
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
C
H
H
H
C
H
H
C
H
H
壬烷
十一烷
烷烃的分子通式:
CnH2n+2(n≥1)
【练习 】写出下列烷烃的分子式:
(1)含有20个碳原子的烷烃
(2)含有20个氢原子的烷烃
C20H42
C9H20
丙烷
乙烷
丁烷
结构式:
结构简式:
省略C—H键
把同一C上的H合并
省略横线上C—C键
CH3-CH3
CH3CH3
CH3-CH2-CH3
CH3CH2CH3
CH3-CH2-CH2-CH3
CH3CH2CH2CH3
C2H6
C3H8
C4H10
分子式:
定义:结构相似、分子组成上相差一个或若干个CH2原子团的物质互相称为同系物。
3.同系物
化学性质相似,物理性质不同
丙烷
乙烷
丁烷
C2H6
C3H8
C4H10
二、烷烃
同:
差:
同类物质,通式同,组成元素同
组成上相差n个CH2原子团
①碳原子数不同
②分子式不同
③相对分子质量相差14n
似:
结构相似(化学键类型相似)
3.同系物
二、烷烃
【练习】
下列物质中属于同系物的是_________。
① CH2=CH-CH3 ②CH4 ③CH3CH2CH3 ④CH3(CH2)5CH(CH3)CH3 ⑤
CH2—CH2
CH2—CH2
②③④
4.同分异构现象和同分异构体
(1)同分异构现象
化合物具有相同的分子式,但具有不同的结构现象,叫做同分异构体现象。
(2)同分异构体
具有同分异构体现象的化合物互称为同分异构体。
二、烷烃
正丁烷
异丁烷
三同
分子式相同
分子组成相同
分子量相同
两不同
结构不同、性质不同
4.同分异构现象和同分异构体
二、烷烃
正戊烷
CH3CH2CH2CH2CH3
异戊烷
CH3CHCH2CH3
CH3
新戊烷
CH3
CH3CCH3
CH3
戊烷的同分异构体
以下是不是丁烷的同分异构体呢?
判断下列物质中属于同分异构体的有 。
①CH3—CH2—CH—CH3
CH3
②CH3CH2CH3
③CH3—CH—CH3
CH3
④CH3—CH2—CH2
CH3
⑥CH3—CH—CH3
CH2
CH3
CH—CH2
H3C
H3C
⑤
③和④
④和⑤
【练习】
名 称
熔点/℃
沸点/℃
相对密度
正丁烷
-138.4
-0.5
0.5788
异丁烷
-159.6
-11.7
0.557
(3) 同分异构体性质
物理性质:
支链越多,熔沸点越低,密度越小
化学性质:
不一定相同
4.同分异构现象和同分异构体
二、烷烃
正丁烷和异丁烷的某些物理性质
同分异构体的书写
书写方法:“碳链缩短法”
步骤:先写最长的碳链,然后逐个减少碳原子,把减少的碳原子作为支链连在主链上
可概括为“两注意,四句话”:
两注意:①选择最长的碳链为主链;②找出中心对称线。
四句话:①主链由长到短;②支链由整到散;③位置由心到边;④排布由对-邻-间。
有机物
碳原子成键特点
烷烃结构
烷烃的习惯命名法
同系物
同分异构
分子式相同,结构不同
甲烷正四面体
结构相似,分子式相差1个或n个CH2原子团
【小结】
概念
内 涵
比较对象
实例
同位素
同素异形体
同系物
同分异构体
质子数等,中子数
不等,原子之间
原子
氕、氚
同一元素形成的不同单质
单质
O2、O3
结构相似,组成上差一个或n个CH2
有机物
C2H6、C4H10
相同分子式,不同结构的化合物
有机物
CH3(CH2)3CH3、
C(CH3)4
【小结】
1.下列分子只表示一种物质的是( )
A.C3H7Cl B.C3H8 C.C5H12 D.C4H10
B
【课堂练习】
2.已知碳原子可以成4个价键,氢原子可以成1个价键,氧原子可以成2个价键,下列分子式或结构简式书写正确的是( )
A. CH3 B. C2H6 C. D.
B
3.下列关于同系物的说法中错误的是( )
A.同系物具有相同的最简式
B.同系物能符合同一通式
C.同系物中,相邻的同系物彼此在组成上相差一个“CH2”原子团
D.同系物的化学性质基本相似,物理性质随碳原子数增加而呈规律性变化
A
【课堂练习】
4.下列关于CH4 和 的叙述 中正确的是( )
A.均能用组成通式CnH2n+2来表示
B.与所有烷烃互为同素异形体
C.因为它们结构相似,所以它们的化学性质相似,物理性质相同
D.通常情况下它们都是气态烷烃
A
【课堂练习】
5.下列有机物中和甲烷互为同系物的为_______(填序号,下同),和CH2=CH2互为同系物的为_____,和
互为同分异构体的为______。
①CH3CH2CH3 ② ③CH2=CH—CH3
④ ⑤ ⑥
①②④
③⑥
③
【课堂练习】
有同分异构体的烷烃的命名:正、异、新
1.无支链称“正”某烷 如:
2.含 称“异”某烷
CH3—CH—
CH3
3.含 称“新”某烷
CH3—C—
CH3
CH3
CH3CH2CH2CH3
CH3—CH—CH2
CH3
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
