7.4 结晶现象 课件(21张PPT)
图片预览








文档简介
7.4 结晶现象
1.了解晶体与结晶,初步了解结晶现象;
2.掌握除去粗盐中难溶性杂质的实验方法。
3.了解过滤和结晶两种混合物分离方法的适用范围、原理和实验操作;
学习目标
一、晶体与结晶
硫酸铜
金刚石
石英
方解石
明矾
雪花
1、晶体是具有规则的几何外形的固体
怎样可以制得美丽的晶体呢?
2、形成晶体的过程叫做结晶。
在水中加入研碎的溶质
配制热的饱和溶液
冷却
有晶体析出
将水加热至沸腾
晶体可由饱和溶液形成
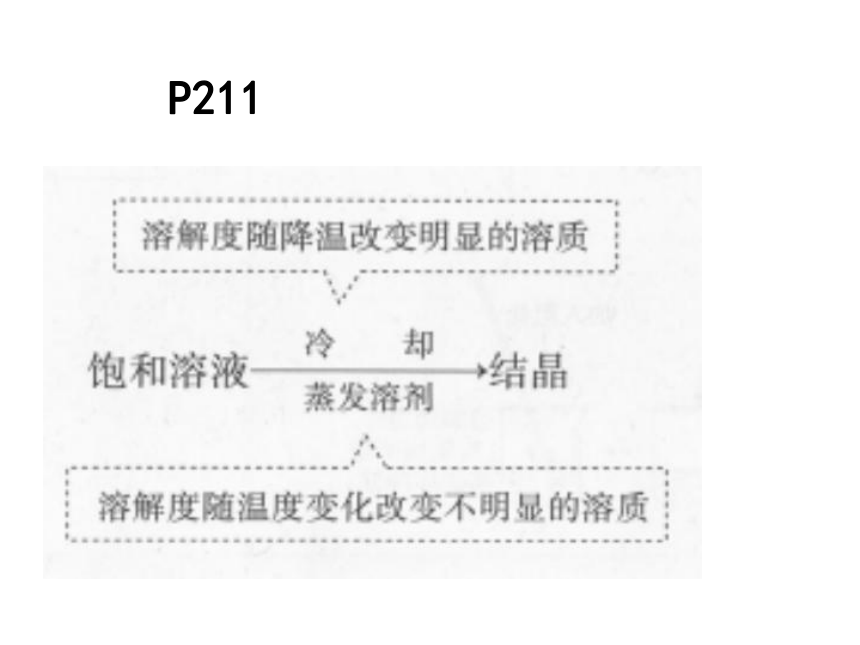
(2)蒸发溶剂结晶法:
恒温蒸发,使溶剂的量减少;
(适合用溶解度受温度影响不大的物质)
3、结晶的方法
(1)冷却结晶法:(冷却热的饱和溶液法)
保持溶剂的量不变,使溶液的温度降低。
(适用于溶解度随温度改变明显的物质)
P211
怎样制造较大的晶体?
晶体不是生物,可它也能生长。将一颗小的现成的硫酸铜晶体悬着浸入其饱和溶液中,晶体会缓慢地“生长”。如果在烧杯中继续倒入饱和硫酸铜溶液,则结晶体的增长会持续几周甚至几个月。你将会得到一颗美丽的大晶体。
二、结晶法的应用
利用结晶法,可以将我们需要的物质从含杂质的混合物中分离或提纯出来
例如,海水晒盐、蔗汁制糖
海水晒盐
粗盐的提纯
1.步骤:______________________。
2.目的:除去粗盐中_________的杂质。
溶解、过滤、蒸发
难溶性
1、溶解
不溶性
不澄清
搅拌,以加速溶解
玻璃棒的作用:
混合物
操作注意事项
滤纸要紧贴漏斗内壁;
①滤纸边缘要低于漏斗边缘
②液面要低于滤纸边缘
①盛液烧杯口要紧靠玻璃棒
②玻璃棒要紧靠三层滤纸处
③漏斗下端要紧靠烧杯内壁
(1)过滤器组成:漏斗和滤纸。
(2)过滤操作所用的仪器有_________、烧杯、_______、漏斗。
2、过滤操作(P213-214)
铁架台
玻璃棒
一贴:
二低:
三靠:
不溶性固体
食盐溶液
澄清
固
液
玻璃棒的作用:
引流
3、蒸发结晶
较多晶体
水分蒸发,晶体完全析出
氯化钠
蒸发皿尚有余热,利用余热将剩余的水分蒸发可节约能源
玻璃棒的作用:
搅拌,使液体受热均匀,防止液滴飞溅
难溶性固体和液体混合后的分离方法:
(一)过滤法
可溶性固体混合后的分离方法:
(二)结晶法
a、蒸发结晶(海水晒盐)
b、冷却结晶(分离KNO3与NaCl溶液)
小结:分离混合物的方法
1.下列各图所表示的实验操作,可以将食盐水中的食盐结晶析出的是( )
经典例题
C
2、粗盐提纯实验的部分操作如图所示,其中错误的是( )
C
第七章 溶 液
3、上述实验改正错误后,过滤一杯浑浊的水,经过两次过滤后发现滤液仍显浑浊,请你分析原因:______________________________
(写出两点即可)。
滤纸破损、液面高于滤纸边缘
4、欲使硝酸钾从其常温下的饱和溶液中快点结晶出来,应采用的最佳方法是( )
A.冷却硝酸钾的饱和溶液
B.常温下使水蒸发
C.先加热蒸发掉一部分水,然后降温
D.升高饱和溶液的温度
C
课 堂 小 结
第七章 溶 液
作业:P 214
7.4习题 4、5、
1.了解晶体与结晶,初步了解结晶现象;
2.掌握除去粗盐中难溶性杂质的实验方法。
3.了解过滤和结晶两种混合物分离方法的适用范围、原理和实验操作;
学习目标
一、晶体与结晶
硫酸铜
金刚石
石英
方解石
明矾
雪花
1、晶体是具有规则的几何外形的固体
怎样可以制得美丽的晶体呢?
2、形成晶体的过程叫做结晶。
在水中加入研碎的溶质
配制热的饱和溶液
冷却
有晶体析出
将水加热至沸腾
晶体可由饱和溶液形成
(2)蒸发溶剂结晶法:
恒温蒸发,使溶剂的量减少;
(适合用溶解度受温度影响不大的物质)
3、结晶的方法
(1)冷却结晶法:(冷却热的饱和溶液法)
保持溶剂的量不变,使溶液的温度降低。
(适用于溶解度随温度改变明显的物质)
P211
怎样制造较大的晶体?
晶体不是生物,可它也能生长。将一颗小的现成的硫酸铜晶体悬着浸入其饱和溶液中,晶体会缓慢地“生长”。如果在烧杯中继续倒入饱和硫酸铜溶液,则结晶体的增长会持续几周甚至几个月。你将会得到一颗美丽的大晶体。
二、结晶法的应用
利用结晶法,可以将我们需要的物质从含杂质的混合物中分离或提纯出来
例如,海水晒盐、蔗汁制糖
海水晒盐
粗盐的提纯
1.步骤:______________________。
2.目的:除去粗盐中_________的杂质。
溶解、过滤、蒸发
难溶性
1、溶解
不溶性
不澄清
搅拌,以加速溶解
玻璃棒的作用:
混合物
操作注意事项
滤纸要紧贴漏斗内壁;
①滤纸边缘要低于漏斗边缘
②液面要低于滤纸边缘
①盛液烧杯口要紧靠玻璃棒
②玻璃棒要紧靠三层滤纸处
③漏斗下端要紧靠烧杯内壁
(1)过滤器组成:漏斗和滤纸。
(2)过滤操作所用的仪器有_________、烧杯、_______、漏斗。
2、过滤操作(P213-214)
铁架台
玻璃棒
一贴:
二低:
三靠:
不溶性固体
食盐溶液
澄清
固
液
玻璃棒的作用:
引流
3、蒸发结晶
较多晶体
水分蒸发,晶体完全析出
氯化钠
蒸发皿尚有余热,利用余热将剩余的水分蒸发可节约能源
玻璃棒的作用:
搅拌,使液体受热均匀,防止液滴飞溅
难溶性固体和液体混合后的分离方法:
(一)过滤法
可溶性固体混合后的分离方法:
(二)结晶法
a、蒸发结晶(海水晒盐)
b、冷却结晶(分离KNO3与NaCl溶液)
小结:分离混合物的方法
1.下列各图所表示的实验操作,可以将食盐水中的食盐结晶析出的是( )
经典例题
C
2、粗盐提纯实验的部分操作如图所示,其中错误的是( )
C
第七章 溶 液
3、上述实验改正错误后,过滤一杯浑浊的水,经过两次过滤后发现滤液仍显浑浊,请你分析原因:______________________________
(写出两点即可)。
滤纸破损、液面高于滤纸边缘
4、欲使硝酸钾从其常温下的饱和溶液中快点结晶出来,应采用的最佳方法是( )
A.冷却硝酸钾的饱和溶液
B.常温下使水蒸发
C.先加热蒸发掉一部分水,然后降温
D.升高饱和溶液的温度
C
课 堂 小 结
第七章 溶 液
作业:P 214
7.4习题 4、5、
