江苏省泰州市2020-2021年高二下学期4月期中考试模拟训练化学试题三 Word版含答案
文档属性
| 名称 | 江苏省泰州市2020-2021年高二下学期4月期中考试模拟训练化学试题三 Word版含答案 |

|
|
| 格式 | docx | ||
| 文件大小 | 630.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-18 00:00:00 | ||
图片预览


文档简介
江苏省泰州市2020~2021年高二下学期期中考试模拟训三
一、单选题
1.联合国将2011年定为国际化学年,主题为化学——我们的生活,我们的未来。下列叙述中不能体现这一主题的是 ( )
A.合成光纤,让通讯更快捷 B.合成药物,让人类更健康
C.环保涂料,让环境更宜居 D.聚烯饭盒,让生活更便捷
2.下列有机化合物的名称错误的是
A.?2-甲基丁烷
B.?3-乙基戊烷
C.?2-乙基戊烷
D.?2,3-二甲基丁烷
3.分子式为C6H14的有机物共有 ( )
A.5种 B.6种 C.7种 D.8种
4.在标准状况下将11.2L甲烷和22.4L氧气混和后点燃,温度在250℃时,气体的体积是
A.11.2L B.22.4L C.33.6L D.44.8L
5.化学与科技、社会、生活有着密切的联系。下列有关说法正确的是
A.N95口罩的原材料聚丙烯是一种天然有机高分子化合物
B.中国自主研发的首个5G微基站射频芯片YD9601的主要材料是false
C.利用酒精的强氧化性可以灭活新型冠状病毒
D.白砂糖是“黑芝麻糊”的配料之一,它的主要成分是麦芽糖
6.下列说法正确的是
A.甲烷分子的比例模型为,其二氯取代物有2种结构
B.苯和乙烯都能使溴水褪色,且褪色原理相同
C.熔喷布以聚丙烯为主要原料,是生产医用口罩的重要原材料,制造聚丙烯的原料主要来自石油的裂化
D.乙烯为不饱和烃,分子中6个原子处于同一平面
7.CH3—CH=CH—C≡CCF3分子中,共面的碳原子有a个,共线的碳原子有b个,则a、b分别为
A.6,4 B.5,4 C.6,5 D.6,6
8.设阿伏加德罗常数的值为NA,下列说法不正确的是
A.0.1molC6H14中含有的共用电子对数为1.9NA
B.10g质量分数为46%的乙醇溶液中所含氧原子的总数为0.4NA
C.标准状况下,2.24L己烷中含有的分子数为0.1NA
D.1mol苯乙烯()中含有的碳碳双键数为NA
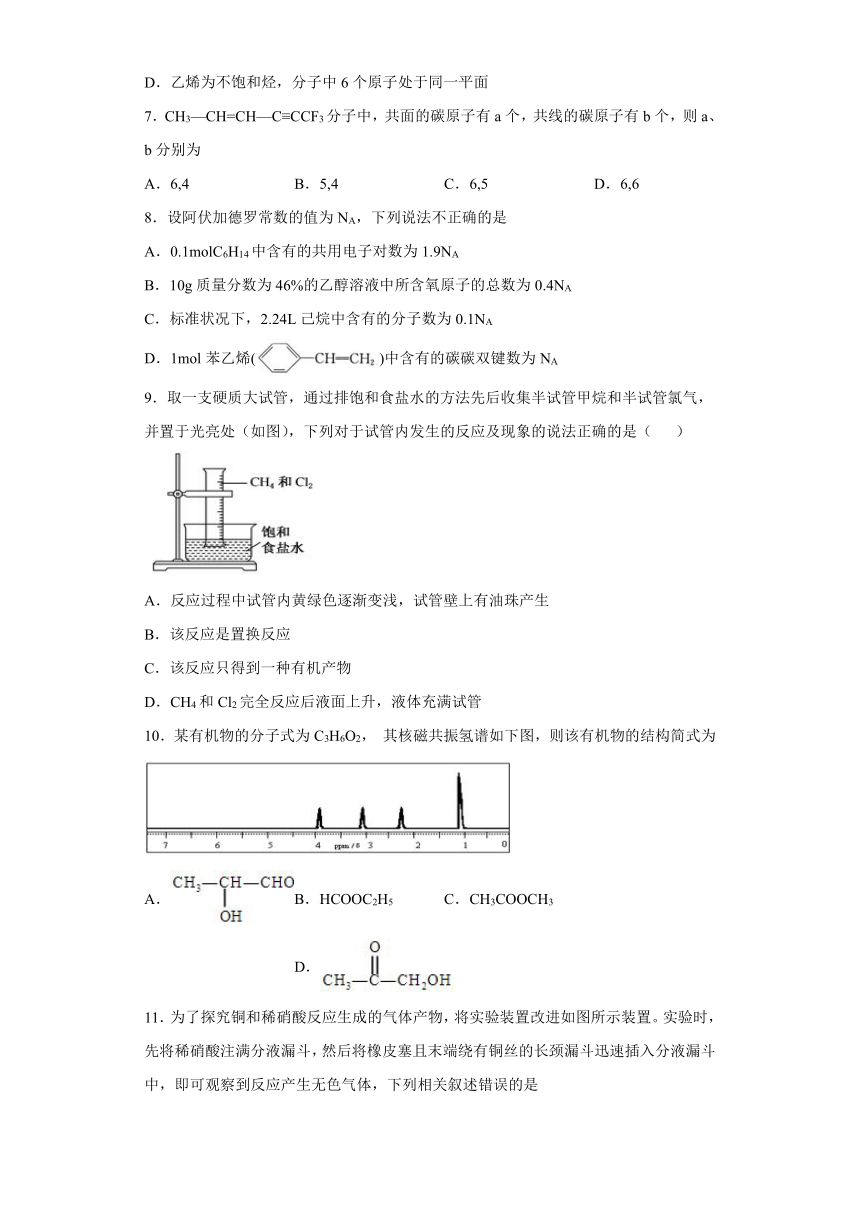
9.取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气,并置于光亮处(如图),下列对于试管内发生的反应及现象的说法正确的是( )
A.反应过程中试管内黄绿色逐渐变浅,试管壁上有油珠产生
B.该反应是置换反应
C.该反应只得到一种有机产物
D.CH4和Cl2完全反应后液面上升,液体充满试管
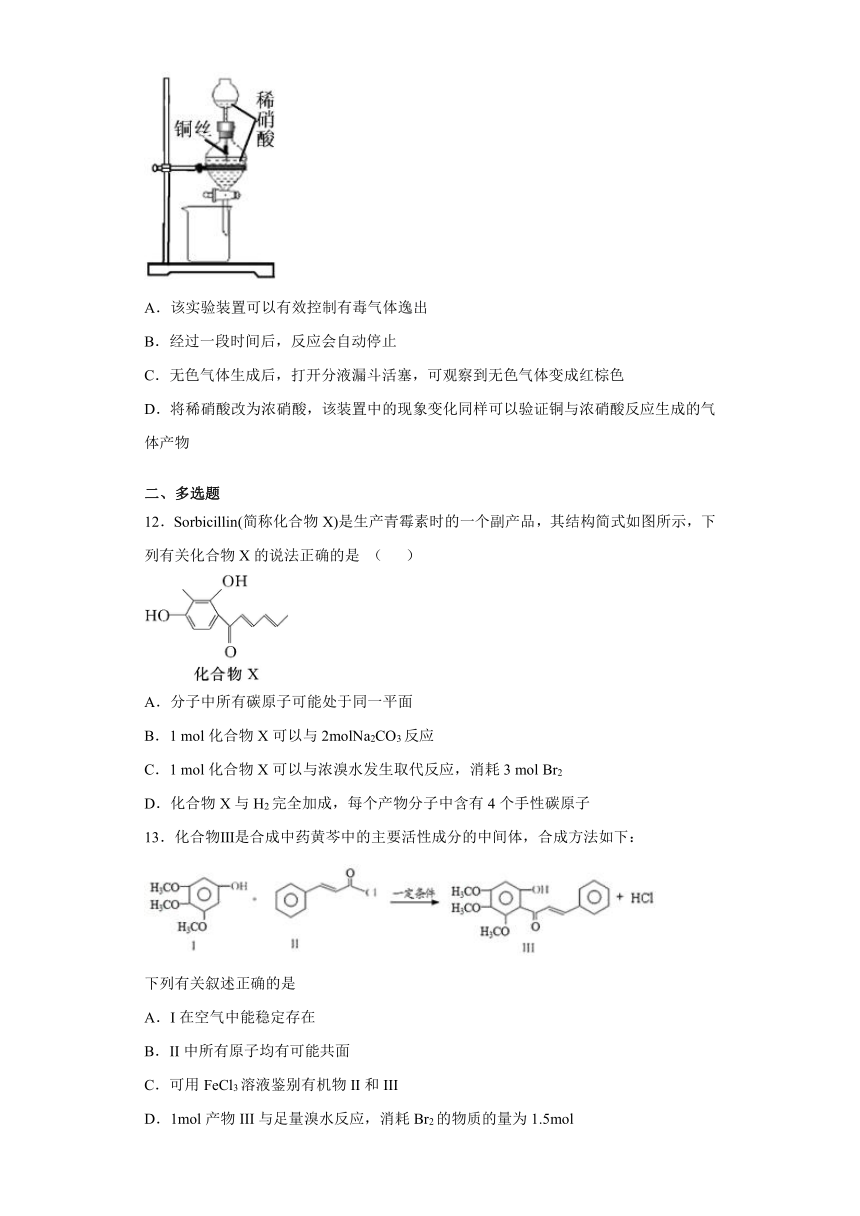
10.某有机物的分子式为C3H6O2, 其核磁共振氢谱如下图,则该有机物的结构简式为
A. B.HCOOC2H5 C.CH3COOCH3 D.
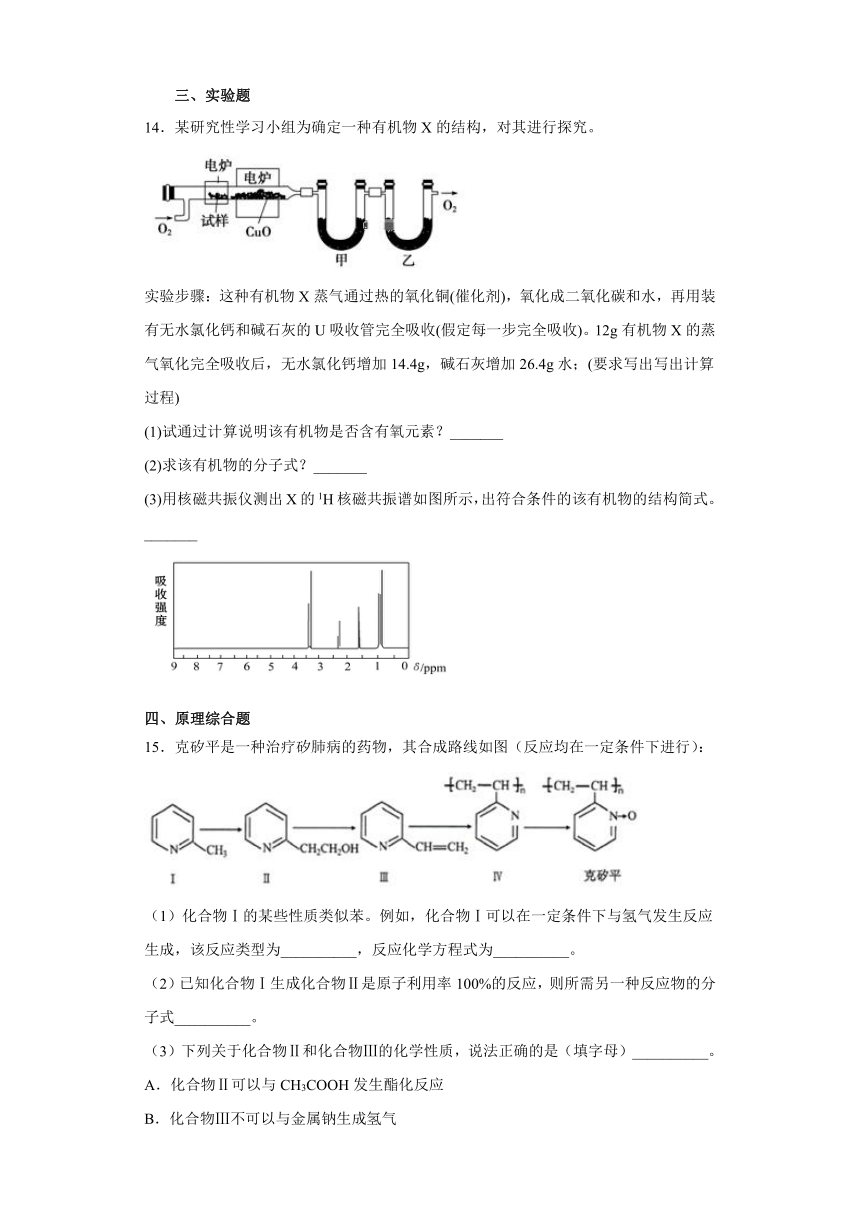
11.为了探究铜和稀硝酸反应生成的气体产物,将实验装置改进如图所示装置。实验时,先将稀硝酸注满分液漏斗,然后将橡皮塞且末端绕有铜丝的长颈漏斗迅速插入分液漏斗中,即可观察到反应产生无色气体,下列相关叙述错误的是
A.该实验装置可以有效控制有毒气体逸出
B.经过一段时间后,反应会自动停止
C.无色气体生成后,打开分液漏斗活塞,可观察到无色气体变成红棕色
D.将稀硝酸改为浓硝酸,该装置中的现象变化同样可以验证铜与浓硝酸反应生成的气体产物
二、多选题
12.Sorbicillin(简称化合物X)是生产青霉素时的一个副产品,其结构简式如图所示,下列有关化合物X的说法正确的是 ( )
A.分子中所有碳原子可能处于同一平面
B.1 mol化合物X可以与2molNa2CO3反应
C.1 mol化合物X可以与浓溴水发生取代反应,消耗3 mol Br2
D.化合物X与H2完全加成,每个产物分子中含有4个手性碳原子
13.化合物Ⅲ是合成中药黄芩中的主要活性成分的中间体,合成方法如下:
下列有关叙述正确的是
A.I在空气中能稳定存在
B.II中所有原子均有可能共面
C.可用FeCl3溶液鉴别有机物II和III
D.1mol产物III与足量溴水反应,消耗Br2的物质的量为1.5mol
三、实验题
14.某研究性学习小组为确定一种有机物X的结构,对其进行探究。
实验步骤:这种有机物X蒸气通过热的氧化铜(催化剂),氧化成二氧化碳和水,再用装有无水氯化钙和碱石灰的U吸收管完全吸收(假定每一步完全吸收)。12g有机物X的蒸气氧化完全吸收后,无水氯化钙增加14.4g,碱石灰增加26.4g水;(要求写出写出计算过程)
(1)试通过计算说明该有机物是否含有氧元素?_______
(2)求该有机物的分子式?_______
(3)用核磁共振仪测出X的1H核磁共振谱如图所示,出符合条件的该有机物的结构简式。_______
四、原理综合题
15.克矽平是一种治疗矽肺病的药物,其合成路线如图(反应均在一定条件下进行):
(1)化合物Ⅰ的某些性质类似苯。例如,化合物Ⅰ可以在一定条件下与氢气发生反应生成,该反应类型为__________,反应化学方程式为__________。
(2)已知化合物Ⅰ生成化合物Ⅱ是原子利用率100%的反应,则所需另一种反应物的分子式__________。
(3)下列关于化合物Ⅱ和化合物Ⅲ的化学性质,说法正确的是(填字母)__________。
A.化合物Ⅱ可以与CH3COOH发生酯化反应
B.化合物Ⅲ不可以与金属钠生成氢气
C.化合物Ⅲ可以使溴的四氯化碳溶液褪色
D.化合物Ⅲ不可以使酸性高锰酸钾溶液褪色
(4)下列化合物中,能发生类似于“Ⅲ→Ⅳ”反应的是(填字母)__________。
A.乙烷 B.乙烯 C.乙醇 D.苯
16.某种兴奋剂的结构简式如图:
回答下列问题:
(1)该兴奋剂与FeCl3溶液混合,现象是________________________________。
(2)滴入KMnO4酸性溶液,振荡,紫色褪去,_______(填“能”或“不能”)证明其结构中含有碳碳双键()。理由是________________________。证明其结构中含有的方法是_____________________________________(若能证明,此空可以不填)。
(3)1mol该物质分别与浓溴水和H2反应时,最多消耗Br2和H2分别为_____mol和_____mol。
五、有机推断题
17.科学家发现某药物M能治疗心血管疾病是因为它在人体内能释放出一种“信使分子”D,并阐明了D在人体内的作用原理。为此他们荣获了1998年诺贝尔生理学或医学奖。
请回答下列问题:
(1)已知M的分子量为227,由C、H、O、N周四种元素组成,C、H、N的质量分数依次为15.86%、2.20%和18.50%。则M的分子式是____________________。D是双原子分子,分子量为30,则D的分子式为_______________。
(2)油脂A经下列途径可得到M。
图中②的提示:
C2H5OH+HO-NO2falseC2H5O-NO2+ H2O
硝酸 硝酸乙酯
反应②的化学方程式是___________________。
(3)C是B和乙酸在一定条件下反应生成的化合物,分子量为134,写出C所有可能的结构简式________________。
18.医用麻醉药苄佐卡因和食品防腐剂J可由芳香烃A(质谱图显示其最大质荷比为92)来制备,其合成路线如下:
已知:I.M代表E分子结构中的一部分; II.
请回答下列问题:
(1)C的化学名称是____________;E中所含官能团的名称是______________。
(2)由A生成B和B生成C的反应类型分别为_________、__________
(3)C能与NaHCO3溶液反应,反应①的化学方程式是_________________。
(4)反应②、③中试剂II和试剂III依次是___________。(填序号)
A.高锰酸钾酸性溶液、氢氧化钠溶液
B.氢氧化钠溶液、高锰酸钾酸性溶液
(5)J有多种同分异构体,写出一种符合下列要求的同分异构体的结构简式:_______________。
a.为苯的二元取代物,其中一个取代基为羟基;
b.与J具有相同的官能团,且能发生银镜反应。
(6)写出以A为起始原料,合成涂改液的主要成分亚甲基环己烷 ( ) 的合成路线(其他无机试剂任选):______________________
19.化合物J是一种重要的有机中间体,可以由苯合成:
(1)物质D中含氧官能团名称为___________,G中官能团名称为___________。
(2)D→E的反应类型为___________。
(3)C的分子式为C10H12O2,经取代反应得到D.写出C的结构简式:___________。
(4)写出同时满足下列条件的J的一种同分异构体的结构简式:___________。
①属于芳香族化合物;②不能与金属钠反应;③有3种不同化学环境的氢原子
(5)已知:(R表示烃基,R1、R2表示氢或烃基)请写出以、为原料制备的合成路线图。(无机试剂任用,合成路线流程图示例见本题题干)。____________
参考答案
1.D
【详解】
A.光纤的化学成分是二氧化硅,合成光纤是化学变化,让通讯更快捷,能让生活更美好,故A正确;
B.用化学方法合成药物,让人类更健康,能让生活更美好,故B正确;
C.用化学方法合成环保涂料,让环境更宜居,能让生活更美好,故C正确;
D.聚烯饭盒,让生活更便捷,但能产生白色污染,不符合化学为我们的生活,我们的未来服务的理念,故D错误;
答案选D。
【点睛】
一部分化工产品在为人类提供服务,提供便捷的同时,会产生对环境的污染,例如聚乙烯,聚氯乙烯,含磷洗衣粉等,所以提倡绿色化学。
2.C
【详解】
根据烷烃的命名原则,主链有6个碳原子,名称是3-甲基己烷,不能叫2-乙基戊烷,A、B、D的命名都是正确的,C错误,故选C。
3.A
【解析】
【详解】
C6H14属于烷烃,主链为6个碳原子有:CH3(CH2)4CH3;主链为5个碳原子有:CH3CH2CH2CH(CH3)2;CH3CH2CH(CH3)CH2CH3;主链为4个碳原子有:CH3CH2C(CH3)3;CH3CH(CH3)CH(CH3)CH3,则C6H14的同分异构体共有5种。
故选A。
【点睛】
书写同分异构体时,关键在于书写的有序性和规律性:①“成直链、一线串”②“从头摘、挂中间”③“往边排、不到端”。
4.C
【详解】
甲烷和氧气反应生成水和二氧化碳:false,反应前后气体总数不变,温度为250℃时,水为气体,故11.2L甲烷和22.4L氧气混和后点燃生成气体总体积为11.2L+22.4L=33.6L,答案为C。
5.B
【详解】
A.聚丙烯是合成有机高分子化合物,不是天然有机高分子化合物,A项错误;
B.芯片的主要材料是Si ,B项正确;
C.酒精可以使蛋白质变性,但不具有强氧化性,C项错误;
D.白砂糖的主要成分是蔗糖,D项错误;
故选B。
6.D
【详解】
A.甲烷分子的比例模型为,甲烷是正四面体结构,二氯代物结构只有1种,故A不选;
B.苯和乙烯都能使溴水褪色,苯是和溴水发生萃取,乙烯是和溴水发生加成反应,故B不选;
C.聚丙烯的原料为丙烯,主要来自石油的裂解,故C不选;
D.乙烯有碳碳双键,为不饱和烃,乙烯为平面结构,分子中6个原子处于同一平面,故选D。
答案选D。
【点睛】
本题主要考查常见有机物的结构、性质、共平面以及同分异构体种类的判断,熟悉其结构特点是解题关键。
7.A
【分析】
碳碳双键上的碳原子及其相连的原子共平面,碳碳三键上的碳原子及其相连的原子共直线,共直线则一定也共平面。
【详解】
有机物共面的碳原子有6个,共线的碳原子有4个,故答案选A。
8.C
【详解】
A.根据碳氢的成键原理,1molC6H14中含有的共用电子对数为19mol,故0.1molC6H14中含有的共用电子对数为1.9NA,A正确,不选;
B.在乙醇溶液中,除了乙醇外,水也含氧原子,而10g 46%的乙醇(C2H6O)水溶液中含乙醇的质量为4.6g,物质的量为n=4.6g÷46g/mol=0.1mol,故含氧原子为0.1mol;含水的质量为5.4g,物质的量为n=5.4g÷18g/mol=0.3mol,故含氧原子为0.3mol,故此溶液中含氧原子共0.4mol,即氧原子的个数为0.4NA,故B正确,不选;
C.己烷是6个碳的烷烃,是液体,故标准状况下,2.24L己烷无法计算物质的量,C错误,符合题意;
D.苯环不含碳碳双键,故1mol苯乙烯()中含有的碳碳双键数为NA,D正确,不选;
答案选C。
9.A
【分析】
甲烷和氯气发生取代反应,产物不唯一,无法控制反应进度,据此回答问题。
【详解】
A. 反应过程中试管内黄绿色逐渐变浅,氯气不断被消耗,试管壁上有油珠产生,产生四氯化碳,A正确;
B. 该反应是取代反应,置换反应为无机反应,B错误;
C. 该反应产物不唯一,C错误;
D. CH4和Cl2完全反应后液面上升,产物一氯甲烷是气体,难溶于水,液体不会充满试管,D错误。
答案为A。
10.A
【分析】
由图示知,该有机物中有四种氢原子,且比例为1:1:1:3。
【详解】
A.该有机物中有四种H且比例为1:1:1:3,A符合题意;
B.该有机物中有三种H, B不符合题意;
C.该有机物中有两种H,C不符合题意;
D.该有机物中有三种H, D不符合题意;
故答案选A。
11.D
【详解】
A.随着反应的不断进行,Cu与稀硝酸反应生成气体,使分液漏斗内压强增大,将分液漏斗中的液体压入长颈漏斗中,可防止有毒气体的溢出,A正确;
B.随着反应的不断进行,Cu与稀硝酸反应生成气体,使分液漏斗内压强增大,将分液漏斗中的液体压入长颈漏斗中,此时分液漏斗中液面下降与Cu分开,达到控制反应开关的目的,B正确;
C.打开分液漏斗活塞,长颈漏斗中的液体下降,分液漏斗中有空气进入,使Cu与稀硝酸反应生成的NO与氧气反应生成NO2,无色气体变成红棕色,C正确;
D.将稀硝酸改为浓硝酸,Cu与浓硝酸反应生成NO2,随着反应的不断进行,硝酸浓度降低,反应产物由NO2变成NO,因原气体中存在红棕色的NO2而无法利用原实验验证NO的存在,D错误;
故选D。
12.AB
【解析】
A.分子中存在的苯环、羰基及碳碳双键均为平面结构,则所有碳原子可能处于同一平面,故A正确;B.酚羧基能与Na2CO3反应生成NaHCO3,且分子中有2个酚羟基,则1mol化合物X可以与2 molNa2CO3反应,故B正确;C.1mol化合物X最多可以3molBr2反应,其中2mol是加成,1mol发生取代,故C错误;D.化合物X中苯环、碳碳双键及羰基均能与H2完全加成反应,每个产物分子中含有3个手性碳原子,故D错误;答案为AB。
13.BC
【详解】
A.化合物I中含有酚羟基,易被氧化,因此在空气中不能稳定存在,A错误;
B.由于苯环和碳碳双键均是平面型结构,则根据化合物II的结构简式可判断,分子中所有原子均有可能共面,B正确;
C.有机物Ⅱ中不存在酚羟基,而有机物Ⅲ中含有酚羟基,则可用FeCl3溶液鉴别有机物II和III,C正确;
D.有机物Ⅲ中含有酚羟基、碳碳双键,则1mol产物III与足量溴水反应,消耗Br2的物质的量为2mol,其中加成和取代各是1mol,D错误;
答案选BC。
14.该有机物中一定含有氧元素 C3H8O CH3CH2CH2OH
【详解】
(1)false, 该有机物一定含有氧元素;
(2)falsefalsefalsefalse,该有机物的实验式为:C3H8O设该有机物的分子式为(C3H8O)n,false,分子式:C3H8O;
(3)由核磁共振谱图可以看出,X含有4种不同环境的H原子,由此推测出X的结构简式为:CH3CH2CH2OH。
15.加成反应 +3H2false CH2O A、B、C B
【详解】
(1)化合物I的结构简式为,由某些性质类似苯可知, 在一定条件下与氢气发生反应生成,反应的化学方程式为+3H2
false,故答案为:加成反应;+3H2false;
(2)由化合物Ⅰ生成化合物Ⅱ是原子利用率100%的反应可知,与甲醛发生加成反应生成,甲醛的分子式为CH2O,故答案为:CH2O;
(3)A.因化合物Ⅱ分子中含有羟基,在浓硫酸作用下,可以和CH3COOH共热发生酯化反应,故正确;
B.化合物Ⅲ不含羟基、羧基等,不可以与金属钠生成氢气,故正确;
C.化合物Ⅲ的分子中含有碳碳双键,能与溴的四氯化碳溶液发生加成反应,使溴的四氯化碳溶液褪色,故正确;
D.化合物Ⅲ的分子中含有碳碳双键,能与酸性高锰酸钾溶液发生氧化反应,使酸性高锰酸钾溶液褪色,故错误;
ABC正确,故答案为:A、B、C;
(4)化合物Ⅲ含有碳碳双键,一定条件下,能发生加聚反应反应生成化合物Ⅳ,乙烯含有碳碳双键,与化合物Ⅲ性质相似,也能发生加聚反应生成聚乙烯,B正确,故答案为:B。
16.溶液显紫色 不能 酚羟基具有还原性也可使KMnO4酸性溶液褪色 先使之与足量NaOH反应,再滴加KMnO4酸性溶液或溴水,若褪色,证明存在 4 7
【分析】
该有机物含有酚羟基,可发生取代、氧化和显色反应;含有碳碳双键,可发生加成、加聚和氧化反应,结合酚和烯烃的性质分析解答。
【详解】
(1) 分子中含有酚羟基,可与氯化铁发生显色反应,与FeCl3溶液混合,溶液显紫色,故答案为:溶液显紫色;
(2) 分子中含有酚羟基、碳碳双键和烃基,都可被酸性高锰酸钾氧化,因此滴入KMnO4酸性溶液,振荡,紫色褪去,不能证明其结构中含有碳碳双键()。要证明碳碳双键的存在,可以先使之与足量NaOH反应,再滴加KMnO4酸性溶液或溴水,若褪色,则可以证明存在,故答案为:不能;酚羟基具有还原性,也可使KMnO4酸性溶液褪色;先使之与足量NaOH反应,再滴加KMnO4酸性溶液或溴水,若褪色,证明存在;
(3)分子中含有酚羟基,共有3个邻位氢原子可被取代,且含有1个碳碳双键,则1mol该物质最多与4mol溴发生反应;分子中含有2个苯环和1个碳碳双键,则1mol该物质最多可与7mol氢气发生加成反应,故答案为:4;7。
【点睛】
本题的易错点为(2),要注意检验碳碳双键需要排除酚羟基的影响。
17.C3H5O9N3 NO
【分析】
由M的相对分子质量227及C、H、O、N的质量分数,推知n(C)=227g×15.86%÷12g/mol=3 mol,n(H)=227g×2.20%÷1g/mol=5 mol,n(N)=227g×18.50%÷14g/mol=3 mol,
n(O)=227g×63.44%÷16g/mol=9 mol,所以M的化学式为C3H5O9N3。又由题意知D是M释放出的双原子分子,相对分子质量为30,可推出D为NO,以此解答。
【详解】
(1)由分析可知,M的化学式为C3H5O9N3,D为NO;
(2)油脂是由高级脂肪酸和甘油(丙三醇)经酯化反应而制得的一类化合物,由油脂的通式及油脂的性质可知,反应①生成甘油和高级脂肪酸,甘油与硝酸反应方程式为。
(3)C是丙三醇与乙酸发生酯化反应生成的相对分子质量为134的化合物,可推知C为。
18.对硝基苯甲酸或4-硝基苯甲酸 酯基、氨基 取代反应 氧化反应 A (任写一种)
【详解】
分析流程图,先分析下面一条流程,A为芳香烃,相对分子质量为92,在Cl2/FeCl3条件下发生苯环上的卤代生成F,则A应为C7H8,所以A为,结合J的结构可知,F为,J中含有酯基,为羧基与羟基反应而来,表明流程中反应会生成羧基,则试剂II为酸性高锰酸钾溶液,甲基被氧化为羧基,则G为,J中含有酚羟基,应由Cl为-OH取代得到,则试III为氢氧化钠溶液,则H为,经过酸化,得到I,则I为,在试剂I中加热,发生酯化反应,生成J,则试剂I为CH3CH2OH和浓硫酸;再分析上面一条流程,A在浓硝酸,浓硫酸加热条件下,发生硝化反应,在对位,则B为,经过酸性高锰酸钾溶液反应,生成羧酸,则C为,在试剂I,即CH3CH2OH发生酯化反应,生成D,则D为,硝基在Fe/HCl作用下,被还原为-NH2,则E为。
(1)C为,名称为对硝基苯甲酸,E为:,其中含有的官能团为-NH2,-COO-,其名称分别为:氨基、酯基,故答案为对硝基苯甲酸;氨基、酯基;
(2)根据上述分析,A生成B为甲苯发生的硝化反应,也属于取代反应;B生成C为中甲基被氧化的反应,故答案为取代反应;氧化反应;
(3)C为,能与NaHCO3溶液反应,反应①为C与CH3CH2OH发生酯化反应,生成,反应方程式为:,故答案为;
(4)根据上述分析,反应②、③中试剂II和试剂III依次是酸性高锰酸钾溶液、NaOH溶液,故选A;
(5)J为,有多种同分异构体,其中符合a.为苯的二元取代物,其中一个取代基为羟基;?b.与J具有相同的官能团,且能发生银镜反应,说明含有酯基和醛基,则为甲酸酯;满足条件的同分异构体有:(包括间位和对位)、(包括间位和对位),共有6种,故答案为(或间位或对位)、(或间位或对位)(任写一种);
(6)A为,以A为起始原料,合成亚甲基环己烷(?),六元环可以由苯环与氢气加成得到,碳碳双键可以首先引入卤素原子,然后消去即可,可考虑如下流程:,故答案为。
19.羰基 溴原子 还原反应
【分析】
由A、B结构可知,A与发生反应生成B,B与锌汞齐(Zn-Hg)在浓盐酸条件下发生反应生成C,由已知反应和B的结构可知C的结构为,C发生反应生成D为,D与锌汞齐(Zn-Hg)在浓盐酸条件下发生反应生成E为,E发生去氢反应生成F为,F发生卤代反应生成G为,G与Mg在乙醚存在的条件下生成H为,H与环氧乙烷反应后再水解生成I为,I被CrO3氧化得到J为,据此解答。
【详解】
(1)由结构简式可知,D中含氧官能团名称为羰基,G中官能团名称为溴原子,故答案为:羰基;溴原子;
(2) D与锌汞齐(Zn-Hg)在浓盐酸条件下发生反应生成E为,反应类型为还原反应,故答案为:还原反应;
(3)C的分子式为C10H12O2,由已知反应和B的结构可知C的结构为,故答案为:;
(4)①属于芳香族化合物,说明含有苯环;②不能与金属钠反应,说明不含有羟基;③有3种不同化学环境的氢原子,说明有3种位置不同的氢原子,符合这三个条件的J的同分异构体为:,故答案为:;
(5)在无水乙醚和Mg的条件下生成,和、H2O反应生成,被CrO3氧化为,根据已知条件和、H2O生成,在浓硫酸、加热条件下发生消去反应生成。合成路线为:
,
故答案为:
。
一、单选题
1.联合国将2011年定为国际化学年,主题为化学——我们的生活,我们的未来。下列叙述中不能体现这一主题的是 ( )
A.合成光纤,让通讯更快捷 B.合成药物,让人类更健康
C.环保涂料,让环境更宜居 D.聚烯饭盒,让生活更便捷
2.下列有机化合物的名称错误的是
A.?2-甲基丁烷
B.?3-乙基戊烷
C.?2-乙基戊烷
D.?2,3-二甲基丁烷
3.分子式为C6H14的有机物共有 ( )
A.5种 B.6种 C.7种 D.8种
4.在标准状况下将11.2L甲烷和22.4L氧气混和后点燃,温度在250℃时,气体的体积是
A.11.2L B.22.4L C.33.6L D.44.8L
5.化学与科技、社会、生活有着密切的联系。下列有关说法正确的是
A.N95口罩的原材料聚丙烯是一种天然有机高分子化合物
B.中国自主研发的首个5G微基站射频芯片YD9601的主要材料是false
C.利用酒精的强氧化性可以灭活新型冠状病毒
D.白砂糖是“黑芝麻糊”的配料之一,它的主要成分是麦芽糖
6.下列说法正确的是
A.甲烷分子的比例模型为,其二氯取代物有2种结构
B.苯和乙烯都能使溴水褪色,且褪色原理相同
C.熔喷布以聚丙烯为主要原料,是生产医用口罩的重要原材料,制造聚丙烯的原料主要来自石油的裂化
D.乙烯为不饱和烃,分子中6个原子处于同一平面
7.CH3—CH=CH—C≡CCF3分子中,共面的碳原子有a个,共线的碳原子有b个,则a、b分别为
A.6,4 B.5,4 C.6,5 D.6,6
8.设阿伏加德罗常数的值为NA,下列说法不正确的是
A.0.1molC6H14中含有的共用电子对数为1.9NA
B.10g质量分数为46%的乙醇溶液中所含氧原子的总数为0.4NA
C.标准状况下,2.24L己烷中含有的分子数为0.1NA
D.1mol苯乙烯()中含有的碳碳双键数为NA
9.取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气,并置于光亮处(如图),下列对于试管内发生的反应及现象的说法正确的是( )
A.反应过程中试管内黄绿色逐渐变浅,试管壁上有油珠产生
B.该反应是置换反应
C.该反应只得到一种有机产物
D.CH4和Cl2完全反应后液面上升,液体充满试管
10.某有机物的分子式为C3H6O2, 其核磁共振氢谱如下图,则该有机物的结构简式为
A. B.HCOOC2H5 C.CH3COOCH3 D.
11.为了探究铜和稀硝酸反应生成的气体产物,将实验装置改进如图所示装置。实验时,先将稀硝酸注满分液漏斗,然后将橡皮塞且末端绕有铜丝的长颈漏斗迅速插入分液漏斗中,即可观察到反应产生无色气体,下列相关叙述错误的是
A.该实验装置可以有效控制有毒气体逸出
B.经过一段时间后,反应会自动停止
C.无色气体生成后,打开分液漏斗活塞,可观察到无色气体变成红棕色
D.将稀硝酸改为浓硝酸,该装置中的现象变化同样可以验证铜与浓硝酸反应生成的气体产物
二、多选题
12.Sorbicillin(简称化合物X)是生产青霉素时的一个副产品,其结构简式如图所示,下列有关化合物X的说法正确的是 ( )
A.分子中所有碳原子可能处于同一平面
B.1 mol化合物X可以与2molNa2CO3反应
C.1 mol化合物X可以与浓溴水发生取代反应,消耗3 mol Br2
D.化合物X与H2完全加成,每个产物分子中含有4个手性碳原子
13.化合物Ⅲ是合成中药黄芩中的主要活性成分的中间体,合成方法如下:
下列有关叙述正确的是
A.I在空气中能稳定存在
B.II中所有原子均有可能共面
C.可用FeCl3溶液鉴别有机物II和III
D.1mol产物III与足量溴水反应,消耗Br2的物质的量为1.5mol
三、实验题
14.某研究性学习小组为确定一种有机物X的结构,对其进行探究。
实验步骤:这种有机物X蒸气通过热的氧化铜(催化剂),氧化成二氧化碳和水,再用装有无水氯化钙和碱石灰的U吸收管完全吸收(假定每一步完全吸收)。12g有机物X的蒸气氧化完全吸收后,无水氯化钙增加14.4g,碱石灰增加26.4g水;(要求写出写出计算过程)
(1)试通过计算说明该有机物是否含有氧元素?_______
(2)求该有机物的分子式?_______
(3)用核磁共振仪测出X的1H核磁共振谱如图所示,出符合条件的该有机物的结构简式。_______
四、原理综合题
15.克矽平是一种治疗矽肺病的药物,其合成路线如图(反应均在一定条件下进行):
(1)化合物Ⅰ的某些性质类似苯。例如,化合物Ⅰ可以在一定条件下与氢气发生反应生成,该反应类型为__________,反应化学方程式为__________。
(2)已知化合物Ⅰ生成化合物Ⅱ是原子利用率100%的反应,则所需另一种反应物的分子式__________。
(3)下列关于化合物Ⅱ和化合物Ⅲ的化学性质,说法正确的是(填字母)__________。
A.化合物Ⅱ可以与CH3COOH发生酯化反应
B.化合物Ⅲ不可以与金属钠生成氢气
C.化合物Ⅲ可以使溴的四氯化碳溶液褪色
D.化合物Ⅲ不可以使酸性高锰酸钾溶液褪色
(4)下列化合物中,能发生类似于“Ⅲ→Ⅳ”反应的是(填字母)__________。
A.乙烷 B.乙烯 C.乙醇 D.苯
16.某种兴奋剂的结构简式如图:
回答下列问题:
(1)该兴奋剂与FeCl3溶液混合,现象是________________________________。
(2)滴入KMnO4酸性溶液,振荡,紫色褪去,_______(填“能”或“不能”)证明其结构中含有碳碳双键()。理由是________________________。证明其结构中含有的方法是_____________________________________(若能证明,此空可以不填)。
(3)1mol该物质分别与浓溴水和H2反应时,最多消耗Br2和H2分别为_____mol和_____mol。
五、有机推断题
17.科学家发现某药物M能治疗心血管疾病是因为它在人体内能释放出一种“信使分子”D,并阐明了D在人体内的作用原理。为此他们荣获了1998年诺贝尔生理学或医学奖。
请回答下列问题:
(1)已知M的分子量为227,由C、H、O、N周四种元素组成,C、H、N的质量分数依次为15.86%、2.20%和18.50%。则M的分子式是____________________。D是双原子分子,分子量为30,则D的分子式为_______________。
(2)油脂A经下列途径可得到M。
图中②的提示:
C2H5OH+HO-NO2falseC2H5O-NO2+ H2O
硝酸 硝酸乙酯
反应②的化学方程式是___________________。
(3)C是B和乙酸在一定条件下反应生成的化合物,分子量为134,写出C所有可能的结构简式________________。
18.医用麻醉药苄佐卡因和食品防腐剂J可由芳香烃A(质谱图显示其最大质荷比为92)来制备,其合成路线如下:
已知:I.M代表E分子结构中的一部分; II.
请回答下列问题:
(1)C的化学名称是____________;E中所含官能团的名称是______________。
(2)由A生成B和B生成C的反应类型分别为_________、__________
(3)C能与NaHCO3溶液反应,反应①的化学方程式是_________________。
(4)反应②、③中试剂II和试剂III依次是___________。(填序号)
A.高锰酸钾酸性溶液、氢氧化钠溶液
B.氢氧化钠溶液、高锰酸钾酸性溶液
(5)J有多种同分异构体,写出一种符合下列要求的同分异构体的结构简式:_______________。
a.为苯的二元取代物,其中一个取代基为羟基;
b.与J具有相同的官能团,且能发生银镜反应。
(6)写出以A为起始原料,合成涂改液的主要成分亚甲基环己烷 ( ) 的合成路线(其他无机试剂任选):______________________
19.化合物J是一种重要的有机中间体,可以由苯合成:
(1)物质D中含氧官能团名称为___________,G中官能团名称为___________。
(2)D→E的反应类型为___________。
(3)C的分子式为C10H12O2,经取代反应得到D.写出C的结构简式:___________。
(4)写出同时满足下列条件的J的一种同分异构体的结构简式:___________。
①属于芳香族化合物;②不能与金属钠反应;③有3种不同化学环境的氢原子
(5)已知:(R表示烃基,R1、R2表示氢或烃基)请写出以、为原料制备的合成路线图。(无机试剂任用,合成路线流程图示例见本题题干)。____________
参考答案
1.D
【详解】
A.光纤的化学成分是二氧化硅,合成光纤是化学变化,让通讯更快捷,能让生活更美好,故A正确;
B.用化学方法合成药物,让人类更健康,能让生活更美好,故B正确;
C.用化学方法合成环保涂料,让环境更宜居,能让生活更美好,故C正确;
D.聚烯饭盒,让生活更便捷,但能产生白色污染,不符合化学为我们的生活,我们的未来服务的理念,故D错误;
答案选D。
【点睛】
一部分化工产品在为人类提供服务,提供便捷的同时,会产生对环境的污染,例如聚乙烯,聚氯乙烯,含磷洗衣粉等,所以提倡绿色化学。
2.C
【详解】
根据烷烃的命名原则,主链有6个碳原子,名称是3-甲基己烷,不能叫2-乙基戊烷,A、B、D的命名都是正确的,C错误,故选C。
3.A
【解析】
【详解】
C6H14属于烷烃,主链为6个碳原子有:CH3(CH2)4CH3;主链为5个碳原子有:CH3CH2CH2CH(CH3)2;CH3CH2CH(CH3)CH2CH3;主链为4个碳原子有:CH3CH2C(CH3)3;CH3CH(CH3)CH(CH3)CH3,则C6H14的同分异构体共有5种。
故选A。
【点睛】
书写同分异构体时,关键在于书写的有序性和规律性:①“成直链、一线串”②“从头摘、挂中间”③“往边排、不到端”。
4.C
【详解】
甲烷和氧气反应生成水和二氧化碳:false,反应前后气体总数不变,温度为250℃时,水为气体,故11.2L甲烷和22.4L氧气混和后点燃生成气体总体积为11.2L+22.4L=33.6L,答案为C。
5.B
【详解】
A.聚丙烯是合成有机高分子化合物,不是天然有机高分子化合物,A项错误;
B.芯片的主要材料是Si ,B项正确;
C.酒精可以使蛋白质变性,但不具有强氧化性,C项错误;
D.白砂糖的主要成分是蔗糖,D项错误;
故选B。
6.D
【详解】
A.甲烷分子的比例模型为,甲烷是正四面体结构,二氯代物结构只有1种,故A不选;
B.苯和乙烯都能使溴水褪色,苯是和溴水发生萃取,乙烯是和溴水发生加成反应,故B不选;
C.聚丙烯的原料为丙烯,主要来自石油的裂解,故C不选;
D.乙烯有碳碳双键,为不饱和烃,乙烯为平面结构,分子中6个原子处于同一平面,故选D。
答案选D。
【点睛】
本题主要考查常见有机物的结构、性质、共平面以及同分异构体种类的判断,熟悉其结构特点是解题关键。
7.A
【分析】
碳碳双键上的碳原子及其相连的原子共平面,碳碳三键上的碳原子及其相连的原子共直线,共直线则一定也共平面。
【详解】
有机物共面的碳原子有6个,共线的碳原子有4个,故答案选A。
8.C
【详解】
A.根据碳氢的成键原理,1molC6H14中含有的共用电子对数为19mol,故0.1molC6H14中含有的共用电子对数为1.9NA,A正确,不选;
B.在乙醇溶液中,除了乙醇外,水也含氧原子,而10g 46%的乙醇(C2H6O)水溶液中含乙醇的质量为4.6g,物质的量为n=4.6g÷46g/mol=0.1mol,故含氧原子为0.1mol;含水的质量为5.4g,物质的量为n=5.4g÷18g/mol=0.3mol,故含氧原子为0.3mol,故此溶液中含氧原子共0.4mol,即氧原子的个数为0.4NA,故B正确,不选;
C.己烷是6个碳的烷烃,是液体,故标准状况下,2.24L己烷无法计算物质的量,C错误,符合题意;
D.苯环不含碳碳双键,故1mol苯乙烯()中含有的碳碳双键数为NA,D正确,不选;
答案选C。
9.A
【分析】
甲烷和氯气发生取代反应,产物不唯一,无法控制反应进度,据此回答问题。
【详解】
A. 反应过程中试管内黄绿色逐渐变浅,氯气不断被消耗,试管壁上有油珠产生,产生四氯化碳,A正确;
B. 该反应是取代反应,置换反应为无机反应,B错误;
C. 该反应产物不唯一,C错误;
D. CH4和Cl2完全反应后液面上升,产物一氯甲烷是气体,难溶于水,液体不会充满试管,D错误。
答案为A。
10.A
【分析】
由图示知,该有机物中有四种氢原子,且比例为1:1:1:3。
【详解】
A.该有机物中有四种H且比例为1:1:1:3,A符合题意;
B.该有机物中有三种H, B不符合题意;
C.该有机物中有两种H,C不符合题意;
D.该有机物中有三种H, D不符合题意;
故答案选A。
11.D
【详解】
A.随着反应的不断进行,Cu与稀硝酸反应生成气体,使分液漏斗内压强增大,将分液漏斗中的液体压入长颈漏斗中,可防止有毒气体的溢出,A正确;
B.随着反应的不断进行,Cu与稀硝酸反应生成气体,使分液漏斗内压强增大,将分液漏斗中的液体压入长颈漏斗中,此时分液漏斗中液面下降与Cu分开,达到控制反应开关的目的,B正确;
C.打开分液漏斗活塞,长颈漏斗中的液体下降,分液漏斗中有空气进入,使Cu与稀硝酸反应生成的NO与氧气反应生成NO2,无色气体变成红棕色,C正确;
D.将稀硝酸改为浓硝酸,Cu与浓硝酸反应生成NO2,随着反应的不断进行,硝酸浓度降低,反应产物由NO2变成NO,因原气体中存在红棕色的NO2而无法利用原实验验证NO的存在,D错误;
故选D。
12.AB
【解析】
A.分子中存在的苯环、羰基及碳碳双键均为平面结构,则所有碳原子可能处于同一平面,故A正确;B.酚羧基能与Na2CO3反应生成NaHCO3,且分子中有2个酚羟基,则1mol化合物X可以与2 molNa2CO3反应,故B正确;C.1mol化合物X最多可以3molBr2反应,其中2mol是加成,1mol发生取代,故C错误;D.化合物X中苯环、碳碳双键及羰基均能与H2完全加成反应,每个产物分子中含有3个手性碳原子,故D错误;答案为AB。
13.BC
【详解】
A.化合物I中含有酚羟基,易被氧化,因此在空气中不能稳定存在,A错误;
B.由于苯环和碳碳双键均是平面型结构,则根据化合物II的结构简式可判断,分子中所有原子均有可能共面,B正确;
C.有机物Ⅱ中不存在酚羟基,而有机物Ⅲ中含有酚羟基,则可用FeCl3溶液鉴别有机物II和III,C正确;
D.有机物Ⅲ中含有酚羟基、碳碳双键,则1mol产物III与足量溴水反应,消耗Br2的物质的量为2mol,其中加成和取代各是1mol,D错误;
答案选BC。
14.该有机物中一定含有氧元素 C3H8O CH3CH2CH2OH
【详解】
(1)false, 该有机物一定含有氧元素;
(2)falsefalsefalsefalse,该有机物的实验式为:C3H8O设该有机物的分子式为(C3H8O)n,false,分子式:C3H8O;
(3)由核磁共振谱图可以看出,X含有4种不同环境的H原子,由此推测出X的结构简式为:CH3CH2CH2OH。
15.加成反应 +3H2false CH2O A、B、C B
【详解】
(1)化合物I的结构简式为,由某些性质类似苯可知, 在一定条件下与氢气发生反应生成,反应的化学方程式为+3H2
false,故答案为:加成反应;+3H2false;
(2)由化合物Ⅰ生成化合物Ⅱ是原子利用率100%的反应可知,与甲醛发生加成反应生成,甲醛的分子式为CH2O,故答案为:CH2O;
(3)A.因化合物Ⅱ分子中含有羟基,在浓硫酸作用下,可以和CH3COOH共热发生酯化反应,故正确;
B.化合物Ⅲ不含羟基、羧基等,不可以与金属钠生成氢气,故正确;
C.化合物Ⅲ的分子中含有碳碳双键,能与溴的四氯化碳溶液发生加成反应,使溴的四氯化碳溶液褪色,故正确;
D.化合物Ⅲ的分子中含有碳碳双键,能与酸性高锰酸钾溶液发生氧化反应,使酸性高锰酸钾溶液褪色,故错误;
ABC正确,故答案为:A、B、C;
(4)化合物Ⅲ含有碳碳双键,一定条件下,能发生加聚反应反应生成化合物Ⅳ,乙烯含有碳碳双键,与化合物Ⅲ性质相似,也能发生加聚反应生成聚乙烯,B正确,故答案为:B。
16.溶液显紫色 不能 酚羟基具有还原性也可使KMnO4酸性溶液褪色 先使之与足量NaOH反应,再滴加KMnO4酸性溶液或溴水,若褪色,证明存在 4 7
【分析】
该有机物含有酚羟基,可发生取代、氧化和显色反应;含有碳碳双键,可发生加成、加聚和氧化反应,结合酚和烯烃的性质分析解答。
【详解】
(1) 分子中含有酚羟基,可与氯化铁发生显色反应,与FeCl3溶液混合,溶液显紫色,故答案为:溶液显紫色;
(2) 分子中含有酚羟基、碳碳双键和烃基,都可被酸性高锰酸钾氧化,因此滴入KMnO4酸性溶液,振荡,紫色褪去,不能证明其结构中含有碳碳双键()。要证明碳碳双键的存在,可以先使之与足量NaOH反应,再滴加KMnO4酸性溶液或溴水,若褪色,则可以证明存在,故答案为:不能;酚羟基具有还原性,也可使KMnO4酸性溶液褪色;先使之与足量NaOH反应,再滴加KMnO4酸性溶液或溴水,若褪色,证明存在;
(3)分子中含有酚羟基,共有3个邻位氢原子可被取代,且含有1个碳碳双键,则1mol该物质最多与4mol溴发生反应;分子中含有2个苯环和1个碳碳双键,则1mol该物质最多可与7mol氢气发生加成反应,故答案为:4;7。
【点睛】
本题的易错点为(2),要注意检验碳碳双键需要排除酚羟基的影响。
17.C3H5O9N3 NO
【分析】
由M的相对分子质量227及C、H、O、N的质量分数,推知n(C)=227g×15.86%÷12g/mol=3 mol,n(H)=227g×2.20%÷1g/mol=5 mol,n(N)=227g×18.50%÷14g/mol=3 mol,
n(O)=227g×63.44%÷16g/mol=9 mol,所以M的化学式为C3H5O9N3。又由题意知D是M释放出的双原子分子,相对分子质量为30,可推出D为NO,以此解答。
【详解】
(1)由分析可知,M的化学式为C3H5O9N3,D为NO;
(2)油脂是由高级脂肪酸和甘油(丙三醇)经酯化反应而制得的一类化合物,由油脂的通式及油脂的性质可知,反应①生成甘油和高级脂肪酸,甘油与硝酸反应方程式为。
(3)C是丙三醇与乙酸发生酯化反应生成的相对分子质量为134的化合物,可推知C为。
18.对硝基苯甲酸或4-硝基苯甲酸 酯基、氨基 取代反应 氧化反应 A (任写一种)
【详解】
分析流程图,先分析下面一条流程,A为芳香烃,相对分子质量为92,在Cl2/FeCl3条件下发生苯环上的卤代生成F,则A应为C7H8,所以A为,结合J的结构可知,F为,J中含有酯基,为羧基与羟基反应而来,表明流程中反应会生成羧基,则试剂II为酸性高锰酸钾溶液,甲基被氧化为羧基,则G为,J中含有酚羟基,应由Cl为-OH取代得到,则试III为氢氧化钠溶液,则H为,经过酸化,得到I,则I为,在试剂I中加热,发生酯化反应,生成J,则试剂I为CH3CH2OH和浓硫酸;再分析上面一条流程,A在浓硝酸,浓硫酸加热条件下,发生硝化反应,在对位,则B为,经过酸性高锰酸钾溶液反应,生成羧酸,则C为,在试剂I,即CH3CH2OH发生酯化反应,生成D,则D为,硝基在Fe/HCl作用下,被还原为-NH2,则E为。
(1)C为,名称为对硝基苯甲酸,E为:,其中含有的官能团为-NH2,-COO-,其名称分别为:氨基、酯基,故答案为对硝基苯甲酸;氨基、酯基;
(2)根据上述分析,A生成B为甲苯发生的硝化反应,也属于取代反应;B生成C为中甲基被氧化的反应,故答案为取代反应;氧化反应;
(3)C为,能与NaHCO3溶液反应,反应①为C与CH3CH2OH发生酯化反应,生成,反应方程式为:,故答案为;
(4)根据上述分析,反应②、③中试剂II和试剂III依次是酸性高锰酸钾溶液、NaOH溶液,故选A;
(5)J为,有多种同分异构体,其中符合a.为苯的二元取代物,其中一个取代基为羟基;?b.与J具有相同的官能团,且能发生银镜反应,说明含有酯基和醛基,则为甲酸酯;满足条件的同分异构体有:(包括间位和对位)、(包括间位和对位),共有6种,故答案为(或间位或对位)、(或间位或对位)(任写一种);
(6)A为,以A为起始原料,合成亚甲基环己烷(?),六元环可以由苯环与氢气加成得到,碳碳双键可以首先引入卤素原子,然后消去即可,可考虑如下流程:,故答案为。
19.羰基 溴原子 还原反应
【分析】
由A、B结构可知,A与发生反应生成B,B与锌汞齐(Zn-Hg)在浓盐酸条件下发生反应生成C,由已知反应和B的结构可知C的结构为,C发生反应生成D为,D与锌汞齐(Zn-Hg)在浓盐酸条件下发生反应生成E为,E发生去氢反应生成F为,F发生卤代反应生成G为,G与Mg在乙醚存在的条件下生成H为,H与环氧乙烷反应后再水解生成I为,I被CrO3氧化得到J为,据此解答。
【详解】
(1)由结构简式可知,D中含氧官能团名称为羰基,G中官能团名称为溴原子,故答案为:羰基;溴原子;
(2) D与锌汞齐(Zn-Hg)在浓盐酸条件下发生反应生成E为,反应类型为还原反应,故答案为:还原反应;
(3)C的分子式为C10H12O2,由已知反应和B的结构可知C的结构为,故答案为:;
(4)①属于芳香族化合物,说明含有苯环;②不能与金属钠反应,说明不含有羟基;③有3种不同化学环境的氢原子,说明有3种位置不同的氢原子,符合这三个条件的J的同分异构体为:,故答案为:;
(5)在无水乙醚和Mg的条件下生成,和、H2O反应生成,被CrO3氧化为,根据已知条件和、H2O生成,在浓硫酸、加热条件下发生消去反应生成。合成路线为:
,
故答案为:
。
同课章节目录
